 图 1
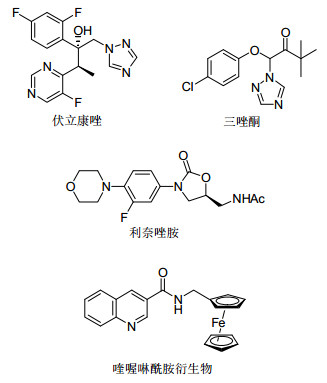
含有1, 2, 4-均三唑、吗啉和对氯苯基等活性组块的药物
Figure 1.
Containing 1, 2, 4-triazole, morpholine and p-chloro-phenyl and other active drugs
图 1
含有1, 2, 4-均三唑、吗啉和对氯苯基等活性组块的药物
Figure 1.
Containing 1, 2, 4-triazole, morpholine and p-chloro-phenyl and other active drugs

Citation: Zhang Chenglu, Tang Jie, Yin Liying, Xi Huan, Guo Yang, Sun Lijie. One Pot Synthesis of 3-Substituted-1-morpholino-1, 2, 4-triazole Mannich Bases and Their Activity Evaluation[J]. Chinese Journal of Organic Chemistry, 2015, 36(2): 358-362. doi: 10.6023/cjoc201507029

一锅法合成3-取代-1-吗啉基-1, 2, 4-均三唑Mannich碱及其活性评价
English
One Pot Synthesis of 3-Substituted-1-morpholino-1, 2, 4-triazole Mannich Bases and Their Activity Evaluation
-
Key words:
- Mannich base
- / Cdc25B inhibitor
- / plant growth regulator
- / herbicidal activity
-
多组分一锅法反应是将不同活性组快一次性构筑在一个分子中, 其主要优点是缩短了反应时间、增加了反应速率、提高了产率和再现性[1], Mannich反应是其中的重要代表, 成为构筑新型分子热点反应[2].
含1, 2, 4-均三唑结构的杂环类分子具有广泛的生物活性, 如抗炎、抗病毒和抗微生物和抗肿瘤等[3~6], 如已在临床应用的伏立康唑(图 1)中即含药效基团三唑; 通过将不同活性基团构筑于同一分子中能够有效的改善其生物活性, 如已应用于农业生产中的三唑酮(图 1)分子中同时具有三唑和对氯苯基, 成为一种高效、低毒的杀菌剂和除草剂; 吗啉环作为一种重要药效基团也已存在于多种药物和农药中[7~10], 如已用于治疗由特定微生物引起感染的利奈唑胺(图 1); 在药物分子中引入二茂铁基元, 可提高其药效, 已成为设计筛选用于治疗耐药性的癌症和疾病的重要方法之一, 如二茂铁喹喔啉酰胺(图 1)因引入二茂铁基团从而提高了化合物的抗结核活性.
 图 1
含有1, 2, 4-均三唑、吗啉和对氯苯基等活性组块的药物
Figure 1.
Containing 1, 2, 4-triazole, morpholine and p-chloro-phenyl and other active drugs
图 1
含有1, 2, 4-均三唑、吗啉和对氯苯基等活性组块的药物
Figure 1.
Containing 1, 2, 4-triazole, morpholine and p-chloro-phenyl and other active drugs
Mannich碱是潜在的生物制剂, 具有抗炎[11]、抗菌、抗真菌[12, 13]、抗肿瘤[14]和抗惊厥[15]等活性.一锅法Mannich反应[16~18], 将含有药效基团的三组分对接在一个分子中, 有望筛选出获得具有复合性能的药物分子.
Cdc25B (cell division cycle 25)是一种类蛋白酶的重要激酶, 对人体中的细胞分裂和基因表达起着重要的影响, 是一种潜在的致癌基因而成为靶点, 因此筛选优良的Cdc25B抑制剂可有效阻断癌细胞的增殖, 抑制癌症[19].人工合成植物生长调节剂是与植物激素具有类似生理和生物学效应的物质, 在农业生产上使用, 能有效调节作物的生育过程, 成为改善品质、增强作物抗逆性等重要措施[20], 设计研发新型植物生长调节剂, 调控植物的生长发育无疑具有重要意义.
为了探究不同药效基团在分子中相同位点和相同基团在不同位点对分子生物活性的影响, 本文以1, 2, 4-均三唑为模板, 分别在其3号位引入二茂铁基、对氯苯基、对甲氧苯基和正十一烷基, 然后借助4号位氨基分别引入二茂铁、对氯苯基、对甲氧苯基, 以从两个不同角度研究其构效关系.同时为了比较取代苯基、二茂铁基与吡啶、呋喃等杂环基团在4-位生物活性的差别, 分别将吡啶、呋喃基团引入到4种三唑分子中, 设计了19种Schiff碱, 最后通过多组分一锅法将3-取代基-1, 2, 4-均三唑Schiff碱和吗啉对接在同一个分子, 设计了新型系列Mannich碱, 并对其抑制Cdc25B、植物生长调节和除草活性进行了评价, 期待筛选出良好的Cdc25B抑制剂和性能优良的植物生长调节剂.目标分子合成路线如Scheme 1所示.
1 结果与讨论
1.1 目标化合物的合成与表征
IR谱图中, 在3100和2900 cm-1左右出现的峰为苯环上C—H的吸收峰, 1650和1500 cm-1左右出现的峰分别为C=N和C=C的吸收峰, 在1280 cm-1左右出现的峰为C=S的吸收峰, 在1150和1100 cm-1左右的峰分别为C—O和C—N的吸收峰; 1H NMR谱图中, HC=N上的质子信号在δ 10.0左右, 在δ 7.00~8.00处为芳环的质子信号, 吗啉环的质子信号在δ 2.8和3.7左右. HRMS谱图中, 所有的化合物均出现了[M+1]+峰.
1.2 目标化合物的生物活性测试
利用黄瓜子叶生根法测定了细胞分裂素活性, 用小麦芽鞘法测定细胞生长素活性, 用抑制稗草生根的方法测试除草活性, 测试方法参照文献[21]进行, 其中三唑酮(Triadimefon, Tri)和N-羟基-N-异丙基草酰胺(N-Hydroxy-N-isopropyloxamate, IPOHA)分别作为细胞分裂素活性测试和除草活性测试的参照物, 结果参见表 1.
Compd. Ar'/Ar'' Cytokinin activity Auxin activity Herbicidal activity effect/% Effect/% Grade Effect% Grade 7a 4-ClC6H4 92.9 A 17.5 C 58.9 7b 4-CH3OC6H4 38.4 B 32.8 B 67.3 7c 2-C5H4N 51.4 A 4.10 D 78.8 7d 2-C4H3O 17.1 C 5.80 D 74.8 8a 4-ClC6H4 80.3 A 39.8 B 76.2 8b 4-CH3OC6H4 30.6 B 38.3 B 82.1 8c 2-C5H4N 93.5 A 18.1 C 90.7 8d 2-C4H3O 55.8 A 25.1 C 65.1 8e C10H9Fe 68.5 A 35.9 B 72.7 9a 4-ClC6H4 55.3 A 15.3 C 76.3 9b 4-CH3OC6H4 86.9 A 34.8 B 77.5 9c 2-C5H4N 25.7 C 65.2 A 52.9 9d 2-C4H3O 36.7 B 54.9 A 65.9 9e C10H9Fe 78.5 A 16.9 C 85.7 10a 4-ClC6H4 65.1 A 36.9 B 92.1 10b 4-CH3OC6H4 47.9 A 43.9 A 77.3 10c 2-C5H4N 65.2 A 22.7 B 72.1 10d 2-C4H3O 58.1 A 37.1 B 70.9 10e C10H9Fe 61.8 A 56.7 A 69.8 Tri — 50.2 A — — — IPOHA — — — — — 50.2 表 1 目标化合物的植物生长调节测试
Table 1. plant growth regulating activity of target compounds1.3 Cdc25B和PTP1B的抑制活性测试
目标化合物初筛选择的浓度均为5 μg/mL, Cdc25B抑制活性的对照药物为Na3VO4, 然后选择抑制率大于50%的化合物进行复筛, 得出抑制活性剂量依赖关系, 即IC50值.抑制活性筛选实验方法:按照参考文献[22]的方法进行.本实验由国家新药中心协助完成, 测试结果见表 2所示.
Compd. 7a 7b 7c 7d 7e 8a 8b 8c IC50a/(mg·mL-1) 5.57±1.28 3.43±0.98 1.10±0.33 5.47±1.13 — 3.12±0.78 NA NA Compd. 8d 8e 9a 9b 9c 9d 9e 10a C50a/(mg·mL-1) 2.76±0.11 0.21±0.11 NA 3.45±1.26 NA NA 0.18±0.02 2.66±0.15 Compd. 10b 10c 10d 10e Na3VO4d C50a/(mg·mL-1) 1.79±0.28 1.29±0.11 1.06±0.10 0.23±0.01 1.86±0.24 a V alues calculated by nonlinear fitting through the inhibition rate at 5 μg/mL concentration. 表 2 目标化合物对Cdc25B的IC50值
Table 2. Target compounds IC50 values for Cdc25B2 结论
首次通过简便的一锅法合成了19种不同取代基含有吗啉基团的Mannich碱FcTABM、PCTABM、PMTABM和PUTABM, 评价了其对Cdc25B抑制活性及植物生长调节活性和除草活性.结果表明, 目标分子的细胞分裂素活性大都表现为A级, 其中8c促进效果最明显, 作用率高达93.5%;目标分子具有一定的细胞生长素活性, 多为B级或C级, 其中9c促进效果最明显, 作用率高达62.5%;所有分子均表现优良的除草剂活性, 10a表现最为明显, 作用率可达92.1%, 说明目标分子有望成为植物生长活性调节剂和除草剂.在Cdc25B的抑制活性中, 19个目标分子中有14个对Cdc25B具有优良的抑制活性, 其中7c、8e、9e、10b~10e 7个分子的IC50值低于阳性参照物Na3VO4, 有望成为潜在的Cdc25B抑制剂, 作为潜在的抗肿瘤药物先导物.
构效分析结果发现, 当该类分子结构中引入甲氧基、氯、吡啶、呋喃及二茂铁等基团时, 因分子中电子密度的升高而使分子表现出良好的生物活性.在3-位点引入二茂铁基团时, 目标分子均具有良好的抑制活性, 这可能是因叠加了二茂铁活性; 3-位点引入脂肪基时, 由于脂肪碳链增加时, 可改善分子的脂溶性, 从而使目标分子的生物活性提高, 因此呈现出较高的抑制活性; 3-位点取代基为对氯苯基和对甲氧苯基时, 部分目标分子具有抑制活性, 说明是由3-位点与4-位点共同作用影响分子的生物活性.由8a、9a和9b对比发现: 3-位点与4-位点同为对氯苯基或对甲氧苯基时, 抑制活性良好, 可能由于电子云密度分布较为均匀导致目标分子生物活性增加, 但当3-位点与4-位点的取代基不同时, 目标分子的抑制活性不明显.在4-位上引入杂环基团吡啶和呋喃, 对目标分子的生物活性有选择性改善.由此可见, 通过对1, 2, 4-三唑不同位点进行结构修饰, 可筛选出对Cdc25B具有优良的抑制活性的目标分子, 该类分子有望成为抗癌药物先导物.
3 实验部分
3.1 仪器与试剂
AVANCE 500 MHz NMR核磁共振波谱仪; Waters X evo Q-TOF MS液相色谱-质谱联用仪; TENSOR 27傅立叶变换红外光谱仪; X-5型数字显微熔点测定仪(温度计未经校正); WFH-203B型三用紫外分析仪.所用的试剂均为市售的分析纯, 两个测试蛋白PTP1B、Cdc25B均由国家新药筛选中心实验室利用大肠杆菌表达并纯化得到的, 纯度在90%以上.
3.2 实验方法
3.2.3 Mannich碱PCTABM、PMTABM和PUTABM的合成通法
于50 mL的圆底烧瓶中, 加入Schiff碱(0.5 mmol)和5 mL乙醇, 加热至回流后, 加入0.06 mL 37%甲醛(0.6 mmol), 搅拌10 min后, 加入吗啉(0.6 mmol); TLC检测反应完全后, 降至室温, 过滤得粗产品, 乙醇重结晶, 得目标产物PCTABM、PMTABM和PUTABM.其中8a已有文献[26]报道, 所得结果与文献值相符.
4-甲氧基苯烯基氨基-1-吗啉代甲基-3-4-氯苯基-1H-1, 2, 4-三唑-5(4H)-硫酮(8b):白色粉末, 收率79.2%. m.p. 139.1~130.2 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.86 (s, 1H), 7.84~7.77 (m, 4H), 7.52 (d, J=8.4 Hz, 2H), 7.06 (d, J=8.8 Hz, 2H), 5.11 (s, 2H), 3.78 (s, 3H), 3.65 (t, J=4.6 Hz, 4H), 2.83 (t, J=4.7 Hz, 4H); IR (KBr) ν: 3138, 3030, 2958, 1623, 1585, 1319, 1297, 1167, 969, 853 cm-1. HRMS calcd for C21H22ClN5O2S[M+1]+443.1183, found 443.1209.
1-吗啉代-3-4-氯苯基-4-吡啶-2-基甲烯基氨基-1H-1, 2, 4-三唑-5(4H)-硫酮(8c):淡黄色粉末, 收率80.7%. m.p. 91.8~92.9 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.99 (s, 1H), 8.78 (d, J=4.5 Hz, 1H), 8.09~8.04 (m, 2H), 7.93 (t, J=8.6 Hz, 2H), 7.66~7.43 (m, 3H), 5.18 (s, 2H), 3.59 (t, J=4.6 Hz, 4H), 2.71 (t, J=4.6 Hz, 4H); IR (KBr) ν: 3142, 3030, 2944, 1678, 1614, 1534, 1292, 1143, 850, 827 cm-1. HRMS calcd for C19H19Cl-N6OS [M+1]+ 414.1030, found 414.1056.
4-呋喃-2-基甲烯基氨基-1-吗啉代-3-4-氯苯基-1H-1, 2, 4-三唑-5(4H)-硫酮(8d):灰色粉末, 收率81.5%. m.p. 94.1~95.7 ℃; 1H NMR (D500 MHz, MSO-d6) δ: 9.59 (s, 1H), 8.11 (d, J=1.4 Hz, 1H), 7.87~7.61 (m, 2H), 7.58~7.50 (m, 2H), 7.45 (d, J=3.5 Hz, 1H), 7.13 (t, J=5.2 Hz, 1H), 5.16 (s, 2H), 3.77 (t, J=4.8 Hz, 4H), 2.94 (t, J=4.8 Hz, 4H); IR (KBr) ν: 3130, 3029, 2956, 1659, 1589, 1288, 1123, 883, 770 cm-1; HRMS calcd for C18H18Cl-N5O2S [M+1]+ 364.0870, found 403.0856.
4-二茂铁基-1-吗啉代甲基-3-4-氯苯基-1H-1, 2, 4-三唑-5(4H)-硫酮(8e):橘黄色粉末, 收率68.9%. m.p. 101.4~103.0 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.71 (s, 1H), 7.85~7.75 (m, 2H), 7.56 (t, J=8.6 Hz, 2H), 5.11 (s, 2H), 4.76 (t, J=1.8 Hz, 2H), 4.57 (t, J=1.8 Hz, 2H), 4.35 (s, 5H), 3.72 (t, J=4.6 Hz, 4H), 2.82 (t, J=4.7 Hz, 4H); IR (KBr) ν: 3134, 3030, 2944, 1670, 1587, 1412, 1271, 1159, 847, 450 cm-1. HRMS calcd for C26H30Cl-FeN5OS [M+1]+ 551.1209, found 551.1222.
4-4-氯苯烯基氨基-1-吗啉代甲基-3-(4-甲氧苯基)-1H-1, 2, 4-三唑-5(4H)-硫酮(9a):白色粉末, 收率75.3%. m.p. 134.1~135.4 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.86 (s, 1H), 7.81 (d, J=8.8 Hz, 2H), 7.70~7.64 (m, 2H), 7.30 (d, J=8.8 Hz, 2H), 7.21~7.15 (m, 2H), 5.21 (s, 2H), 3.81 (t, J=4.8 Hz, 4H), 3.68 (s, 3H), 2.91 (t, J=4.8 Hz, 4H); IR (KBr) ν: 3143, 3030, 2954, 1681, 1575, 1285, 1156, 852 cm-1. HRMS calcd for C21H22ClN5O2S[M+1]+ 443.1183, found 443.1145.
4-甲氧基苯烯基氨基-1-吗啉代甲基-3-(4-甲氧苯基)-1H-1, 2, 4-三唑-5(4H)-硫酮(9b):白色粉末, 收率78.0%. m.p. 129.1~130.2 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.41 (s, 1H), 7.72 (d, J=8.5 Hz, 2H), 7.61~7.58 (m, 2H), 7.39 (d, J=8.5 Hz, 2H), 7.36~7.25 (m, 2H), 5.48 (s, 2H), 3.78 (s, 3H), 3.65 (t, J=4.6 Hz, 4H), 2.83 (t, J=4.7 Hz, 4H); IR (KBr) ν: 3138, 3030, 2952, 1677, 1589, 1227, 1143, 844, 810 cm-1.HRMS calcd for C22H25N5O3S[M+1]+439.1678, found 439.170.
1-吗啉代-3-(4-甲氧苯基)-4-(吡啶-2-基甲烯基氨基)-1H-1, 2, 4-三唑-5(4H)-硫酮(9c):浅氯色粉末, 收率63.6%.m.p. 87.8~88.9 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.75 (s, 1H), 8.32 (d, J=4.7 Hz, 1H), 8.18 (d, J=7.87 Hz, 1H), 8.06 (dd, J=1.39, 7.64 Hz, 1H), 7.65 (dd, J=1.57, 6.83 Hz, 2H), 7.55~7.47 (m, 3H), 5.44 (s, 2H), 3.81 (s, 3H), 3.66 (t, J=4.6 Hz, 4H), 2.80 (t, J=4.6 Hz, 4H); IR (KBr) ν: 3134, 3030, 2945, 1678, 1601, 1238, 1061, 828, 775 cm-1. HRMS calcd for C20H22N6O2S[M+1]+ 410.1525, found 410.1530.
4-(呋喃-2-基甲烯基氨基)-1-吗啉代-3-(4-甲氧苯基)-1H-1, 2, 4-三唑-5(4H)-硫酮(9d):灰色粉末, 收率66.7%. m.p. 65.1~66.7 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.54 (s, 1H), 8.02 (s, 1H), 7.69 (d, J=8.5 Hz, 2H), 7.43 (d, J=3.6 Hz, 1H), 7.20 (d, J=8.6 Hz, 2H), 6.75 (dd, J=1.8, 3.4 Hz 1H), 5.12 (s, 2H), 3.77 (t, J=4.8 Hz, 4H), 3.64 (s, 3H), 2.88 (t, J=4.8 Hz, 4H); IR (KBr) ν: 3132, 3030, 2932, 1659, 1576, 1410, 1244, 1071, 830, 492 cm-1. HRMS calcd for C19H21N5O3S[M+1]+ 399.1365, found 399.1342.
4-二茂铁基-1-吗啉代甲基-3-(4-甲氧苯基)-1H-1, 2, 4-三唑-5(4H)-硫酮(9e):橘黄色粉末, 收率73.1%. m.p. 78.4~79.0 ℃; 1H NMR (500 MHz, DMSO-d6) δ: 9.80 (s, 1H), 7.80~7.72 (m, 2H), 7.56 (t, J=8.6 Hz, 2H), 5.10 (s, 2H), 4.76 (t, J=1.8 Hz, 2H), 4.57 (t, J=1.8 Hz, 2H), 4.35 (s, 5H), 3.80 (s, 3H), 3.72 (t, J=4.6 Hz, 4H), 2.85 (t, J=4.7 Hz, 4H); IR (KBr) ν: 3122, 3030, 2898, 1684, 1588, 1265, 1121, 845 cm-1. HRMS calcd for C27H33FeN5O2S [M+1]+547.1704, found 547.1688.
4-(4-氯苯烯基氨基)-1-吗啉代甲基-3-十一烷基-1H-1, 2, 4-三唑-5(4H)-硫酮(10a):白色粉末, 收率85.2%. m.p. 70.5~72.1 ℃, 1H NMR (500 MHz, CDCl3) δ: 10.53 (s, 1H), 7.81~7.77 (m, 2H), 7.47~7.42 (m, 2H), 5.10 (s, 2H), 3.71 (t, J=4.7 Hz, 4H), 2.83 (t, J=4.8 Hz, 4H), 2.80 (t, J=7.6 Hz, 2H), 1.76~1.71 (m, 2H), 1.40~1.36 (m, 2H), 1.34~1.25 (m, 14H), 0.89 (t, J=6.9 Hz, 3H); IR (KBr) ν: 3124, 2922, 2844, 1665, 1587, 1386, 867 cm-1. HRMS calcd for C25H39ClN5OS [M+1]+ 492.2558, found 492.2555.
4-甲氧基苯烯基氨基-1-吗啉代甲基-3-十一烷基-1H-1, 2, 4-三唑-5(4H)-硫酮(10b):白色粉末, 收率83.1%. m.p. 75.4~77.0 ℃; 1H NMR (500 MHz, CDCl3) δ: 10.15 (s, 1H), 7.82 (dd, J=1.8, 7.0 Hz, 2H), 7.00 (dd, J=1.8, 7.0 Hz, 2H), 5.10 (s, 2H), 3.88 (s, 3H), 3.71 (t, J=4.6 Hz, 4H), 2.84 (t, J=4.7 Hz, 4H), 2.80 (t, J=7.6 Hz, 2H), 1.76~1.71 (m, 2H), 1.40~1.36 (m, 2H), 1.34~1.25 (m, 14H), 0.89 (t, J=6.9 Hz, 3H); IR (KBr) ν: 3134, 2921, 2853, 1665, 1598, 1507, 1404, 1255, 1167, 1113, 1069, 855 cm-1. HRMS calcd for C26H42N5O2S[M+1]+ 488.3054, found 488.3058.
1-吗啉代-3-十一烷基-4-(吡啶-2-基甲烯基氨基)-1H-1, 2, 4-三唑-5(4H)-硫酮(10c):淡黄色粉末, 收率77.6%. m.p. 90.1~91.2 ℃; 1H NMR (500 MHz, CDCl3) δ: 10.63 (s, 1H), 8.75~8.74 (m, 1H), 8.09 (d, J=8.0 Hz, 1H), 7.83~7.80 (m, 1H), 7.41~7.39 (m, 1H), 5.10 (s, 2H), 3.71 (t, J=4.6 Hz, 4H), 2.84 (t, J=4.7 Hz, 4H), 2.81~2.78 (m, 2H), 1.77~1.63 (m, 2H), 1.40~1.36 (m, 2H), 1.33~1.25 (m, 14H), 0.89 (t, J=6.8 Hz, 3H); IR (KBr) ν: 3125, 2952, 2854, 2372, 1655, 1607, 1560, 1450, 1326, 855 cm-1. HRMS calcd for C24H39N6OS [M+1]+459.2901, found 459.2904.
4-(呋喃-2-基甲烯基氨基)-1-吗啉代-3-十一烷基-1H-1, 2, 4-三唑-5(4H)-硫酮(10d):灰色粉末, 收率71.2%. m.p. 95.7~97.4 ℃; 1H NMR (500 MHz, CDCl3) δ: 10.32 (s, 1H), 7.67 (d, J=1.7 Hz, 1H), 7.06 (t, J=3.4 Hz, 1H), 6.60 (dd, J=1.8 Hz, 3.5 Hz, 1H), 5.16 (s, 2H), 3.77 (t, J=4.8 Hz, 4H), 2.94 (t, J=4.8 Hz, 4H), 2.81 (t, J=7.7 Hz, 2H), 1.77~1.74 (m, 2H), 1.39~1.34 (m, 2H), 1.32~1.25 (m, 14H), 0.91 (t, J=6.8 Hz, 3H); IR (KBr) ν: 3192, 2921, 2854, 1645, 1394, 845 cm-1. HRMS calcd for C23H38N5O2S[M+1]+448.2741, found 448.2745.
4-二茂铁基-1-吗啉代甲基-3-十一烷基-1H-1, 2, 4-三唑-5(4H)-硫酮(10e):橘黄色粉末, 收率79.3%. m.p. 119.4~121.1 ℃; 1H NMR (500 MHz, CDCl3) δ: 9.71 (s, 1H), 5.11 (s, 2H), 4.76 (t, J=1.8 Hz, 2H), 4.57 (t, J=1.8 Hz, 2H), 4.35 (s, 5H), 3.72 (t, J=4.6 Hz, 4H), 2.85 (t, J=4.7 Hz, 4H), 1.77~1.73 (m, 2H), 1.39~1.35 (m, 2H), 1.31~1.26 (m, 14H), 0.92 (t, J=7.0 Hz, 3H); IR (KBr) ν: 3443, 2940, 2786, 1617, 1414, 1346, 1279, 1174, 875 cm-1. HRMS calcd for C29H44FeN5OS [M+1]+ 566.2611, found 566.2617.
辅助材料(Supporting Information) 所有目标化合物的核磁共振氢谱.这些材料可以免费从本刊网站(http://sioc-journal.cn/)上下载.
3.2.2 Schiff碱FcTAB、PCTAB、PMTAB、PUTAB的合成
Schiff碱FcTAB、PCTAB、PMTAB、PUTAB的合成和Mannich FcTABM碱根据文献[25]的方法合成, 所得结果与文献值相符.
3.2.1 化合物FcTA、PCTA、PMTA和PUTA的合成
-
-
[1]
Ashok, M.; Holla, B. S.; Poojary, B. Eur. J. Med. Chem. 2007, 42, 1095. doi: 10.1016/j.ejmech.2007.01.015
-
[2]
Roman, G. Eur. J. Med. Chem. 2015, 89, 743. doi: 10.1016/j.ejmech.2014.10.076
-
[3]
李国华, 杨红, 有机化学, 2008, 28, 1918. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract337708.shtmlLi, G. H.; Yang, H. Chin. J. Org. Chem. 2008, 28, 1918 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract337708.shtml
-
[4]
Navidpour, L.; Shafaroodi, H.; Abdi, K.; Amini, M.; Ghahremani, H. M.; Dehpour, A. R.; Shafiee, A. Bioorg. Med. Chem. 2006, 14, 2507. doi: 10.1016/j.bmc.2005.11.029
-
[5]
Holla, B. S.; Veerendra, B.; Shivananda, M. K.; Poojary, B. Eur. J. Med. Chem. 2003, 38, 759. doi: 10.1016/S0223-5234(03)00128-4
-
[6]
Wang, B. L.; Shi, Y. X.; Ma, Y.; Liu, X. H.; Li, Y. H.; Song, H. B.; Li, B. J.; Li, Z. M. J Agric Food Chem. 2010, 58, 5515. doi: 10.1021/jf100300a
-
[7]
Deng, X. M.; Wang, J. H.; Zhang, J. M.; Sim, T.; Kim, N. D.; Sasaki, T.; Luther, W.; George, R. E.; Janne, P. A.; Gray, N. S. Med. Chem. Lett. 2011, 2, 379. doi: 10.1021/ml200002a
-
[8]
Kunj, B. M.; Vinod, K. T. J. Org. Chem. 2014, 79, 5752. doi: 10.1021/jo500890w
-
[9]
Burbuliene, M. M.; Jakubkiene, V.; Mekuskiene, G.; Udrenaitea, E.; Smiciusa, R.; Vainilaviciusa, P. Farmaco 2004, 59, 767. doi: 10.1016/j.farmac.2004.05.007
-
[10]
Koparir, M.; Orek, C.; Parlak, A. E.; Söylemez, A.; Koparir, P.; Karatepe, M.; Dastan, S. D. Eur. J. Med. Chem. 2013, 63, 340. doi: 10.1016/j.ejmech.2013.02.025
-
[11]
Jakubkiene, V.; Burbuliene, M. M.; Mekuskiene, G.; Emilija, U.; Gaidelis, P.; Vainilavičius, P. Farmaco 2003, 58, 323. doi: 10.1016/S0014-827X(02)00022-8
-
[12]
Ashok, M.; Holla, B. S.; Poojary, B. Eur. J. Med. Chem. 2007, 42, 1095. doi: 10.1016/j.ejmech.2007.01.015
-
[13]
Holla, B. S.; Rao, B. S.; Shridhara, K.; Akberali, P. M. Farmaco 2000, 55, 338. doi: 10.1016/S0014-827X(00)00033-1
-
[14]
Hu, G. Q.; Wang, G. Q.; Duan, N. N.; Wen, X. Y.; Cao, T.Y.; Xie, S. Q.; Huang, W. L. Acta Pharm. Sin. B 2012, 2, 312. doi: 10.1016/j.apsb.2011.11.003
-
[15]
Kaminski, K.; Obniska, J.; Chlebek, I.; Wiklik, B.; Rzepka, S. Bioorg. Med. Chem. 2013, 21, 6821. doi: 10.1016/j.bmc.2013.07.029
-
[16]
Arafa, W. A. A; Mohamed, A. S. Chin. J. Chem. 2011, 29, 1661. doi: 10.1002/cjoc.v29.8
-
[17]
Mohamed, R. A. Molecules 2014, 19, 18897. doi: 10.3390/molecules191118897
-
[18]
Mostafa, A. H.; Refaat, M. S.; Mohammed, A. A.; Mohammed, F. M. Arch. Pharm. Res. 2011, 34, 1239. doi: 10.1007/s12272-011-0802-z
-
[19]
Tsuchiya, A.; Hirai, G.; Koyama, Y.; Oonuma, K.; Otani, Y.; Osada, H.; Sodeoka, M. Med. Chem. Lett. 2012, 3, 294. doi: 10.1021/ml2002778
-
[20]
李清寒, 王苗苗, 化学研究与应用, 2010, 22, 186. http://www.cnki.com.cn/Article/CJFDTotal-HXYJ201002012.htmLi, Q. H.; Wang, M. M. Chem. Res. Appl. 2010, 22, 186 (in Chinese). http://www.cnki.com.cn/Article/CJFDTotal-HXYJ201002012.htm
-
[21]
朱长安, 武飞宇, 王雪, 高丽娜, 翁前锋, 石丽, 张成路, 应用化学, 2014, 31, 455. http://www.cnki.com.cn/Article/CJFDTotal-YYHX201404014.htmZhu, C. A.; Wu, F. Y.; Wang, X.; Gao, L. N.; Weng, Q. F.; Shi, L.; Zhang, C. L. Chin. J. Appl. Chem. 2014, 31, 455 (in Chinese). http://www.cnki.com.cn/Article/CJFDTotal-YYHX201404014.htm
-
[22]
Lavecchia, A.; Giovanni, C. D.; Pesapane, A.; Montuori, N.; Ragno, P.; Martucci, N. M.; Masullo, M.; Vendittis, E. D. J. Med. Chem. 2012, 55, 4142. doi: 10.1021/jm201624h
-
[23]
Sahoo, P. K.; Sharma, R.; Pattanayak, P. Med. Chem. Res. 2010, 19, 127. doi: 10.1007/s00044-009-9178-8
-
[24]
George, T.; Mehta, D. V.; Tahilramani, R.; David, J.; Talwalker, P. K. J. Med. Chem. 1971, 14, 335. doi: 10.1021/jm00286a016
-
[25]
张成路, 王雪, 国阳, 吴一非, 高丽娜, 孙丽杰, 柴金华, 朱长安, 有机化学, 2014, 34, 2331. doi: 10.6023/cjoc201405015Zhang, C. L.; Wang, X.; Guo, Y. Wu, Y. F.; Gao, L. N.; Sun, L. J.; Chai, J. H.; Zhu, C. A. Chin. J. Org. Chem. 2014, 34, 2331 (in Chinese). doi: 10.6023/cjoc201405015
-
[26]
Gupta, A, K.; Prachand, S.; Patel, A.; Jain, S. Int. J. Pharm. Life Sci. 2012, 3, 1848.
-
[1]
-
表 1 目标化合物的植物生长调节测试
Table 1. plant growth regulating activity of target compounds
Compd. Ar'/Ar'' Cytokinin activity Auxin activity Herbicidal activity effect/% Effect/% Grade Effect% Grade 7a 4-ClC6H4 92.9 A 17.5 C 58.9 7b 4-CH3OC6H4 38.4 B 32.8 B 67.3 7c 2-C5H4N 51.4 A 4.10 D 78.8 7d 2-C4H3O 17.1 C 5.80 D 74.8 8a 4-ClC6H4 80.3 A 39.8 B 76.2 8b 4-CH3OC6H4 30.6 B 38.3 B 82.1 8c 2-C5H4N 93.5 A 18.1 C 90.7 8d 2-C4H3O 55.8 A 25.1 C 65.1 8e C10H9Fe 68.5 A 35.9 B 72.7 9a 4-ClC6H4 55.3 A 15.3 C 76.3 9b 4-CH3OC6H4 86.9 A 34.8 B 77.5 9c 2-C5H4N 25.7 C 65.2 A 52.9 9d 2-C4H3O 36.7 B 54.9 A 65.9 9e C10H9Fe 78.5 A 16.9 C 85.7 10a 4-ClC6H4 65.1 A 36.9 B 92.1 10b 4-CH3OC6H4 47.9 A 43.9 A 77.3 10c 2-C5H4N 65.2 A 22.7 B 72.1 10d 2-C4H3O 58.1 A 37.1 B 70.9 10e C10H9Fe 61.8 A 56.7 A 69.8 Tri — 50.2 A — — — IPOHA — — — — — 50.2 表 2 目标化合物对Cdc25B的IC50值
Table 2. Target compounds IC50 values for Cdc25B
Compd. 7a 7b 7c 7d 7e 8a 8b 8c IC50a/(mg·mL-1) 5.57±1.28 3.43±0.98 1.10±0.33 5.47±1.13 — 3.12±0.78 NA NA Compd. 8d 8e 9a 9b 9c 9d 9e 10a C50a/(mg·mL-1) 2.76±0.11 0.21±0.11 NA 3.45±1.26 NA NA 0.18±0.02 2.66±0.15 Compd. 10b 10c 10d 10e Na3VO4d C50a/(mg·mL-1) 1.79±0.28 1.29±0.11 1.06±0.10 0.23±0.01 1.86±0.24 a V alues calculated by nonlinear fitting through the inhibition rate at 5 μg/mL concentration. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 91
- HTML全文浏览量: 4



 下载:
下载:

 下载:
下载:

