Progress in Syntheses and Biological Activities of 1, 3, 4-Thiadiazole Derivatives
几十年来,杂环化合物如嘧啶、吡咯、噻唑、噁唑和咪唑等及其衍生物因具有较高的生物活性,而被广泛应用于医药、农业及材料等领域,逐渐引起化学家们的关注。噻二唑是众多唑类杂环化合物中的重要一员,具有较多的生物和药理活性。由于噻二唑独特的结构-五元芳香杂环中包括了2个N原子和1个S原子,对其进行化学修饰可能得到较高生物活性的衍生物,因此噻二唑衍生物的合成方法及其生物活性已成为国内外研究的热点[1]。噻二唑结构有4个同分异构体,即1, 2, 3-噻二唑、1, 3, 4-噻二唑、1, 3, 5-噻二唑及1, 2, 4-噻二唑(图式1)。其中,1, 3, 4-噻二唑生物活性较高,研究最多,应用最广泛。为此,本文主要对1, 3, 4-噻二唑衍生物的最新合成方法及其在医药领域的应用进行了介绍。
脱水环合法是1, 3, 4-噻二唑类衍生物合成的最常见方法之一。反应通过亲核试剂进攻羰基碳原子,在合适的脱水剂条件下脱水成环,最后形成目标化合物。常见的有如下几种:
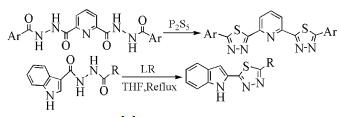
1, 2-二酰肼类化合物在P2S5或者Lawesson试剂(LR)的催化下[2],可环合成1, 3, 4-噻二唑类衍生物。Kumar等[3]和Liao等[4]以DMF、CHCl3、THF等作为反应溶剂,在P2S5或Lawesson试剂的作用下环合成1, 3, 4-噻二唑衍生物(式(1))。这种方法十分常见,但此类方法具有反应时间长、反应温度高、产率低、副产物多等缺点。
|
(1)
|
Augustine等[5]也以P2S5或者LR作为硫代试剂以及脱水环合剂,在丙基磷酸酐(T3P)作用下直接将羧酸和酰肼反应生成1, 3, 4-噻二唑衍生物(式(2))。此方法步骤简单并提高了产率,反应会有少量(3%~5%)1, 3, 4-噁二唑副产物产生,通过重结晶和柱层析可有效提纯得到目标产物。
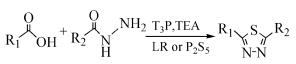
|
(2)
|
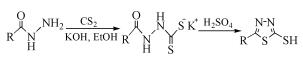
浓硫酸作为一种高效的脱水剂,在1, 3, 4-噻二唑及其衍生物的合成中也占有重要地位。Wei等[6]和Kadi等[7]分别报道由二硫代氨基甲酸盐衍生物经浓硫酸脱水可环合成2-巯基-5-取代-1, 3, 4-噻二唑衍生物(式(3)),此方法反应条件比较苛刻,需要0~5℃下反应24h,通常产率只有17%~35%。
|
(3)
|
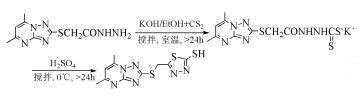
酰肼与CS2、二硫代氨基甲酸酯反应也可以得到1, 3, 4-噻二唑衍生物[8]。Luo等[9]利用酰肼类化合物和CS2在碱性条件下反应,随后在浓硫酸脱水作用下生成一系列2-巯基-1, 3, 4-噻二唑衍生物(式(4))。
|
(4)
|
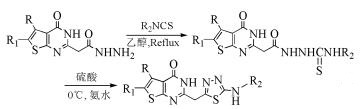
Mavrova等[10]利用酰肼类化合物与异硫氰酸酯类化合物反应生成中间体,然后经浓硫酸脱水环合合成了一系列1, 3, 4-噻二唑衍生物(式(5))。以上反应都需经过多步反应,操作繁琐,产率较低,且反应中采用浓硫酸作为脱水剂,反应条件苛刻。
|
(5)
|
磷酸类化合物也是一种常见的脱水试剂,与硫酸相比,磷酸的氧化性较弱,对带有还原性较强基团的底物更为适用。Sathisha等[11]以磷酸为脱水试剂,将酰胺基硫脲衍生物脱水成环,形成1, 3, 4-噻二唑衍生物(式(6))。
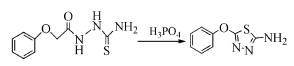
|
(6)
|
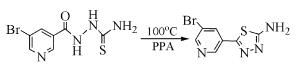
Jiang等[12]则通过选择多聚磷酸(PPA)作为脱水环合试剂,由酰胺基硫脲衍生物合成1, 3, 4-噻二唑衍生物(式(7))。
|
(7)
|
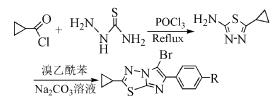
Noolvi等[13]利用环丙酰氯和氨基硫脲反应,在三氯氧磷催化下生成2-氨基-5-环丙基-1, 3, 4-噻二唑,再与取代的溴乙酰苯反应生成咪唑并[2, 1-b]噻二唑衍生物。此类反应产率大多在60%~80%,但三氯氧磷毒性较强,对环境危害较大(式(8))。
|
(8)
|
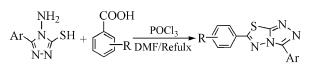
Almajan等[14]通过使用三氯氧磷作为环化剂,以4-氨基-5-芳基-3-巯基-1, 2, 4-三氮唑为原料与取代的苯甲酸反应生成一系列三氮唑并噻二唑类衍生物(式(9))。
|
(9)
|
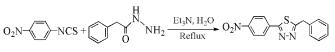
Aryanasab等[15]发现在以三乙胺作为催化剂条件下,二硫代氨基甲酸酯类化合物可以与酰肼类化合物反应,在水相中加热回流得到2, 5位取代的1, 3, 4-噻二唑衍生物(式(10))。其可能的反应机理如式(11)所示。该类方法避免了大量的繁琐操作,但是仍需要在苛刻的反应条件下进行[16, 17]。
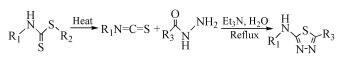
|
(10)
|
|
(11)
|
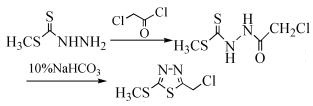
Wang等[18]利用氯乙酰氯将二硫代氨基甲酸甲酯衍生物酰基化,然后在碳酸氢钠作用下脱水环合成2, 5-取代-1, 3, 4-噻二唑衍生物(式(12)),方法中用到的酰化试剂会对环境造成污染,危害较大。
|
(12)
|
通过选择合适的催化剂,反应底物可以直接环化成1, 3, 4-噻二唑衍生物。与脱水环合法相比,反应通常不涉及剧毒化合物的使用且原子利用率较高,但一些反应仍然具有严苛的条件要求。
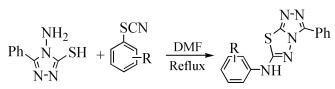
Almajan等[14]以4-氨基-5-芳基-3-巯基-1, 2, 4-三氮唑为基本原料与苯异硫氰酸酯反应生成三氮唑并噻二唑类衍生物(式(13))。
|
(13)
|
异硫氰酸酯类化合物可以与肼反应生成联二硫脲类衍生物(式(14))[19]。Hassan等[20]利用联二硫脲类化合物和苯醌衍生物反应生成2, 5位取代的1, 3, 4-噻二唑衍生物(式(15))。
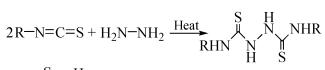
|
(14)
|

|
(15)
|
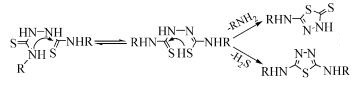
联二硫脲类衍生物还可以通过分子内的亲核进攻环合成2, 5位为-NHR取代的1, 3, 4-噻二唑衍生物(式(16))[21]。
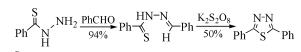
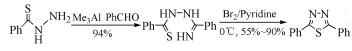
Fararr等[22]通过硫代苯酰肼与苯甲醛或苯甲腈反应生成腙类中间体,进而环合成2, 5-二苯基-1, 3, 4-噻二唑(式(17),(18))。此类噻二唑衍生物的合成,分别经过了硫代酰肼的去质子化、分子内的亲核进攻、脱去H2或NH3分子,最后生成2, 5-二苯基-1, 3, 4-噻二唑。
|
(16)
|
|
(17)
|
|
(18)
|
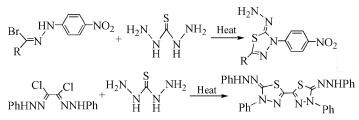
硫代卡巴肼又称硫代甲酰二肼。以硫代卡巴肼为原料,在不同反应条件下与多种物质反应生成1, 3, 4-噻二唑衍生物。Sayed等[23]利用硫代卡巴肼和卤代的腙类化合物反应得到1, 3, 4-噻二唑衍生物。同样的反应条件下,与联卤代的腙类反应生成联1, 3, 4-噻二唑衍生物(式(19))。
|
(19)
|
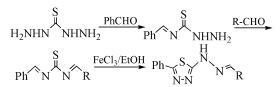
除了卤代的腙类,Shawali等[24, 25]用硫代卡巴肼衍生物和醛类化合物反应生成腙类化合物,再进一步生成1, 3, 4-噻二唑衍生物(式(20))。
|
(20)
|
羧酸类化合物和氨基硫脲也可在离子液体中反应生成单环或双环的2-氨基-5-取代-1, 3, 4-噻二唑类衍生物(式(21))[26],此方法避免使用毒性较大的三氯氧磷,反应条件相对温和。
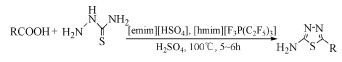
|
(21)
|
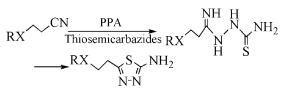
腈类化合物也可和氨基硫脲反应生成1, 3, 4-噻二唑衍生物[27]。反应过程中以PPA为反应媒介,将腈类化合物转变成亚氨酯,再与氨基硫脲反应转变氨基腙,随即失去一个NH3分子环合成1, 3, 4-噻二唑衍生物(式(22))。
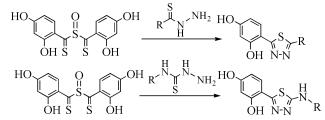
亚磺酰基-双(2, 4-二羟基苯基)甲基硫酮(STB)在甲醇中与氨基硫脲衍生物或硫代酰肼衍生物反应分别生成2, 5-取代-1, 3, 4-噻二唑衍生物(式(23))[28]。STB在反应过程中既是反应物又作为亲电的环合剂,使得反应能够高效地发生,获得较高的产率。
|
(22)
|
|
(23)
|
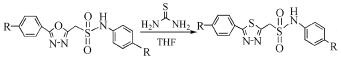
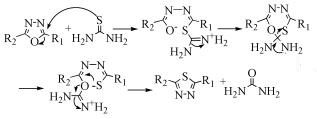
近年来,一些氧杂环通过与硫氰酸酯或硫脲作用转化为硫杂环的反应已见报道。Padmavathi等[29, 30]报道了1, 3, 4-噁二唑衍生物与硫脲或硫氰酸脂在四氢呋喃中反应,高产率地生成1, 3, 4-噻二唑衍生物(式(24)),其反应机理如式(25)。
|
(24)
|
|
(25)
|
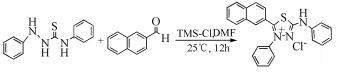
Kappel等[31]通过固相树脂,利用三甲基氯硅烷合成1, 3, 4-噻二唑衍生物(式(26))。该方法步骤简单,得到的产物易于分离且产率较高,合成过程绿色环保。
|
(26)
|
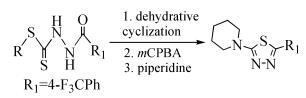
Hwang等[32]以氯甲基树脂作为高分子载体,与二硫化碳和不同酰肼化合物于室温下生成二硫代氨基甲酸酯类衍生物,再通过选择性脱水环化固相合成了一系列1, 3, 4-噻二唑衍生物(式(27)),并考察了不同脱水剂对环化反应的影响以及不同底物胺对生成2-取代氨基-5-芳基1, 3, 4-噻二唑衍生物的影响[33]。
微波技术在有机合成中的运用越来越广泛,已成为目前化学研究领域最活跃的领域之一。与一些传统加热合成方法相比,将微波合成技术运用到1, 3, 4-噻二唑的合成中,可以高效、高产率地合成出1, 3, 4-噻二唑衍生物。
|
(27)
|
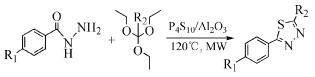
Polshettiwar等[34]利用微波加热将苯甲酰肼与多种原酸乙酯在无溶剂中直接反应,短时间内高产率地合成出了一系列1, 3, 4-噻二唑衍生物(式(28))。
|
(28)
|
Kiryanov等[35]利用1, 2-二酰肼类衍生物在无溶剂下微波辐射反应高效、快速地环合生成1, 3, 4-噻二唑衍生物(式(29))。

|
(29)
|
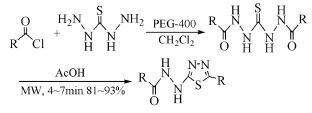
李政等[36]使用硫代卡巴肼为起始原料,以可回收的硅胶二氯磷酸酯为脱水剂,在微波辐射下高产率地合成1, 3, 4-噻二唑衍生物。此类方法简单、快速、且对环境污染较小(式(30))。
|
(30)
|
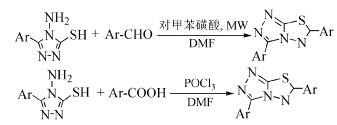
Mathew等[38]利用微波加热,将4-氨基-5-芳基-3-巯基-1, 2, 4-三氮唑分别与芳醛类和芳酸类化合物反应生成一系列三氮唑并噻二唑类衍生物(式(31))。
|
(31)
|
笔者课题组[37]也以甲氧基苯甲酸、氨基硫脲为原料,通过直接加热和微波加热两种方式得到1, 3, 4-噻二唑类衍生物,实验表明,采用微波加热比传统加热可大大缩短反应时间,提高反应产率。
含1, 3, 4-噻二唑结构的衍生物作为药物中间体,具有很高的药理活性,对其进行化学修饰得到的多种衍生物也可能具有更高的生物活性。本文主要对含有1, 3, 4-噻二唑结构的衍生物在抗菌、抗癌、抗肿瘤等方面的研究进行概述。
以1, 3, 4-噻二唑为基本母环,引入其他活性基团,有望得到具有更高生物活性的噻二唑衍生物,为抗菌类药物提供先导化合物。
Chandrakantha等[39]对合成的咪唑并[2, 1-b][1, 3, 4]-噻二唑衍生物(式(33))进行抑菌活性测试,发现该化合物在0.5~1.0 mg/mL浓度下,与同浓度的传统抗菌药物氟康唑相比,对黄曲霉和白色念珠菌具有更好的抑制活性。
|
(32)
|
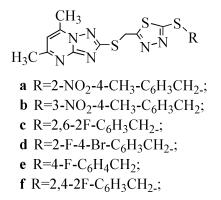
Luo等[9]所合成的化合物33a~33f(式(33))对轮纹病菌和纹枯病菌均有抑制活性,其中化合物33a、33c对荧光假单胞菌具有最好的抑制作用,最小抑菌浓度(MIC)分别为1.56和6.25 μg/mL;而化合物33d、33f对大肠杆菌展示出了较好的抑制能力,MIC分别为3.13和6.25 μg/mL。
|
(33)
|
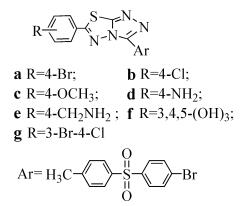
Almajan等[34]对所合成的三氮唑并噻二唑类化合物34a~34g(式(34))进行了体外抑菌实验,结果表明,大部分测试物对革兰氏阳性菌比对革兰氏阴性菌具有更好的抑制活性,其中化合物34g对表皮葡萄球菌和粪肠球菌表现出了更好的抗菌活性,MIC分别为64和32μg/mL。
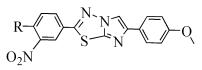
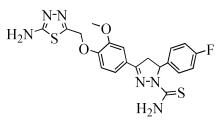
Noolvi等[40]用所合成的噻二唑醚类衍生物对9种菌株进行体外抗菌活性研究,结果发现带有4-氟苯基取代基的化合物(式(35))对上述9种菌均有不同程度的抑制作用,其中对肠道沙门氏菌和霍乱弧菌具有较强的抑制活性,浓度为50 μg/mL时的抑制率分别为97%和95%。
|
(34)
|
|
(35)
|
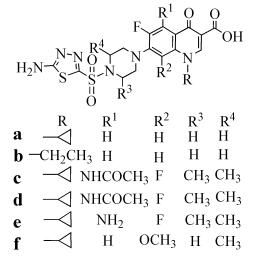
Talath等[41]合成的氟代喹诺酮基-1, 3, 4-噻二唑衍生物(式(36))对金黄色葡萄球菌、粪肠球菌、芽孢杆菌均表现出了很好的抑制能力,其中部分化合物对结核杆菌菌株H37Rv具有抑制作用。
|
(36)
|
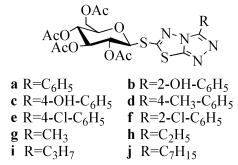
王美君等[42]通过体外抑菌活性测试发现,葡萄糖基取代三氮唑并噻二唑类化合物(式(37))对革兰氏阴性菌(大肠杆菌)、革兰氏阳性菌(金黄色葡萄球菌和枯草芽抱杆菌)和真菌(白色念球菌)均具有一定的抗菌活性。其中,化合物37b~37e、37g和37j对大肠杆菌的抗菌活性均优于市售药物氟康唑,其他化合物的抗菌活性与氟康唑等效;并且所有化合物都表现出良好的抗真菌活性,其中化合物37b、37c和37f~37h对真菌(白色念珠球菌)的抗菌活性优于三氯生,并且接近于氟康唑。在所有化合物中,化合物37c对4种菌株的最小抑菌浓度皆最低,表现出较好的抗菌活性。
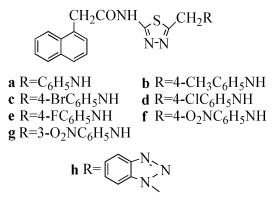
2, 5-二取代-1, 3, 4-噻二唑化合物具有抗炎、止痛、抗溃疡、抗脂质过氧化作用,可作为抗炎类药物。环加氧酶2(COX-2)是炎症发生发展的关键因子之一,而环加氧酶1 (COX-1)则主要调控生理功能。选择性抑制剂在抗炎的同时,避免干扰生理功能,是抗炎治疗的很好的靶点。李英俊等[43]对所合成的化合物(式(38))进行了COX-2活性抑制实验。发现化合物38f对COX-2具有很强的抑制活性,抑制率高达95.59%;化合物38g对COX-2也具有一定的抑制活性,但抑制率仅为0.61%。其余化合物对COX-2无抑制作用。
|
(37)
|
|
(38)
|
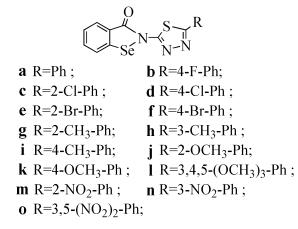
1, 3, 4-噻二唑衍生物被广泛地用于临床的抗肿瘤药物中。Luo等[44]合成了2-(苯并硒内酰胺基)-1, 3, 4-噻二唑衍生物(式(39)),研究其对3种肿瘤细胞的体外抗增殖活性,结果表明,部分化合物对人乳腺癌细胞和肺癌细胞表现出很好的抑制增生能力,其中3, 4, 5-三甲氧苯基取代的1, 3, 4-噻二唑化合物对肝癌细胞株SSMC-7721、人乳腺癌细胞MCF-7和肺癌细胞A-549均具有很好的抑制活性,IC50分别为7.15、3.34和3.24μmol/L。
|
(39)
|
Ibrahim等[45]合成了3, 6-取代-[1, 2, 4]三氮唑并[3, 4-b] [1, 3, 4]-噻二唑类衍生物(式(40)),通过体外抗肿瘤细胞增殖活性研究发现,部分化合物对细胞周期蛋白依赖性激酶CDK1/B、细胞周期蛋白依赖性激酶CDK2/A和细胞周期蛋白依赖性激酶CDK4/D具有较好的抑制能力,其中化合物40c对CDK1/B、CDK2/A和CDK4/D有最高的抑制活性,IC50分别为0.9、0.4和0.4μmol/L。
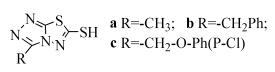
|
(40)
|
1, 3, 4-噻二唑类衍生物在抗肿瘤方面研究已久,近年来,越来越多的此类衍生物被应用到抗癌研究中,某些噻二唑类衍生物被证明具有很好的抗癌活性。
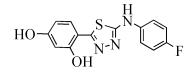
Rzeski等[46]对所合成的2-(4-氟苯基氨基)-5-(2, 4-二羟基苯基)-1, 3, 4-噻二唑(式(41))进行了体外抗癌活性研究,发现此化合物对人神经系统癌细胞、腺癌和肺癌具有很好的抗增殖活性,而且对正常的星形胶质细胞、肝细胞和纤维母细胞没有影响。
|
(41)
|
|
(42)
|
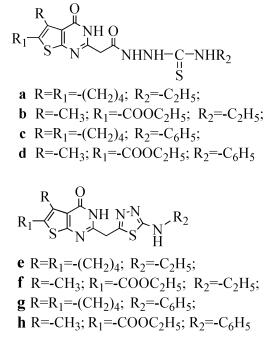
Mavrova等[10]采用MTS法对一系列1, 3, 4-噻二唑衍生物及其前体(式(42))进行体外人体结肠癌细胞株HT-29、乳腺癌细胞MDA-MB-231、宫颈癌细胞HeLa、肝癌细胞HepG2的抑制实验,结果表明化合物42b对MDA-MB-231有很强的抑制活性,IC50为0.039μmol/L,化合物42e对HepG2有很强的抑制活性,IC50为0.21μmol/L,化合物42f对MDA-MB-231和HeLa均具有较好的抑制作用,IC50分别为0.0012 μmol/L和3.31 μmol/L。
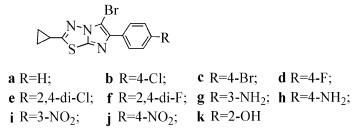
Noolvi等[13]对合成的咪唑并[2, 1-b]噻二唑衍生物(式(43))进行了体外白血病、肺癌、结肠癌、卵巢癌、黑色素瘤等癌细胞抑制实验研究,发现化合物43b对白血病癌细胞表现出了最好的抑制效果,其GI50为1.79μmol/L,有望成为一种新型的白血病癌细胞抑制剂。
|
(43)
|
近年来,1, 3, 4-噻二唑衍生物的合成方法及其生物活性已取得诸多进展。本文概述了1, 3, 4-噻二唑衍生物的多种合成方法,有些是常用的,但是大都存在一个或者多个缺点,如反应条件苛刻、环合时间较长、副产物较多、催化剂昂贵、底物使用范围较窄以及对环境不友好等。因此,积极寻找一种方便、绿色、高产的合成方法对于1, 3, 4-噻二唑衍生物的合成是十分必要的。
总之,随着人们对噻二唑衍生物研究的不断深入,噻唑类化合物已在抗菌、抗癌、抗肿瘤等方面取得重大突破,但是该类化合物运用于临床药物并不多,有待合成出更多新型的噻二唑类衍生物,并被运用于生物医药等领域。因此,设计、合成结构多样的噻二唑衍生物对于丰富杂环化学的内容以及构建唑类化合物药物数据库具有十分重要的意义。
 2016,
Vol. 79
2016,
Vol. 79 Issue (10): 929-935
Issue (10): 929-935 2016,
Vol. 79
2016,
Vol. 79 Issue (10): 929-935
Issue (10): 929-935