1 合肥工业大学化学与化工学院 合肥 230009;
2 安徽大学化学化工学院 合肥 230601
2016-01-06 收稿, 2016-02-24 接受
基金项目: 国家自然科学基金项目(21273008)资助
1 School of Chemistry and Chemical Engineering, Hefei University of Technology, Hefei 230009;
2 College of Chemistry & Chemical Engineering, Anhui University, HeFei 230601
物质的微观结构决定着它的宏观性能。长期以来,盐溶液中的离子-溶剂间的相互作用受到了人们的广泛关注[1~3]。水是最常见的质子溶剂,水分子之间通过氢键相互连接。当水溶液中加入盐后,离子水合层中水的结构将发生改变,产生溶剂化作用,为了研究溶液中的离子水合作用,科学工作者进行了长期的理论及实验研究,但许多未知问题依然存在。
氯化铜溶液是一种常用的电解质溶液,广泛应用于有机合成、湿法冶金和电镀等工业[4~7]。目前,对氯化铜溶液的微观结构已做了大量研究。Sverjensky等[8]通过测定二价铜离子与氯离子形成配合物的稳定常数,得出氯化铜溶液中可能存在[Cu]2+、[CuCl]+、[CuCl2]0、[CuCl3]-、[CuCl4]2-等不同的水合物。Xia等[9]采用密度泛函理论(DFT)计算铜氯盐水溶液中的理论团簇结构以及电子吸收光谱,并对溶液中可能存在的团簇结构的接触离子对和共享离子对进行考虑,通过相应热力学参数分析溶液中的团簇。在光谱方面,为了得到氯化铜溶液的结构信息,Khan等[10]应用电子光谱,得出溶液中可能存在的团簇及其稳定性。杨丹等[11]分别研究氯化铜体系和氯化铁体系络合物的拉曼光谱,通过对特征峰的积分面积和浓度之间的关系进行研究,虽然实现了氯化铜溶液在络合物角度的定量分析,但却缺乏对实验光谱的理论分析。
本文采用理论计算和实验光谱研究氯化铜溶液中短程离子间的相互作用,对溶液中可能存在的微观结构进行优化和热力学常数及动力学过程计算,并计算其理论拉曼光谱。通过实验光谱与理论光谱进行对比,得出盐对水结构破坏的原因以及溶液中主要存在的团簇构型。
DFT是一种较为精确的量子化学计算方法,在预测材料性能、合成反应、吸附和溶剂化现象等方面具有广泛的应用[12~15]。本文在计算过程中只考虑溶液中第一溶剂化层的性质,采用DFT/B3LYP方法优化溶液中可能存在的团簇构型以及它们的过渡态,选用“6-31G (d, p)+LanL2TZ”混合基组,基组的设定使用关键词GENECP,其中Cl、H、O元素选取6-31G (d, p)基组,对Cu2+采用LanL2TZ赝势基组,以减少对金属优化的计算量。对过渡态构型进行频率计算,确认所得结构是否为势能面上的极小值或一阶鞍点,计算过程中考虑溶剂效应,并通过内禀反应坐标(IRC)计算进一步验证了过渡态的连接性。
氯化铜(分析纯,国药集团化学试剂有限公司)、使用前未作进一步纯化,实验用水为去离子水。分别配置0.0、0.5、1.0、1.5、2.0、2.5、3.0 mol·L-1氯化铜溶液进行拉曼光谱分析。实验采用Evolution型显微共焦激光拉曼光谱仪(法国HORIBA集团Jobin-Yvon公司),激发光波长为633nm。
水是极性很强的分子,使得水分子间容易形成氢键而缔合形成团簇分子[16]。为了得到氯化铜溶液中团簇的主要存在形式,分别对团簇(H2O)n、[CuClm]2-m、[CuClm(H2O)n]2-m、[Cl (H2O)n]-、[Cu (H2O)n]2+的构型进行计算,优化的部分低能量结构见图 1,并在标准状态下得到团簇的热力学常数和键参数,见表 1和表 2。
表 1
Table 1
表 1(Table 1)
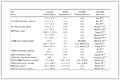
表 1 标准状态下[(H2O)n](n=2~8)的键参数和热力学常数
Table 1 Bond parameters and thermodynamic equilibrium constants of [(H2O)n] (n=2~8) under the standard condition
|
O-H
/pm |
Δ
E
/(kJ·mol-1) |
Δ
H
/(kJ·mol-1) |
Δ
G
/(kJ·mol-1) |
| (H2O)2 |
96.9 |
-22.0 |
-24.5 |
-3.3 |
| (H2O)3 |
98.4 |
-62.0 |
-64.5 |
-18.0 |
| (H2O)4 |
99.3 |
-55.7 |
-58.1 |
-19.6 |
| (H2O)5 |
99.2 |
-47.2 |
-49.6 |
-4.6 |
| (H2O)6 |
99.5 |
-43.9 |
-46.4 |
-3.1 |
| (H2O)7 |
98.7 |
-45.3 |
-47.8 |
-14.5 |
| (H2O)8 |
97.2 |
-40.3 |
-42.8 |
-54.9 |
|
表 1 标准状态下[(H2O)n](n=2~8)的键参数和热力学常数
Table 1 Bond parameters and thermodynamic equilibrium constants of [(H2O)n] (n=2~8) under the standard condition
|
表 2
Table 2
表 2(Table 2)

表 2 氯化铜溶液不同配位构型键参数和吉布斯自由能变
Table 2 Bond parameters and Gibbs free energy of different configurations
|
Cu-Cl
/pm |
Cu-O
/pm |
O-H
/pm |
Δ
G
/(kJ·mol-1) |
| [CuCl]+ |
214.4 |
|
|
-1796.9 |
| [CuCl2] |
209.9 |
|
|
-854.7 |
| [CuCl3]- |
223.7 |
|
|
-265.2 |
| [CuCl4]2- |
236.5 |
|
|
215.0 |
| [CuCl5]3- |
273.7 |
|
|
738.2 |
| [CuCl (H2O)]+ |
209.3 |
188.8 |
97.1 |
-204.3 |
| [CuCl (H2O)2]+ |
210.1 |
197.1 |
96.9 |
-118.6 |
| [CuCl (H2O)3]+ |
220.0 |
199.6 |
96.8 |
-82.3 |
| [CuCl (H2O)4]+ |
223.1 |
203.2 |
96.8 |
-45.6 |
| [CuCl (H2O)5]+ |
225.0 |
202.8 |
97.3 |
-51.9 |
| [CuCl (H2O)6]+ |
224.9 |
206.4 |
97.5 |
-28.7 |
| [CuCl2(H2O)] |
212.9 |
198.9 |
96.4 |
-44.9 |
| [CuCl2(H2O)2] |
225.2 |
201.5 |
96.9 |
-56.4 |
| [CuCl2(H2O)3] |
228.3 |
203.9 |
97.2 |
-22.7 |
| [CuCl2(H2O)4] |
229.9 |
198.9 |
97.0 |
-26.9 |
| [CuCl2(H2O)5] |
232.5 |
207.5 |
97.2 |
-10.1 |
| [CuCl2(H2O)6] |
232.4 |
200.7 |
97.0 |
-19.8 |
| [CuCl3(H2O)]- |
233.2 |
214.5 |
97.6 |
-0.6 |
| [CuCl3(H2O)2]- |
221.6 |
209.5 |
96.9 |
-16.2 |
| [CuCl3(H2O)3]- |
230.4 |
207.5 |
97.2 |
-3.7 |
| [CuCl3(H2O)4]- |
234.0 |
200.2 |
97.5 |
-28.9 |
| [CuCl3(H2O)5]- |
237.3 |
199.6 |
97.3 |
-47.8 |
| [CuCl3(H2O)6]- |
234.6 |
204.6 |
97.9 |
-1.4 |
| [Cl (H2O)]- |
|
|
96.5 |
-46.3 |
| [Cl (H2O)2]- |
|
|
97.1 |
-37.2 |
| [Cl (H2O)3]- |
|
|
98.0 |
-39.1 |
| [Cl (H2O)4]- |
|
|
98.5 |
-8.4 |
| [Cl (H2O)5]- |
|
|
97.7 |
-32.2 |
| [Cl (H2O)6]- |
|
|
98.6 |
-7.8 |
| [Cu (H2O)]2+ |
|
190.8 |
99.8 |
-493.8 |
| [Cu (H2O)2]2+ |
|
186.1 |
98.6 |
-348.6 |
| [Cu (H2O)3]2+ |
|
191.6 |
97.5 |
-253.1 |
| [Cu (H2O)4]2+ |
|
194.1 |
97.1 |
-167.6 |
| [Cu (H2O)5]2+ |
|
197.9 |
97.0 |
-99.1 |
| [Cu (H2O)6]2+ |
|
201.5 |
96.8 |
-67.6 |
|
表 2 氯化铜溶液不同配位构型键参数和吉布斯自由能变
Table 2 Bond parameters and Gibbs free energy of different configurations
|
氯化铜溶液中团簇结构形成包括如下反应过程:
|
$
\begin{array}{*{20}{c}}
{{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_{n- 1}} + {{\rm{H}}_2}{\rm{O}} \to {{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_n}}\\
{{{\left[{{\rm{CuC}}{{\rm{L}}_{m-1}}} \right]}^{3 - m}} + {\rm{C}}{{\rm{l}}^ - } \to {{\left[{{\rm{CuC}}{{\rm{L}}_{\rm{m}}}} \right]}^{2 - m}}}\\
{{{\left[{{\rm{CuC}}{{\rm{L}}_{\rm{m}}}{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_{n-1}}} \right]}^{2 - m}} + {{\rm{H}}_2}{\rm{O}} \to {{\left[{{\rm{CuC}}{{\rm{L}}_m}{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_n}} \right]}^{2 - m}}}\\
{{{\left[{{\rm{CL}}{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_{n-1}}} \right]}^ - } + {{\rm{H}}_2}{\rm{O}} \to {{\left[{{\rm{CL}}{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_n}} \right]}^ - }}\\
{{{\left[{{\rm{CL}}{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_{n-1}}} \right]}^{2{\rm{ + }}}}{\rm{ + }}{{\rm{H}}_2}{\rm{O}} \to {{\left[{{\rm{CL}}{{\left( {{{\rm{H}}_2}{\rm{O}}} \right)}_n}} \right]}^{2{\rm{ + }}}}}
\end{array}
$
|
|
从表 1可以看出,当n=2~8时,ΔE<0、ΔH<0、ΔG<0,表明各种水团簇都能够自发产生,与文献结果[17]一致,但其吉布斯自由能变在-60~0 kJ·mol-1之间,说明产生水分子微团簇的自发程度不大,当离子加入水溶液后,可能会与水分子中的氢键相互作用,导致原有的结构遭到破坏。
表 2结果显示O-H键长在96~98 pm之间变化,比表 1中水团簇O-H键长小,说明CuCl2的加入可能破坏了原有水分子之间的团簇结构。对于团簇[CuClm]2-m,当m=1~3时ΔG<0;m=4,5时ΔG>0,说明前三种结构是能够自发产生的,[CuCl4]2-、[CuCl5]3-两种结构在理论上是不能存在的。从Cu-Cl键长也可以看出,随着氯原子数的增加,键长逐渐变长,键长越长,结构的稳定性越差。对比团簇[CuClm(H2O)n]2-m、[Cl (H2O)n]-中O-H键长的微小变化,可见Cl-对O-H键长的影响比Cu2+及Cl-共同作用时的稍大,这是由于在溶液中Cl-和O-H中的O2-互相排斥,而Cu2+、Cl-以及O-H存在下时,O-H中氧的电子云会偏向Cu2+使得这种短程离子间的相互作用减弱。
此外,[CuClm(H2O)n]2-m、[Cl (H2O)n]-(m=1~3,n=1~6)等团簇的吉布斯自由能变虽然为负值,但大多数的ΔG为-50~0 kJ·mol-1,可知除了[CuCl (H2O)]+、[CuCl (H2O)2]+、[CuCl (H2O)3]+自发程度比较高外,其他构型都可以忽略。因此,虽然Cl-对O-H的影响较大,但是由于产生团簇的自发程度不高,可以认为溶液中大多数Cl-都处于游离状态,通过静电相互作用影响水团簇中的氢键。对团簇[Cu (H2O)n]2+(n=1~6)构型优化得到势能面最低点的结果表明,当n=1~6,[Cu (H2O)n]2+结构都可以自发产生,随着溶剂化数目的增加,自发程度降低,平衡常数逐渐减小,得到团簇的数目逐渐减少,团簇[Cu (H2O)]2+含量最多,团簇[Cu (H2O)6]2+含量最少。
为了进一步验证溶液中微团簇的主要存在形式,对团簇[Cu (H2O)n]2+(n=2~6)形成过程的动力学进行分析。分别寻找各团簇形成过程中的过渡态,同时进行频率计算,结果只有一个虚频,并以过渡态为中心计算反应路径,图 2为团簇[Cu (H2O)5]2+形成过程的反应路径图,各能量及势垒值见表 3,其中ER为反应物能量之和,即ER=ECu2++nEH2O(n=2~6),E为水合团簇的能量,ER0为反应物零点能之和,ER0=E0, Cu2++nE0, H2O,ETS0为过渡态的零点能,ΔE0=ETS0-ER0为反应物与过度态之间的势垒。
表 3
Table 3
表 3(Table 3)

表 3 团簇[Cu (H2O)n]2+(n=2~6)形成过程中相关能量参数
Table 3 Energy parameters of [Cu (H2O)n]2+ (n=2~6) in the formation process
|
n
|
ER
/(105kJ·mol-1) |
E
/(105kJ·mol-1)
|
ER0
/kJ·mol-1
|
ETS0
/kJ·mol-1
|
Δ
E0
/kJ·mol-1 |
| 2 |
-9.1345 |
-9.1437 |
112.2827 |
131.5680 |
19.2853 |
| 3 |
-11.1408 |
-11.1530 |
168.4241 |
195.4169 |
26.9928 |
| 4 |
-13.1472 |
-13.1653 |
224.5655 |
262.7092 |
38.1437 |
| 5 |
-15.1536 |
-15.1693 |
280.7069 |
326.1916 |
45.4847 |
| 6 |
-17.1599 |
-17.1768 |
336.8482 |
390.5917 |
53.7435 |
|
表 3 团簇[Cu (H2O)n]2+(n=2~6)形成过程中相关能量参数
Table 3 Energy parameters of [Cu (H2O)n]2+ (n=2~6) in the formation process
|
由表 3可以看出,Cu2+与H2O形成的团簇的能量比二者单独存在时的能量之和低,符合能量最低原理,能量越低越稳定。优化过渡态的结果显示,过渡态的零点能比反应物的零点能大,说明Cu2+与H2O络合成团簇[Cu (H2O)n]2+需要在分子碰撞中跨越势垒经历过渡态才能形成稳定的结构,当稳定构型[Cu (H2O)n-1]2+与一个水分子发生碰撞时,可能回到原来构型也可能再与水分子结合变成构型[Cu (H2O)n]2+,反应是否进一步进行取决于势垒的大小,势垒越大,反应越难进行。n=2~6,随着水分子数目的增加,势垒逐渐变大,这与表 2中ΔG的变化一致,说明随着溶剂化数目的增加,在动力学和热力学上自发程度都逐渐降低。但这些团簇的形成过程中的能量势垒都不是很大,表明形成过程是自发的。
为研究溶液中团簇的存在形式,在上述分析的基础上,对优化好的低能结构执行Freq=Raman命令进行拉曼光谱计算,得出理论拉曼峰的振动方式,图 3为CuO、部分低能团簇以及H2O的理论拉曼光谱。结果表明在100~500 cm-1之间主要为Cu-Cl、Cu-O两种振动方式,考虑到[CuClm]2-m可以再和水结合成[CuCl (H2O)]+、[CuCl (H2O)2]+、[CuCl (H2O)3]+等结构,因此在100~500 cm-1之间主要为Cu-O的振动方式,在3400~4000 cm-1范围内为O-H的对称和不对称伸缩振动。
团簇[Cu (H2O)n]2+(n=1~6)波数为3400~4000 cm-1的振动形式及拉曼位移如表 4所示,包括羟基的对称伸缩振动(νs)和不对称伸缩振动(νas)。从表 4中可以看出,O-H νs的拉曼位移比νas小,且随着溶剂化程度的增加,拉曼位移逐渐向更高波数移动。
表 4
Table 4
表 4(Table 4)

表 4 团簇[Cu (H2O)n]2+(n=1~6)在3400~4000 cm-1的振动方式
Table 4 Vibration modes of [Cu (H2O)n]2+(n=1~6) at 3400~4000 cm-1
|
[Cu (H2O)]2+ |
[Cu (H2O)2]2+ |
[Cu (H2O)3]2+ |
[Cu (H2O)4]2+ |
[Cu (H2O)5]2+ |
[Cu (H2O)6]2+ |
|
νs/cm-1 |
3404 |
3581 |
3675、3707 |
3753 |
3765 |
3768 |
|
νas/cm-1 |
3473 |
3641 |
3750、3790 |
3841 |
3858 |
3862 |
|
表 4 团簇[Cu (H2O)n]2+(n=1~6)在3400~4000 cm-1的振动方式
Table 4 Vibration modes of [Cu (H2O)n]2+(n=1~6) at 3400~4000 cm-1
|
通常情况下,水分子中通过氢键相连的O-H伸缩振动峰位于低波数区域,不带氢键的O-H伸缩振动位于高波数区域[14]。本文只考虑溶液中第一溶剂化层的性质,因此,下面将针对CuCl2的加入对水溶液的影响进行考察。
图 4从下到上分别为纯水和0.5、1.0、1.5、2.0、2.5、3.0 mol·L-1氯化铜溶液在150~1000 cm-1的拉曼光谱图,从中可以看出,氯化铜溶液与纯水相比,在200~340 cm-1出现明显新峰,且随着溶液浓度增加,新峰的强度逐渐增加。由上述理论拉曼光谱可知,新峰的产生主要为Cu-O的振动引起的,表明,当水中加入CuCl2时,会发生短程离子间的相互作用而产生新的团簇。
图 5中2500~4000 cm-1拉曼光谱峰主要为O-H伸缩振动引起的。随着溶液浓度的增加,峰的强度逐渐减小,峰形有明显变化。说明溶液浓度不同,CuCl2对水的结构影响不同,溶剂化产生的团簇结构及含量不同,导致溶液极化率发生改变。
为了深入了解溶液浓度对溶剂化作用的影响,对图 5中的拉曼光谱进行了高斯分解。考虑到理论拉曼光谱图中,随着溶剂化数目的增加,O-H伸缩振动峰逐渐向更高波数移动,溶剂化数目小的团簇O-H伸缩振动峰在低波数位置,分别在3200cm-1和3400cm-1处对其拟合与计算,见表 5。其中A1、A2分别为较低波数和较高波数的峰面积,A1/A2为两峰面积的比值。从表中可以看出,随着溶液浓度增加,面积比逐渐增加,表明浓度增加产生小团簇的数目增加,大团簇的数目减少,即溶剂化数目随浓度的增加而减小。
表 5
Table 5
表 5(Table 5)

表 5 2500~4000 cm-1范围内拉曼光谱高斯分解图相关参数
Table 5 Parameters of Gaussian deconvolution at 2500~4000 cm-1
| 浓度/mol·L-1 |
A1
|
A2 |
A1/A2 |
| 0.0 |
333476.6 |
743123.5 |
0.4488 |
| 0.5 |
312891.2 |
642866.6 |
0.4867 |
| 1.0 |
406452.6 |
541628.5 |
0.7504 |
| 1.5 |
360517.6 |
499126.1 |
0.7230 |
| 2.0 |
373205.5 |
440619.9 |
0.8470 |
| 2.5 |
292350.0 |
277709.3 |
1.0527 |
| 3.0 |
265049.2 |
169033.0 |
1.5680 |
|
表 5 2500~4000 cm-1范围内拉曼光谱高斯分解图相关参数
Table 5 Parameters of Gaussian deconvolution at 2500~4000 cm-1
|
对氯化铜溶液中可能存在的团簇构型优化结果进行热力学和各团簇形成过程寻找过渡态的分析,发现溶液中存在的主要团簇结构为[CuClm]2-m (m=1~3)、[CuCl (H2O)n]- (n=1~3)、[Cu (H2O)n]2+ (n=1~6)。
理论拉曼光谱在100~500 cm-1主要为Cu-O的伸缩振动峰,在3400~4000 cm-1范围内为O-H伸缩振动峰,实验光谱在200~340 cm-1出现明显新峰,在误差允许范围内,理论计算与实验光谱一致。拉曼光谱实验得出溶液浓度可以改变拉曼峰的强度,对拉曼光谱进行高分峰发现,随着溶液浓度增加,溶剂化数目减小。
致谢:
作者非常感谢日本福冈大学理学院Toshio Yamaguchi教授在实验和计算过程中给予我们的建议和帮助。
 2016,
Vol. 79
2016,
Vol. 79 Issue (8): 754-759
Issue (8): 754-759 2016,
Vol. 79
2016,
Vol. 79 Issue (8): 754-759
Issue (8): 754-759