齐齐哈尔大学化学与化学工程学院 齐齐哈尔 161006
2015-11-10 收稿, 2016-03-18 接受
基金项目: 黑龙江省自然科学基金项目(B201218)齐齐哈尔大学研究生创新科研项目(YJSCX2015-017X)资助
作者简介:
李英杰, 男, 54岁, 硕士生导师, 主要从事电色谱分析
College of Chemistry and Chemical Engineering, Qiqihar University, Qiqihar 161006
β-环糊精(β-CD)[1]具有独特的疏水内腔和亲水外壳,内腔能与多种疏水化合物通过偶极-偶极作用形成包结化合物,空腔两侧边缘的羟基能进行化学修饰增强其对特定分析物的分离能力和选择性,因此,β-CD及其衍生物被广泛应用于分离领域[2]。近年来,改性环糊精电色谱整体柱成为研究热点,其优点在于制备方法简单、柱效高、柱子牢固稳定,并且环糊精及其衍生物作为固定相具有分离效率高、分析速度快、检测灵敏度高和应用范围广泛等特点,特别适合于高沸点、大分子、强极性和热稳定性差的化合物的分离分析[3]。顺丁烯二酸酐-β-环糊精(MAH-β-CD)拥有β-CD的手性拆分能力,同时因其带有双键与甲基丙烯酸缩水甘油酯(GMA)、二甲基丙烯酸乙二醇酯(EDMA)共同作为功能单体,可简化整体柱制备过程,其中功能单体之间的协同作用也增大了固定相的手性拆分能力。
毛细管电色谱-质谱联用技术(CEC-MS)综合了CEC的高效快速、高分离能力与MS的高灵敏度与较强的定性能力,在一次分析中可以同时得到样品离子的迁移时间、分子量和碎片等信息,已受到研究人员的关注[4, 5]。由于这两种方法能够很好的互补,它们的联用可以用于定性分析重叠峰甚至没有被完全分离的混合物,并且具有较高的灵敏度。
手性药物的两个对映体虽然物理、化学和热力学性质极其相似,但是其生物活性、毒性及药理作用常有不同。如果忽视了对映体间药理活性的差异,会造成严重的后果[6]。深入研究与探索手性拆分技术无论在医疗方面还是科研角度都具有重大意义[7]。沙丁胺醇(Salbutamol,SAL)的结构式如图式1所示,为选择性β2-受体激动剂,能选择性激动支气管平滑肌的β2-受体,有较强的支气管扩张作用,用于防治支气管哮喘、哮喘型支气管炎和肺气肿患者的支气管痉挛。目前,SAL仍主要以外消旋体形式给药。然而有研究表明,对于这类β2受体兴奋药物,其不同的对映体药效可能不同[8]。因此,进行对映体分离对于进一步研究其药理具有重要意义。本文制备了MAH-β-CD新型毛细管电色谱手性整体柱,并利用毛细管电色谱法对该手性药物对映体进行拆分,为其对映体的研究提供了一种快速、有效的分离分析方法。
毛细管电泳-飞行时间质谱联用仪(7100 CE-6230 TOF MS,美国安捷伦公司);扫描电子显微镜(S-4300,日本日立公司);傅里叶变换红外光谱仪(Nicolet 380,美国热电公司);石英毛细管(75 μm i.d.,365 μm o.d.,中国锐丰色谱器材公司)。
甲基丙烯酸三甲基硅烷丙酯(γ-MAPS)、EDMA、GMA (上海阿拉丁试剂公司);偶氮二异丁腈(AIBN)和2-丙烯酰胺基-2-甲基-1-丙磺酸(AMPS)(美国Flake公司);N,N-二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)(分析纯,天津科密欧试剂公司);DL-精氨酸(北京化学试剂有限公司产品,生化试剂);SAL购自中国药品生物制品检定所,国药标准品。其他试剂均为市售分析纯级,实验用水均为超纯水。
称取5.0g顺丁烯二酸酐溶于30mL DMF中,常温搅拌下加入5.6g β-CD。80℃恒温水浴中反应10h。反应结束后,产物冷却至室温,用30mL氯仿沉淀出产物。丙酮充分洗涤,抽干,80℃真空干燥24h,备用。
将毛细管依次用1 mol/L NaOH、超纯水、1mol/L HCl、超纯水、甲醇冲洗,N2吹干,备用。将硅烷化试剂(γ-MAPS:丙酮=1:1)注入毛细管中,硅胶塞封口。室温放置24h后,甲醇冲洗,用N2吹干,待用。称量0.15g GMA、0.10g EDMA、0.10g环己醇、0.24g正十二醇、0.0018g AIBN、0.0016g AMPS和0.10g MAH-β-CD配制成0.2g/mL的DMSO溶液,超声混匀。将混合物填充入上述预处理的毛细管中,填料部分26.0cm。两端封口,40℃水浴反应12h后依次用甲醇和超纯水冲洗。
电色谱条件:自制MAH-β-CD电色谱整体柱;缓冲溶液:20mmol/L NH4Ac (pH=8.50);毛细管温度:20℃;工作电压:25kV;5kPa压力进样5s;紫外检测波长:200nm。
质谱条件:离子源:dual ESI;干燥气温度:300℃;干燥气流速:8L/min;全扫描范围:20~300 m/z;鞘流液组成:5mmol/L NH4Ac-50%CH3OH;流速:0.5mL/min。
为了确定是否对β-CD改性成功,采用红外光谱进行分析,其结果如图 1。曲线(a)中3400cm-1处为-OH的伸缩振动吸收峰;2927cm-1处为-CH2的反对称伸缩振动吸收峰;1640、1416 cm-1处为C-H面外变形振动和-CH2变形振动;1028cm-1处为C-O-C的伸缩振动和β-CD内腔C-O伸缩振动的吸收峰。曲线(b)与(a)相比,保持了β-CD的特征吸收,又出现了1638cm-1的C=C键的伸缩振动吸收峰及1725cm-1的C=O伸缩振动吸收峰,表明存在C=C键及羰基,从而可以初步确定衍生物为MAH-β-CD。
为进一步验证合成产物为MAH-β-CD,采用ESI -TOF/MS,正离子全扫描方式对合成产物进行质谱分析,其结果如图 2。图中m/z 1233.41856的离子峰对应MAH-β-CD的[M+H]+峰,当其失去质量数为18(H2O)的碎片后产生m/z 1214.7529的碎片峰;m/z 1255.35456与m/z 1271.32933分别为[M+Na]+峰与[M+K]+峰。从而可以确定合成的环糊精衍生物为MAH-β-CD。
一步键合法制备的整体柱的分离能力及使用寿命受多种因素影响。单体比例在固定相中起关键性作用,在当GMA与EDMA的质量比为3:2,MAH-β-CD功能单体溶液的浓度为0.2g/mL时,所制备的毛细管整体柱的电渗流和通透性较为理想[10],且具有良好的分离选择性,柱效达到99856 plates/m。根据原位聚合机理,反应温度主要影响聚合反应过程中引发剂的分解速度,进而影响固定相的孔径分布,温度越高分解速度越快,孔径也越致密,温度稍低时,无法诱导引发剂发生反应,所以本实验最终确定反应温度为40℃。最后考察了反应时间对制柱的影响,反应时间不足会导致环糊精衍生物的结合量不足,整体柱性能受到很大影响;而反应时间过长易引起聚合物官能团遭到破坏,整体柱使用寿命大幅降低。经试验对比聚合10、11、12和13h时整体柱的性能,确定12h的聚合情况最佳。
为了更好观察整体柱固定相结构,通过扫描电镜对优化条件下制备的电色谱整体柱内部结构进行表征。从图 3可以看出,聚合物成功键合到毛细管内壁上,并且在柱内形成了致密的网状结构,其形态错综复杂,由此可以推测该柱有较强的机械强度,能承受较大的压力,且整体柱内孔隙均匀,有较大的孔径,说明该柱具有良好的通透性。
在优化的制柱条件下制备3根电色谱整体柱,以硫脲为中性标记物,对所制备整体柱柱效进行评价,其结果见表 1。3根柱子平均柱效均达到95000 plates/m以上,并且单根柱子柱效的相对标准偏差(RSD)分别为0.012%、0.022%、0.018%,说明该方法制备的整体柱具有良好重现性。
表 1
Table 1
表 1(Table 1)
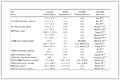
表 1 整体柱重复性实验
Table 1 Repeatability experiments of monolithic column
| 序号 |
柱效
/(plates/m) |
平均柱效
/(plates/m) |
柱效
(RSD) |
|
99856 |
|
|
| 柱1 |
99784 |
99798 |
0.012% |
|
99755 |
|
96452 |
| 柱2 |
96539 |
96446 |
0.022% |
|
96347 |
|
97583 |
| 柱3 |
97482 |
97509 |
0.018% |
|
97461 |
|
|
|
表 1 整体柱重复性实验
Table 1 Repeatability experiments of monolithic column
|
以DL-精氨酸为手性分离物,在25kV的工作电压下用20mmol/L NH4Ac (pH=8.50)作为缓冲溶液进行连续5次分离。其结果见表 2,精氨酸的单一对映体保留时间(ta,tb)的RSD分别为0.77%、1.05%。整体柱有良好的分离能力,分离度均达到2.5以上。该柱可连续使用14h,间歇性使用2个月以上仍具有良好的手性分离性能,可见该柱具有良好的稳定性。
表 2
Table 2
表 2(Table 2)

表 2 整体柱分离性能实验
Table 2 Separating property of monolithic column
| 样品 |
ta/min |
RSD (ta) |
tb/min |
RSD (tb) |
Rs
|
RSD (Rs) |
|
1.093 |
|
2.193 |
|
2.75 |
|
|
1.078 |
|
2.196 |
|
2.80 |
| 精氨酸 |
1.069 |
0.77% |
2.193 |
1.05% |
2.81 |
0.79% |
|
1.084 |
|
2.187 |
|
2.76 |
|
1.066 |
|
2.180 |
|
2.79 |
|
|
表 2 整体柱分离性能实验
Table 2 Separating property of monolithic column
|
为考察所制备电色谱整体柱的实际应用价值,利用该整体柱对SAL (C13H21NO3)对映体进行分离。本实验采用1.3节所述CEC分离条件和MS检测条件,成功分离了SAL对映体。图 4为SAL的电色谱分离图,对映体在19 min内达到基线分离,分离度为1.67,该柱手性拆分能力明显高于液相色谱柱,分离度与电泳法相近,并且结合MS检测器定性分析更加准确[11, 12]。但是,通过该柱分离得到的电色谱峰展宽及拖尾问题还需改进。
图 5为SAL对映体的质谱总离子流图(TIC),TIC中每个组分的提取质谱图见图 6。图 6(a)为保留时间39.237min对映体(a)的提取质谱图,其中m/z 240.1593的离子峰对应SAL的[M+H]+峰,当其失去质量数为18(H2O)和74([NH3+C (CH3)3])的碎片后分别产生m/z 222.1274和166.0861的质谱峰、同时失去两碎片时产生m/z 148.1091的质谱峰,当[M+H]+失去质量数为86([CH2NHC (CH3)3])的碎片后产生了m/z 154.1426的质谱峰,质量数为99的质谱峰为[CH2CH2NHC (CH3)3]碎片。图 6(b)为保留时间40.012min对映体(b)的提取质谱图,同理,m/z 240.1592的离子峰对应SAL的[M+H]+峰,m/z 222.1485、166.0859、154.1217、148.0755、98.9771分别对应SAL的相应碎片峰,因此可以判断图 5中的(a),(b)为SAL的对映体峰。
本实验采用一步键合法制备了MAH-β-CD毛细管电色谱整体柱,整体柱内部具有均匀网状结构,通透性及机械强度良好。通过精氨酸对映体对柱子手性分离性能进行评价,该柱的手性分离能力、稳定性及重现性较好。通过CEC-MS分析,利用毛细管电色谱法拆分了沙丁胺醇对映体,分离度达到1.67。
 2016,
Vol. 79
2016,
Vol. 79 Issue (8): 749-753
Issue (8): 749-753 2016,
Vol. 79
2016,
Vol. 79 Issue (8): 749-753
Issue (8): 749-753