 图式 1
探针4识别Al3+的机理[10]
Scheme1.
Proposed mechanisms for detection of Al3+ with 4[10]
图式 1
探针4识别Al3+的机理[10]
Scheme1.
Proposed mechanisms for detection of Al3+ with 4[10]

Citation: Zhong Keli, Wang Yutong, Yu Qixuan, Tang Yiwei, Hou Shuhua, Bian Yanjiang, Tang Lijun. Progress in Fluorescence Probes Based on 4-(N, N-Diethylamino) salicylaldehyde Schiff Base[J]. Chemistry, 2018, 81(1): 37-44.

基于4-N, N-二乙氨基)水杨醛席夫碱类荧光探针的研究进展
-
关键词:
- 4-(N, N-二乙氨基)水杨醛
- / 席夫碱
- / 荧光探针
- / 识别
English
Progress in Fluorescence Probes Based on 4-(N, N-Diethylamino) salicylaldehyde Schiff Base
-
Key words:
- 4-(N, N-Diethylamino)salicylaldehyde
- / Schiff base
- / Fluorescent probe
- / Recognition
-
4-(N, N-二乙氨基)水杨醛是由一个平面的二乙基氨基官能团通过sp2杂化N原子连接到一个近平面的水杨醛4位上形成的化合物[1]。它是染料及有机合成的重要中间体,也是具有亲水性质的生色团,其醛基常被用来制备席夫碱进而开发新颖的探针分子[2]。席夫碱主要是指含有亚胺或甲亚胺特性基团(—RC=N—)的一类有机化合物,通常是由胺和活性羰基缩合而成。席夫碱类化合物及其金属配合物在医学、催化、分析化学、光致变色等领域有着重要应用[3, 4]。例如缩氨脲类、杂环类席夫碱具有抑菌、杀菌、抗病毒等独特药用效果[5]。此外,席夫碱合成简单,其良好的光电特性及较强的金属离子螯合能力,使其常被用做荧光探针进行金属离子识别[6]。本文主要介绍了基于4-(N, N-二乙氨基)水杨醛席夫碱类荧光探针的合成,及其在几种常见阴阳离子荧光识别和检测中的应用。希望本文可以对此类荧光探针在环境、生物、食品中的实际检测和应用研究提供理论依据和实践基础。
1 荧光探针对阳离子的识别
1.1 荧光探针对Al3+的识别
2012年,Neeraj等[7]开发了在水溶液中识别Al3+、具有纳摩尔灵敏度、可渗透至活细胞中的荧光探针1(式(1))。通过结合N, N-二乙基氨基(DEA)基团作为精细调控单元,可在灵敏度、水溶性、识别机理等方面显著影响1的识别性能。由于扭曲分子内电荷转移(TICT),DEA基团导致1产生双通道发射。1的疏水性影响了Al3+在水介质中的水合作用,最终导致其对Al3+具有较高的选择性和灵敏度。
2013年,Wang等[8]用4-(N, N-二乙基氨基)水杨醛与6-氨基-7-羟基香豆素反应,制备了席夫碱化合物2(式(2)),其可在MeOH中通过荧光“关-开”选择性识别Al3+和Fe3+。Al3+和Fe3+分别可使2在最大发射波长488nm处的荧光强度增强7倍和4倍,其他金属离子对2的荧光没有明显影响。此外,他们还通过调控光异构化产物2′中分子内O-H…N=CH相互作用,可以实现荧光“关-开”快速光响应,分别使最大发射波长488和516 nm处的荧光强度增强130倍和65倍,而2′对金属离子没有识别作用。
2014年,Patil等[9]报道了一种基于苯并噻唑的可在活细胞中监测Al3+荧光探针3(式(3))。在CH3CN/H2O(1:1,体积比)溶液中,向探针3中加入0.5倍化学计量的Al3+时,荧光发射峰发生红移,其强度显著猝灭,表现出高灵敏度和高选择性荧光响应,并可实现裸眼检测。这种简单低成本的探针可快速检测浓度低至0.42μmol/L的Al3+,有望被用于高效的生物传感器的制备。
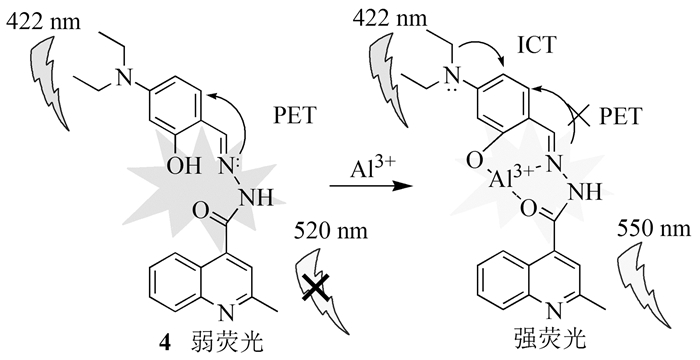
2014年,Qin等[10]合成了4-(N, N-二乙氨基)水杨醛-(2’-甲基喹啉-4-甲酰基)腙类荧光探针4,在向4的EtOH/H2O(4:1,体积比)溶液中加入Al3+时,其在550nm处荧光强度增强125倍,具有较好的选择性,最低检测限为6×10-7mol/L。他们通过光诱导电子转移(PET)和分子内电荷转移(ICT)过程解释了观察到的光谱响应(如图式 1)。良好的水溶性和较低的检测限使该探针可以在生物体系及环境中实现对Al3+的检测。
2014年,Cheng等[11]系统研究了利用Salen型席夫碱与K+、Ca2+、Zn2+、Cu2+和Pt2+制备Salen络合物,通过金属置换反应来检测Al3+,这些简单新颖的探针(式(4))具有高选择性、高灵敏性、光学显色(比色和荧光)等特点。Salen配体的化学结构和中心金属离子对识别性能有很大影响,主要由复合物的稳定常数决定。此外,基于Salen络合物的荧光探针选择性比相应游离Salen配体的选择性好得多,这是因为复合物中填充的金属离子具有屏蔽作用。该研究利用金属置换来达到检测,为光学探针的设计提供了一种新思路。
2015年,Liu等[12]利用4-(N, N-二乙氨基)水杨醛和碳酰肼反应,合成了结构简单的化合物6,在超声条件下获得了β-环糊精与6的主-客体体系(式(5)),具有优异的水溶性。荧光光谱研究表明,在纯水中β-CD-6与Al3+配位产生强的蓝色荧光,具有较高的结合常数(k=3.16×1011L·mol-1)。此外,洋葱表皮细胞与β-CD-6-Al3+的荧光显微镜图表明,水溶性主客体体系具有很高的细胞通透能力。
2016年,Hwang等[13]通过一步反应合成了2-氨基苯甲酸席夫碱类化合物7(式(6)),该探针可在MeOH/H2O(1:1,体积比)溶液以及活细胞中对Al3+荧光增强识别,检测限为290nmol/L,结合常数为3.1×108L·mol-1,这是简单席夫碱类化合物在水溶液中对Al3+的最高结合力之一。计算结果表明,荧光增强是由于与Al3+结合抑制了探针7的C=N异构化以及激活了螯合荧光增强(CHEF)共同导致的。
1.2 荧光探针对Cu2+的识别
2012年,吴海强等[14]以若丹明6G酰肼与4-(N, N-二乙氨基)水杨醛反应制备了荧光探针8。紫外-可见吸收和荧光光谱研究表明,该探针在MeCN/H2O(3:7,体积比)溶液中对Cu2+显示出高选择性。随着Cu2+加入,探针8的螺环被打开,溶液由无色变为红色,而荧光发生猝灭。该探针的响应过程迅速且可逆,有望用于水介质中Cu2+的快速检测。
2012年,Gao等[15]合成了具有双检测通道的N’1,N’2-双(4-(N, N-二乙基氨基)-2-羟基亚苄基)草酰肼化合物9(式(7))。探针9的吸收和发射光谱都对Cu2+敏感,且具有较高的检测灵敏度及优异的选择性。此外,9在DMSO/H2O(8:2,体积比)溶液中对Cu2+响应非常快,可以在1min内完成,有望实现快速检测。
2012年,Narayanaswamy等[16]通过4-(N, N-二乙氨基)水杨醛与水合肼简单缩合,得到一种用于高选择性识别Cu2+的新型比色荧光探针10(式(8))。在CH3CN溶液中和Cu2+存在下,10在425nm处的吸收带位移到545nm,溶液从淡黄色变为紫色,且荧光强度发生猝灭。作者认为其识别机理是双重去质子化和扭曲的平面分子内电荷转移导致的。
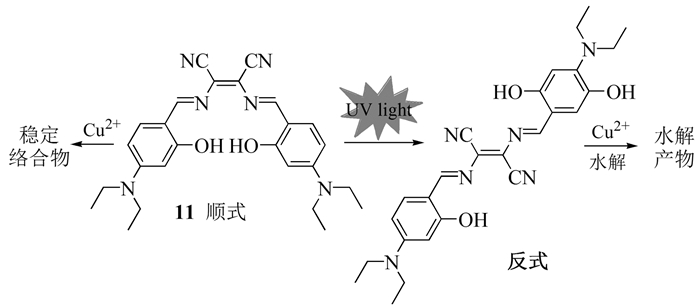
2013年,Cheng等[17]利用马来腈制备Salen配体,通过光诱导得到顺式和反式异构体,在CH3CN中分别通过形成稳定的络合物和Cu2+促进水解,对Cu2+表现出完全不同的响应和识别机制(如图式 2)。此外,该探针可通过顺反异构体的质子化、去质子化、水解三种不同机理实现对pH的比色和荧光传感。这种新颖的顺反异构化探针为光学探针的设计提供了新范例。
2013年,Ye等[18]通过5-二茂铁基-1, 3, 4-噻二唑-2-胺与4-(N, N-二乙基氨基)水杨醛反应,合成了新型探针12,该探针在EtOH/HEPES(9:1,体积比)溶液中可比色传感和高选择性荧光识别Cu2+,并可用于监测活体细胞中的Cu2+。此外,该探针可通过电化学方法检测Cu2+,这种多通道检测方式大大提高了该探针的应用价值。
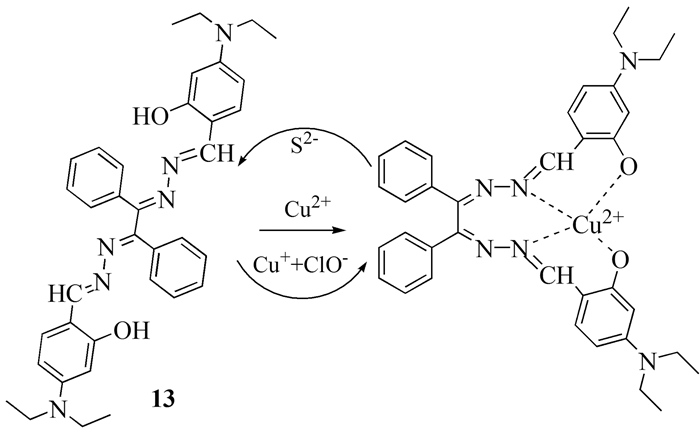
2013年,Xie等[19]制备了用于高选择性检测Cu2+的比色荧光探针13。在CH3CN/H2O(4:1,体积比)溶液中加入Cu2+后,其最大吸收谱带从398 nm红移至552nm(Δ=154nm),溶液从橙黄色变成紫色,而加入S2-后颜色又可恢复,进而实现肉眼检测Cu2+和接力识别S2-。此外,该探针与Cu+配位后,利用次氯酸盐的氧化性,也可以达到上述效果,而其他阴离子不能产生这种变化,从而可实现对ClO-的有效识别(如图式 3)。该研究为设计识别氧化物探针提供了新思路。
2014年,王建红等[20]合成了新型的基于香豆素的荧光探针14(式(10))。该探针在HEPES缓冲溶液中对Cu2+有较好的选择性和灵敏度,且当浓度在0.66~10 μmol/L范围内,探针14的荧光强度与Cu2+浓度有较好的线性关系。
2014年,Choi等[21]制备了4-(N, N-二乙氨基)水杨醛作为结合和信号传导单元的比色荧光探针15(式(11))。在探针15的DMSO/Bis-tris(1:1,体积比)溶液中加入Cu2+后,颜色从无色变为黄色,15对Cu2+的比色传感具有专一选择性,并且在pH 4~11范围内都可检测。此外,探针15的DMSO溶液中加入F-后,其荧光发射峰红移并增强,说明15还可检测氟化物。
2014年,Meng等[22]报道了一种基于7-硝基苯并-2-氧杂-1, 3-二唑(NBD)的新型荧光探针16。在HEPES缓冲液中,该探针可在其他竞争阳离子存在下特异性结合Cu2+,检测限为1.6nmol/L。原位产生的16-Cu2+络合物能够在其他阴离子和生物硫醇存在的情况下选择性识别S2-(式(12))。16和16-Cu2+显示较低的细胞毒性和较好的细胞膜通透性,能在活细胞中对Cu2+和S2-进行成像和定量检测。
2015年,Meng等[23]描述了一种基于1, 8-萘酰亚胺的低毒性和具有较好细胞膜通透性的探针17,在THF/H2O(3:7,体积比)溶液中,17表现出对Cu2+的特异性识别,并伴随92.2%的荧光猝灭。此外,组氨酸(His)可将配合物17-Cu2+解络合,释放出17使荧光恢复(式(13))。17-Cu2+的特异性荧光增强与His浓度呈良好的线性关系,检测限可达70nmol/L。细胞成像和计数分析表明,17-Cu2+主要分布在活细胞的溶酶体中,可用作His在亚细胞水平成像的荧光生物传感器。
1.3 荧光探针对Zn2+的识别
2013年,Kaur等[24]用4, 4’-二氨基联苯甲烷与4-(N, N-二乙氨基)水杨醛反应,合成了具有“开-关”多响应功能的荧光探针18(式(14))。在DMF/H2O(7:3,体积比)溶液中,该探针可通过激发态分子内质子转移(ESIPT)和电荷转移(CT)机理对Zn2+高灵敏度和高选择性识别。18-Zn2+复合物可通过阳离子置换法定量检测磷酸盐或有效检测ATP、ADP、AMP、NADP和NAD等磷酸化生物分子。
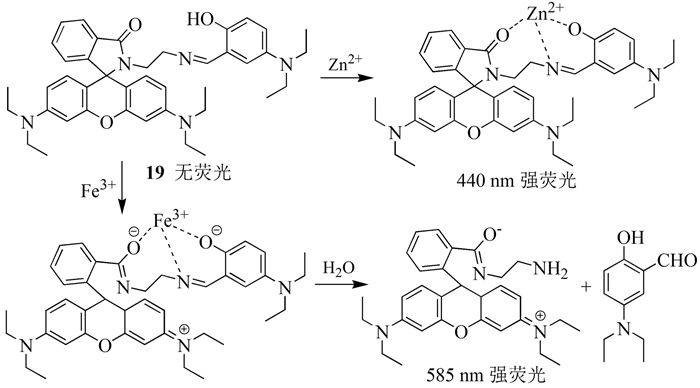
2013年,Luxami等[25]合成了一种新的若丹明类探针19。在19的MeOH/H2O(1:1,体积比)溶液中分别加入Zn2+和Fe3+时,Zn2+导致380nm处吸光度增加,440nm处荧光显著增强;而Fe3+导致555nm处吸光度增加,585nm处荧光增强。该探针可同时或分别定性、定量检测Zn2+和Fe3+(如图式 4),为开发多分析物荧光探针提供了有效参考。
2014年,Park等[26]制备出一种在DMSO/Bis-tris(6:4,体积比)中荧光“关-开”高灵敏识别Zn2+的新颖探针20(式(15))。该探针可重复使用无干扰,检测限可达68nmol/L,远低于世界卫生组织规定的76μmol/L。他们认为20与Zn2+结合后抑制了ESIPT和C=N异构化,并激活了CHEF导致荧光增强。
2015年,Liu等[27]合成了一种低毒性、高水溶性、基于β-环糊精的球形传感器21(式(16))。在纯水(pH=7.2)中,21可高选择性和高灵敏度识别Zn2+,结合常数为2.55×1013L·mol-1。洋葱表皮细胞的荧光照片表明21具有很高的细胞通透能力。他们认为螯合诱导荧光增强(CIFE)和PET导致了21识别Zn2+荧光增强。该探针为纯水中检测痕量Zn2+提供了有效参考。
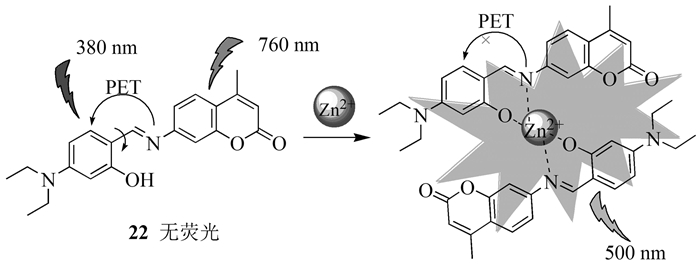
2016年,Qin等[28]设计和合成了一种单光子和双光子Zn2+荧光探针22。在DMF/H2O(9:1,体积比)溶液中,用380和760 nm波长激发22,只有Zn2+能引起500nm处荧光强度显著增强,具有高选择性。在形成的化学计量比为2:1的22-Zn络合物中,C=N异构化受限及PET被抑制导致了荧光增强(如图式 5)。此外,22识别Zn2+的过程是可逆的。
1.4 荧光探针对Co2+的识别
2016年,Lee等[29]通过缩合反应设计和合成了简单、易制备的比色荧光探针23(式(17))。在接近纯水溶液中,23与Co2+以化学计量比1:1结合,颜色由无色变成黄色,检测限为0.65μmol/L,与联邦状态毒物学和风险分析委员会(FSTRAC)规定的饮用水指标(0.68μmol/L)相当。23可制成二氧化硅板测试条,能定量检测实际水样中的Co2+,是现场和实时检测Co2+的良好选择。
1.5 荧光探针对Hg2+的识别
2015年,Li等[30]设计合成了基于若丹明的化合物24(式(18)),并结合上转换NaYF4纳米晶作为荧光探针的激发主体,在CH3CN/NaAc-HAc(1:1,体积比)体系中,上转换材料可以荧光“关-开”识别Hg2+,具有良好的选择性和线性响应。将传感器与激发宿主嵌入到固态基质中有助于分析物扩散和防止探针泄露。
2015年,Shen等[31]合成了两种若丹明衍生物25和26(式(18)),并用NaYF4纳米晶构建上转换激发主体,通过980nm激发上转换发射使探针被照亮,目的是使探针具有更好的光稳定性。通过光谱分析和比较发射衰减寿命,确认上转换宿主和探针之间有能量转移。两种探针在CH3CN/NaAc-HAc(1:1,体积比)中与Hg2+均是1:1络合,探针发射强度随Hg2+浓度增大而线性增加,且不受其他常见金属离子的影响,对Hg2+具有良好的选择性。
2015年,Mahaja等[32]报道了一种新颖的基于酞嗪-腙的荧光探针27(式(20)),在DMSO/H2O(8:2,体积比)溶液中,27对Hg2+ 550nm处荧光增强识别,具有高选择性和高灵敏性,检测限可达26.1nmol/L。此外,27可检测出人类宫颈癌HeLa细胞中的Hg2+,表明其有望在生物样品中得到实际应用。
2 荧光探针对阴离子的识别
2.1 荧光探针对F-的识别
2016年,Leng等[33]设计合成了含有两个亚胺基团的比色和荧光双通道氟化物荧光探针28(式(21))。这种结构简单的探针在DMSO中对氟化物比其他常见阴离子具有更快响应和高选择性,检测限为5.78×10-7mol/L。机理研究表明,28首先与F-通过氢键结合,然后在较高浓度时两个OH基团与F-经历去质子化过程。试纸条实验表明28可作为现场检测F-的方便有效的试剂盒。
2.2 荧光探针对CN-的识别
2014年,Lin等[34]合成了具有独特的激发态分子内电荷转移-激发态分子内质子转移(ESICT-ESIPT)偶联体系的新型荧光传感器29(式(22))。在THF/H2O(8:2,体积比)溶液中,29通过开关ESICT和ESIPT来高灵敏度特异性识别CN-。此外,基于29的试纸条成本低且易于制造,是一种有效实用的CN-测试试剂盒。
2016年,Hu等[35]设计并合成了一种基于异烟酰胺的高选择性比色和荧光识别氰化物的荧光探针30(式(23))。在30的DMSO/H2O(7:3,体积比)溶液中加入CN-后,552nm处的荧光增强了14倍,荧光颜色从浅黄色变成黄色,肉眼即可检测,方法检测限可达5.12×10-8mol/L。该探针还可构建INHIBIT分子逻辑门,可用作方便高效的CN-检测试剂盒来检测水溶液中和食品样品中的CN-。
3 结语
基于4-(N, N-二乙氨基)水杨醛席夫碱类的荧光探针对Al3+、Cu2+、Zn2+、Hg2+、Co2+等离子荧光识别和检测的报道较多,且大多数探针识别后荧光增强明显,颜色变化可直接用肉眼观察,并具有较高选择性和灵敏度,有一定的实用价值。不过,应用于阴离子检测的报道很少,这主要是由席夫碱的结构决定的。设计合成可在纯水介质中实现重要离子专一性识别或接力识别多种阴阳离子,并可应用于生命体系中的示踪与成像,将是该类探针研究的重点领域。
-
-
[1]
J Vančo, J Marek, O Švajlenová. Acta Crystallogr. E, 2005, 61(12):o4209~o4211. doi: 10.1107/S1600536805037323/full
-
[2]
S Jana, S Dalapati, N Guchhait. J. Phys. Chem. A, 2013, 117(21):4367~4376. doi: 10.1021/jp3120463
-
[3]
S Abdel-Latif, H Hassib, Y Issa. Spectrochim. Acta, Part A, 2007, 67(3):950~957.
-
[4]
曹义, 陆云.化学通报, 2017, 80(6):539~543. http://www.hxtb.org/ch/reader/view_abstract.aspx?flag=1&file_no=20161020003&journal_id=hxtb
-
[5]
王澈, 侯鹏, 李崧等.化学通报, 2009, 72(4):334~340. http://en.cnki.com.cn/Article_en/CJFDTOTAL-HXTB200904008.htm
-
[6]
X Yang, W Zhang, Z Yi et al. New J. Chem., 2017, 41(19):11079~11088. doi: 10.1039/C7NJ01186E
-
[7]
A Kumar, V Kumar, R Prajapati et al. Dalton Transac., 2014, 43(15):5831~5839. doi: 10.1039/C3DT53263A
-
[8]
L Wang, H Li, D Cao. Sens. Actuat., B, 2013, 181:749~755. doi: 10.1016/j.snb.2013.01.090
-
[9]
R Patil, A Moirangthem, R Butcher et al. Dalton Transac., 2014, 43(7):2895~2899. doi: 10.1039/C3DT52770K
-
[10]
J Qin, T Li, B Wang et al. Synth. Met., 2014, 195:141~146. doi: 10.1016/j.synthmet.2014.06.002
-
[11]
J Cheng, X Ma, Y Zhang et al. Inorg. Chem., 2014, 53(6):3210~3219. doi: 10.1021/ic5000815
-
[12]
Z Liu, W Zhu, Y Chen et al. Dalton Transac., 2015, 44(37):16528~16533. doi: 10.1039/C5DT02220G
-
[13]
I H Hwang, Y W Choi, K B Kim et al. New J. Chem., 2016, 40(1):171~178. doi: 10.1039/C5NJ02334C
-
[14]
吴海强, 王宇, 谭新强等.功能材料, 2012, 43(24):3468~3471. doi: 10.3969/j.issn.1001-9731.2012.24.033
-
[15]
Y Gao, W Ma. Opt. Mater., 2012, 35(2):211~216. doi: 10.1016/j.optmat.2012.07.008
-
[16]
N Narayanaswamy, T Govindaraju. Sens. Actuat. B, 2012, 161(1):304~310. doi: 10.1016/j.snb.2011.10.036
-
[17]
J Cheng, Y Zhang, X Ma et al. Chem. Commun., 2013, 49(100):11791~11793. doi: 10.1039/c3cc47137c
-
[18]
H Ye, F Ge, Y M Zhou et al. Spectrochim. Acta, Part A, 2013, 112:132~138. doi: 10.1016/j.saa.2013.03.093
-
[19]
X Xie, X Chen, B Li et al. Dyes Pigments, 2013, 98(3):422~427. doi: 10.1016/j.dyepig.2013.03.022
-
[20]
王建红, 郭心灵, 赵会君等.化学研究, 2014, 25(4):345~348. http://www.cqvip.com/QK/91277X/201404/661723710.html
-
[21]
Y J Na, Y W Choi, J Y Yun et al. Spectrochim. Acta, Part A, 2015, 136:1649~1657. doi: 10.1016/j.saa.2014.10.060
-
[22]
Q Meng, Y Shi, C Wang et al. Org. Biomol. Chem., 2015, 13(10):2918~2926. doi: 10.1039/C4OB02178A
-
[23]
Q Meng, H Jia, X Gao et al. Chem. Asian J., 2015, 10(11):2411~2418. doi: 10.1002/asia.v10.11
-
[24]
K Kaur, V K Bhardwaj, N Kaur et al. Inorg. Chim. Acta, 2013, 399:1~5. doi: 10.1016/j.ica.2012.12.030
-
[25]
V Luxami, K Paul, S Kumar. RSC Adv., 2013, 3(24):9189~9192. doi: 10.1039/c3ra41648h
-
[26]
G J Park, M M Lee, G R You et al. Tetrahed. Lett., 2014, 55(15):2517~2522. doi: 10.1016/j.tetlet.2014.03.018
-
[27]
Z Liu, W Yang, Y Li et al. RSC Adv., 2015, 5(122):100482~100487. doi: 10.1039/C5RA21038K
-
[28]
J C Qin, L Fan, Z Y Yang. Sens. Actuat. B, 2016, 228:156~161. doi: 10.1016/j.snb.2016.01.031
-
[29]
S Y Lee, J J Lee, K H Bok et al. RSC Adv., 2016, 6(33):28081~28088. doi: 10.1039/C6RA03364D
-
[30]
S Li, X Zhao, D Tao et al. Spectrochim. Acta, Part A, 2015, 137:581~588. doi: 10.1016/j.saa.2014.08.109
-
[31]
L Shen, Y He, X Yang et al. Spectrochim. Acta, Part A, 2015, 135:172~179. doi: 10.1016/j.saa.2014.07.007
-
[32]
D Mahajan, N Khairnar, B Bondhopadhyay et al. New J. Chem., 2015, 39(4):3071~3076. doi: 10.1039/C4NJ02149E
-
[33]
Y L Leng, J H Zhang, Q Li et al. Spectrochim. Acta, Part A, 2016, 167:116~121. doi: 10.1016/j.saa.2016.05.040
-
[34]
W C Lin, S K Fang, J W Hu et al. Anal. Chem., 2014, 86(10):4648~4652. doi: 10.1021/ac501024d
-
[35]
J H Hu, Y Sun, J Qi et al. RSC Adv., 2016, 6(102):100401~100406. doi: 10.1039/C6RA16378E
-
[1]
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 9
- 文章访问数: 2570
- HTML全文浏览量: 369


 下载:
下载:




 下载:
下载:

