 图 1
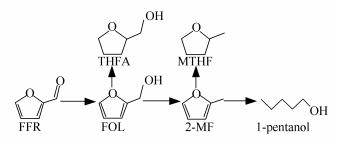
糠醛加氢过程中主要产物的分布
Figure 1.
Distribution of the main products in the process of furfural hydrogenation
图 1
糠醛加氢过程中主要产物的分布
Figure 1.
Distribution of the main products in the process of furfural hydrogenation

Citation: HUANG Yu-hui, REN Guo-qing, SUN Jiao, CHEN Xiao-rong, MEI Hua. Study on the vapor phase hydrogenation of furfural to 2-methylfuran on Cu/ZnO catalyst[J]. Journal of Fuel Chemistry and Technology, 2016, 44(11): 1349-1355.

Cu/ZnO催化糠醛气相加氢制2-甲基呋喃的研究
English
Study on the vapor phase hydrogenation of furfural to 2-methylfuran on Cu/ZnO catalyst
-
Key words:
- co-precipitation method
- / Cu/ZnO catalyst
- / furfural
- / gas hydrogenation
- / 2-methylfuran
-
糠醛(FFR) 作为一种可再生的生物质能源,通过各种农作物中提取的糖类脱水制备[1, 2]。目前,中国每年从生物质中提取的糠醛量约为2.8×105 t[3], 主要用于加氢制备糠醇(FOL)、2-甲基呋喃(2-MF)、2-甲基四氢呋喃(MTHF)、四氢糠醇(THFA)、1-戊醇(1-pentanol) 等一系列衍生物[4, 5]。2-甲基呋喃作为糠醛加氢最重要的产物之一,广泛应用于医药合成[6],另外,由于其高辛烷值被认为是汽油的代替品[7]。
工业上使用铜铬催化剂作为糠醛加氢制2-甲基呋喃的催化剂[8]。由于铬对环境污染较大,人们开始研究无铬铜基催化剂[9, 10]。但是,铜基催化剂的选择性和稳定性仍有待提高,这主要是因为糠醛在铜基催化剂下能发生多种加氢反应[11],见图 1。Huang等[12]认为,铜基催化剂上糠醛加氢的催化剂活性和还原后Cu的数量有关,文献[13-15]认为,催化剂上的弱酸性位数量越多对2-甲基呋喃的生成越有利。因此,在糠醛加氢制备2-甲基呋喃反应中,所选铜系催化剂不但要求有合适的活性中心数量,而且催化剂要具备一定弱酸性位,这样才能在加氢过程中获得较高的2-甲基呋喃选择性[16]。
 图 1
糠醛加氢过程中主要产物的分布
Figure 1.
Distribution of the main products in the process of furfural hydrogenation
图 1
糠醛加氢过程中主要产物的分布
Figure 1.
Distribution of the main products in the process of furfural hydrogenation
本研究采用共沉淀法制备活性较高、成本较低环境友好的铜锌催化剂,在固定床上考察不同铜锌物质的量比对糠醛加氢制2-甲基呋喃的影响。并且结合相关表征,对催化剂性能和物理性质关系进行探讨。
1 实验部分
1.1 催化剂的制备
按照所需质量计量比准确称取Cu (NO3)2·3H2O和Zn (NO3)2·6H2O配成1.2 mol/L的混合溶液。以物质的量比为1.3:1称取NaOH与Na2CO3混合沉淀剂配成1.0 mol/L溶液。在预先盛放100 mL去离子水的四口烧瓶中同时滴入混合液和沉淀剂,控制pH值在7.0左右,沉淀温度65 ℃,待沉淀完全后在65 ℃烘箱中老化过夜,滤饼过滤用去离子水洗至中性,在120 ℃烘箱中干燥过夜,在空气气氛下400 ℃焙烧4 h,压片成型备用。将铜锌物质的量比为1:4、1:2、1:1、1:0.67、1:0的铜锌氧化态催化剂分别表示为Cu1Zn4、Cu1Zn2、Cu1Zn1、Cu1Zn0.67和Cu1Zn0。
1.2 催化剂的表征
催化剂XRD分析在Bruker公司D8 Advance型X射线衍射仪上进行,Cu靶Kα线,管电压为40 kV,管电流为30 mA,10°-80°扫描,扫描速率20 (°)/min。用Scherrer公式计算CuO、ZnO、Cu的半峰宽分别取衍射角38.8°、31.8°和43.3°时所对应的CuO (111)、ZnO (100) 和Cu (111) 衍射峰。
催化剂采用日本Hitachi公司S-4800高分辨场发射扫描电镜对催化剂进行形貌分析,电镜分辨率为1 μm,加速电压5 kV,放大倍数为40 000-50 000倍。
催化剂采用Ankersmid公司BELSORPⅡ型吸附仪N2吸附法测定样品的BET比表面积。试样在200 ℃真空预处理3 h,在液氮温度下吸附。
催化剂氢气程序升温还原(H2-TPR) 在自制TPR及脉冲吸附联合装置上进行,30.0 mg样品在200 ℃的Ar气氛预处理2 h,降至室温,切换至10% H2-Ar混合气,气体流量20 mL/min,以10 ℃/min升温至350 ℃,TCD响应脱附信号,记录样品H2-TPR谱图。
催化剂氨气程序升温脱附实验(NH3-TPD) 在日本BEL公司BEL-CAT-B-82型程序升温脱附仪测试。称取0.100 g催化剂置于石英反应器中,氦气氛围300 ℃下处理30 min。降温至50 ℃吸收NH3 30 min,然后氦气吹扫至TCD基线稳定。脱附时氦气流量40 mL/min,以10 ℃/min升温至1 000 ℃。
1.3 催化剂的评价
糠醛气相加氢制2-甲基呋喃在固定床反应器中进行,准确称取20 mL催化剂装入长600 mm,内径20 mm不锈钢反应管。反应之前,以100 mL/min通入氢气,从室温以2 ℃/min升温至240 ℃,恒温还原6 h。还原结束后降温至200 ℃,切换氢气流量为120 mL/min,常压下使用恒流泵输入糠醛,进料量为6.0 mL/h,反应稳定之后,收集冷凝产物用于分析。反应产物采用岛津GC-2014C型气相色谱仪分析,XE-60毛细管柱,气化室温度220 ℃,FID检测,检测器温度250 ℃,柱温40 ℃,保持2 min,以10 ℃/min升温到180 ℃,保留10 min,采用面积归一化法定量分析。
2 结果与讨论
2.1 铜锌物质的量比对铜锌催化剂理化性质及催化性能的影响
2.2 Cu1Zn2催化剂上糠醛加氢制备2-甲基呋喃工艺条件的优化
2.3 Cu1Zn2催化糠醛加氢制2-甲基呋喃的稳定性
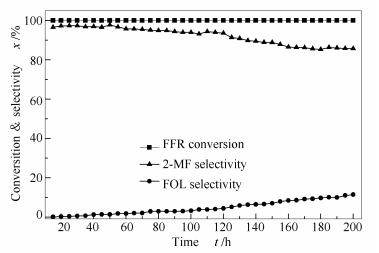
常压、反应温度200 ℃、氢醛物质的量比4:1、体积空速0.3 h-1的条件下探究Cu1Zn2催化剂稳定性,结果见图 10。由图 10可知,在200 h反应时间内,糠醛的转化率保持不变。但是随着反应时间的延长,2-甲基呋喃的选择性开始下降,糠醇的选择性增加。在反应前100 h内,2-甲基呋喃的选择性保持在90.0%以上,最好能达到93.6%,而到达200 h时,2-甲基呋喃的选择性下降到80.0%,糠醇选择性为11.4%左右,但此时糠醛转化率仍为100.0%。
2.1.2 BET表征
表 1为铜锌催化剂比表面积及还原前后晶粒粒径。由表 1可知,铜锌物质的量比对催化剂的比表面积影响较大,Cu1Zn0作为催化剂时,比表面积最小。加入ZnO后,随着ZnO的含量增加铜锌催化剂的比表面积呈现出先增大后减小的趋势,进一步表明适当的加入ZnO利于催化剂表面的分散。
 表 1
铜锌催化剂的比表面积及还原前后的晶粒粒径
Table 1.
BET analysis, crystal sizes of calcined and reduced Cu/ZnO catalysts
表 1
铜锌催化剂的比表面积及还原前后的晶粒粒径
Table 1.
BET analysis, crystal sizes of calcined and reduced Cu/ZnO catalysts
Catalyst ABET /(m2·g-1) Crystal size d/nm calcined sample reduced sample CuO ZnO Cu0 ZnO Cu1Zn4 40.6 10.4 14.6 13.4 16.4 Cu1Zn2 41.7 11.1 13.5 16.4 14.4 Cu1Zn1 38.0 11.2 12.0 16.7 18.2 Cu1Zn0.67 25.0 12.1 11.9 17.4 22.4 Cu1Zn0 6.0 14.8 - 28.6 - 表 1 铜锌催化剂的比表面积及还原前后的晶粒粒径
Table 1. BET analysis, crystal sizes of calcined and reduced Cu/ZnO catalysts2.1.1 SEM表征
图 2为催化剂的SEM照片。由图 2可知,催化剂Cu1Zn4和Cu1Zn1表面形态为多孔叶状,Cu1Zn2催化剂的表面形态为松糕状,Cu1Zn0催化剂表面形态为颗粒状。图 2说明ZnO的加入可以提高催化剂的比表面积。
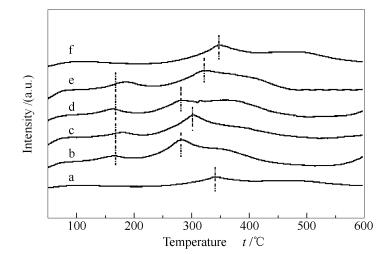
2.1.5 NH3-TPD表征
图 6为催化剂NH3-TPD谱图。
由图 6可知,纯CuO和ZnO在340 ℃左右出现一个氨气脱附峰,表明纯CuO和ZnO含有一个中强酸中心。而铜锌样品在谱图上出现两个氨气脱附峰,表明铜锌催化剂均有两种强度的酸性中心,在180 ℃出现一个氨气脱附峰为弱酸中心,在300 ℃左右的氨气脱附峰为中强酸性中心。说明CuO和ZnO之间存在一种相互作用,从而改变催化剂的酸性位。
2.1.6 铜锌物质的量比对铜锌催化剂性能的影响
在常压、反应温度200 ℃、氢醛物质的量比为4:1、糠醛体积空速为0.3 h-1时铜锌催化剂上糠醛加氢制2-甲基呋喃的催化性能,反应稳定15 h后取样分析,结果见表 2。由表 2可知,Cu1Zn0为催化剂时,糠醛的转化率为99.2%,此时糠醇的选择性较高,为86.4%,2-甲基呋喃选择性较差。Cu1Zn2为催化剂时,糠醛的转化率为100.0%,对2-甲基呋喃的选择性最高,为93.6%。
Catalyst FFR
conversion x/%Product selectivity s/% 2-MF FOL THFA MTHF 1-pentanol others Cu1Zn4 100.0 88.7 4.1 - 0.8 0.4 6.0 Cu1Zn2 100.0 93.6 0.5 - 1.4 0.6 3.9 Cu1Zn1 100.0 92.0 - - 2.3 1.8 3.9 Cu1Zn0.67 100.0 87.9 - - 3.3 3.3 5.5 Cu1Zn0 99.2 8.8 86.4 2.5 0.4 - 1.9 表 2 铜锌催化剂的性能评价
Table 2. Evaluation of catalytic performance over Cu/ZnO结合表征可知,Cu1Zn0作为催化剂时,由于其比表面积较小、不易还原,且还原后Cu0的晶粒粒径较大,加氢性能较差,同时NH3-TPD谱图没有观察到弱酸性位存在,因此,糠醛加氢产物主要为糠醇,进一步加氢2-甲基呋喃的量较少。铜催化剂中加入氧化锌后,催化剂的比表面积明显增大,催化剂易于还原且还原后Cu0的晶粒粒径较小,氧化锌加入使得催化剂表面弱酸性位数量明显增加,糠醛加氢产物主要为2-甲基呋喃。相同装填量的情况下,Cu1Zn1、Cu1Zn0.67催化剂经还原后,其Cu0活性中心数量较Cu1Zn0、Cu1Zn2和Cu1Zn4多,易发生深度加氢,生成较多的副产物,如2-甲基四氢呋喃(MTHF)、1-戊醇(1-pentanol)。因此,适宜的铜锌物质的量比为1:2。
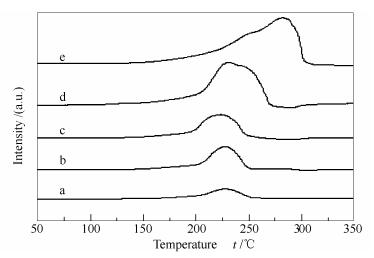
2.1.4 H2-TPR表征
图 5为催化剂的H2-TPR谱图。根据文献报道[20]ZnO还原温度在950 ℃左右,表明样品中H2吸附峰均为CuO的还原。由图 5可知,随着铜锌物质的量比的增加,氧化铜含量增加,其还原峰面积增大,说明其活性中心数量增加,并且,进一步表明催化剂中只有CuO的还原。Cu1Zn0催化剂的还原温度约275 ℃,随着ZnO含量的增加,催化剂的还原峰均向低温方向移动,这是因为氧化铜高度分散在载体上,而高分散的CuO在低温下即可还原[21]。
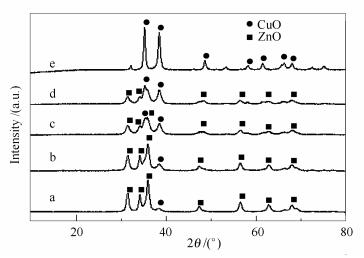
2.1.3 XRD表征
图 3为铜锌氧化态样品的XRD谱图。由图 3可知,Cu1Zn0催化剂有较强的CuO衍射峰,表明CuO结晶度较好。而加入ZnO后,Cu/ZnO样品中CuO峰强度明显降低,表明ZnO促进CuO分散。并且CuO (35.5°) 和ZnO (36.1°) 发生部分重合,形成大量CuO-ZnO固溶体[17],该固溶体中以CuO为中心四周排布着较多的ZnO,可保证催化剂中CuO充分细化,使催化剂有更多的活性中心,同时又能有效阻止CuO在还原过程和反应中因局部过热而导致Cu0烧结的长大,从而使催化剂保持较高的稳定性[18]。随着铜锌物质的量比的增加,CuO的衍射峰逐渐变得尖锐,ZnO衍射峰强度下降。
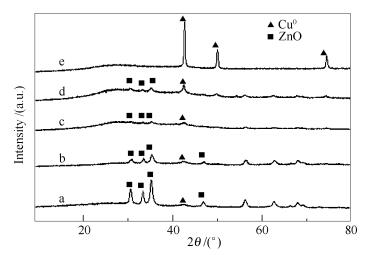
图 4为Cu/ZnO催化剂经过氢气还原后的XRD谱图。由图 4可知,经过还原后的不同物质的量比的铜锌催化剂,CuO的衍射峰均消失,形成Cu0衍射峰。Cu1Zn0还原后形成结晶度较好的Cu0衍射峰,而加入ZnO的催化剂经过还原后Cu0峰强度明显减弱,表明ZnO的加入高度促进Cu0的分散。
另外,根据图 3和图 4,以Scherrer方程计算铜锌样品还原前后各物种的晶粒粒径,结果见表 1。由表 1可知,氧化态铜锌样品随ZnO加入量的增多,CuO的晶粒粒径逐渐减小,ZnO的晶粒粒径逐渐增大。还原后的Cu1Zn0样品中Cu0晶粒最大,加入ZnO后铜锌样品中的Cu0晶粒均变小。表 1说明ZnO的加入提高CuO的分散,并且在还原过程中可以抑制Cu0的晶粒的长大[19]。
2.2.2 氢醛物质的量比对催化性能的影响
在常压、反应温度200 ℃、糠醛体积空速为0.3 h-1的条件下,考察氢醛物质的量比对糠醛加氢制2-甲基呋喃的影响,反应稳定15 h后取样分析,结果见图 8。由图 8可知,在所考察的氢醛物质的量比范围内,糠醛转化率始终保持在100.0%,但2-甲基呋喃选择性,表现出先增加后降低的趋势,糠醇选择性逐渐降低。这是因为较低的氢醛物质的量比会导致加氢反应不完全生成较多的糠醇,2-甲基呋喃选择性较低;氢醛比过高则会发生深度加氢反应,使2-甲基呋喃选择性下降。因此,最佳氢醛物质的量比为4:1。
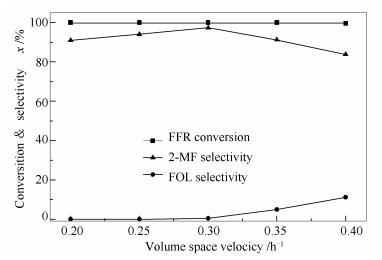
2.2.3 糠醛体积空速对催化性能的影响
在反应温度200 ℃、氢醛物质的量比为4:1、常压的条件下,考察糠醛体积空速对糠醛加氢制2-甲基呋喃的影响,反应稳定15 h后取样分析,结果见图 9。
由图 9可知,糠醛体积空速对糠醛的转化率影响较小。但是对2-甲基呋喃选择性表现出先增加后减少的趋势,糠醇表现出逐渐增加的趋势。这是因为当糠醛体积空速过小时,原料在催化剂床层内停留时间延长,导致反应发生深度加氢,使得2-甲基呋喃选择性降低。当糠醛体积空速为0.3 h-1时,糠醛转化率为100.0%,此时,2-甲基呋喃选择性为93.6%。继续提高体积空速,原料在催化剂上的停留时间缩短,一方面,使糠醛加氢反应不完全,当糠醛体积空速为0.4 h-1时,糠醛的转化率下降为99.5%;另一方面,也使生成的糠醇不能进一步加氢生成2-甲基呋喃,导致2-甲基呋喃选择性降低,糠醇选择性增加。所以适当的糠醛体积空速为0.3 h-1。
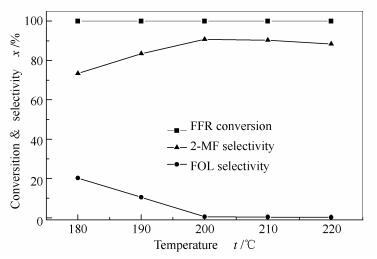
2.2.1 反应温度对催化剂性能的影响
在常压、氢醛物质的量比为4:1、糠醛体积空速为0.3 h-1的条件下,考察反应温度对铜锌催化剂上糠醛加氢制2-甲基呋喃的影响,反应稳定15 h后取样分析,结果见图 7。
由图 7可知,考察的反应温度范围内,糠醛的转化率保持在100.0%,2-甲基呋喃的选择性表现为先增加后减少的趋势,糠醇表现为逐渐递减的趋势。温度在200 ℃以下时,糠醛加氢生成的中间产物糠醇较多,致使2-甲基呋喃选择性较低。温度为200 ℃时,2-甲基呋喃选择性达到最高,为93.6%。温度在200 ℃以上时,发生深度加氢,使2-甲基呋喃选择性下降。因此, 选取200 ℃为最佳反应温度。
3 结论
通过共沉淀法制备不同铜锌物质的量比的铜锌催化剂,经还原后Cu0是糠醛加氢的活性中心。引入ZnO后,增加了催化剂弱酸性位,增大了催化剂的比表面积,同时形成大量CuO-ZnO固溶体,抑制还原过程中Cu0烧结长大,并且降低催化剂还原温度,从而对2-甲基呋喃具有较高的选择性,并且提高催化剂稳定性。
铜锌催化剂中活性中心数量对催化性能有较大影响,Cu1Zn2催化剂对糠醛加氢制2-甲基呋喃具有适宜的活性中心数量。该催化剂在常压、反应温度为200 ℃、氢醛物质的量比为4:1、糠醛体积空速为0.3 h-1条件下,2-甲基呋喃选择性最高为93.6%,反应稳定运行200 h后,糠醛转化率仍为100.0%,2-甲基呋喃选择性为80.0%,糠醇选择性为11.4%。
-
-
[1]
VAN P, R J, JCV D W, DE J E. Hydroxymethylfurfural, a versatile platform chemical made from renewable resources[J]. Chem Rev, 2013, 113(3): 1499-1597. doi: 10.1021/cr300182k
-
[2]
BINDER J B, RAINES R T. Simple chemical transformation of lignocellulosic biomass into furans for fuels and chemicals[J]. J Am Chem Soc, 2009, 131(5): 1979-1985. doi: 10.1021/ja808537j
-
[3]
MAMMAN A S, LEE J M, KIM Y C. Furfural:Hemicellulose/xylosederived biochemical[J]. Biofuel Bioprod Bior, 2008, 2(5): 438-454. doi: 10.1002/bbb.v2:5
-
[4]
PACE V, HOYOS P, CASTOLDI L. ChemInform abstract:2-methyltetrahydrofuran (2-MeTHF):A biomass-derived solvent with broad application in organic chemistry[J]. ChemSusChem, 2012, 5(8): 1369-1379. doi: 10.1002/cssc.v5.8
-
[5]
BIRADAR N S, HENNGNE A M, BIRAJDAR S N. Single-pot formation of THFAL via catalytic hydrogenation of FFR over Pd/MFI catalyst[J]. Acs Sustainable Chem Eng, 2013, 2(2): 272-281.
-
[6]
HUBER G W, SARA I A, CORMA A. Synthesis of transportation fuels from biomass:Chemistry, catalysts, and engineering[J]. Chem Rev, 2006, 106(9): 4044-4498. doi: 10.1021/cr068360d
-
[7]
XIAO M, JING C, XU H. Laminar burning characteristics of 2-methylfuran and isooctane blend fuels[J]. Fuel, 2014, 116(1): 281-291.
-
[8]
BURNETTL W, JOHNS I B, HOLDREN R F. Production of 2-methylfuran by vapor-phase hydrogenation of furfural[J]. Ind Eng Chem, 2002, 74(2): 129-130.
-
[9]
吴静, 申延明, 王坤院. CuO-CaO/SiO2超细催化剂结构及糠醛加氢反应性能的研究[J]. 分子催化, 2003,17,(5): 321-325. WU Jing, SHEN Yan-ming, WANG Kun-yuan. Study on structure of CuO-CaO/SiO2 ultrafine catalysts and reaction performance for hydrogenation of furfural[J]. J Mol Catal, 2003, 17(5): 321-325.
-
[10]
苗小培, 冯海强, 黄文氢. 纳米级CuO催化剂的制备及其糠醛加氢催化性能[J]. 石油化工, 2015,44,(8): 975-999. MIAO Xiao-pei, FENG Hai-qiang, HUANG Wen-qing. Preparation and catalytic properties of nanometer CuO catalyst for hydrogena[J]. Petrochem Technol, 2015, 44(8): 975-999.
-
[11]
KAI Y, XU W, XIA A, XIAN M X. Novel preparation of nano-composite CuO-Cr2O3 using ctab-template method and efficient for hydrogenation of biomass-derived furfural[J]. Funct Mater Lett, 2013, 6(1): 130-140.
-
[12]
HUANG W, LI H, ZHU B, FENG Y. Selective hydrogenation of furfural to furfuryl alcohol over catalysts prepared via sonochemistry[J]. Ultrason Sonochem, 2007, 14(1): 67-74. doi: 10.1016/j.ultsonch.2006.03.002
-
[13]
DONG F, ZHU Y, ZHENG H. Cr-free Cu-catalysts for the selective hydrogenation of biomass-derived furfural to 2-methylfuran:The synergistic effect of metal and acid sites[J]. J Mol Catal A:Chem, 2015, 398: 140-148. doi: 10.1016/j.molcata.2014.12.001
-
[14]
NAKAGAWA Y, TAMURA M, TOMISHIGE K. Catalytic reduction of biomass-derived furanic compounds with hydrogen[J]. Acs Catal, 2013, 3(12): 2655-2668. doi: 10.1021/cs400616p
-
[15]
黄玉辉, 任国卿, 孙蛟, 王重庆, 陈晓蓉, 梅华. 沉淀剂对CuZnAl催化剂糠醛气相加氢制糠醇选择性的影响[J]. 燃料化学学报, 2016,44,(6): 726-731. HUANG Yu-hui, REN Guo-qing, SUN Jiao, WANG Chong-qing, CHEN Xiao-rong, MEI Hua. Effect of precipitant on the performance of CuZnAl catalysts in the gas phase selective hydrogenation of furfural to furfuryl alcohol[J]. J Fuel Chem Technol, 2016, 44(6): 726-731.
-
[16]
YANG J, ZHENG H Y, ZHU Y L. Effects of calcination temperature on performance of Cu-Zn-Al catalyst for synthesizing γ-butyrolactone and 2-methylfuran through the coupling of dehydrogenation and hydrogenation[J]. Catal Commun, 2004, 5(9): 505-510. doi: 10.1016/j.catcom.2004.06.005
-
[17]
房德仁, 刘中民, 张慧敏. 沉淀温度对CuO/ZnO/Al2O3系催化剂前驱体性质的影响[J]. 天然气化工:C1化学与化工, 2004,29,(4): 28-32. FANG De-ren, LIU Zhong-ming, ZHANG Hui-ming. Influence of temperature on the properties of precursors of CuO/ZnO/Al2O3 catalysts[J]. Nat Gas Chem Ind, 2004, 29(4): 28-32.
-
[18]
姜广申, 胡云峰, 蔡俊. 仲丁醇脱氢制甲乙酮的Cu-ZnO催化剂[J]. 化工进展, 2013,32,(2): 352-358. JIANG Guang-shen, HU Yun-feng, CAI Jun. Research of Cu-ZnO catalysts for sec-butanol dehydrogenation to methyl ethyl ketone[J]. Chem Ind Eng Prog, 2013, 32(2): 352-358.
-
[19]
CHOI Y, FUTAGAMI K, FUJITANI T. The role of ZnO in Cu/ZnO methanol synthesis catalysts morphology effect or active site model[J]. Appl Catal A:Gen, 2001, 208(1/2): 163-167.
-
[20]
PARK S W, JOO O S, JUNG K D. Development of ZnO/Al2O3 catalyst for reverse-water-gas-shift reaction of CAMERE (carbon dioxide hydrogenation to form methanol via a reverse-water-gas-shift reaction) process[J]. Appl Catal A:Gen, 2001, 211(1): 81-90. doi: 10.1016/S0926-860X(00)00840-1
-
[21]
PEI T, LIU L, XU L. A novel glass fiber catalyst for the catalytic combustion of ethyl acetate[J]. Catal Commun, 2015, 74: 19-23.
-
[1]
-
表 1 铜锌催化剂的比表面积及还原前后的晶粒粒径
Table 1. BET analysis, crystal sizes of calcined and reduced Cu/ZnO catalysts
Catalyst ABET /(m2·g-1) Crystal size d/nm calcined sample reduced sample CuO ZnO Cu0 ZnO Cu1Zn4 40.6 10.4 14.6 13.4 16.4 Cu1Zn2 41.7 11.1 13.5 16.4 14.4 Cu1Zn1 38.0 11.2 12.0 16.7 18.2 Cu1Zn0.67 25.0 12.1 11.9 17.4 22.4 Cu1Zn0 6.0 14.8 - 28.6 - 表 2 铜锌催化剂的性能评价
Table 2. Evaluation of catalytic performance over Cu/ZnO
Catalyst FFR
conversion x/%Product selectivity s/% 2-MF FOL THFA MTHF 1-pentanol others Cu1Zn4 100.0 88.7 4.1 - 0.8 0.4 6.0 Cu1Zn2 100.0 93.6 0.5 - 1.4 0.6 3.9 Cu1Zn1 100.0 92.0 - - 2.3 1.8 3.9 Cu1Zn0.67 100.0 87.9 - - 3.3 3.3 5.5 Cu1Zn0 99.2 8.8 86.4 2.5 0.4 - 1.9 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 12
- 文章访问数: 1663
- HTML全文浏览量: 775




 下载:
下载:









 下载:
下载:

