 图1
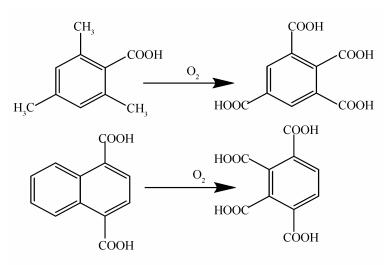
人工合成苯羧酸的氧化机理示意图
Figure1.
Mechanism for the oxidation of benzene carboxylic acid
图1
人工合成苯羧酸的氧化机理示意图
Figure1.
Mechanism for the oxidation of benzene carboxylic acid

Citation: ZHOU Jian, RAN Jing-yu, ZHANG Li. A DFT study on the reaction pathway for the oxidation of C6H2(OH)3CH3 to hydroxyl benzoic acid[J]. Journal of Fuel Chemistry and Technology, 2018, 46(2): 189-197.

C6H2(OH)3CH3氧化成羟基苯甲酸反应路径的DFT研究
English
A DFT study on the reaction pathway for the oxidation of C6H2(OH)3CH3 to hydroxyl benzoic acid
-
随着中国国家经济的高速发展,能源的消耗也逐年增加,石油进口量逐年增加。然而中国是一个富煤贫油的大国,煤的含量较多石油储备较少,因此, 许多学者着手研究通过对煤进行液化来获得燃料或利用煤制备有用的化学用品[1-3]。
煤的直接加氢液化和间接液化均可以获得燃料产物[4-6],但由于反应所需的高温高压及催化剂的限制[7-9],许多研究者开始寻求一种能够在比较温和的条件下发生液化的方法。目前, 通过氧化性物质在低温低压下实现煤液化的实验结果表明, 通过氧化性物质进行煤的液化是可行的,其反应温度低、压力小、催化剂要求不高且最终产物主要是苯羧酸及小分子醇[10, 11]。如Jun-ichiro[12]在100 ℃以下、碱性环境中利用空气中的氧对褐煤进行氧化得到氧化产物有苯羧酸、酚及小分子醇类物质。Kazuhiro等[13]在室温下用H2O2对褐煤进行氧化处理发现, 褐煤分子结构内的部分共价键断裂分解形成许多的羧基和碳氧键,其氧化产物主要是小分子醇、羧酸和芳香族化合物。冯波等[14]在碱性环境下利用H2O2氧化褐煤,经过测定反应产物得到小分子醇,脂肪羧酸和苯酚羧酸类化合物。以上通过氧化性物质对煤进行氧化液化的实验方法确实获得小分子醇、苯羧酸、酚酸等产物,但是在产物的生成机理方面的研究报道较少。
同时,在利用煤制备苯羧酸等化学品工艺方面,由于苯羧酸作为重要的化工原料和化工中间体, 在合成纤维、增塑剂、医药、农药、黏结剂、工程塑料、香料及染料中间体等领域有着普遍的应用。许多研究者如Yang等[15]探究煤的选择性氧化获得的苯羧酸产物与煤阶的关系,发现随着煤中碳含量的增加,经过选择性氧化后获得的苯羧酸产物产量随之增加。Wang等[16]研究高温条件下烟煤在碱氧环境下反应温度对苯羧酸产率的影响,结果显示随着反应温度的升高,生成苯羧酸的反应时间缩短,碱的消耗量降低,苯羧酸的产率最高达到41%。赵宇薇[17]通过氧化性物质作用于与苯环相连的甲基、环状碳原子来制备合成多羧基的苯羧酸,其反应原理见图 1。汪文化[18]探究了碱-煤比、反应温度、氧气的初始压力、反应时间对苯羧酸生成的影响。然而对于苯羧酸的生成路径及机理方面的研究报道较少。
由于褐煤氧化液化生成苯羧酸和褐煤制备苯羧酸研究均缺乏机理分析,导致反应产物苯羧酸生成路径不清楚,不能给煤氧化液化生成苯羧酸及煤制备苯羧酸提供理论依据,因而探究苯羧酸的生成路径显得尤为重要。本研究利用密度泛函(DFT)方法对煤在氧气条件下液化,探究主要反应物C6H2(OH)3CH3氧化成羟基苯甲酸的反应路径,以明确反应过程中的主反应路径的反应势垒及反应速率常数,给煤氧化液化生成苯羧酸及煤制备苯羧酸工艺提供理论支持。
1 C6H2(OH)3CH3分子特性及选择
1.1 甲苯与丙基苯结构的确定
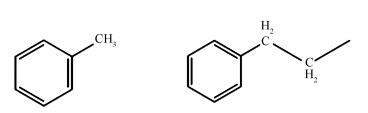
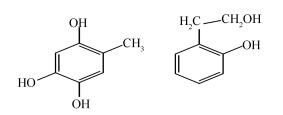
目前制备的苯羧酸种类约有12种[15, 16],对于苯甲酸的生成研究中Yang等[19]利用13C NMR(核磁共振)对煤进行结构分析并根据波峰的形式确定煤结构中含有下面两种结构:甲苯和丙基苯。这两个结构是生成苯甲酸的主要结构,见图 2。
吴桐[20]就煤在碱-氧氧化生成苯羧酸的反应机理讨论中得出甲苯和氧芴为生成苯甲酸的主要反应物,Wang等[21]利用褐煤制备小分子脂肪酸和苯羧酸得知模型化合物苯甲酸来源于苯丙烷的碱-氧氧化,故此可以确定煤的分子结构模型中均含有甲苯和丙基苯结构。
1.2 褐煤分子模型的选择
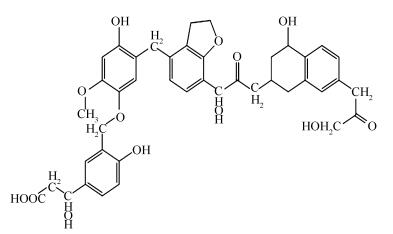
煤的分子结构繁杂,考虑到现有的实验方法大多以化学反应的方式来考察,根据反应物的生成机理从而反推断出煤分子结构模型,为了适应煤的化学反应特性,采用高晋生、朱培之等[22]基于中国褐煤的化学特性提出的一种无杂原子结构为分子模型,见图 3。
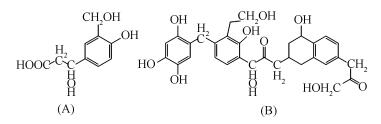
考虑到其结构内的醚键容易发生水解断裂形成酚羟基和醇羟基[23],于此将上述的无杂原子分子水解形成A和B两种分子结构,见图 4。
1.3 C6H2(OH)3CH3分子的确定
观察图 4中的A和B两分子结构,不难发现,与苯环直接相连的碳原子所在结构为甲醇、亚甲基及亚甲醇。由于B分子中亚甲基和亚甲醇氧化成羧基的过程与A分子中甲醇氧化成甲酸的过程重合,故可仅考虑B分子内的亚甲基及亚甲醇氧化成羧酸的过程。由于B分子仍比较繁杂,为了便于计算分析同时又不影响结果的含义,在此对B分子模型进行简化处理,将前面确定的煤中含有甲苯和丙基苯的结论与煤的早期分子模型内存在甲苯结构[24, 25]的结果综合考虑,B分子进行以下简化:将甲苯氧化成苯甲酸的过程取代A分子中苯甲醇氧化成羧基的过程;亚甲基氧化为羧基的过程中由于包含了亚甲醇氧化为羧基的过程,因此, 也将两者合并为亚甲基氧化为羧基的探究;最后依据液化实验产物[10, 11]将B分子简化成具有代表性的两个小分子C6H2(OH)3CH3和C6H4OHCH2CH2OH,具体见图 5。由于两个分子上的甲基和亚甲基氧化成羧基的过程可以完全反映褐煤大分子内与苯环相连的甲醇、亚甲醇、乙基、亚甲基氧化成羧基的氧化过程,故确定C6H2(OH)3CH3和C6H4OHCH2CH2OH为研究的简化模型。
对于上述确定的结构分子C6H2(OH)3CH3和C6H4OHCH2CH2OH,本研究在此先对分子C6H2(OH)3CH3结构内的甲基在氧化条件下最终形成羧基的反应路径进行探讨。
2 计算方法与参数设置
在此研究中应用Materials Studio 8.0中的Dmol3[26],在GGA/BP方法下对C6H2(OH)3CH3与氧原子、氧气分子反应形成的复合物进行几何结构优化[27],结构优化基本参数设置质量要求:Fine;基组选择:DNP;收敛参数范围:能量收敛为1.0 e-5 Ha,最大力收敛为0.02 Ha/nm,最大位移收敛为0.0005 nm,通过对形成的所有复合物进行了频率计算,结果显示均没有虚频,证明是基态稳定构型。过渡态寻找采用TS/LST/QST方法其RMS收敛范围为0.02 Ha/nm,在对过渡态的寻找过程中先确定过渡态存在唯一虚频,最后利用TS confirmation(过渡态验证)方法建立反应物、中间体、过渡态和产物的相关性,证明过渡态的正确连接。
为了寻找反应路径,需要获得各基元反应过程中反应物、过渡态、中间体及产物的总能量、反应势垒、反应能量。通过比较各基元反应所需克服的反应势垒来比较判断各基元反应发生的难易,利用基元反应的反应能量来判断反应的吸放热,其中, 反应势垒Eb的计算如下:
式中,Eb表示的是反应势垒,单位:kJ/mol;Ei表示的是过渡态总能量,单位:kJ/mol;Er表示的是反应物总能量,单位:kJ/mol;
其反应过程中反应能量Ee计算如下:
式中,Ee表示的是反应能量,单位:kJ/mol;Ep表示的是中间体或产物总能量,单位:kJ/mol;Er表示的是反应物总能量,单位:kJ/mol;
反应活化能Ea,反应速率常数k计算如下:
式中,Ea表示的是反应活化能,单位:kJ/mol;kb表示的是玻尔兹曼常数,h表示的是普朗克常数,R表示的是气体常数,p0表示的是标准大气压,T表示的是反应温度,n表示的是反应级数(由于反应物、过渡态、中间产物均视为单一的分子构型,故而反应物→过渡态→中间产物的反应过程均为一级反应,n的值取为1)。现有实验研究温度一般在373.15 K左右, 考虑到室温下氧气作为氧化剂的液化反应仍能有效获得苯羧酸,为了便于推广室温下氧气作为氧化剂的液化工艺,本文在此将所有反应均定在298.15 K下进行。
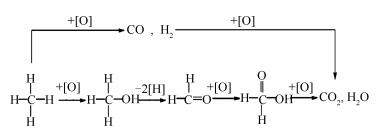
本研究为了便于探究分子C6H2(OH)3CH3结构内的甲基氧化成羧基的过程,在此对各反应过程的中间产物进行合理的假定。Clemens等[29]探究煤在低温下氧化形成CO2的过程中得出亚甲基在氧化条件下形成羧基的路径为亚甲基先被氧化形成羟基,然后进一步被氧化成醛基最后被氧化形成羧基的结论。Qi等[24]说明甲烷催化燃烧的脱氢反应机理过程为:CHx*+O*→CHx-1*+OH*(x=4、3、2),CHx*+OH*→CHxOH*(x=2、1)。James等[25]研究低烷烃的脱氢反应中提到甲烷氧化成水和二氧化碳的反应过程见图 6。
Guo等[30]对甲醇氧化脱氢形成一氧化碳的反应机理分析得出甲醇中醇羟基的氢原子会先一步脱离形成游离态的氢原子,然后甲基上的一个氢原子也随后脱离形成醛基,其路径是:CH3OH → CH2OH → CH2O → CHO。
最后基于上述研究,在此对反应中间产物可按如下进行设定:分子中的甲基、亚甲基先一步被氧化成羟基;新形成的羟基被氧化成醛基或酮基;最后醛基、酮基被氧化成羧基。同时由于单、三原子反应路径如果使用氧分子作为反应物均会多出一个游离态的氧原子,而多余的游离态氧原子会使得反应物构型变得复杂,不利于分析计算,本研究在此采用氧原子作为反应物进行计算,其中氧气分子分解成氧原子需要克服76.831 kJ/mol的反应势垒。
3 C6H2(OH)3CH3化学反应路径分析
基于上述得出甲基、亚甲基的氧化特性是甲基上的一个氢原子容易先被氧化成羟基,随后羟基进一步被氧化成醛基最后被氧化成羧基[24-28],本研究将分子C6H2(OH)3CH3氧化过程分为三种不同的反应路径进行研究。
单个氢原子氧化反应路径:C6H2(OH)3CH3+O→C6H2(OH)3CH2OH,C6H2(OH)3CH2OH+O→C6H2(OH)3CHO+H2O,C6H2(OH)3CHO+O→C6H2(OH)3COOH;
两个氢原子氧化反应路径:C6H2(OH)3CH3+2O→C6H2(OH)3CH(OH)2→C6H2(OH)3CHO+H2O,C6H2(OH)3CHO+O→C6H2(OH)3COOH;
三个氢原子氧化反应路径:C6H2(OH)3CH3+3O→C6H2(OH)3C(OH)3→C6H2(OH)3COOH+H2O。
3.1 单个氢原子氧化反应路径
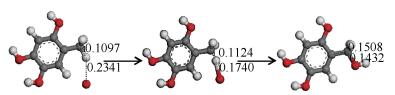
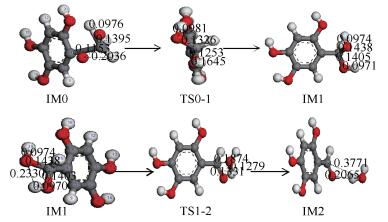
图 7为分子C6H2(OH)3CH3甲基上的一个氢原子被氧原子氧化成羟基过程中键长的变化。在IM0中,当单个氧原子靠近甲基上的氢原子时,它对该氢原子产生一种牵引作用,使得氢原子与碳原子之间的键距由0.1097 nm拉长0.1124 nm,碳氢键断裂,表现为氢原子被氧原子牵引而靠近氧原子。同时单个氧原子与游离氢原子距离由0.2341 nm拉近到0.1740 nm时形成羟基。此时羟基不断靠近甲基,当氧原子与碳原子的距离缩为0.1432 nm时最终得到稳定结构IM1。该反应过程需克服2.276 kJ/mol的反应势垒,整体放热量452.010 kJ/mol。
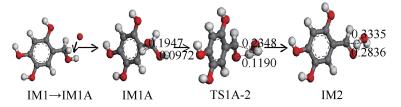
随着羟基的形成,加上大量氧原子存在反应中,羟基由于分子间力的作用容易与氧原子发生进一步氧化。图 8为IM1→IM1A(单个氧原子靠近羟基并产生作用前的过渡过程)及羟基进一步被氧化成醛基过程中键长的变化。在IM1A中,单个氧原子同时对甲基和羟基上的氢原子产生作用。首先氧原子对甲基上的氢原子产生牵引作用,碳氢键的键距从0.1947 nm拉长到0.2348 nm,碳氢键断裂。同时氧原子靠近羟基的氢原子,借助原子间的作用力,使氢原子绕氧原子转动,羟基键长由0.0972 nm拉长到0.1190 nm,最终羟基键断裂形成醛基和水分子,此过程需克服的反应势垒为142.352 kJ/mol。随后水分子开始远离使整个系统处于稳定状态得到IM2,该过程放热9.791 kJ/mol的能量。
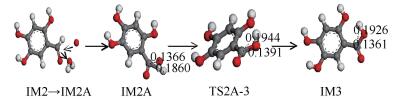
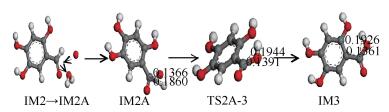
当醛基形成后,水分子由于分子力减弱而远离醛基,同时氧原子开始靠近醛基并发生氧化过程。图 9为IM2→IM2A(水分子远离醛基,氧原子靠近醛基并产生作用前的过渡过程)及醛基被氧化成羧基过程中键长的变化。在IM2A中,醛基被氧化成羧基的过程为单个氧原子靠近醛基上的氢原子,利用原子间的作用力,使得醛基上的碳氢键距由0.1860 nm不断拉长直至断裂,并让氢原子绕其转动形成共价键。同时氧原子不断靠近碳原子,碳氧间距由0.1366 nm拉大到0.1391 nm时两者间形成共价键。最后分子趋于稳定时碳氧键距缓慢收缩到0.1361 nm,同时氢原子转动到原平面形成羧基得到IM3。此过程需克服50.103 kJ/mol的反应势垒,放热量2.402 kJ/mol。
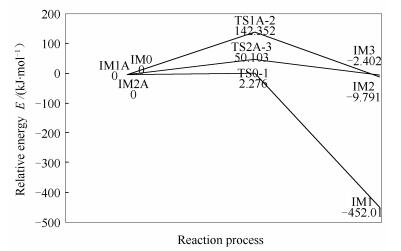
此处,表 1为单个氢原子氧化反应路径过程中反应物、中间体、生成物及过渡态的总能量,过渡态的频率,基元反应的反应能量, 反应势垒及反应速率常数。IM0表示初始反应物,IM1、IM1A、IM2、IM2A表示中间产物,IM3表示最终产物,TS0-1、TS1A-2、TS2A-3表示过渡态。图 10为单个氢原子氧化反应路径的各反应势垒。
 表 1
反应物、中间体、过渡态及生成物的总能量,过渡态频率、反应能量、反应势垒及反应速率常数
Table 1.
Total energies of reactants, products, intermediate, and transition states; frequency of transition states; reaction energies, energy barrier, and reaction rate constant
表 1
反应物、中间体、过渡态及生成物的总能量,过渡态频率、反应能量、反应势垒及反应速率常数
Table 1.
Total energies of reactants, products, intermediate, and transition states; frequency of transition states; reaction energies, energy barrier, and reaction rate constant
Total energies
E/HaFrequency of transition
states /cm-1Reaction energies
Ee/(kJ·mol-1)Energy barrier
Eb/(kJ·mol-1)Reaction rate constant
ln(k)/s-1IM0 -572.4485192 TS0-1 -572.4476524 -124.77 -452.010 2.276 28.539 IM1 -572.6206809 IM1A -572.6206558 TS1A-2 -572.4952856 -1526.41 -9.791 142.352 -27.970 IM2 -572.5993533 IM2A -646.7025609 TS2A-3 -646.6834768 -647.04 -2.402 50.103 9.245 IM3 -646.7034749 3.2 两个氢原子氧化反应路径
图 11为分子C6H2(OH)3CH3甲基上的两个氢原子先被氧原子氧化成羟基后脱水形成醛基过程中键长的变化。由于出现两个氧原子这里对原子进行编号标记。从IM0看到13、14号氧原子分别靠近10号碳原子,当O14靠近C10时,其对H19产生的牵引作用使得H19与C10之间的碳氢键变长作用力减弱。当O14与H19距离由0.2036 nm缩小为0.1645 nm时,H19与C10间的共价键断裂,H19与O14形成共价键。同时O14与C10距离由0.1453 nm缩小到0.1253 nm时,O14与C10开始形成共价键。对于O13而言,当O13与C10、H17靠近过程中,O13与H17间距由0.0976 nm变为0.0981 nm形成共价键。同时O13与C10间距由0.1395 nm缩小为0.1326 nm也形成共价键,该过程共需克服528.406 kJ/mol的反应势垒,然后分子为达到稳定状态,这时O14与C10的键距伸长为0.1405 nm。同理O13与C10键距拉伸到0.1438 nm保持稳定并得到IM1,整个反应过程放热为33.962 kJ/mol。
当一个甲基上存在两个羟基时其稳定性变弱,两个羟基容易去掉一个水分子变成醛基。由于两个羟基的属性是相同的,故两个羟基去掉任何一个结果都一样。在此对两羟基重新标记,这里是去掉O17所在的羟基与H20。当IM1所对应的O17与H20相互吸引靠近,其距离从0.2330 nm减小到0.1279 nm时形成共价键,此时O17与C10的距离由0.1438 nm拉伸到0.1874 nm时共价键断裂。O18与H20的距离由0.0971 nm拉伸到共价键断裂,同时O18与C10的距离由0.1405 nm缩小到0.1321 nm时形成双键,该过程需克服137.193kJ/mol的反应势垒。随后小分子开始远离使整个系统处于稳定状态得到IM2,该反应放热25.383 kJ/mol的能量。
当醛基形成后,水分子由于分子力减弱而远离醛基,同时氧原子靠近醛基并发生氧化过程。图 12为IM2→IM2A(水分子远离醛基,氧原子靠近醛基并产生作用前的过渡过程)及醛基被氧化成羧基的过程中键长的变化。醛基被氧化成羧基的过程和单个氢原子反应路径中的醛基氧化过程相同。当醛基形成后,水分子由于分子力减弱远离醛基。单个氧原子靠近醛基上的氢原子并利用原子间的作用力使得碳氢键的长度由0.1860 nm不断拉大到断裂,同时氧原子让氢原子绕其转动形成共价键。当氧原子与碳原子距离由0.1366 nm拉大到0.1391 nm时两者间形成共价键。最后分子趋于稳定时碳氧键缓慢收缩到0.1361 nm,同时氢原子转动到原平面,此过程需克服50.103 kJ/mol的反应势垒,放热量2.402 kJ/mol。
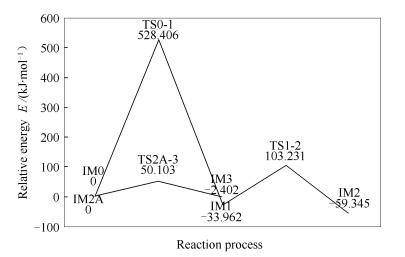
表 2为两个氢原子氧化反应路径过程中的反应物、中间体、生成物及过渡态的总能量,过渡态的频率,基元反应的反应能量、反应势垒及反应速率常数。IM0表示初始反应物,IM1、IM2、IM2A表示中间产物,IM3表示最终产物,TS0-1、TS1-2、TS2A-3表示过渡态。图 13为两个氢原子氧化反应的各反应势垒。
 表 2
反应物、中间体、过渡态及生成物的总能量、过渡态频率、反应能量、反应势垒及反应速率常数
Table 2.
Total energies of reactants, products, intermediate, and transition states; frequency of transition states; reaction energies, energy barrier, and reaction rate constant
表 2
反应物、中间体、过渡态及生成物的总能量、过渡态频率、反应能量、反应势垒及反应速率常数
Table 2.
Total energies of reactants, products, intermediate, and transition states; frequency of transition states; reaction energies, energy barrier, and reaction rate constant
Total energies
E/HaFrequency of transition
states /cm-1Reaction energies
Ee/(kJ·mol-1)Energy barrier
Eb/(kJ·mol-1)Reaction rate constant
ln(k) /s-1IM0 -647.8643879 TS0-1 -647.6631287 -1381.09 -33.962 528.406 -183.711 IM1 -647.8773231 TS1-2 -647.8250685 -1574.66 -25.383 137.193 -25.889 IM2 -647.8869909 IM2A -646.7025609 TS2A-3 -646.6834768 -647.04 -2.402 50.103 9.245 IM3 -646.7034749 3.3 三个氢原子氧化反应路径
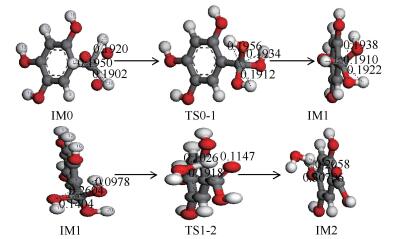
图 14为分子C6H2(OH)3CH3甲基上的三个氢原子先被氧原子氧化成羟基,然后直接被氧化成羧基过程中键长的变化。由于出现三个氧原子这里对原子进行编号标记,记19、20、21为标记氧原子,15、17、18为标记氢原子。IM0中当O20靠近H17、O19靠近H15及O21靠近H18时,由于氧原子对氢原子产生的牵引作用使得H17与碳原子的距离由0.1950 nm拉伸到0.1956 nm时共价断裂,同时H18与碳原子的距离由0.1902 nm拉伸到0.1912 nm,H15与碳原子的距离由0.1920 nm拉伸到0.1934 nm共价键均断裂,氢原子与氧原子形成新的共价键。此时三个氧原子均与碳原子构成共价键。由于反应物结构内的甲基与氧原子通过较小的空间旋转便可以得到过渡态,所以虚频较小,此过程需克服14.372 kJ/mol的反应势垒,然后分子为趋于稳定结构,碳氧键的距离做了较小的调整得到IM1,整个反应放热量为2.774 kJ/mol。
随后这三个羟基容易去掉一个水分子形成羧基,由于三者性质相同故在此对羟基重新标记,将O17所在的羟基与O15连接的氢原子以一水分子的形式脱除。当IM1所对应的O17与碳原子的距离由0.1404 nm拉伸到0.1918 nm时共价键断裂,同时与O15相连的H21受到O17的牵引作用,其与O15的键距由0.0978 nm拉伸到0.1147 nm时共价键也断裂最终形成羧基,此过程需克服129.859 kJ/mol的反应势垒。然后分子为趋于稳定结构慢慢远离水分子得到IM2,总的反应放热量为62.560 kJ/mol。
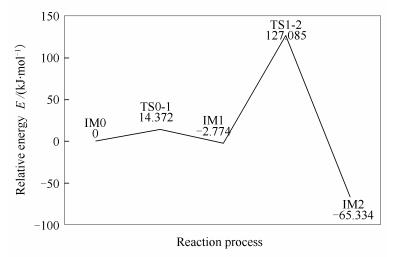
表 3为三个氢原子氧化反应路径过程中的反应物、中间体、生成物及过渡态的总能量,过渡态的频率,基元反应的反应能量、反应势垒及反应速率常数。IM0表示初始反应物,IM1表示中间产物,IM2表示最终产物,TS0-1、TS1-2表示过渡态。图 15为三个氢原子氧化反应的反应势垒。
 表 3
反应物、中间体、过渡态及生成物的总能量、过渡态频率、反应能量、反应势垒及反应速率常数
Table 3.
Total energies of reactants, products, intermediate, and transition states, frequency of transition states, reaction energies, energy barrier, and reaction rate constant
表 3
反应物、中间体、过渡态及生成物的总能量、过渡态频率、反应能量、反应势垒及反应速率常数
Table 3.
Total energies of reactants, products, intermediate, and transition states, frequency of transition states, reaction energies, energy barrier, and reaction rate constant
Total energies
E/HaFrequency of transition
states /cm-1Reaction energies
Ee/(kJ·mol-1)Energy barrier
Eb/(kJ·mol-1)Reaction rate constant
ln(k) /s-1IM0 -723.1418687 TS0-1 -723.1363946 -104.99 -2.774 14.372 23.659 IM1 -723.1429255 TS1-2 -723.0934644 -1327.50 -62.560 129.859 -22.930 IM2 -723.1667535 3.4 三种反应路径比较分析
观察前面数据得到的各反应路径中羟基、醛基、羧基的形成所需克服的反应势垒大小以及各反应路径在不同反应阶段的反应速率常数ln(k)可知,醛基被氧化成羧基的反应势垒最小为50.103 kJ/mol,反应速率常数ln(k)达到9.245。三个氢原子被氧化成的羟基后,其再被氧化成羧基的反应势垒为129.859 kJ/mol,两个氢原子先被氧化成羟基后,其再被氧化成羧基的总反应势垒为187.296 kJ/mol,最后单个氢原子先被氧化成羟基后,其再被氧化成醛基的总反应势垒为192.455 kJ/mol。所以羟基、醛基优先被氧化成羧基的顺序为:-CHO>-C(OH)3>-HC(OH)2>-H2C(OH),其中,-HC(OH)2结构的形成较为困难;在羟基的形成过程中单个氢原子氧化反应路径和三个氢原子氧化反应路径所需克服的反应势垒较小且相差不大,两个氢原子氧化反应路径则需克服较大的反应势垒;在醛基的氧化过程中双原子氧化反应路径比单原子氧化反应路径更易进行,三个氢原子氧化反应路径则跳过此过程最后被氧化为羧基;在羧基的形成过程中三个氢原子氧化反应路径较单个氢原子氧化、两个氢原子氧化反应路径克服更多的反应势垒,但总体上三个氢原子氧化反应路径的反应过程最短且所克服总的反应势垒最低,故三个氢原子氧化反应路径为主反应路径,其反应控制步骤为三个羟基直接氧化成羧基过程,该过程反应速率常数ln(k)为-22.96 s-1,其次是单个氢原子氧化反应路径。
从表中结果还可以得知,要提高C6H(OH)3CH3氧化成羟基苯甲酸的反应速率,促使苯甲酸的生成,应及时满足单、两、及三个氢原子氧化反应路径中需克服的反应势垒,此外,如提高氧原子的浓度促使三个氢原子氧化反应路径的进行、提高反应温度以促进单个氢原子氧化过程中羟基向醛基的氧化进程、以及利用催化剂促进两个氢原子氧化成羟基的反应,同时促进其他反应的进行等。
4 结论
甲基上的氢原子被氧化成羟基、羟基氧化为醛基及醛基氧化成羧基均为放热过程;分子C6H2(OH)3CH3中的甲基氧化成羧基的主路径为三原子氧化反应路径,其路径为C6H2(OH)3CH3+3O→C6H2(OH)3C(OH)3→C6H2(OH)3COOH+H2O, 该过程受限于羟基直接氧化成羧基,需克服129.859 kJ/mol的反应势垒,反应速率常数ln(k)为-22.96 s-1;醛基、羟基优先被氧化成羧基的顺序为:-CHO>-C(OH)3>-HC(OH)2>-H2C(OH);提高反应温度、氧气浓度均有利于羟基苯甲酸的生成,适当的催化剂有利于促进整体反应的进行。
-
-
[1]
高建业. 煤液化燃料替代石油的开发应用[J]. 煤气与热力, 2007,27,(1): 37-43. GAO Jian-ye. The development of alternative fuels for coal liquefaction fuels[J]. Gas Heat, 2007, 27(1): 37-43.
-
[2]
SIMSEK E H, KARADUMAN A, OLCAY A. Liquefaction of turkish coals in tetralin with microwaves[J]. Fuel Process Technol, 2001, 73(2): 111-125. doi: 10.1016/S0378-3820(01)00196-5
-
[3]
AMESTICA L A, WOLF E E. Catalytic liquefaction of coal with supercritical water/CO/solvent media[J]. Fuel, 1986, 65(9): 1226-1233. doi: 10.1016/0016-2361(86)90234-6
-
[4]
王春萍. 我国煤液化概况[J]. 化学工程师, 2005,19,(12): 40-41. doi: 10.3969/j.issn.1002-1124.2005.12.016WANG Chun-ping. General situation of coal liquefaction in china[J]. Chem Eng, 2005, 19(12): 40-41. doi: 10.3969/j.issn.1002-1124.2005.12.016
-
[5]
ESPINOZA R L, STEYNBERG A P, JAGER B, VOSLOO A C. Low temperature Fischer-Tropsch synthesis from a sasol perspective[J]. Appl Catal A:Gen, 1999, 186(1/2): 13-26.
-
[6]
STEYNBERG A P, ESPINOZA R L, JAGER B, VOSLOO A C. High temperature Fischer-Tropsch synthesis in commercial practice[J]. Appl Catal A:Gen, 1999, 186(1/2): 41-54.
-
[7]
吴春来. 南非SASOL的煤炭间接液化技术[J]. 煤化工, 2003(2): 3-6. WU Chun-lai. Coal indirect liquefaction technology of south africa's SASOL[J]. Coal Chem Ind, 2003, (2): 3-6.
-
[8]
VAN WECHEM V M H, SENDEN M M G. Conversion of natural gas to transportation fuels via the shell middle distillate synthesis process (SMDS)[J]. Catal Today, 1991, 8(3): 43-71.
-
[9]
相宏伟, 唐宏青, 李永旺. 煤化工工艺评述与展望Ⅳ.煤间接液化技术[J]. 燃料化学学报, 2001,29,(4): 289-298. XIANG Hong-wei, TANG Hong-qing, LI Yong-wang. Review and prospect of coal chemical technologyⅣ.Coal indirect liquefaction technology[J]. J Fuel Chem Technol, 2001, 29(4): 289-298.
-
[10]
LIU Z X, LIU Z C. GC/MS analysis of water-soluble products from the mild oxidation of longkou brown coal with H2O2[J]. Energy Fuels, 2003, 17(2): 424-426. doi: 10.1021/ef020071e
-
[11]
KOUICHI M, KAZUHIRO M. New oxidative degradation method for producing fatty acids in hgh yields and high selectivity from low-rank coals[J]. Energy Fuels, 1996, 10(6): 1196-1201.
-
[12]
JUN-ICHIRO H. Depolymerization of lower rank coals by low-temperature O2 oxidation[J]. Energy Fuels, 1997, 11(1): 227-235. doi: 10.1021/ef960104o
-
[13]
KAZUHIRO M. Extraction of low-rank coals oxidized with hydrogen peroxide in conventionally used solvents at room temperature[J]. Energy Fuels, 1997, 11(4): 825-831. doi: 10.1021/ef960225o
-
[14]
冯波, 其鲁, 张敬华. 弱氧化环境下褐煤氧化产物的定性分析[J]. 冶金分析, 2009,29,(1): 21-24. FENG Bo, QI Lu, ZHANG Jing-hua. Qualitative and metallurgical analysis of lignite oxidation products in weak oxidized environment[J]. Metall Anal, 2009, 29(1): 21-24.
-
[15]
YANG F, HOU Y, WU W, WANG Q, NIU M G, REN S H. The relationship between benzene carboxylic acids from coal via selective oxidation and coal rank[J]. Fuel Process Technol, 2017, 160: 207-215. doi: 10.1016/j.fuproc.2017.02.035
-
[16]
WANG W, HOU Y, NIU M, WU T, WU W Z. Production of benzene polycarboxylic acids from bituminous coal by alkali-oxygen oxidation at high temperatures[J]. Fuel Process Technol, 2013, 110(6): 184-189.
-
[17]
赵宇薇. 褐煤碱-氧氧化的产物分析及其结构的基础研究[D]. 北京: 北京化工大学, 2015. http://d.wanfangdata.com.cn/Thesis/Y2862009ZHAO Yu-wei. Product and structure analysis of basic research for lignite oxidation in oxygen alkaline environment[D]. Beijing: Beijing University of Chemical Technology, 2015. http://d.wanfangdata.com.cn/Thesis/Y2862009
-
[18]
汪文化. 煤炭、生物质选择性催化氧化制备化学品的研究[D]. 北京: 北京化工大学, 2013.WANG Wen-hua. The research of selective catalytic oxidation for preparation chemicals by coal and biomass[D]. Beijing: Beijing University of Chemical Technology, 2013.
-
[19]
YANG F, HOU Y, WU W, WANG Q. A new insight into the structure of Huolinhe lignite based on the yields of benzene carboxylic acids[J]. Fuel, 2017, 189: 408-418.
-
[20]
吴桐. 多种煤碱氧化制备苯羧酸及其产物分离的研究[D]. 北京: 北京化工大学, 2014.WU Tong. The study of preparation of Benzene carboxylic acid and its separation by kinds of coal oxidation in oxygen alkaline[D]. Beijing: Beijing University of Chemical Technology, 2014.
-
[21]
WANG W, HOU Y, WU W, NIU M G. Simultaneous production of small-molecule fatty acids and benzene polycarboxylic acids from lignite by alkali-oxygen oxidation[J]. Fuel Process Technol, 2013, 112(4): 7-11.
-
[22]
朱培之, 高晋生.煤化学[M].上海:上海科技出版社. 1984.ZHU Pei-zi, GAO Jin-shen. Coal Chemistry[M]. Shanghai:Shanghai Scientific & Technical Publishers, 1984.
-
[23]
虞继舜.煤化学[M].北京:冶金工业出版社. 2000.YU Ji-shun. Coal Chemistry[M]. Beijing:Metallurgical Industry Press, 2000.
-
[24]
QI W, RAN J, WANG R, SHI J, DU X S, RAN M C. Kinetic mechanism of effects of hydrogen addition on methane catalytic combustion over Pt(111) surface:A DFT study with cluster modeling[J]. Comput Mater Sci, 2016, 111: 430-442. doi: 10.1016/j.commatsci.2015.09.002
-
[25]
JAMES O O, MANDAL S, ALELE N, CHOWDHURY B, MAITY S. Lower alkanes dehydrogenation:Strategies and reaction routes to corresponding alkenes[J]. Fuel Process Technol, 2016, 149: 239-255. doi: 10.1016/j.fuproc.2016.04.016
-
[26]
DELLEY B. From molecules to solids with the DMol3 approach[J]. J Chem Phys, 2000, 113(18): 7756-7764. doi: 10.1063/1.1316015
-
[27]
PERDEW J P, CHEVARY J A, VOSKO S H, PEDERSON M R, SINGH D J, PHYS F C. Erratum:Atoms, Molecules, Solids, And Surfaces:Applications of the Generalized Gradient Approximation for Exchange and Correlation[M]. Phys Rev B:Condens Matter, 1993.
-
[28]
WANG B, WEI X, XIE K. Study on reaction of N-methyl-2-pyrrolidinone with carbon disulfide using density functional theory[J]. J Chem Ind Eng, 2004, 55(4): 569-574.
-
[29]
CLEMENS A H, MATHESON T W, ROGERS D E. Low temperature oxidation studies of dried new zealand coals[J]. Fuel, 1991, 70(2): 215-221. doi: 10.1016/0016-2361(91)90155-4
-
[30]
GUO W, TIAN W Q, LIAN X, LIU F L, ZHOU M, XIAO P, ZHANG Y H. A comparison of the dominant pathways for the methanol dehydrogenation to CO on Pt 7, and Pt 7-x Ni x, (x=1, 2, 3) bimetallic clusters:A DFT study[J]. Comput Theor Chem, 2014, 1032(5): 73-83.
-
[1]
-
表 1 反应物、中间体、过渡态及生成物的总能量,过渡态频率、反应能量、反应势垒及反应速率常数
Table 1. Total energies of reactants, products, intermediate, and transition states; frequency of transition states; reaction energies, energy barrier, and reaction rate constant
Total energies
E/HaFrequency of transition
states /cm-1Reaction energies
Ee/(kJ·mol-1)Energy barrier
Eb/(kJ·mol-1)Reaction rate constant
ln(k)/s-1IM0 -572.4485192 TS0-1 -572.4476524 -124.77 -452.010 2.276 28.539 IM1 -572.6206809 IM1A -572.6206558 TS1A-2 -572.4952856 -1526.41 -9.791 142.352 -27.970 IM2 -572.5993533 IM2A -646.7025609 TS2A-3 -646.6834768 -647.04 -2.402 50.103 9.245 IM3 -646.7034749 表 2 反应物、中间体、过渡态及生成物的总能量、过渡态频率、反应能量、反应势垒及反应速率常数
Table 2. Total energies of reactants, products, intermediate, and transition states; frequency of transition states; reaction energies, energy barrier, and reaction rate constant
Total energies
E/HaFrequency of transition
states /cm-1Reaction energies
Ee/(kJ·mol-1)Energy barrier
Eb/(kJ·mol-1)Reaction rate constant
ln(k) /s-1IM0 -647.8643879 TS0-1 -647.6631287 -1381.09 -33.962 528.406 -183.711 IM1 -647.8773231 TS1-2 -647.8250685 -1574.66 -25.383 137.193 -25.889 IM2 -647.8869909 IM2A -646.7025609 TS2A-3 -646.6834768 -647.04 -2.402 50.103 9.245 IM3 -646.7034749 表 3 反应物、中间体、过渡态及生成物的总能量、过渡态频率、反应能量、反应势垒及反应速率常数
Table 3. Total energies of reactants, products, intermediate, and transition states, frequency of transition states, reaction energies, energy barrier, and reaction rate constant
Total energies
E/HaFrequency of transition
states /cm-1Reaction energies
Ee/(kJ·mol-1)Energy barrier
Eb/(kJ·mol-1)Reaction rate constant
ln(k) /s-1IM0 -723.1418687 TS0-1 -723.1363946 -104.99 -2.774 14.372 23.659 IM1 -723.1429255 TS1-2 -723.0934644 -1327.50 -62.560 129.859 -22.930 IM2 -723.1667535 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 17
- 文章访问数: 9101
- HTML全文浏览量: 1046


 下载:
下载:














 下载:
下载:

