 图1
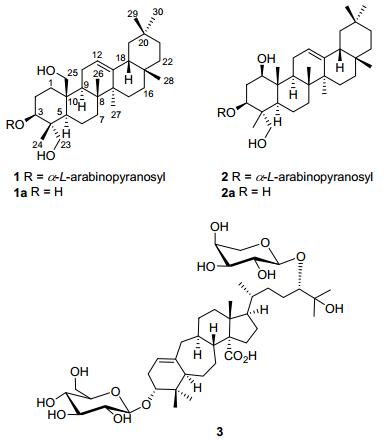
三萜皂苷化合物1~3以及化合物1和2的苷元1a和2a的化学结构
Figure1.
Chemical structures of triterpenoid glycosides 1~3, and the aglycones 1a and 2a of compounds 1 and 2
图1
三萜皂苷化合物1~3以及化合物1和2的苷元1a和2a的化学结构
Figure1.
Chemical structures of triterpenoid glycosides 1~3, and the aglycones 1a and 2a of compounds 1 and 2

Citation: Teng Yang, Zhang Hanqi, Zhou Junfei, Li Yongji, Yao Guangmin. Triterpenoid Glycosides from the Leaves of Lyonia ovalifolia var. hebecarpa and Their Antitumor Activities[J]. Chinese Journal of Organic Chemistry, 2017, 37(9): 2416-2422. doi: 10.6023/cjoc201705007

毛果南烛叶中的三萜皂苷化合物及其抗肿瘤活性
English
Triterpenoid Glycosides from the Leaves of Lyonia ovalifolia var. hebecarpa and Their Antitumor Activities
-
Key words:
- Lyonia ovalifolia var. hebecarpa
- / ericaceae
- / Lyonia
- / triterpenoid glycosides
- / antitumor activities
-
杜鹃花科(Ericaceae)珍珠花属(Lyonia)植物为落叶灌木或小乔木, 全世界约有35种, 主要分布在亚洲东部和北美地区.我国有6种和5变种, 多分布于东部和西南部[1].毛果南烛(Lyonia ovalifolia var. hebecarpa), 也称为毛果珍珠花、毛果米饭花, 是珍珠花(L. ovalifolia)的一个变种, 生于海拔1400~3400 m的阳坡灌丛中, 主要产于江苏、安徽、浙江、广东、广西、四川、云南西北部等地, 茎、叶可药用, 有强筋益气、收敛止泻效用.文献调研发现, 日本学者早在1959年就开始对珍珠花的变种小果珍珠花(L. ovalifolia var. elliptica)进行了研究[2~9], 最近几年才开始对原变种珍珠花(L. ovalifolia var. ovalifolia)[10~16]进行研究, 从中分离得到了二萜[6, 7, 10, 12]、三萜[8, 9, 11]、木脂素[2, 3, 5, 13, 14, 16]、黄酮[4, 15, 16]等多种结构类型的化合物, 部分化合物具有显著的抗菌[10]、抗病毒活性[11]和神经药理活性[12].然而, 对变种毛果南烛(L. ovalifolia var. hebecarpa)的化学成分研究较少[17], 仅分离得到了一个新的megastigamane型倍半萜苷化合物毛果南烛素甲, 以及β-谷甾醇和胡萝卜苷, 但未报道其生物活性.为了进一步开发利用毛果南烛, 本文对采自浙江缙云县的毛果南烛(Lyonia ovalifolia var. hebecarpa)叶子进行了化学成分研究, 从中分离得到了3个三萜皂苷类化合物, 借助HRESIMS和NMR等现代波谱手段以及化学方法鉴定了其结构.其中化合物1及其苷元1a是新化合物, 已知化合物2和3均为首次从该植物中分离得到, 并首次报道了化合物2及其苷元2a的NMR数据归属.此外, 筛选了所得3个三萜皂苷化合物1~3的体外抗肿瘤活性, 结果显示化合物2对五种肿瘤细胞HL-60、MCF-7、SMMC-7221、A-549和SW480的增殖均有显著的抑制作用, 且对MCF-7、A-549和SW480细胞增殖的抑制活性优于阳性对照药物顺铂.本文将报道毛果南烛叶3个三萜皂苷类化合物1~3的提取、分离、结构鉴定和抗肿瘤活性.
1 结果与讨论
毛果南烛叶子用95%乙醇提取三次, 提取物液合并、减压浓缩后得浸膏, 用温水混悬后, 依次用石油醚、氯仿、乙酸乙酯和正丁醇萃取得四个部位.氯仿部位经正相硅胶、反相硅胶和Sephadex LH-20等反复柱层析, 最后经HPLC纯化分离得到3个三萜皂苷类化合物1~3, 结构见图 1.
 图1
三萜皂苷化合物1~3以及化合物1和2的苷元1a和2a的化学结构
Figure1.
Chemical structures of triterpenoid glycosides 1~3, and the aglycones 1a and 2a of compounds 1 and 2
图1
三萜皂苷化合物1~3以及化合物1和2的苷元1a和2a的化学结构
Figure1.
Chemical structures of triterpenoid glycosides 1~3, and the aglycones 1a and 2a of compounds 1 and 2
1.1 新化合物1的结构鉴定
化合物1为白色粉末, 易溶于甲醇.化合物1的高分辨电喷雾质谱(HRESIMS)在m/z 613.4097处显示出[M+Na]+离子峰, 结合化合物1的13C NMR数据推测, 其分子式为C35H58O7 (C35H58O7Na的计算值为613.4080), 计算其不饱和度为7.
化合物1的1H NMR (表 1)谱图中在δH 5.18 (t, J=3.3 Hz, H-12) 处显示1个烯质子信号, 在δH 0.77 (s, H3-24), 0.86 (s, H3-28), 0.88 (s, H3-29), 0.89 (s, H3-30), 1.12 (s, H3-26), 1.17 (s, H3-27) 处显示6个单峰甲基信号, 在δH 4.01 (d, J=12.3 Hz, H-25a), 4.07 (d, J=12.3 Hz, H-25b), 3.29 (d, J=11.5 Hz, H-23a), 3.63 (d, J=11.5 Hz, H-23b)处显示两组具有AB自旋系统的连氧亚甲基信号, 在δH 4.33 (d, J=6.8 Hz, H-1'), 3.52~3.55 (m, H-2'), 3.51 (d, J=3.3 Hz, H-3'), 3.78~3.81 (m, H-4'), 3.55 (dd, J=12.3, 2.7 Hz, H2-5'a), 3.85 (dd, J=12.3, 2.7 Hz, H2-5'b)显示出一组典型的阿拉伯吡喃糖的信号[10].
 表 1
化合物1, 1a, 2和2a的1H NMR (δH, J in Hz, 400 MHz, CD3OD)波谱数据
Table 1.
1H NMR (δH, J in Hz, 400 MHz, CD3OD) spectroscopic data of compounds 1, 1a, 2 and 2a
表 1
化合物1, 1a, 2和2a的1H NMR (δH, J in Hz, 400 MHz, CD3OD)波谱数据
Table 1.
1H NMR (δH, J in Hz, 400 MHz, CD3OD) spectroscopic data of compounds 1, 1a, 2 and 2a
No. 1 1a 2 2a 1α 0.79, dd, 13.1, 4.8 0.79, dd, 13.2, 4.8 3.34, dd, 12.1, 3.4 3.34, dd, 11.8, 3.1 1β 2.29, dt, 13.1, 3.4 2.30, dt, 13.2, 3.4 2α 0.97~1.02, m 0.98~1.02, m 0.98~1.01, m 0.98~1.01, m 2β 1.84~1.88, m 1.84~1.88, m 1.82~1.88, m 1.82~1.86, m 3α 3.63, dd, 5.2, 11.3 3.64, dd, 5.1, 11.3 3.66, dd, 5.7, 12.8 3.65, dd, 5.7, 12.9 5α 1.74~1.79, m 1.69~1.74, m 1.12~1.14, m 1.12~1.14, m 6α 1.07~1.11, m 1.09~1.11, m 1.08~1.11, m 1.09~1.11, m 6β 1.35~1.39, m 1.35~1.41, m 1.51~1.54, m 1.51~1.55, m 7α 1.68, ddd, 16.5, 12.3, 4.8 1.66, ddd, 16.5, 12.3, 4.8 1.62, ddd, 16.2 12.2, 4.8 1.62, ddd, 16.2, 12.2, 4.5 7β 1.32, ddd, 16.5, 5.2, 3.4 1.32, ddd, 16.5, 5.2, 3.4 1.31, dt, 12.3, 2.8 1.31, dt, 12.3, 2.8 9α 1.70, dd, 5.9, 11.9 1.71, dd, 5.4, 11.5 1.82, dd, 11.4, 5.8 1.83, dd, 11.3, 5.9 11α 2.04, ddd, 16.5, 12.0, 5.7 2.10, ddd, 16.5, 12.0, 5.7 2.07, ddd, 16.6, 12.4, 3.4 2.07, ddd, 14.1, 13.3, 3.4 11β 2.46, ddd 16.5, 12.0, 5.7 2.46, ddd, 16.5, 12.0, 5.7 2.47, ddd, 16.6, 12.3, 4.8 2.47, ddd, 14.1, 13.5, 4.4 12 5.18, t, 3.3 5.17, t, 3.4 5.18, t, 3.5 5.18, t, 3.5 15α 0.97~1.03, m 0.97~1.03, m 0.97~0.99, m 0.97~0.99, m 15β 2.01~2.07, m 2.01~2.07, m 2.01~2.07, m 2.01~2.07, m 16α 0.95~1.00, m 0.99~1.11, m 0.97~1.03, m 0.97~1.02 m 16β 1.80~1.82, m 1.82~1.87, m 1.72~1.77, m 1.76~1.78, m 18β 1.92, dd, 13.4, 3.6 1.93, dd, 13.4, 3.6 1.92, dd, 12.4, 4.6 1.96, dd, 13.6, 4.0 19α 0.98~1.01, m 0.97~1.02, m 0.99~1.02, m 1.00~1.03, m 19β 1.69~1.74, m 1.68~1.73, m 1.71~1.75, m 1.70~1.76, m 21α 1.09~1.12, m 1.09~1.12, m 1.09~1.13, m 1.10~1.13, m 21β 1.34~1.40, m 1.34~1.40, m 1.37~1.39, m 1.38~1.42, m 22α 1.45, dd, 12.7, 3.5 1.45, dd, 12.7, 3.5 1.45, dd, 12.7, 3.4 1.45, dd, 12.7, 3.4 22β 1.23, dt, 12.7, 3.2 1.23, dt, 12.7, 3.2 1.23, dt, 12.7, 3.2 1.23, dt, 12.7, 3.2 23a 3.29, d, 11.5 3.29, d, 11.5 3.28, d, 11.2 3.30, d, 11.2 23b 3.63, d, 11.5 3.53, d, 11.5 3.60, d, 11.2 3.62, d, 11.2 24 0.77, s 0.75, s 0.70, s 0.68, s 25a 4.01, d, 12.3 3.98, d, 12.6 1.01, s 1.01, s 25b 4.07, d, 12.3 4.08, d, 12.6 26 1.12, s 1.11, s 1.03, s 1.02, s 27 1.17, s 1.17, s 1.18, s 1.17, s 28 0.86, s 0.86, s 0.84, s 0.85, s 29 0.88, s 0.88, s 0.88, s 0.88, s 30 0.89, s 0.89, s 0.89, s 0.89, s 1' 4.33, d, 6.8 4.32, d, 6.7 2' 3.52~3.55, m 3.50~3.54 m 3' 3.51, d, 3.3 3.51, d, 3.3 4' 3.78~3.81, m 3.78~3.81, m 5'a 3.55, dd, 12.3, 2.7 3.55, dd, 12.3, 2.7 5'b 3.85, dd, 12.3, 2.7 3.85, dd, 12.3, 2.7 在13C NMR (表 2)谱中显示化合物1有35个碳信号, 结合其DEPT和HSQC谱, 可以将35个碳信号归属为6个甲基(δC 13.8, C-24; 18.2, C-26; 27.2, C-27; 29.1, C-28; 34.0, C-29; 24.2, C-30); 13个亚甲基, 其中包含3个连氧亚甲基(δC 62.4, C-25; 65.1, C-23; 66.9, C-5'); 9个次甲基, 其中包含5个连氧次甲基(δC 69.9, C-4'; 73.1, C-2'; 74.9, C-3'; 83.7, C-3; 106.6, C-1')和1个sp2杂化次甲基(δC 124.1, C-12); 7个季碳, 其中包含6个sp3杂化季碳(δC32.1, C-20; 33.7, C-17; 41.4, C-8; 42.1, C-14; 43.3, C-10; 44.0, C-4) 和1个sp2杂化季碳(δC 146.1, C-13).化合物1糖部分的13C NMR数据(δC 66.9, C-5'; 69.9, C-4'; 73.1, C-2'; 74.9, C-3'; 106.6 C-1')与文献报道的3α-[(α-L-arabi-nopyranosyl)-oxy]-24S-[(α-L-arabinopyranosyl)-oxy]-25-hydroxy-9, 10-seco-cycloartan-1(10)-en-30-oic acid的阿拉伯糖部分13C NMR数据基本一致[11], 初步证实化合物1的糖部分是阿拉伯吡喃糖.从化合物1的分子式C35H58O7可知其不饱和度为7, 分子中还有的一个双键和一个阿拉伯吡喃糖环各占去一个不饱和度, 还剩5个不饱和度, 说明分子中还应有五个环.因此, 化合物1可能是一个五环三萜阿拉伯吡喃糖苷化合物.
 表 2
化合物1, 1a, 2和2a的13C NMR波谱数据(100 MHz, CD3OD)
Table 2.
13C NMR (100 MHz, CD3OD) spectroscopic data of compounds 1, 1a, 2, and 2a
表 2
化合物1, 1a, 2和2a的13C NMR波谱数据(100 MHz, CD3OD)
Table 2.
13C NMR (100 MHz, CD3OD) spectroscopic data of compounds 1, 1a, 2, and 2a
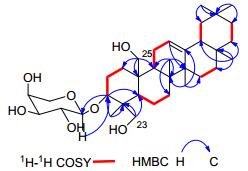
No. 1 1a 2 2a 1 34.5 34.5 80.7 80.6 2 33.4 33.7 37.0 38.0 3 83.7 74.0 80.4 71.1 4 44.0 43.5 44.0 44.0 5 48.2 48.1 46.0 46.7 6 18.6 18.9 18.6 18.9 7 27.4 27.4 33.5 33.6 8 41.4 41.4 41.7 41.7 9 49.7 49.9 49.8 49.9 10 43.3 43.3 44.0 43.5 11 26.5 26.5 28.4 28.4 12 124.1 124.0 124.4 124.4 13 146.1 146.1 145.4 145.4 14 42.1 42.3 43.0 42.9 15 28.2 28.1 28.2 28.1 16 27.4 27.4 27.5 27.5 17 33.7 33.7 33.7 33.7 18 48.8 48.7 48.7 48.7 19 48.2 48.2 48.2 48.2 20 32.1 32.1 32.1 32.1 21 36.0 36.0 36.0 36.0 22 38.4 38.4 38.4 38.4 23 65.1 67.4 64.8 66.9 24 13.8 13.1 13.3 13.1 25 62.4 62.3 12.6 12.7 26 18.2 18.2 18.0 18.0 27 27.2 27.2 26.7 26.7 28 29.1 29.1 29.1 29.1 29 34.0 34.0 34.0 34.0 30 24.2 24.2 24.2 24.2 1' 106.6 106.6 2' 73.1 73.1 3' 74.9 74.7 4' 69.9 69.9 5' 66.9 67.1 除了阿拉伯吡喃糖部分以外, 化合物1的苷元部分的NMR数据与文献报道的(3β)-olean-12-ene-3, 23-diol[18]的NMR数据相似, 主要不同之处在于化合物1中有一个连氧亚甲基(δH 4.01, d, J=12.3 Hz, H-25a; 4.07, d, J=12.3 Hz, H-25b; δC 62.4, C-25), 取代了已知化合物(3β)-olean-12-ene-3, 23-diol中的甲基(δH 0.99, s, H3-25; δC 16.1, C-25).化合物1中的HMBC谱图中出现的从H2-25到C-1 (δC 34.5), C-5 (δC 48.2), C-9 (δC 49.7) 和C-10 (δC 43.3) 的交叉峰说明了连氧亚甲基C-25确实连在C-10上.此外, 化合物1中出现的阿拉伯吡喃糖的端基质子H-1' (δH 4.33, d, J=6.8 Hz)到C-3 (δC 83.7) 的HMBC相关峰, 以及H-3 (δH 3.63, dd, J=5.2, 11.3 Hz)到阿拉伯吡喃糖的端基碳C-1' (δC 106.6) 的HMBC相关峰说明阿拉伯吡喃糖连接在C-3上.综合分析化合物1的1H-1H COSY, HSQC和HMBC相关二维谱图(图 2), 可以确定化合物1的平面结构为3-O-阿拉伯吡喃糖氧基-齐墩果-12-烯-23, 25-二醇.
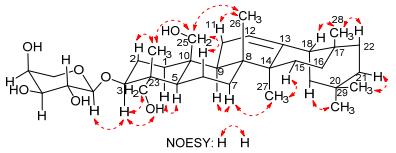
化合物1的相对构型(图 3)是通过偶合常数和NOESY谱图分析来确定的. H-3 (δ 3.63, dd)与H2-2的偶合常数分别为J=5.2和11.3 Hz, 偶合常数较大说明H-3处于环己烷椅式构象的直立键(a键)上.因此H-3应为ɑ方向[18], 相应的C-3位氧苷键处在β方向.在化合物1的NOESY谱图中, H-3与H-23 (δH 3.29, d)之间有交叉峰, 说明H2-23也处在ɑ方向, 那么C-4上的甲基24-CH3 (δH 0.77, s)就在β方向. 24-CH3与H2-25 (δH 4.01, 4.07) 存在NOESY相关, 说明H2-25也在β方向, 这与经典的齐墩果烷三萜化合物的相对构型一致[19].化合物1的其它NOESY相关信息进一步确定了其相对构型(图 3).
为了确定阿拉伯吡喃糖的绝对构型, 将化合物1 (6 mg)进行酸水解, 并进一步分离纯化, 分别得到了苷元1a (1.2 mg)和阿拉伯糖(0.5 mg).水解得到的阿拉伯糖(0.5 mg)溶于无水吡啶, 在65 ℃下与2 mg L-半胱氨酸甲酯盐酸盐反应2 h, 制备阿拉伯糖的手型噻唑啉衍生物.不经分离, 直接加入N-三甲基硅咪唑继续反应1.5 h, 生成阿拉伯糖手型噻唑啉衍生物的三甲基硅醚衍生物.用同样的方法制备标准L-和D-阿拉伯糖的三甲基硅醚衍生物.之后用气相色谱(GC)在同样条件下分析三种阿拉伯糖的三甲基硅醚衍生物的保留时间.结果显示, 化合物1中阿拉伯糖、标准D-和L-阿拉伯糖的硅烷化衍生物的保留时间分别为8.906、9.136和8.829 min, 由此可以确定化合物1中的糖为L-阿拉伯糖.化合物1中阿拉伯吡喃糖端基质子(δ 4.33, d)的偶合常数J=6.8 Hz, 由此可以确定化合物1中阿拉伯糖的构型为ɑ-L-阿拉伯吡喃糖.
除了得到阿拉伯糖外, 酸水解化合物1还得到苷元1a, 通过比较1a和(3β)-olean-12-ene-3, 23-diol[18]的NMR数据相似, 并经1H-1H COSY, HSQC, HMBC和NOESY等2D NMR数据分析确定其结构为齐墩果-12-烯-3β, 23, 25-三醇.齐墩果烷类三萜化合物的绝对构型均已确定[19], 且没有对映-齐墩果烷类三萜化合物报道, 因此, 从生源关系角度可以推测其绝对构型为3S*, 4R*, 5R*, 8R*, 9S*, 10S*, 14S*, 17R*, 18R*.
综上所述, 化合物1的结构确定为3β-O-ɑ-L-阿拉伯吡喃糖氧基-齐墩果-12-烯-23, 25-二醇.
1.2 化合物2的结构鉴定
化合物2为白色粉末, 易溶于甲醇. HRESIMS 在m/z: 613.4078显示该化合物的[M+Na]+为准分子离子峰, 结合化合物的NMR数据, 推测其分子式为C35H58O7 (C35H58O7Na理论计算值为613.4080), 与化合物1的分子式一致, 其不饱和度为7.
考虑到化合物2和1具有相同的分子式, 化合物2应该是化合物1的同分异构体, 可能主要是氧化位置不同.化合物2的NMR数据(表 1和2)和化合物1的NMR数据有一定的相似性, 主要的不同之处在于: (1) 化合物2的1H NMR中有1个甲基信号(δH 1.01, s, H3-25; δC 12.6, C-25), 而没有化合物1中连氧亚甲基信号(δH 4.01, d, J=12.3 Hz, H-25a; 4.07, d, J=12.3 Hz, H-25b; δC 62.4, C-25); (2) 化合物2有一个连氧次甲基(δH 3.34, dd, H-1; δC 80.7, C-1), 而不是化合物1的亚甲基(δC 34.5, C-1).因此, 化合物2是化合物1的1-OH衍生物, 且C-25为甲基.化合物2的HMBC谱中, 从Me-25到C-1 (δC 80.7), C-5 (δC 46.0), C-9 (δC 49.8) 和C-10 (δC 44.0) 的相关峰, 说明25-Me连在C-10季碳上, 且C-1位有羟基取代.
酸水解化合物2得到阿拉伯糖和苷元2a.采用化合物1中糖部分绝对构型的化学方法, 鉴定了化合物2中的阿拉伯糖为L-阿拉伯吡喃糖.经NMR数据分析, 并采用1H-1H COSY、HSQC、HMBC和NOESY等二维NMR技术, 苷元化合物2a的结构为齐墩果-12-烯-1β, 3β, 23-三醇.最终确定化合物2的结构为3β-O-α-L-阿拉伯吡喃糖氧基-齐墩果-12-烯-1β, 23-二醇.
检索Scifinder Scholar数据库发现, 该化合物最早于1974年从小果珍珠花L. ovalifolia var. elliptica[9]中分离得到, 但是文献中仅报道了该化合物的7个甲基1H NMR信号, 而没有报道其它质子的信号及其归属, 更没有报道其13C NMR数据.本文利用1D和2D NMR技术, 首次报道了化合物2及其苷元2a的1H NMR和13C NMR谱数据, 数据归属见表 1和2.化合物2为首次从毛果南烛L. ovalifolia var. hebecarpa中分离得到.
1.3 化合物3的结构鉴定
经1H NMR、13C NMR和HRESIMS等波谱方法分析, 并与文献数据[11]对照, 确定了化合物3的结构为3β-O-β-D-葡萄吡喃糖基-24-ɑ-L-阿拉伯吡喃糖基-9, 10-开环-羊毛甾-10-烯-25-羟基-30-酸.化合物3为首次从毛果南烛L. ovalifolia var. hebecarpa中分离得到.
1.4 抗肿瘤活性研究
本文采用MTS [3-(4, 5-二甲基吡啶-2-基-5-(3-羧基甲氧基苯基)-2-(4-磺苯基)-2H-四唑]法[20], 以顺铂(DDP)为阳性对照, 筛选了从毛果南烛中分离得到的化合物1~3对五种肿瘤细胞: HL-60 (人早幼粒白血病细胞)、MCF-7(乳腺癌细胞)、SMMC-7221(人肝癌细胞)、A-549(人肺腺癌细胞)和SW480(人结肠癌细胞)的抗增殖活性.先在40 μmol•L−1浓度下对化合物进行初步筛选, 如果抑制率>50%, 再设置40、8、1.6、0.32、0.064 μmol•L−1五个浓度梯度复筛, 根据五个浓度下的抑制率计算半数抑制浓度(IC50)值.结果(表 3)显示, 化合物1和3在40 μmol•L−1浓度下对5种肿瘤细胞增殖的抑制作用均低于50%, 未表现出显著的抗增殖活性.而化合物2对五种肿瘤细胞株HL-60、MCF-7、SMMC-7221、A-549和SW480的细胞增殖均有显著的抑制作用, IC50分别为(16.35±0.25)、(17.05±0.52)、(17.66±0.21)、(15.87±0.26) 和(12.30±0.36) μmol•L−1.阳性药DDP对五种肿瘤细胞株IC50值分别为(3.42±0.17)、(35.02±2.17)、(13.23±1.17)、(28.23±2.95) 和(26.90±1.93) μmol•L−1.因此, 化合物2对MCF-7、A-549和SW480增殖的抑制作用要强于阳性药DDP.
 表 3
化合物1~3对五种肿瘤细胞株的增殖抑制作用a
Table 3.
Anti-proliferative activities of compounds 1~3 against five cancer cell lines
表 3
化合物1~3对五种肿瘤细胞株的增殖抑制作用a
Table 3.
Anti-proliferative activities of compounds 1~3 against five cancer cell lines
化合物 白血病HL-60 乳腺癌MCF-7 肝癌SMMC-7221 肺癌A-549 结肠癌SW480 1 >40 >40 >40 >40 >40 2 16.35±0.25 17.05±0.52 17.66±0.21 15.87±0.26 12.30±0.36 3 >40 >40 >40 >40 >40 DDPb 3.42±0.17 35.02±2.17 13.23±1.17 28.23±2.95 26.90±1.93 a半数抑制浓度(IC50)采用平均值(mean)±标准方差(SD)表示, 单位: μmol•L−1. b DDP:阳性对照药顺铂(cisplatin). 化合物1和2都是齐墩果烷阿拉伯糖苷类化合物, 结构也比较类似, 但是活性却有较大差别.比较二者的结构, 推测1β-OH可能是其活性基团, 不可缺少.这一初步结果为基于齐墩果烷类三萜化合物的抗肿瘤先导化合物的结构修饰提供依据.
2 结论
本文利对毛果南烛L. ovalifolia var. hebecarpa叶子的化学成分进行了初步研究, 从中分离得到了3个三萜皂苷类化合物.利用现代波谱技术并结合化学方法鉴定了3个化合物的结构, 其中化合物1为新化合物, 已知化合物2和3为首次从毛果南烛L. ovalifolia var. hebe-carpa中分离得到.并对所得的3个化合物进行了体外抗肿瘤活性评价, 发现化合物2对五种肿瘤细胞株HL-60、MCF-7、SMMC-7221、A-549和SW480的细胞增殖都表现出了显著的抑制作用, 而且对MCF-7、A-549和SW480肿瘤细胞增殖的抑制作用超过了阳性对照药物顺铂,
3 实验部分
3.1 仪器与试剂
旋光度由Rudolph-Autopol Ⅳ型数字旋光仪测定; NMR由Bruker AM-400核磁共振仪测定, 1H NMR位移值以氘代溶剂中残存的CD3OD (δH 3.31) 为内标, 13C NMR位移值以CD3OD (δC 49.15) 为内标, 高分辨电喷雾质谱(HRESIMS)由 Bruker micrOTOF Ⅱ spectrometer质谱仪测定; 化合物最终纯化由戴安P680高效液相色谱仪, UVD170紫外检测器, 反向C-18柱子(250 mm×10 mm, Welch)完成; 糖部分绝对构型鉴定采用Agilent 7820A气相质谱仪分析; 活性检测利用多功能酶标仪(Multiskan FC)完成.层析用硅胶(100~200, 200~300目)及TLC薄层板(HSGF-254) 由烟台江友硅胶开发有限公司提供; ODS填料为YMC GEL ODS-AS 50 μm, Japan; 凝胶Sephadex LH-20, GE Healthcare Bioscience AB, Sweden.色谱甲醇、乙腈, Sigma; 二氯甲烷、石油醚、氯仿、正己烷等各种溶剂均为分析纯, 由国药集团化学试剂有限公司提供.
3.2 植物材料
毛果南烛(L. ovalifolia var. hebecarpa)叶于2015年6月采自浙江省缙云县, 由温州大学丁炳杨教授鉴定.样品标本保存在华中科技大学同济医学院药学院天然药物化学教研室, 编号2015-0616.
3.3 提取、分离
干燥毛果南烛叶50 kg经粉碎, 用95%乙醇(24 h/次, 220 L, 45 ℃)提取3次, 减压浓缩得到总浸膏9.15 Kg.将总浸膏加适量蒸馏水混悬, 依次用石油醚、氯仿、乙酸乙酯和正丁醇萃取, 氯仿部位得到萃取物5.09 kg.氯仿提取物用100~200目硅胶按照质量1:1拌样, 以CH2Cl2-MeOH (V:V=50:1~0:1) 进行洗脱, 得到14个部分Fr.1~Fr.14.经TLC薄层色谱检测与本实验室已有的熊果酸和齐墩果酸标准品对比, 发现Fr.1~Fr.6的主要成分是熊果酸和齐墩果酸, 薄层色谱(TLC)拖尾严重, 并含有大量叶绿素.而Fr.7部分除了含有熊果酸和齐墩果酸和叶绿素外, TLC板显示Fr.7还含有极性较大的新点.因此, 在后续分离过程中均以TLC薄层色谱检测法为指导, 来分离得到Fr.7中极性较大的新点. Fr.7 (43.5 g)经正相硅胶柱层析分离, 以CH2Cl2-MeOH (V:V=40:1~0:1) 进行梯度洗脱, 得到9个组分Fr.7.1~Fr.7.9.其中, V(CH2Cl2):V(MeOH)=15:1洗脱得到的组分Fr.7.4含有极性较大的新点.所以Fr.7.4 (6.4 g)经反相ODS柱层析分离, 以MeOH-H2O (V:V=10:1~100:0) 进行梯度洗脱得到14个部分Fr.7.4.1~Fr.7.4.14.量较大的组分Fr.7.4.3 (5 g)经反复正相硅胶、反相硅胶、凝胶Sephadex LH-20柱层析进一步细分纯化, 得到组分Fr.7.4.3.1~Fr.7.4.3.3. Fr.7.4.3.1 (43.0 mg)经半制备HPLC进一步分离, 以流动相MeCN-H2O (V:V=75:25, 流速: 1.5 mL/min), 得到化合物1 (12 mg, tR 35.3 min); Fr.7.4.3.2 (4.2 g)也经反复正相硅胶、反相硅胶、凝胶Sephadex LH-20纯化, 得到粗品(3.8 g).取其中的150 mg经HPLC纯化, 以流动相MeCN-H2O (V:V=100:0, 流速1.5 mL/min), 得到化合物2 (117 mg, tR 25.1 min). Fr.7.4.3.3 (102 mg)经正相硅胶、半制备HPLC进一步分离, 以流动相MeCN-H2O (V:V=70:30, 流速: 1.5 mL/min), 得到化合物3 (3.8 mg, tR 38.4 min).
3β-O-ɑ-L-阿拉伯吡喃糖氧基-齐墩果-12-烯-23, 25-二醇(1):白色粉末, 易溶于甲醇. [a]D25+43 (c 0.12, MeOH); 1H NMR (CD3OD, 400 MHz)和13C NMR (CD3OD, 100 MHz)数据见表 1和2. HRESIMS calcd for C35H58O7Na [M+Na]+ 613.4080, found 613.4097.
3β-O-α-L-阿拉伯吡喃糖氧基-齐墩果-12-烯-1β, 23-二醇(2):白色粉末, 易溶于甲醇. [a]D25+90 (c 0.70, MeOH); 1H NMR (CD3OD, 400 MHz)和13C NMR (CD3OD, 100 MHz)数据见表 1和2. HRESIMS calcd for C35H58O7Na [M+Na]+ 613.4080, found 613.4078.
3.4 化合物1和2的酸水解及苷元1a和2a的制备
将化合物1 (6 mg)溶于0.2 mL甲醇中, 加入3 mol/L的HCl水溶液, 75 ℃下水解7 h, 反应液减压蒸干至中性, 加入1 mL蒸馏水混匀, 再用1 mL乙酸乙酯萃取3次.水层减压浓缩蒸干得到阿拉伯糖(0.5 mg).乙酸乙酯萃取物合并, 减压浓缩至干得粗苷元, 经半制备HPL C纯化(检测波长205 nm, MeCN-H2O, V:V=81:19, 流速: 1.5 mL/min), 得到纯的齐墩果-12-烯-3β, 23, 25-三醇(1a) (1.2 mg, tR 31.3 min)[11], 白色粉末, 易溶于甲醇. [α]D25+81 (c 0.16, MeOH); 1H NMR (CD3OD, 400 MHz)和13C NMR (MeOD, 100 MHz)数据见表 1; HRESIMS calcd for C30H50O3Na [M+Na]+ 481.3658, found 481.3667.
采用上述方法, 酸水解化合物2 (8 mg)得到阿拉伯糖(0.7 mg)和苷元(2.6 mg), 苷元部分经半制备HPLC纯化(检测波长205 nm, MeCN-H2O, V:V=100:0, 流速: 1.5 mL/min), 得到纯的齐墩果-12-烯-1β, 3β, 23-三醇(2a) (1.6 mg, tR 41.1 min), 白色粉末, 易溶于甲醇. [a]D25+66 (c 0.12, MeOH); 1H NMR (CD3OD, 400 MHz)和13C NMR (CD3OD, 100 MHz)数据见表 1和2. HRESIMS calcd for C30H50O3Na [M+Na]+ 481.3658, found 481.3660.
3.5 化合物1和2中糖的绝对构型的确定
分别向水解化合物1和2所得的阿拉伯糖(0.5 mg)、标准D-阿拉伯糖(1 mg)和L-阿拉伯糖(1 mg)中分别加入2 mg的L-半胱氨酸甲酯盐酸盐, 0.2 mL的无水吡啶, 65 ℃下反应2 h.随后在混合液中加入0.2 mL N-三甲基硅咪唑, 65 ℃下继续反应1.5 h, 减压浓缩至干, 加入1 mL蒸馏水, 用0.2 mL正己烷萃取.正己烷萃取物用GC检测[11].
GC检测条件: WM-1毛细管柱(30 m×0.25 mm×0.5 μm, Welch); 柱温: 230 ℃保留5 min, 10 ℃/min升温到270 ℃, 进样口温度: 250 ℃, 载气: N2, 1.0 mL/min, 分流比: 10:1; FID检测器, 检测温度: 250 ℃.
化合物1和2水解所得阿拉伯糖以及标准L-阿拉伯糖和D-阿拉伯糖的衍生物在同样GC条件下的保留时间分别8.906、8.820、8.829和9.136 min, 因此, 化合物1和2中的糖为L-阿拉伯糖.
3.6 抗肿瘤活性测试
MTS为一种全新的MTT类似物, 全称为3-(4, 5-二甲基吡啶-2-基)-5-(3-羧基甲氧基苯基)-2-(4-磺苯基)-2H-四唑, 是一种黄颜色的染料.活细胞线粒体中琥珀酸脱氢酶能够代谢还原MTS, 生成可溶性的甲臜(Formazan)化合物, 甲臜的含量可以用酶标仪在492 nm处进行测定.在通常情况下, 甲臜生成量与活细胞数成正比, 因此可根据光密度OD值推测出活细胞的数目[20].
本文通过采用MTS法[20]测试化合物1~3对五种肿瘤细胞株HL-60(人早幼粒白血病细胞)、MCF-7(乳腺癌细胞)、SMMC-7221(人肝癌细胞)、A-549(人肺腺癌细胞)和SW480(人结肠癌细胞)的抗增殖活性, 从而评价其体外抗肿瘤活性.主要方法是用含10%胎牛血清的培养液(DMEM)配成单个细胞悬液, 以每孔5000个细胞接种到96孔板, 每孔体积100 μL, 化合物用DMSO溶解, 以终浓度40 μmol•L−1初筛, 每孔终体积200 μL, 每种处理均设3个复孔. 37℃培养48 h, 弃上清液, 每孔加20 μL的MTS溶液(MTS溶液20 μL和培养液100 μL的混合液), 继续孵育2~4 h, 使反应充分, 利用多功能酶标仪在492 nm处测定光吸收值, 记录结果.抑制率计算公式: [1-(OD实验组-OD空白组)÷(OD对照组-OD空白组)]×100%.在40 μmol•L−1浓度下对肿瘤细胞生长抑制率大于50%的化合物进入梯度复筛, 设五个浓度40、8、1.6、0.32和0.064 μmol•L−1, 每孔终体积200 μL, 设3个平行孔, 以浓度为横坐标, 细胞存活率为纵坐标绘制细胞生长曲线, 应用两点法(Reed and Muench法)计算化合物的IC50值.
致谢 感谢温州大学丁炳杨教授鉴定植物材料.华中科技大学分析测试中心测试谱图数据.
辅助材料(Supporting Information) 化合物1、1a、2和2a的HRESIMS、1H NMR、13C NMR、DEPT、HSQC、HMBC、1H-1H COSY、NOESY及化合物1和2经酸水解得到的阿拉伯糖、标准L-阿拉伯糖和D-阿拉伯糖的手性噻唑啉TSIM衍生物GC分析谱图.这些材料可以免费从本刊网站(http://sioc-journal.cn/)上下载.
-
-
[1]
Fang, M.; Fang, R.; He, M.; Hu, L.; Yang, H.; Qin, H.; Min, T.; Chamberlain, D. F.; Stevens, P. F.; Wallace, G. D.; Anderberg, A. Ericaceae. In Flora of China, Vol. 14, Eds.:Wu, Z. Y.; Raven, P. H.; Hong, D. Y., Science Press, Beijing & Missouri Botanical Garden Press, St. Louis, 2005, p. 242.
-
[2]
Yasue, M.; Kato, Y. Yakugaku Zasshi 1959, 79, 403. doi: 10.1248/yakushi1947.79.3_403
-
[3]
Kato, Y. Phytochemistry 1973, 12, 2302. doi: 10.1016/0031-9422(73)85143-X
-
[4]
Kato, Y.; Yasue, M. Shoyakugaku Zasshi 1983, 37, 412.
-
[5]
Kato, Y.; Kato, N.; Baba, M. Pharmazie 1984, 39, 425.
-
[6]
Ohta, T.; Hikino, H. Chem. Pharm. Bull. 1981, 29, 280. doi: 10.1248/cpb.29.280
-
[7]
Sakakibara, J.; Ikai, K.; Yasue, M. Yakugaku Zasshi 1974, 94, 1534. doi: 10.1248/yakushi1947.94.12_1534
-
[8]
Sakakibara, J.; Hotta, Y.; Yasue, M. Yakugaku Zasshi 1975, 95, 911. doi: 10.1248/yakushi1947.95.8_911
-
[9]
Sakakibara, J.; Hotta, Y.; Yasue, M. Yakugaku Zasshi 1974, 94, 170. doi: 10.1248/yakushi1947.94.2_170
-
[10]
Lv, X. J.; Li, Y.; Ma, S. G.; Qu, J.; Liu, Y. B.; Li, L.; Wang, R. B.; Yu, S. S. Tetrahedron 2017, 73, 776. doi: 10.1016/j.tet.2016.12.060
-
[11]
Lv, X. J.; Li, Y.; Ma, S. G.; Qu, J.; Liu, Y. B.; Li, Y. H.; Zhang, D.; Li, L.; Yu, S. S. J. Nat. Prod. 2016, 79, 2824. doi: 10.1021/acs.jnatprod.6b00585
-
[12]
Wu, Z. Y.; Li, H. Z.; Wang, W. G.; Li, H. M.; Chen, R.; Li, R. T.; Luo, H. R. Chem. Biodiversity 2011, 8, 1182. doi: 10.1002/cbdv.v8.6
-
[13]
Kashima, K.; Sano, K.; Yunity, Y. S.; Ina, H.; Kunugi, A.; Inoue, H. Chem. Pharm. Bull. 2010, 58, 191. doi: 10.1248/cpb.58.191
-
[14]
Rahman, M. A.; Katayama, T.; Suzuki, T.; Nakagawa, T. J. Wood Sci. 2007, 53, 161. doi: 10.1007/s10086-006-0832-1
-
[15]
Subramanian, S. S.; Kotiyal, J. P. Indian J. Pharm. Sci. 1978, 40, 131.
-
[16]
Yasue, M.; Sakakibara, J.; Nakagami, J. Yakugaku Zasshi 1974, 94, 1349. doi: 10.1248/yakushi1947.94.10_1349
-
[17]
王彩芳, 刘延泽, 李灿军, 陈绍农, 秦国伟, 河南医科大学学报, 2001, 36, 743. doi: 10.3969/j.issn.1671-6825.2001.06.043Wang, C.; Liu, Y.; Li, C.; Chen, S.; Qin, G. J. Henan Med. Univ. 2001, 36, 743(in Chinese). doi: 10.3969/j.issn.1671-6825.2001.06.043
-
[18]
Wang, K. W.; Sun, H, X. Wu, B.; Pan, Y. J. Helv. Chim. Acta 2005, 88, 990. doi: 10.1002/(ISSN)1522-2675
-
[19]
熊娟, 黄亚, 唐宁, 尤梅, 胡金锋, 有机化学, 2013, 33, 1304. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract342081.shtmlXiong, J.; Huang, Y.; Tang, N.; You, M.; Hu, J. Chin. J. Org. Chem. 2013, 33, 1304(in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract342081.shtml
-
[20]
Zheng, H.; Chen, Q.; Zhang, M.; Lai, Y.; Lei, L.; Shu, P.; Xue, Y.; Luo, Z.; Zhang, J.; Li, Y.; Yao, G.; Zhang, Y. J. Nat. Prod. 2013, 76, 2253. doi: 10.1021/np400600c
-
[1]
-
表 1 化合物1, 1a, 2和2a的1H NMR (δH, J in Hz, 400 MHz, CD3OD)波谱数据
Table 1. 1H NMR (δH, J in Hz, 400 MHz, CD3OD) spectroscopic data of compounds 1, 1a, 2 and 2a
No. 1 1a 2 2a 1α 0.79, dd, 13.1, 4.8 0.79, dd, 13.2, 4.8 3.34, dd, 12.1, 3.4 3.34, dd, 11.8, 3.1 1β 2.29, dt, 13.1, 3.4 2.30, dt, 13.2, 3.4 2α 0.97~1.02, m 0.98~1.02, m 0.98~1.01, m 0.98~1.01, m 2β 1.84~1.88, m 1.84~1.88, m 1.82~1.88, m 1.82~1.86, m 3α 3.63, dd, 5.2, 11.3 3.64, dd, 5.1, 11.3 3.66, dd, 5.7, 12.8 3.65, dd, 5.7, 12.9 5α 1.74~1.79, m 1.69~1.74, m 1.12~1.14, m 1.12~1.14, m 6α 1.07~1.11, m 1.09~1.11, m 1.08~1.11, m 1.09~1.11, m 6β 1.35~1.39, m 1.35~1.41, m 1.51~1.54, m 1.51~1.55, m 7α 1.68, ddd, 16.5, 12.3, 4.8 1.66, ddd, 16.5, 12.3, 4.8 1.62, ddd, 16.2 12.2, 4.8 1.62, ddd, 16.2, 12.2, 4.5 7β 1.32, ddd, 16.5, 5.2, 3.4 1.32, ddd, 16.5, 5.2, 3.4 1.31, dt, 12.3, 2.8 1.31, dt, 12.3, 2.8 9α 1.70, dd, 5.9, 11.9 1.71, dd, 5.4, 11.5 1.82, dd, 11.4, 5.8 1.83, dd, 11.3, 5.9 11α 2.04, ddd, 16.5, 12.0, 5.7 2.10, ddd, 16.5, 12.0, 5.7 2.07, ddd, 16.6, 12.4, 3.4 2.07, ddd, 14.1, 13.3, 3.4 11β 2.46, ddd 16.5, 12.0, 5.7 2.46, ddd, 16.5, 12.0, 5.7 2.47, ddd, 16.6, 12.3, 4.8 2.47, ddd, 14.1, 13.5, 4.4 12 5.18, t, 3.3 5.17, t, 3.4 5.18, t, 3.5 5.18, t, 3.5 15α 0.97~1.03, m 0.97~1.03, m 0.97~0.99, m 0.97~0.99, m 15β 2.01~2.07, m 2.01~2.07, m 2.01~2.07, m 2.01~2.07, m 16α 0.95~1.00, m 0.99~1.11, m 0.97~1.03, m 0.97~1.02 m 16β 1.80~1.82, m 1.82~1.87, m 1.72~1.77, m 1.76~1.78, m 18β 1.92, dd, 13.4, 3.6 1.93, dd, 13.4, 3.6 1.92, dd, 12.4, 4.6 1.96, dd, 13.6, 4.0 19α 0.98~1.01, m 0.97~1.02, m 0.99~1.02, m 1.00~1.03, m 19β 1.69~1.74, m 1.68~1.73, m 1.71~1.75, m 1.70~1.76, m 21α 1.09~1.12, m 1.09~1.12, m 1.09~1.13, m 1.10~1.13, m 21β 1.34~1.40, m 1.34~1.40, m 1.37~1.39, m 1.38~1.42, m 22α 1.45, dd, 12.7, 3.5 1.45, dd, 12.7, 3.5 1.45, dd, 12.7, 3.4 1.45, dd, 12.7, 3.4 22β 1.23, dt, 12.7, 3.2 1.23, dt, 12.7, 3.2 1.23, dt, 12.7, 3.2 1.23, dt, 12.7, 3.2 23a 3.29, d, 11.5 3.29, d, 11.5 3.28, d, 11.2 3.30, d, 11.2 23b 3.63, d, 11.5 3.53, d, 11.5 3.60, d, 11.2 3.62, d, 11.2 24 0.77, s 0.75, s 0.70, s 0.68, s 25a 4.01, d, 12.3 3.98, d, 12.6 1.01, s 1.01, s 25b 4.07, d, 12.3 4.08, d, 12.6 26 1.12, s 1.11, s 1.03, s 1.02, s 27 1.17, s 1.17, s 1.18, s 1.17, s 28 0.86, s 0.86, s 0.84, s 0.85, s 29 0.88, s 0.88, s 0.88, s 0.88, s 30 0.89, s 0.89, s 0.89, s 0.89, s 1' 4.33, d, 6.8 4.32, d, 6.7 2' 3.52~3.55, m 3.50~3.54 m 3' 3.51, d, 3.3 3.51, d, 3.3 4' 3.78~3.81, m 3.78~3.81, m 5'a 3.55, dd, 12.3, 2.7 3.55, dd, 12.3, 2.7 5'b 3.85, dd, 12.3, 2.7 3.85, dd, 12.3, 2.7 表 2 化合物1, 1a, 2和2a的13C NMR波谱数据(100 MHz, CD3OD)
Table 2. 13C NMR (100 MHz, CD3OD) spectroscopic data of compounds 1, 1a, 2, and 2a
No. 1 1a 2 2a 1 34.5 34.5 80.7 80.6 2 33.4 33.7 37.0 38.0 3 83.7 74.0 80.4 71.1 4 44.0 43.5 44.0 44.0 5 48.2 48.1 46.0 46.7 6 18.6 18.9 18.6 18.9 7 27.4 27.4 33.5 33.6 8 41.4 41.4 41.7 41.7 9 49.7 49.9 49.8 49.9 10 43.3 43.3 44.0 43.5 11 26.5 26.5 28.4 28.4 12 124.1 124.0 124.4 124.4 13 146.1 146.1 145.4 145.4 14 42.1 42.3 43.0 42.9 15 28.2 28.1 28.2 28.1 16 27.4 27.4 27.5 27.5 17 33.7 33.7 33.7 33.7 18 48.8 48.7 48.7 48.7 19 48.2 48.2 48.2 48.2 20 32.1 32.1 32.1 32.1 21 36.0 36.0 36.0 36.0 22 38.4 38.4 38.4 38.4 23 65.1 67.4 64.8 66.9 24 13.8 13.1 13.3 13.1 25 62.4 62.3 12.6 12.7 26 18.2 18.2 18.0 18.0 27 27.2 27.2 26.7 26.7 28 29.1 29.1 29.1 29.1 29 34.0 34.0 34.0 34.0 30 24.2 24.2 24.2 24.2 1' 106.6 106.6 2' 73.1 73.1 3' 74.9 74.7 4' 69.9 69.9 5' 66.9 67.1 表 3 化合物1~3对五种肿瘤细胞株的增殖抑制作用a
Table 3. Anti-proliferative activities of compounds 1~3 against five cancer cell lines
化合物 白血病HL-60 乳腺癌MCF-7 肝癌SMMC-7221 肺癌A-549 结肠癌SW480 1 >40 >40 >40 >40 >40 2 16.35±0.25 17.05±0.52 17.66±0.21 15.87±0.26 12.30±0.36 3 >40 >40 >40 >40 >40 DDPb 3.42±0.17 35.02±2.17 13.23±1.17 28.23±2.95 26.90±1.93 a半数抑制浓度(IC50)采用平均值(mean)±标准方差(SD)表示, 单位: μmol•L−1. b DDP:阳性对照药顺铂(cisplatin). -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 4
- 文章访问数: 1935
- HTML全文浏览量: 429


 下载:
下载:


 下载:
下载:

