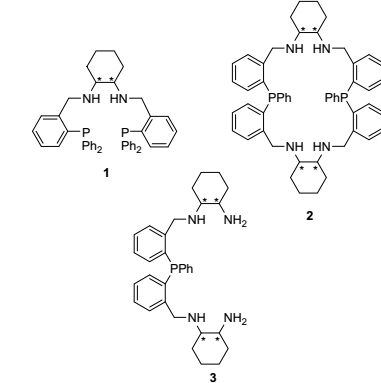
 图 1
手性胺膦配体
Figure 1.
Chiral aminophosphine ligands
图 1
手性胺膦配体
Figure 1.
Chiral aminophosphine ligands

Citation: Wu Fang, Zhang Wenjing, An Dongli, Li Yanyun, Gao Jingxing. Asymmetric Transfer Hydrogenation of Ketones Catalyzed by Chiral Multidentate Aminophosphine Ligands/Iron Cluster[J]. Chinese Journal of Organic Chemistry, 2017, 37(5): 1295-1299. doi: 10.6023/cjoc201702043

手性多齿胺膦配体/铁簇合物催化酮的不对称转移氢化反应
English
Asymmetric Transfer Hydrogenation of Ketones Catalyzed by Chiral Multidentate Aminophosphine Ligands/Iron Cluster
-
Key words:
- chiral aminophosphine ligand
- / iron cluster
- / cheap metal
- / ketones
- / asymmetric transfer hydrogenation
-
手性芳香醇是高附加值的精细化学品, 可作为多种芳香醇胺类手性药物的重要中间体[1, 2].目前, 通过前手性酮的不对称氢化(AH)或不对称转移氢化(ATH)反应制备手性芳香醇的过程中, 大多使用钌、铑、铱等贵金属催化剂[3~10], 价格昂贵而且有毒; 因此, 寻找价格低廉、绿色环保的不对称催化体系用以替代目前广泛使用的手性贵金属催化剂具有非常重要的意义.近年来, 铁催化剂因其具有价廉易得、环境友好等诸多优势成为不对称催化研究中的热点[11~17]. 2004年, 我们较早将手性胺膦配体1(图 1)与三核铁簇合物[Et3NH][HFe3(CO)11]原位生成的催化体系用于芳香酮的不对称转移氢化反应, 所得手性醇产物的对映选择性最高可达98% ee [18].在此基础上, Morris研究小组取得了很好的研究成果.他们采用模板合成路线, 方便制备了一系列手性铁络合物催化剂, 将其用于多种酮的不对称转移氢化反应, 室温下TOF(转换频率)值最高达720000 h-1, 获得相应手性二级醇的光学纯度达到99% ee以上[19~27].最近, 我们又设计合成了一种结构新颖的手性环状胺膦配体2(图 1), 以氢气或异丙醇作为氢源, 配体2与Fe3(CO)12原位生成的催化体系均能有效实现多种芳香酮的不对称氢化以及不对称转移氢化反应, 对映选择性最高达99% ee[28, 29].受此启发, Mezzetti等[30]合成出了一类环状手性胺膦-铁络合物, 并在酮及亚胺的不对称转移氢化中获得了最高达99% ee的对映选择性.迄今为止, 较之钌、铑、铱等贵金属催化剂, 成功用于不对称还原的铁催化剂为数不多, 因而开发新型高效的手性铁催化剂是不对称催化研究领域的一项重要课题.
通常, 手性催化剂由中心金属和与之键联的手性配体组成, 其中手性配体是产生不对称诱导力的源泉.在众多结构各异的手性配体中, 含有磷和氮原子混合功能团的手性PxNy-型配体由于兼具手性膦配体和手性胺配体的特征引起了人们的极大关注[31].目前用于铁催化酮的不对称转移氢化反应中的手性配体多为P2Ny-型配体, 即配体分子中含有两个膦基团, 而单膦PNy-型配体用于该类反应的例子则极为罕见.这里, 我们首次报道手性多齿胺膦配体(R, R, R, R)-PN4H6(3, 图 1)与铁簇合物原位催化酮的不对称转移氢化反应, 进一步探索最佳的反应条件.
1 结果与讨论
手性多齿胺膦配体(R, R, R, R)-PN4H6按照文献方法合成[32].以异丙醇兼作溶剂和氢源, 将手性多齿胺膦配体3与铁络合物原位生成的催化体系用于酮的不对称转移氢化反应, 考察不同反应条件下的催化性能.实验初始, 我们选择苯丙酮作为不对称转移氢化反应的模型底物(表 1).从表 1可以看出, 配体3与不同的铁络合物组合, 其催化苯丙酮不对称转移氢化的反应活性有明显差别.二价铁盐Fe(BF4)2•6H2O、三价铁盐FeCl3以及双核铁簇合物Fe2(CO)9与配体3原位生成的催化体系在所施反应条件下几乎不具有催化活性(表 1, Entries 1~3).有趣的是, 三核铁簇合物Fe3(CO)12与配体3生成的催化体系于50 ℃反应16 h, (S)-苯丙醇的产率为14%, 对映选择性为90% ee(表 1, Entry 4).该结果表明三核铁簇合物Fe3(CO)12的结构更易于与手性多齿胺膦配体3发生相互作用, 从而在不对称催化过程中实现手性诱导.
 表 1
不同铁催化剂及反应条件对苯丙酮不对称转移氢化反应的影响a
Table 1.
Screening of catalysts and conditions for ATH of propiophenone
表 1
不同铁催化剂及反应条件对苯丙酮不对称转移氢化反应的影响a
Table 1.
Screening of catalysts and conditions for ATH of propiophenone

Entry Iron complex KOH/mol% Additive/20 mol% Yieldb/% eeb/% 1 Fe(BF4)2•6H2O 28 None — — 2 FeCl3 28 None — — 3 Fe2(CO)9 28 None 1 — 4 Fe3(CO)12 28 None 14 90 5 Fe3(CO)12 28 KCl 33 95 6 Fe3(CO)12 None KCl — — 7 Fe3(CO)12 10 KCl 5 82 8 Fe3(CO)12 40 KCl 15 88 9c Fe3(CO)12 28 KCl 13 78 a反应条件:苯丙酮(0.5 mmol), i-PrOH (10 mL), 50 ℃, 16 h; b产率及ee值由气相色谱分析确定, 手性色谱柱: CP-Chriasil-Dex CB column; c70 ℃. 表 1 不同铁催化剂及反应条件对苯丙酮不对称转移氢化反应的影响a
Table 1. Screening of catalysts and conditions for ATH of propiophenone之前的研究我们发现, 添加少量无机盐有助于提高某些不对称转移氢化反应体系的催化活性和对映选择性, 其中的机理尚不清楚[28].我们将适量KCl添加到配体3与Fe3(CO)12原位生成的催化体系中, 产率和对映选择性均有不同程度的提高(表 1, Entry 5).碱在酮的不对称转移氢化中起着重要作用[6].以KOH作为碱, 我们考察了不同碱量对苯丙酮不对称转移氢化反应的影响.研究结果表明, 当不加碱时反应体系无活性(表 1, Entry 6).随着碱量的增加, (S)-苯丙醇的产率逐渐提高(表 1, Entries 7, 5).然而过多的碱却会导致催化活性和对映选择性降低(表 1, Entry 8).此外, 温度对苯丙酮不对称转移氢化反应也有一定的影响.当温度升高至70 ℃时, 该反应的催化活性和对映选择性均明显下降(产率13%, 78% ee, 表 1, Entry 9), 因此选择50 ℃为适宜的反应温度.
对于手性多齿胺膦配体(R, R, R, R)-3和Fe3(CO)12原位生成的催化剂, 我们考察了温度、添加剂、碱量等因素对苯丙酮不对称转移氢化反应的影响, 并得到了最佳反应条件.在此基础上, 我们进一步将该催化体系拓展应用至其它底物酮的不对称转移氢化反应(表 2).由表可知, 由配体(R, R, R, R)-3和Fe3(CO)12原位生成的催化剂对多种芳香酮的不对称转移氢化反应均表现出高的对映选择性.对于苯乙酮、苯丙酮、苯戊酮等一系列苯基烷基酮, 其不对称转移氢化反应产物的对映选择性最高可达96% ee(表 2, Entries 1~6).以烷基取代的苯乙酮作为底物时, 该催化体系也表现出了高对映选择性(表 2, Entries 7~10).对于卤素取代的苯乙酮, 对位卤素取代苯乙酮比邻、间位取代的苯乙酮具有更高的对映选择性(表 2, Entries 11~16).值得一提的是, 当底物为2-溴苯乙酮时, 反应具有很高的催化活性, 其产率可高达99%, 但是只得到中等的对映选择性(表 2, Entry 14).与3-甲氧基苯乙酮相比, 2-甲氧基苯乙酮在所施反应条件下的不对称转移氢化反应进行得十分缓慢, 反应20 h后, (S)-2-甲氧基苯乙醇产率仅为6%, 对映选择性也只有14% ee(表 2, Entries 18, 19).当空间位阻较大的酮如2-萘乙酮及1, 1-二苯基丙酮作为底物时, 不对称转移氢化反应仍能获得很高的对映选择性(表 2, Entries 21, 22).
 表 2
Fe3(CO)12/(R, R, R, R)-3体系催化多种芳香酮的不对称转移氢化反应a
Table 2.
ATH of a broad scope of ketones catalyzed by Fe3(CO)12/(R, R, R, R)-3
表 2
Fe3(CO)12/(R, R, R, R)-3体系催化多种芳香酮的不对称转移氢化反应a
Table 2.
ATH of a broad scope of ketones catalyzed by Fe3(CO)12/(R, R, R, R)-3

Entry Ketone Time/h Yieldb/% eeb/% Config.b 1 
16 30 91 S 2 16 33 95 S 3 16 12 94 S 4c 16 23 96 R 5 16 13 85 S 6c 16 12 94 R 7 16 24 94 S 8 16 30 94 S 9 16 24 94 S 10 16 20 93 S 11 16 15 77 S 12 
16 14 69 S 13 16 27 87 S 14 5 99 67 S 15 16 27 48 S 16 16 34 91 S 17 16 24 43 S 18 20 6 14 S 19 16 40 93 S 20 16 38 64 S 21 16 24 92 S 22c 16 26 94 R a反应条件:酮0.5 mmol, 酮:Fe3(CO)12:(R, R, R, R)-3:KCl:KOH=50:1:1:10:14 (molar ratio), i-PrOH 10 mL, 50 ℃; b产率及ee值由气相色谱分析确定, 手性色谱柱: CP-Chriasil-Dex CB column.主要产物手性醇的绝对构型与文献[29]比较得出; c手性配体为(S, S, S, S)-3. 表 2 Fe3(CO)12/(R, R, R, R)-3体系催化多种芳香酮的不对称转移氢化反应a
Table 2. ATH of a broad scope of ketones catalyzed by Fe3(CO)12/(R, R, R, R)-32 结论
从廉价易得、绿色环保的铁络合物出发, 考察了其与手性多齿胺膦配体(R, R, R, R)-PN4H6原位生成的催化体系在芳香酮不对称转移氢化中的应用.与之前报道的手性P2Ny-型配体/铁催化体系相比, 该体系的特点是手性配体为单膦PN4-型配体.研究表明, (R, R, R, R)-PN4H6/Fe3(CO)12催化体系用于多种芳香酮的不对称转移氢化反应, 表现出很高的对映选择性(最高达96% ee), 但催化活性仍有待进一步提高.该催化体系优秀的对映选择性来源于手性配体分子中环己二胺基团的不对称诱导, 氮原子与中心金属原子生成较弱的配位键, 在催化反应过程中, 该配位键容易离解, 提供有利于底物络合的配位位置; 另一方面, 配体中的磷原子具有π受体的特性, 可以增加中心金属的碱性进而提高配合物的稳定性.较之于双膦配体, 单膦配体在催化过程中稳定中心金属铁原子时发挥的作用可能略显不足, 从而导致该催化体系的活性较低.这些研究结果为我们今后设计合成新型手性铁催化剂提供了有价值的参考.
3 实验部分
3.1 仪器与试剂
Mettler Toledo分析天平(AB104-N型); Bruker Avance Ⅱ 400 MHz、Bruker Avance Ⅱ 500 MHz核磁共振波谱仪; 上海海欣色谱仪器有限公司GC950气相色谱仪; CP-Chriasil-Dex CB column手性色谱柱.无水异丙醇按照标准方法处理, 其余药品和试剂未经进一步纯化直接使用.
3.2 手性多齿胺膦配体(R, R, R, R)-PN4H6的合成
手性多齿胺膦配体(R, R, R, R)-PN4H6合成方法参考文献[32].将双(2-甲酰基苯基)苯基膦(159 mg, 0.5 mmol)及(1R, 2R)-2-氨基-环己氨基甲酸叔丁酯(214 mg, 1.0 mmol)依次加至25 mL双颈瓶中, 氮气保护下加入甲醇(15 mL).反应液升温回流, 颜色由黄色逐渐变浅, 反应34 h, 后于氮气下缓慢冷却至室温.减压除去溶剂, 得到淡黄色固体产物350 mg, 产率98%. 1H NMR (500 MHz, CDCl3) δ: 8.79 (s, 1H), 8.76 (s, 1H), 8.02 (s, 1H), 7.94 (s, 1H), 7.68~7.56 (m, 1H), 7.40~7.18 (m, 10H), 6.90~6.77 (m, 2H), 3.58~3.42 (m, 2H), 2.94~2.77 (m, 2H), 2.23~2.08 (m, 2H), 2.08~1.95 (m, 2H), 1.75~1.62 (m, 4H), 1.50~1.42 (m, 4H), 1.34 (s, 18H), 1.25~1.16 (m, 4H).
将上述合成的化合物(650 mg, 0.91 mmol)和硼氢化钠(1.3 g, 34.3 mmol)加至50 mL双颈瓶中, 于氮气气氛下加入甲醇(30 mL), 升温回流, 搅拌反应12 h后停止反应.在氮气保护下冷却至室温, 加入二氯甲烷(50 mL)和蒸馏水(30 mL), 分液萃取.有机层分别用蒸馏水、饱和食盐水洗涤多次, 经无水硫酸钠干燥后过滤, 减压除去溶剂, 真空干燥得白色固体590 mg, 产率91%. 1H NMR (500 MHz, CDCl3) δ: 7.62~7.45 (m, 2H), 7.43~7.30 (m, 5H), 7.29~7.20 (m, 2H), 7.20~7.18 (m, 2H), 6.87~6.72 (m, 2H), 5.05~4.42 (br m, 2H), 4.08~3.82 (m, 4H), 3.35~3.11 (m, 2H), 2.26~2.14 (m, 2H), 2.10~2.00 (m, 2H), 1.98~1.85 (m, 4H), 1.69~1.56 (m, 4H), 1.44 (s, 18H), 1.30~1.21 (m, 2H), 1.13~0.98 (m, 6H).
在25 mL Schlenk管中加入上述合成的化合物(357 mg, 0.50 mmol), 氮气氛下加入二氯甲烷(5 mL), 于0 ℃下滴加三氟乙酸(0.8 mL, 10 mmol), 室温下继续搅拌12 h后停止反应.加入二氯甲烷(5 mL)稀释, 将反应液倒入饱和碳酸氢钠溶液中, 用二氯甲烷(15 mL×3) 萃取, 合并有机相, 用无水硫酸钠干燥, 静置, 过滤, 减压除去溶剂, 真空干燥得白色固体248 mg, 此即为手性多齿胺膦配体(R, R, R, R)-PN4H6, 产率96%. 1H NMR (400 MHz, CDCl3) δ: 7.58~7.36 (m, 3H), 7.35~7.28 (m, 4H), 7.26~7.13 (m, 4H), 6.92~6.75 (m, 2H), 4.12~3.73 (m, 4H), 3.25 (br s, 6H), 2.46~2.28 (m, 2H), 2.28~2.00 (m, 4H), 1.98~1.84 (m, 2H), 1.75~1.60 (m, 4H), 1.28~1.12 (m, 6H), 1.03~0.82 (m, 2H).
3.3 不对称转移氢化反应
催化反应按如下程序操作:将一定量的手性多齿胺膦配体(R, R, R, R)-PN4H6和Fe3(CO)12加入25 mL Schlenk反应管中, 氮气保护下, 加入10 mL异丙醇, 在一定温度下搅拌反应30 min后, 加入一定量的KOH/i-PrOH溶液, 继续搅拌15 min, 加入底物酮.搅拌反应液直至所需时间, 经气相色谱测定产率和对映体含量.
3.4 目标化合物结构表征
目标化合物为已知化合物, 表征数据参考文献[29].不对称催化反应产率及ee值由气相色谱分析确定, 手性色谱柱为CP-Chriasil-Dex CB column.主要产物手性醇的绝对构型与文献[29]比较得出.
辅助材料(Supporting Information) 不对称转移氢化反应产物的气相色谱图.这些材料可以免费从本刊网站(http://sioc-journal.cn/)上下载.
-
-
[1]
de Vries, J. G.; Elsevier, C. J. The Handbook of Homogeneous Hydrogenation, Wiley-VCH, Weinheim, 2007.
-
[2]
Dupau, P. In Organometallics as Catalysts in the Fine Chemical Industry, Eds.: Beller, M.; Blaser, H. U., Springer-Verlag, Berlin, 2012.
-
[3]
Noyori, R. Adv. Synth. Catal. 2003, 345, 15. doi: 10.1002/adsc.200390002
-
[4]
Gladiali, S.; Alberico, E. Chem. Soc. Rev. 2006, 35, 226. doi: 10.1039/B513396C
-
[5]
Saudan, L. A. Acc. Chem. Res. 2007, 40, 1309. doi: 10.1021/ar700140m
-
[6]
Ikariya, T.; Blacker, A. J. Acc. Chem. Res. 2007, 40, 1300. doi: 10.1021/ar700134q
-
[7]
Wang, C.; Wu, X.; Xiao, J. Chem. Asian. J. 2008, 3, 1750. doi: 10.1002/asia.200800196
-
[8]
Blaser, H. U. Top Catal. 2010, 53, 997. doi: 10.1007/s11244-010-9559-8
-
[9]
Malacea, R.; Poli, R.; Manoury, E. Coord. Chem. Rev. 2010, 254, 729. doi: 10.1016/j.ccr.2009.09.033
-
[10]
Etayo, P.; Vidal Ferran, A. Chem. Soc. Rev. 2013, 42, 728. doi: 10.1039/C2CS35410A
-
[11]
Bolm, C. Nat. Chem. 2009, 1, 420. doi: 10.1038/nchem.315
-
[12]
Morris, R. H. Chem. Soc. Rev. 2009, 38, 2282. doi: 10.1039/b806837m
-
[13]
Junge, K.; Schroeder, K.; Beller, M. Chem. Commun. 2011, 47, 4849. doi: 10.1039/c0cc05733a
-
[14]
Darwish, M.; Wills, M. Catal. Sci. Technol. 2012, 2, 243. doi: 10.1039/C1CY00390A
-
[15]
Gopalaiah, K. Chem. Rev. 2013, 113, 3248. doi: 10.1021/cr300236r
-
[16]
Morris, R. H. Acc. Chem. Res. 2015, 48, 1494. doi: 10.1021/acs.accounts.5b00045
-
[17]
Li, Y.-Y.; Yu, S.-L.; Shen, W.-Y.; Gao, J.-X. Acc. Chem. Res. 2015, 48, 2587. doi: 10.1021/acs.accounts.5b00043
-
[18]
陈建珊, 陈玲玲, 邢雁, 陈贵, 沈伟艺, 董振荣, 李岩云, 高景星, 化学学报, 2004, 62, 1745. doi: 10.3321/j.issn:0567-7351.2004.18.014Chen, J.-S.; Chen, L.-L.; Xing, Y.; Chen, G.; Shen, W.-Y.; Dong, Z.-R.; Li, Y.-Y.; Gao, J.-X. Acta Chim. Sinica 2004, 62, 1745 (in Chinese) doi: 10.3321/j.issn:0567-7351.2004.18.014
-
[19]
Sui-Seng, C.; Freutel, F.; Lough, A. J.; Morris, R. H. Angew. Chem., Int. Ed. 2008, 47, 940. doi: 10.1002/(ISSN)1521-3773
-
[20]
Mikhailine, A. A.; Lough, A. J.; Morris, R. H. J. Am. Chem. Soc. 2009, 131, 1394. doi: 10.1021/ja809493h
-
[21]
Meyer, N.; Lough, A. J.; Morris, R. H. Chem. Eur. J. 2009, 15, 5605. doi: 10.1002/chem.v15:22
-
[22]
Lagaditis, P. O.; Lough, A. J.; Morris, R. H. J. Am. Chem. Soc. 2011, 133, 9662. doi: 10.1021/ja202375y
-
[23]
Sues, P. E.; Lough, A. J.; Morris, R. H. Organometallics 2011, 30, 4418. doi: 10.1021/om2005172
-
[24]
Mikhailine, A. A.; Maishan, M. I.; Lough, A. J.; Morris, R. H. J. Am. Chem. Soc. 2012, 134, 12266.
-
[25]
Mikhailine, A. A.; Maishan, M. I.; Morris, R. H. Org. Lett. 2012, 14, 4638. doi: 10.1021/ol302079q
-
[26]
Sonnenberg, J. F.; Coombs, N.; Dube, P. A.; Morris, R. H. J. Am. Chem. Soc. 2012, 134, 5893. doi: 10.1021/ja211658t
-
[27]
Zuo, W.; Lough, A. J.; Li, Y. F.; Morris, R. H. Science 2013, 342, 1080. doi: 10.1126/science.1244466
-
[28]
Yu, S.-L.; Shen, W.-Y.; Li, Y.-Y.; Dong, Z.-R.; Xu, Y.-Q.; Li, Q.; Zhang, J.-N.; Gao, J.-X. Adv. Synth. Catal. 2012, 354, 818. doi: 10.1002/adsc.201100733
-
[29]
Li, Y.-Y.; Yu, S.-L.; Wu, X.-F.; Xiao, J.-L.; Shen, W.-Y.; Dong, Z.-R.; Gao, J.-X. J. Am. Chem. Soc. 2014, 136, 4031. doi: 10.1021/ja5003636
-
[30]
Bigler, R.; Huber, R.; Mezzetti, A. Angew. Chem., Int. Ed. 2015, 54, 5171. doi: 10.1002/anie.v54.17
-
[31]
Kostas, I. D. Curr. Org. Synth. 2008, 5, 227. doi: 10.2174/157017908785133447
-
[32]
Xu, Y.-Q.; Yu, S.-L.; Li, Y.-Y.; Dong, Z.-R.; Gao, J.-X. Chin. Chem. Lett. 2013, 24, 527. doi: 10.1016/j.cclet.2013.03.043
-
[1]
-
表 1 不同铁催化剂及反应条件对苯丙酮不对称转移氢化反应的影响a
Table 1. Screening of catalysts and conditions for ATH of propiophenone

Entry Iron complex KOH/mol% Additive/20 mol% Yieldb/% eeb/% 1 Fe(BF4)2•6H2O 28 None — — 2 FeCl3 28 None — — 3 Fe2(CO)9 28 None 1 — 4 Fe3(CO)12 28 None 14 90 5 Fe3(CO)12 28 KCl 33 95 6 Fe3(CO)12 None KCl — — 7 Fe3(CO)12 10 KCl 5 82 8 Fe3(CO)12 40 KCl 15 88 9c Fe3(CO)12 28 KCl 13 78 a反应条件:苯丙酮(0.5 mmol), i-PrOH (10 mL), 50 ℃, 16 h; b产率及ee值由气相色谱分析确定, 手性色谱柱: CP-Chriasil-Dex CB column; c70 ℃. 表 2 Fe3(CO)12/(R, R, R, R)-3体系催化多种芳香酮的不对称转移氢化反应a
Table 2. ATH of a broad scope of ketones catalyzed by Fe3(CO)12/(R, R, R, R)-3

Entry Ketone Time/h Yieldb/% eeb/% Config.b 1 
16 30 91 S 2 16 33 95 S 3 16 12 94 S 4c 16 23 96 R 5 16 13 85 S 6c 16 12 94 R 7 16 24 94 S 8 16 30 94 S 9 16 24 94 S 10 16 20 93 S 11 16 15 77 S 12 
16 14 69 S 13 16 27 87 S 14 5 99 67 S 15 16 27 48 S 16 16 34 91 S 17 16 24 43 S 18 20 6 14 S 19 16 40 93 S 20 16 38 64 S 21 16 24 92 S 22c 16 26 94 R a反应条件:酮0.5 mmol, 酮:Fe3(CO)12:(R, R, R, R)-3:KCl:KOH=50:1:1:10:14 (molar ratio), i-PrOH 10 mL, 50 ℃; b产率及ee值由气相色谱分析确定, 手性色谱柱: CP-Chriasil-Dex CB column.主要产物手性醇的绝对构型与文献[29]比较得出; c手性配体为(S, S, S, S)-3. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 3
- 文章访问数: 1699
- HTML全文浏览量: 269


 下载:
下载:
 下载:
下载:

