 图 1
生色团EFNFC的合成路线及EFFC和EFNC的结构
Figure 1.
Synthetic route of chromophore EFNFC and structures of EFFC and EFNC
图 1
生色团EFNFC的合成路线及EFFC和EFNC的结构
Figure 1.
Synthetic route of chromophore EFNFC and structures of EFFC and EFNC

Citation: Chen Lei, Tang Xiang, Jia Kun, Tang Xianzhong. Synthesis and Properties of Organic Nonlinear Optical Chromophores Containing Azo-and Furan-Based Conjugated Bridge[J]. Chinese Journal of Organic Chemistry, 2016, 36(9): 2197-2203. doi: 10.6023/cjoc201601005

以偶氮和呋喃基团作为共轭桥的有机非线性光学生色团分子合成与性能研究
English
Synthesis and Properties of Organic Nonlinear Optical Chromophores Containing Azo-and Furan-Based Conjugated Bridge
-
关于有机非线性光学材料作为集成光学器件的重要材料, 因其相对无机材料具有更好的分子可设计性, 分子柔性以及更大的非线性光学性能, 相关研究已成为当今高新技术研究的一大热点[1~5].根据电荷转移理论, 目前对有机二阶非线性光学材料结构设计的研究主要集中在如何得到电荷转移能力更强的D(给体)-π(共轭桥)-A(受体)结构这一问题上.多年来, 人们在研究有机非线性光学生色团分子的合成过程中, 慢慢形成了一类公认的性能较为理想的二烷氨基作为给体(二乙氨基), 含氰的环状多烯作为受体(TCF[6])的生色团分子.但对于性能更好的共轭桥的探索研究却一直在进行着.
在共轭桥的研究初期, 乙烯基和苯相连作为共轭桥, 但这类共轭桥却因透光性太差, 以及苯环本身的离域能太高, 锁住了一部分电子从而不利于分子整体的电荷转移而被证实了并不适用于生色团分子.后来人们提出用离域能更低的杂环取代苯环作为共轭桥的主要结构, 成功合成了噻吩共轭桥的生色团并证明了其优良性能[6, 7].随后, 关于呋喃环共轭桥的研究也开始进行[8~10], 在对分子电荷转移能力的贡献这一方面, 呋喃环显然具有比噻吩更好的性能.
人们在研究中同时发现, 偶氮类基团也是一类性能非常不错的共轭桥结构[11~14], 它避免了苯乙烯基所存在的透光性差和不利于分子整体的电荷转移等问题, 同时由于苯环结构比杂环稳定, 当在分子中间引入支链基团时它的平面结构被破坏的可能性也较小.
当杂环和偶氮这两类共轭桥都显现出优良性能后, 有研究者将二者结合, 形成偶氮杂环类共轭桥, 合成出含有偶氮噻吩共轭桥的生色团分子, 其性能也非常不错[15, 16].既然偶氮杂环类分子显现出了较好的非线性光学性能, 那么当偶氮键与呋喃相结合其性能也理应不弱, 但这种共轭桥结构的分子目前还未见报道.
本文中, 我们合成了一种新型的含有偶氮呋喃基团共轭桥的有机非线性光学生色团分子, 将这种分子分别与含有偶氮基苯、乙烯基呋喃的分子进行对比, 通过对比研究, 观察偶氮呋喃共轭桥对分子性能的贡献情况, 找寻三种分子当其共轭桥在有规律地发生变化时, 分子的热学性能和光学性能的变化规律.为进一步生色团分子合成研究和器件制备研究提供重要的参考依据.
1 结果与讨论
1.1 合成问题讨论
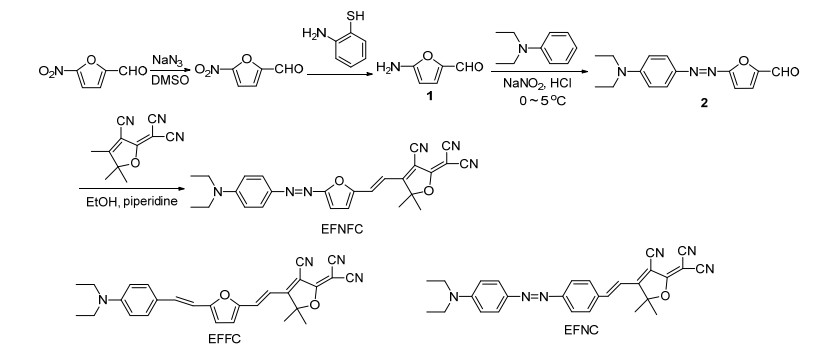
生色团分子2-二氰亚甲基-3-氰基-4-[2-(4-二乙胺基-偶氮苯基-呋喃基-5)-乙烯基]-5, 5-二甲基-2, 5-二氢呋喃(EFNFC)的合成路线以及2-二氰亚甲基-3-氰基-4-[2-(4-二乙胺基-苯乙烯基-呋喃基-5)-乙烯基]-5, 5-二甲基-2, 5-二氢呋喃(EFFC)和2-二氰亚甲基-3-氰基-4-[2-(4-对二乙胺基偶氮苯基-4)-乙烯基]-5, 5-二甲基-2, 5-二氢呋喃(EFNC)的分子结构如图 1所示.
 图 1
生色团EFNFC的合成路线及EFFC和EFNC的结构
Figure 1.
Synthetic route of chromophore EFNFC and structures of EFFC and EFNC
图 1
生色团EFNFC的合成路线及EFFC和EFNC的结构
Figure 1.
Synthetic route of chromophore EFNFC and structures of EFFC and EFNC
生色团分子EFFC和EFNC合成方法相对不难.分子EFNFC的合成则要复杂一些, 5-氨基糠醛不稳定, 易自聚合, 因此需制备后马上进入下一步反应.我们使用叠氮钠和2-氨基苯硫醇将5-硝基糠醛上的硝基进行还原, 得到5-氨基糠醛(中间体1), 再通过类似于EFNC合成过程中偶氮化合物的制备方法得到最终的目标产物.
通过分子结构的设计与合成, 最终得到的三种生色团分子在共轭桥的结构上呈现出一种递进的变化关系, 即偶氮基苯到乙烯基呋喃再到偶氮基呋喃.乙烯基苯作为一种早已被证实性能较差的结构[8]则未在本次研究之列.
三种目标生色团分子通过羟醛缩合反应得到, 在哌啶做催化剂的条件下, 这三种分子都可以直接从反应体系中结晶得到.
1.2 理论计算
为了研究分子的微观结构与电荷转移情况, 我们采用量子化学方法密度泛函理论(DFT)对分子前线分子轨道理论中的HOMO-LUMO能级和分子的微观二阶极化率进行了研究.使用GAUSSIAN03软件, 在B3LYP/ 6-311G(d, p)基组下对分子结构进行优化.最后在相同基组下计算生色团分子的HOMO和LUMO能级以及分子在静态的二阶极化率(β0).
经优化后的分子结构图和分子HOMO和LUMO轨道图如图 2所示. HOMO到LUMO的能级差ΔE和分子的微观二阶极化率β0具体数据列于表 1中.由理论理算结果可以看到, 三种分子中的共轭原子基本处于同一平面上, 更有利于形成分子内的大π键, 使电荷转移更容易发生.
Chromophore DE/eV β0a/(10-28 esu) λmaxb/nm Λmaxc/nm λmax/nm ξmax/(104 L•mol-1•cm-1) μgβ1064nm/ (10-49 esu) Td/℃ ξmaxb ξmaxc ξmaxd, e EFFC 2.190 5.459 676 644 633d 1.051 1.731 1.205d 3.194 250 EFNC 2.259 7.498 568 544 585e 3.201 3.680 3.115e 5.971 254 EFNFC 2.104 3.662 573 598 575e 2.263 1.760 1.018e 4.479 270 aβ0=βvec=||β||=(Σβi2)1/2; bMeasured in DMSO; cMeasured in Acetone; dMeasured in Ethyl acetate; eMeasured in Chloroform. 表 1 各生色团的热学和光学性能数据
Table 1. Characterization data of the chromophores从三种分子的β0值来看, EFNC具有最高的二阶非线性光学系数, EFFC次之, EFNFC最低.我们认为, 这些分子的结构对性能的影响主要通过两个方面的作用体现出来的, 一是不同官能团的化学键对电荷转移过程的影响, 这是通常人们认为对分子电荷转移能力产生影响的最重要的因素; 另一方面, 我们认为, 分子的构型也会对电荷转移造成影响, 由于电荷是在分子内发生转移, 电荷转移的方向也必然是沿着分子的结构方向进行的, 在EFNFC中, 电荷转移需经过的“弯度”较大(即折角较小), 而EFNC中电荷转移的“弯度”较小(即折角较大), 显然在EFNC中电荷的转移要更容易完成一些, 基于这一影响, EFNC的β0值表现最大, 而EFNFC的β0值表现最小.
但上述的两种作用应当是同时存在, 共同作用于生色团分子的.三种分子的给体和受体完全一样, 性能变化主要来自于共轭桥本身的电荷转移能力和由共轭桥的变化造成的分子结构变化影响使得分子表现出不同的β0值来, 但哪一方面的影响较大还有待与实际测试结果对比分析后进一步讨论.
1.3 分子的线性与非线性光学性能
多年来, 人们一直致力于得到兼具大的二阶光学非线性与良好透明性的有机生色团的分子[18, 19], 分子的线性与非线性光学性能均非常重要.我们将所合成的生色团分子分别溶解于不同的溶剂中, 扫描其紫外-可见光谱(如图 3), 考察其透光性能.分子最大吸收波长数据列于表 1中.在DMSO和丙酮两种溶剂中考查三种分子的最大吸收峰情况, 由实验数据可以看出, 在这两种溶剂中, 最大吸收峰的位移趋势是相同的:在含有偶氮共轭桥的生色团透光性要优于由乙烯连接共轭桥的分子, 蓝移最大可达到约100 nm.同样是含偶氮共轭桥的生色团分子中, 苯环所表现出的性能要略优于呋喃共轭桥.可见, 偶氮基团的存在可以大大提升分子透光性.在共轭桥同为偶氮基团连接的情况下, 苯环共轭桥所表现出的透光性又要优于呋喃.只是在丙酮作为溶剂的溶液中EFNFC分子相对EFFC分子的蓝移比在DMSO中要小一些.
溶致变色(Solvatochromism)法是一种较为简便的测定分子二阶非线性光学系数的方法.量子力学应用含时扰动理论给出了分子二阶极化率的简明表达式:
其中, βadd对应于取代基诱导的电荷不对称转移引起的极化效应, 其值较小, 通常情况下可忽略不计; βCT为外电场诱导下分子电荷转移引起的二阶极化率, 这才是β的主要贡献者. Paley等[20]以双能级模型为基础, 认为当溶剂折射率相近时, μgβCT可作如下近似处理:
其中μg是分子的基态偶极矩, μe是激发态偶极矩, ωeg是气相中电子发生跃迁时的跃迁频率, μeg则为跃迁偶极矩, ω为所用激光频率, 即工作波长处的频率, 由于后续器件制备研究需要, 我们选用了的工作波长为1064 nm.其中的μeg可以通过计算吸收峰的面积得到:
其中, NA为阿伏加德罗常数, c为真空中光速, ε0是真空介电常数, h为普朗克常数, n为溶剂的折射率, ξ是摩尔消光系数.式中还包括一个修正值f, 用来校正溶剂的透光性对于吸收峰的影响: f2/n=(n2+2)2/9n.
峰面积S也可以从紫外光谱中得到, 近似用Lorentzian函数有[21]:
其中, ΔV1/2为半高峰宽, 从UV-Vis谱图中可以直接读出.
μg(μe-μg)中的各个量也不用单独测定, 由McRae方程便可知[22]:
其中, ωegs和ωeg分别是待测分子在溶液以及气相情况下基态与激发态间的跃迁频率, ε为溶剂的介电常数, A和B为常数.因此, 只要通过分子的λmax值得到生色团分子在三种不同溶剂中的ωegs值以及三种溶剂的ε和n值, 就可以解出ωeg、A和B值.
对于B有:
其中, a是分子在溶剂中的Onsager笼半径, 取a=ru+0.5rv, ru和rv分别为溶质和溶剂分子的半径.对于溶质分子, 先按Immirzi等[23]提出的由原子团单位体积按化学乘数叠加的方法求其分子的体积Vu, 由下式求得a值:
求解出B值后, 根据Eqs. (6)、(7)即可以得到μg(μe-μg)的值, 将μg(μe-μg)和ωeg代入Eq. (2)中, 再将之前求得的μeg代入Eq. (2), 即可以得到非线性光学材料的品质参数μgβ.在筛选用于极化聚合物的生色团时重要的参数是μgβCT值, 因此μg值并不需要单独测定, 而可以整体保留.
溶致变色法测得的非线性光学系数绝对准确率相对较差, 但在相同条件下用于对比不同分子间二阶极化率的相对情况还是较为可信的.在本研究中, 我们仅对分子的非线性光学系数相对大小及变化规律感兴趣, 因此溶致变色法是一种较为理想的简便方法.测定中的重要参数和各生色团的μgβ值测定结果列于表 1中.
由对比结果可以看到, 两种含偶氮基团的生色团μgβ值优于乙烯连接的生色团, 而在同为偶氮连接的情况下, 苯环共轭桥所表现出的性能要比呋喃作为共轭桥的分子更好.
从不同基团的化学键性能方面看, 在EFNC中偶氮基与苯环连接, 可以明显改善因苯环离域能太高而阻碍了电荷转移的情况, 使得其二阶非线性光学系数相比EFFC高出许多, 可见偶氮基对μgβ值的贡献是要优于乙烯基的, 这一推论与实测结果也是一致的.对于EFFC和EFNC来说, 与EFNC同理, 偶氮基的连接也能降低呋喃环的离域能从而使得整个分子中电荷转移更容易发生, 于是在实际测试中EFNFC的μgβ值也高于EFFC的.然而这一结果却与理论计算的β0值所得结果相反, 我们认为, 这与上一节中所讨论的不同方面因素的影响大小有关.
在理论计算中, 计算程序显然认为分子构型的影响要远远大于不同基团的化学键性能影响, 但实际上却是化学键的性能影响作为主要因素在决定着生色团分子的二阶非线性光学系数大小.这种结构相似但构型不同的分子理论计算值与实测值不一致的情况在之前的报导中也曾出现过[7].不论如何, 理论计算结果在分子构型和电子性能上还是具有非常大的参考价值的.
在无论从化学键性能还是从分子构型上看, EFNC分子的结构均能促进电荷转移的发生, 因此在计算和实测中, 它的性能都是最好的.
1.4 热稳定性
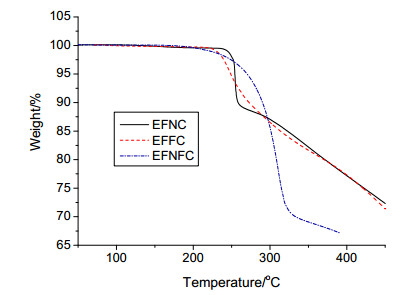
生色团分子的TGA曲线如图 4所示.各分子的热分解温度列于表 1中, 热分解温度Td按照5%热失重计算.由热分解温度数据可以看出, EFNFC分子的热稳定性最好, Td值达到了270 ℃, EFFC和EFNC分子的热稳定性则相差不多. EFFC和EFNC虽然Td值仅相差4 ℃, 但其热分解温度比EFNFC低的原因可能完全不一样. EFFC是由于分子中靠近TCF的呋喃环相比苯环在强拉电子的受体作用下更容易开环而发生分解; 而EFNC虽然苯环不易开环, 但正由于苯环离域能较高, 更加稳定, 因此与之结合的偶氮基团反而容易断裂开来.相比之下, EFNFC在受体一端和偶氮基团一端的电子分布相对更为均匀, 所以最终表现出的热稳定性显得略高, 不过也仅高了20 ℃左右.
综合考虑三种分子的热稳定性, 其Td值均在250 ℃以上, 都具有较高的热稳定性, 可以达到器件制备的要求.
2 结论
为了研究不同的共轭桥结构对生色团分子性能的影响, 我们共合成了3种有机非线性光学生色团分子.其中偶氮基呋喃作为共轭桥的结构是一种未见报道的新型结构.我们对生色团的热性能和光学性能进行了对比研究, 研究发现:从理论计算上看, 以偶氮基苯结构作为共轭桥的分子EFNC在电荷转移方向上为直线构型, 有利于电荷转移, 其β0值最高, 达到了7.498× 10-28 esu; 从透光性上看, 仍是EFNC表现出最好的透光性, 最大吸收波长λmax为567 nm; 以溶致变色法测定得到的非线性光学性能上看, 还是EFNC二阶极化率最高, μgβ1064nm=5.971×10-49 esu, 达到以乙烯基呋喃共轭桥的EFFC的1.9倍.由于分子构型的影响, EFNFC分子的μgβ1064nm值略低于EFNC.具有偶氮基呋喃结构的生色团EFNFC具有最高的热稳定性, Td值达到270 ℃.但三种材料的Td值均在250 ℃以上, 热稳定性均较好.
3 实验部分
3.1 仪器与试剂
日本岛津FTIR-8000红外光谱仪; Brucker avance-300型核磁共振仪; Vario EL元素分析仪; 日本岛津UV-2450紫外可见分光光谱仪.热重分析仪(TGA)为美国TA公司Q50型, 在氮气气氛中, 流速为50 mL/min, 升温速率20 ℃/min.
TCF按文献[6]合成, 生色团分子EFFC和EFNC分别根据文献[10]和[17]的方法进行合成; 其它试剂均为市售分析纯.
3.2 实验方法
3.2.3 5-(对二乙胺基偶氮苯基)糠醛(2)的合成
取0.46 g (4 mmol) 1于100 mL烧瓶中, 加入2.5 mL浓盐酸, 再加入4 mL去离子水稀释, 室温下搅拌30 min使5-氨基糠醛充分溶解, 溶液呈黑色.放入冰浴中, 控制温度在0~5 ℃.另配制0.28 g (4 mmol)亚硝酸钠的10 mL水溶液, 在冰浴下逐滴加入到上述5-氨基糠醛溶液中, 滴完后再在冰浴下搅拌30 min以使反应完全, 最终得到黄色的4-醛基呋喃重氮盐悬浊液.
取0.6 g (4 mmol) N, N-二乙基苯胺溶于36%乙酸中, 加入适当乙酸钠调节pH值在3~5.冰浴使溶液温度保持在0~5 ℃, 并在搅拌下滴入上述制备好的重氮盐溶液中.滴完后在0~5 ℃下搅拌2 h, 在室温下再搅拌2 h.反应完成后调节体系的pH值为7, 静置过夜, 抽滤.所得固体用95%乙醇重结晶得到红色晶体0.68 g, 产率70.0%. IR (KBr) ν: 1145, 1247, 1365, 1454, 1519, 1600, 1675, 3058 cm-1.
3.2.2 5-氨基糠醛(1)的合成
将2 mL 2-氨基苯硫酚(1.5 g, 12 mmol)的四氢呋喃(THF)溶液逐滴加入到4 mL 5-叠氮基-2-呋喃甲醛(0.86 g, 6 mmol)的THF溶液中, 保持0 ℃, 加入2-氨基苯硫酚15 min后反应结束, 将黄色沉淀物过滤出来, 用冷乙醚洗后真空干燥, 得到0.5 g黄色产物, 产率72.4%.
3.2.5 2-二氰亚甲基-3-氰基-4-[2-(4-二乙胺基-苯乙烯基-呋喃基-5)-乙烯基]-5, 5-二甲基-2, 5-二氢呋喃(EFFC)的结构表征
EFFC: m.p. 224~227 ℃; 1H NMR (CDCl3, 300 MHz) δ: 1.25 (t, J=6.9 Hz, 6H), 1.63 (s, 6H), 3.49 (q, J=6.9 Hz, 4H), 6.73 (q, J=6.3 Hz, 3H), 7.55 (t, J=7.8 Hz, 2H), 7.74 (d, J=9.0 Hz, 1H); IR (KBr) ν: 1155, 1186, 1274, 1321, 1346, 1398, 1496, 1560, 1589, 2221, 2927, 2974 cm-1. Anal. calcd for C32H34N6O2: C 73.74, H 6.15, N 15.64; found C 73.45, H 6.15, N 15.64.表征结果与参考文献[10]一致.
3.2.5 2-二氰亚甲基-3-氰基-4-[2-(4-对二乙胺基偶氮苯基-4)-乙烯基]-5, 5-二甲基-2, 5-二氢呋喃(EFNC)的结构表征
EFNC: m.p. 240~243 ℃; 1H NMR (CDCl3, 300 MHz) δ: 1.27 (d, J=6.9 Hz, 2H), 1.82 (s, 6H), 3.50 (q, J=4.5 Hz, 4H), 6.76 (d, J=9.0 Hz, 2H), 7.04 (d, J=16.2 Hz, 1H), 7.67 (q, J=8.7 Hz, 3H), 7.90 (q, J=3.3 Hz, 4H); IR (KBr) ν: 1126, 1157, 1218, 1276, 1311, 1373, 1463, 1541, 1577, 1600, 2227, 2979 cm-1. Anal. calcd for C32H34N6O2: C 72.71, H 5.67, N 18.17; found C 73.06, H 5.87, N 18.15.表征结果与参考文献[17]一致.
辅助材料(Supporting Information) EFFC的红外光谱以及核磁共振氢谱的原始谱图, EFNC的红外光谱以及核磁共振氢谱的原始谱图, EFNFC及相应中间体红外光谱的原始谱图, EFNFC的核磁共振氢谱的原始谱图, EFFC、EFNC、EFNFC在不同溶剂中测定的详细数据, 利用溶致变色法计算的有关EFFC、EFNC、EFNFC的μgβ值和相对值.这些材料可以免费从本刊网站(http://sioc-journal.cn/)上下载.
3.2.4 2-二氰亚甲基-3-氰基-4-[2-(4-二乙胺基-偶氮苯基-呋喃基-5)-乙烯基]-5, 5-二甲基-2, 5-二氢呋喃(EFNFC)的合成
取2 (0.61 g; 2.5 mmol)和TCF (0.5 g; 2.5 mmol)在乙醇溶液中回流, 回流开始后加入1滴哌啶.反应2 h, 蒸干溶剂, 以二氯甲烷为淋洗剂过柱得到最终产物黑色固体0.76 g, 产率69.1%. m.p. 257~260 ℃; 1H NMR (CDCl3, 300 MHz) δ: 1.05 (t, J=1.8 Hz, 6H), 1.61 (s, 6H), 3.25 (q, J=2.1 Hz, 4H), 6.54 (s, 2H), 6.82 (s, 2H), 6.96 (s, 2H), 8.14 (d, J=10.5 Hz, 2H); IR (KBr) ν: 1157, 1317, 1363, 1427, 1596, 1618, 2235, 3446 cm-1. Anal. calcd for C26H24N6O2: C 69.01, H 5.35, N 18.57; found C 70.03, H 5.67, N 18.25.
3.2.1 5-叠氮基糠醛的合成
将5-硝基糠醛(1 g, 7.1 mmol, 145.11 g/mol)溶于14 mL DMSO中, 一点点加入叠氮钠(0.46 g, 7.1 mmol)(在1.5 h内加完).在水浴中保持20 ℃搅拌2 h后, 反应体系慢慢加入100 mL冰水中, 用氯仿萃取, 有机层用盐水洗后以硫酸钠干燥, 过滤蒸除溶剂后得到棕色固体0.86 g, 产率85.8%.
-
-
[1]
Liu, F.-G.; Wang, H.-R.; Yang, Y.-H.; Xu, H.-J.; Yang, D.; Bo, S.-H.; Liu, J.-H.; Zhen, Z.; Liu, X.-H.; Qiu, L. Dyes Pigm. 2015, 114, 196. doi: 10.1016/j.dyepig.2014.11.015
-
[2]
Morales, A.-R.; Frazer, A.; Woodward, A.-W.; Ahn-White, H.-Y.; Fonari, A.; Tongwa, P.; Timofeeva, T.; Belfield, K.-D. J. Org. Chem. 2013, 78, 1014. doi: 10.1021/jo302423p
-
[3]
Xu, H.-J.; M.-L.; Zhang, A.-R.; Deng, G.-W.; Si, P.; Huang, H.-Y.; Peng, C.-C.; Fu, M.-K.; Liu, J.-L. Qiu, L.; Zhen, Z.; Bo, S.-H.; Liu, X.-H. Dyes Pigm. 2014, 102, 142. doi: 10.1016/j.dyepig.2013.10.042
-
[4]
Wu, J.-Y.; Liu, J.-L.; Zhou, T.-T.; Bo, S.-H.; Qiu, L.; Zhen, Z.; Liu, X.-H. RSC Adv. 2012, 2, 1416. doi: 10.1039/C1RA00838B
-
[5]
Robinson, B.-H.; Dalton, L.-R.; Harper, A.-W. J. Mater. Sci.:Mater. Electron. 2014, 25, 3633. doi: 10.1007/s10854-014-2067-z
-
[6]
Robinson, B.-H.; Dalton, L.-R.; Harper, A.-W. Chem. Phys. 1999, 245, 35. doi: 10.1016/S0301-0104(99)00079-8
-
[7]
Wang, H.-R.; Liu, F.-G.; Yang, Y.-H. Dyes Pigm. 2015, 112, 42. doi: 10.1016/j.dyepig.2014.06.024
-
[8]
Cho, B.-R.; Son, K.-N.; Lee, S.-J.; Kang, T.-I.; Han, M.-S.; Jeon, S.-J.; Song, N.-W.; Kim, D. Tetrahedron Lett. 1998, 39, 3167. doi: 10.1016/S0040-4039(98)00450-X
-
[9]
Gong, W.; Li, Q.-Q.; Li, S.-Y.; Lu, C.-G.; Li, Z. Zhu, J.; Zhu, Z.-C.; Li, Z.-A.; Wang, Q.-R.; Cui, Y.-P.; Qin, J.-G. Mater. Lett. 2007, 61, 1151. doi: 10.1016/j.matlet.2006.06.070
-
[10]
唐翔, 唐先忠, 游英才, 任立柯, 王洋, 严立京, 化学学报, 2012, 70, 1565. doi: 10.6023/A12030006Tang, X.; Tang, X.-Z.; You, Y.-C.; Ren, L.-K.; Wang, Y.; Yan, L.-J. Acta Chim. Sinica 2012, 70, 1565(in Chinese). doi: 10.6023/A12030006
-
[11]
Qiu, L.; Shen, Y.-Q.; Hao, J.-M.; Zhai, J.-F.; Zu, F.-H.; Zhang, T.; Zhao, Y.-X.; Clays, K.; Persoons, A. J. Mater. Sci. 2004, 39, 2335. doi: 10.1023/B:JMSC.0000019994.38191.fe
-
[12]
Ashraf, M.; Teshome, A.; Kay, A.-J.; Gainsford, G.-J.; Bhuiyan, M.-D.; Asselberghs, I.; Clays, K. Dyes Pigm. 2012, 95, 455. doi: 10.1016/j.dyepig.2012.04.022
-
[13]
Ashraf, M.; Teshome, A.; Kay, A.-J.; Gainsford, G.-J.; Bhuiyan, M.-D.; Asselberghs, I.; Clays, K. Dyes Pigm. 2013, 98, 82. doi: 10.1016/j.dyepig.2013.01.010
-
[14]
Traskovskis, K.; Zarins, E.; Laipniece, L.; Tokmakovs, A.; Kokars, V.; Rutkis, M. Mater. Chem. Phys. 2015, 155, 232. doi: 10.1016/j.matchemphys.2015.02.035
-
[15]
Hao, J.-M.; Han, M.-J.; Guo, K.-P.; Zhao, Y.-X.; Qiu, L.; Shen, Y.-Q.; Meng, X.-G. Mater. Lett. 2008, 62, 973. doi: 10.1016/j.matlet.2007.07.023
-
[16]
Guo, K.-P.; Hao, J.-M.; Zhang, T.; Zu, F.-H.; Zhai, J.-F.; Qiu, L.; Zhen, Z.; Liu, X.-H.; Shen, Y.-Q. Dyes Pigm. 2008, 77, 657. doi: 10.1016/j.dyepig.2007.09.006
-
[17]
王洋, 唐先忠, 唐翔, 高等学校化学学报, 2011, 32, 2327.Wang, Y.; Tang, X.-Z.; Tang, X. Chem. J. Chin. Univ. 2011, 32, 2327(in Chinese).
-
[18]
花建丽, 李俊, 罗敬东, 有机化学, 2003, 23(1), 44. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract327321.shtmlHua, J.-L.; Li, J.; Luo, J.-D. Chin. J. Org. Chem. 2003, 23(1), 44(in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract327321.shtml
-
[19]
Luo, J.-D.; Hua, J.-L.; Qin, J.-G.; Cheng, J.-Q.; Shen, Y.-C.; Lu, Z.-H.; Wang, P.; Ye, C. Chem. Commun. 2001, 171-172.
-
[20]
Bosshard, C.; Knpfle, G.; Prêtre, P. J. Appl. Phys. 1992, 71, 1594. doi: 10.1063/1.351237
-
[21]
Paley, M.; Harris, J. J. Polym. Sci. Part A:Polym. Chem. 1987, 25(9), 2447. doi: 10.1002/pola.1987.080250910
-
[22]
Qian, Y.; Lin, B.-Q.; Xiao, G.-M. Opt. Mater. 2004, 27, 125-130. doi: 10.1016/j.optmat.2004.02.017
-
[23]
Immirizi, A.; Perini, B. Acta Crystallogr. Sect. A 1977, 33, 216. doi: 10.1107/S0567739477000448
-
[1]
-
表 1 各生色团的热学和光学性能数据
Table 1. Characterization data of the chromophores
Chromophore DE/eV β0a/(10-28 esu) λmaxb/nm Λmaxc/nm λmax/nm ξmax/(104 L•mol-1•cm-1) μgβ1064nm/ (10-49 esu) Td/℃ ξmaxb ξmaxc ξmaxd, e EFFC 2.190 5.459 676 644 633d 1.051 1.731 1.205d 3.194 250 EFNC 2.259 7.498 568 544 585e 3.201 3.680 3.115e 5.971 254 EFNFC 2.104 3.662 573 598 575e 2.263 1.760 1.018e 4.479 270 aβ0=βvec=||β||=(Σβi2)1/2; bMeasured in DMSO; cMeasured in Acetone; dMeasured in Ethyl acetate; eMeasured in Chloroform. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 1745
- HTML全文浏览量: 318




 下载:
下载:



 下载:
下载:

