 图1
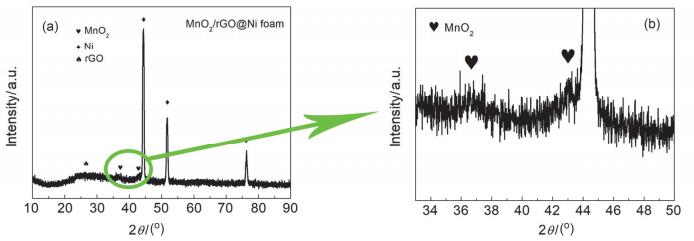
MnO2/rGO@Ni foam电极的XRD谱图(a)和(a)图的局部放大图(b)
Figure1.
XRD patterns of the MnO2/rGO@Ni foam electrode (a) and partial enlargement (b) of (a)
图1
MnO2/rGO@Ni foam电极的XRD谱图(a)和(a)图的局部放大图(b)
Figure1.
XRD patterns of the MnO2/rGO@Ni foam electrode (a) and partial enlargement (b) of (a)

Citation: Song Congying, Sun Xun, Ye Ke, Zhu Kai, Cheng Kui, Yan Jun, Cao Dianxue, Wang Guiling. Electrocatalytic Activity of MnO2 Supported on Reduced Graphene Oxide Modified Ni Foam for H2O2 Reduction[J]. Acta Chimica Sinica, 2017, 75(10): 1003-1009. doi: 10.6023/A17070298

还原氧化石墨烯修饰泡沫镍原位负载MnO2对H2O2电还原反应催化性能的研究
English
Electrocatalytic Activity of MnO2 Supported on Reduced Graphene Oxide Modified Ni Foam for H2O2 Reduction
-
Key words:
- MnO2
- / rGO
- / H2O2
- / electrocatalysis
- / hydrothermal method
-
1 引言
燃料电池是一种新型的能源转换装置, 具有高效、无污染等优点而被广泛关注和研究.传统的氢氧燃料电池是一种目前应用较为广泛的燃料电池, 但是在水下或者太空环境中, 大量携带氧气仍然存在诸多困难, 这一缺点大大限制了氢氧燃料电池的发展.因此寻找一种能够在水下和太空中大量存储和运输并且能够代替氧气作为氧化剂的新燃料具有非常重要的研究意义. H2O2是一种液体强还原剂, 它的还原反应是一个2电子过程.与氧气的还原反应(4电子过程)相比[1, 2], 具有更快的动力学和更低的活化过电势[3].且液体的H2O2储存运输方便, 特别适合空间、水下等无氧环境; 液相进料使得以H2O2为氧化剂的燃料电池在操作过程中不需要润湿过程, 电池结构更简单, 体积功率密度更大, 是一类非常有发展前景的燃料电池[4~7].
电极材料是决定燃料电池性能的重要因素之一.目前, 研究较多的应用于催化H2O2电还原反应的催化剂主要包括以下三类: (1) 贵金属, 包括Au、Pd、Pt等以及它们的合金[8~12]; (2) 过渡金属氧化物, 包括Co3O4, NiCo2O4, MnO2等[13, 14]; (3) 贵金属和过渡金属氧化物的复合物. MnO2是一种对H2O2电还原反应具有良好的催化性能的电极材料[15~17], 然而传统的MnO2催化剂大多由粉末和导电材料利用粘结剂混合制成, 粘结剂的使用不可避免地降低了催化剂材料的利用率并使得电极的成本增加.因此, 研究能够直接生长在集流体表面的催化剂材料具有非常重要的意义.其中, 集流体的选择在电极的设计和制备过程中起到关键作用[18].泡沫镍是一种具有三维孔道结构的导电集流体被大量应用于电极材料的制备.石墨烯具有巨大的比表面积和优异的电性能是一种理想的电极材料[19~21].若将石墨烯与泡沫镍进行进一步复合, 可以制备出电性能更优异, 比表面积更大的导电集流体.
基于以上考虑, 本文利用一步简单易操作的水热法制备出具有良好形貌的还原氧化石墨烯修饰泡沫镍基体, 在其表面直接生长MnO2纳米片作为催化H2O2电还原反应的催化剂.还原氧化石墨烯的添加可以有效增大电极的比表面积并能起到分散MnO2纳米片的作用, 避免团聚现象的发生.且还原氧化石墨烯和MnO2纳米片之间互相穿插, 可以为电极反应提供更多电子转移的通道.
2 结果与讨论
2.1 MnO2/rGO@Ni foam电极的组成和形貌表征
图 1(a)为MnO2/rGO@Ni foam电极的XRD谱图.从图中可以看出该谱图上有三个较为强烈的衍射峰, 分别位于44.5°, 51.8°和76.3°, 通过与标准卡片相比对, 它们分别对应于Ni基体(JCPDS Card NO.40-0850) 的(111)、(200)、(220) 晶面, 且衍射峰比较尖锐并无其他杂峰表明在电极的制备过程中Ni元素并未发生氧化或生成其他含Ni化合物, 仍是以金属态存在.另外, 在2θ为26°时, 出现了一个峰宽较宽、峰强较弱的衍射峰, 对应于rGO的衍射峰, 在2θ为12.4°没有出现明显的GO衍射峰, 说明GO的还原程度较好.在该XRD谱图上, 没有观察到明显的MnO2的衍射峰, 这是由于通过水热法制备的MnO2的含量相对于基体泡沫镍而言非常少, 其衍射峰受泡沫镍衍射峰掩蔽而无法被观察到.为了更清楚地观察和判断是否有MnO2的衍射峰存在, 将图 1(a)中绿色区域的谱线进行放大得到1(b)图, 从1(b)图中可以发现, 在2θ为37.0°和43.2°位置处有两个较弱的衍射峰, 分别对应于MnO2 (JCPDS Card NO.53-0633) 的(330) 和(321) 的晶面, 表明MnO2被成功地制备到了rGO@Ni foam基体上.为了进一步探究电极的组成, 我们还对制备的rGO@Ni foam基体和MnO2/rGO@Ni foam电极的拉曼光谱图进行了测试和分析, 结果如支持信息中的图S1所示.
 图1
MnO2/rGO@Ni foam电极的XRD谱图(a)和(a)图的局部放大图(b)
Figure1.
XRD patterns of the MnO2/rGO@Ni foam electrode (a) and partial enlargement (b) of (a)
图1
MnO2/rGO@Ni foam电极的XRD谱图(a)和(a)图的局部放大图(b)
Figure1.
XRD patterns of the MnO2/rGO@Ni foam electrode (a) and partial enlargement (b) of (a)
图 2分别为rGO@Ni foam (a, c)和MnO2/rGO@Ni foam (b, d)电极的SEM图片.从图 2(a)和2(c)中可以看出, 经过第一步水热处理之后, rGO以片状的形式均匀地生长在泡沫镍的表面, 片与片之间互相交叉形成团簇状结构.从2(c)图中可以看出, 片与片之间形成了大量的孔道, 可以有效增大电极的比表面积, 并能使得电解液与电极表面充分接触.经过第二步水热处理之后, 从图 2(b), 2(d)和2(e)中可以看出, 在rGO片层的表面生长了一层均匀致密的MnO2.从放大的2(d)和2(e)图中可以看出, MnO2呈现出由众多的薄片组成的蜂窝状结构.大量的孔道仍然存在在电极表面, 有利于反应物向催化剂内部扩散并发生充分的反应.从图 2(d)和2(e)中绿色区域显示, 生长的MnO2层存在许多突起, 表面凹凸不平, 这是下部的rGO的支撑作用造成的.为了进一步探究MnO2/rGO@Ni foam电极的微观形貌, 对电极进行了透射电子显微镜的测试.电极的TEM和HRTEM图片如下图 3所示. 图 3(a)中, rGO片层厚度非常薄且带有许多褶皱, 这些褶皱的存在可以对MnO2起到很好的支撑和分散的作用. 图 3(a)中右半部分尺寸较小的薄片为MnO2, 宽度大约在50 nm左右.另外, 从图中可以看出, MnO2纳米片是由尺寸更小的纳米颗粒组成, 且颗粒与颗粒之间形成了大量的纳米孔, 有利于H2O2与MnO2的充分接触和反应. 图 3(b)为图 3(a)中绿色区域的HRTEM图, 可以观察到明显的且有规律的晶格条纹, 宽度大约在0.240 nm左右, 对应于MnO2 (JCPDS Card NO.53-0633) 的(330) 晶面, 表明MnO2被成功地制备到了rGO@Ni foam基体上.与此同时, 我们还对制备的MnO2/rGO@Ni foam电极进行了XPS测试, 测试结果如支持信息中图S2所示. XPS的结果同样表明成功制备了MnO2/rGO@Ni foam电极.
2.2 MnO2/rGO@Ni foam电极的电化学性能
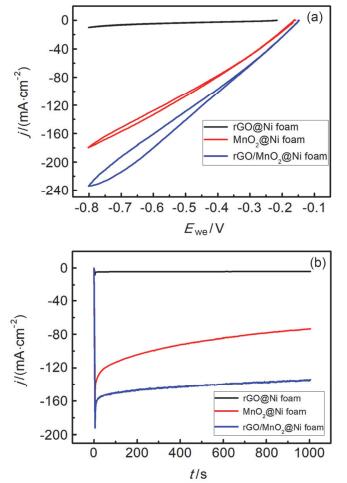
为了探究rGO的添加对电极催化性能的影响, 对三种不同电极(rGO@Ni foam, MnO2@Ni foam, MnO2/rGO@Ni foam)在3 mol/L NaOH和1.0 mol/L H2O2溶液中的循环伏安曲线(CVs)和计时电流曲线(CAs)进行了测试, 结果如下图 4所示.从图 4(a)中可以看出, rGO@Ni foam基体对H2O2的电还原反应几乎不具有催化性能, 在测试的整个电位范围内, 电流密度基本接近于0.而MnO2@Ni foam电极的CV曲线上的电流密度随电极电势的负移而变大, 在电位为-0.8 V时对应的电流密度约为180 mA/cm2, 这说明MnO2对H2O2的电还原反应具有显著地催化作用. MnO2/rGO@Ni foam电极的CV曲线与MnO2@Ni foam电极的CV曲线变化趋势基本相同, 但是在相同的电极电势下MnO2/rGO@Ni foam电极的CV曲线对应的电流密度更高, -0.8 V时对应的电流密度约为240 mA/cm2.这表明MnO2/rGO@Ni foam电极的催化性能要远高于MnO2@Ni foam.主要原因是片状rGO的加入极大地提高了催化剂的比表面积, 增加了单位面积上的电化学活性位数目, 且rGO与MnO2纳米片的互相穿插提供了更多的电子传递通道, 基于这两点原因使其催化H2O2电还原的速率有了显著地提升.为了探究rGO的添加对电极比表面积的影响, 我们采用电化学方法对MnO2/rGO@Ni foam电极和MnO2@Ni foam电极的比表面积进行了测量, 如支持信息中图S3所示, 结果表明rGO的添加有效地增大了电极的比表面积. 图 4(b)为三种电极的CA曲线的对比图, 显示了与图 4(a)相同的规律.另外从图 4(b)中可以看出, 在测试时间范围内, MnO2/rGO@Ni foam电极表现出良好的稳定性, 而MnO2@Ni foam电极上的电流密度随着时间的推移呈现出明显的下降趋势, 表明rGO不仅提高了电极的催化性能, 也使得电极的稳定性得到了改善.
图 5(a)为MnO2/rGO@Ni foam电极在不同NaOH浓度条件下的CV曲线对比图.从图中可以看出, 在不同的NaOH浓度下, 电极反应的开路电位基本保持不变, 均为0.15 V左右.但是电极电势达到-0.8 V时, 不同NaOH浓度下的电解液中H2O2的还原电流密度出现很大差别, 分别为121, 142, 233和176 mA/cm2.当NaOH浓度在1~3 mol/L范围内, 电流密度随NaOH浓度增大而增大, 但当NaOH浓度由3 mol/L增大到4 mol/L时, 电流密度随NaOH浓度增大而减小.在此范围内, 电解液中最佳的NaOH浓度为3 mol/L.这是由于当NaOH浓度较小时, 随着NaOH浓度增大, 电解液的导电率随之增大进而提高了反应速率.但是当NaOH浓度提高到一定程度时, 大量的OH-存在于溶液中会与HO2-竞争吸附到电极表面, 减小了HO2-与电极的有效接触进而导致电极反应速率的降低, 出现电流密度随NaOH浓度升高而下降的现象. 图 5(b)和(c)为MnO2/rGO@Ni foam电极在不同H2O2浓度溶液中的CV和CA曲线, 探究了反应物浓度对电极催化性能的影响.从图中可以发现, 随着反应物浓度的增大, 电极上H2O2的还原电流密度呈现出先增大后减小的趋势.在电位为-0.8 V时, 电流密度分别为79, 113, 236和146 mA/cm2.由此可知, 最佳的H2O2浓度为1.0 mol/L, 反应速率在循环伏安曲线中的直观表现就是电流密度, 所以此时的H2O2电还原速率最大.电流密度可以表示电极反应, 根据法拉第定律可推出以下方程:
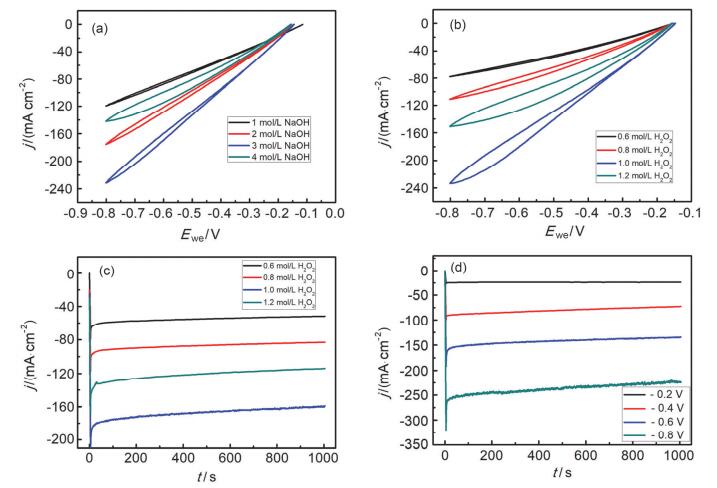 图5
MnO2/rGO@Ni foam电极在1.0 mol/L H2O2和X mol/L NaOH (X=1~4) 溶液中的循环伏安对比图(a); 在3.0 mol/L NaOH和X mol/L H2O2 (X=0.6, 0.8, 1.0, 1.2) 溶液中的循环伏安(b)和计时电流(c)对比图; 在1.0 mol/L H2O2和3 mol/L NaOH溶液中不同电位时的计时电流图(d)
Figure5.
CVs (a) of the MnO2/rGO@Ni foam electrode in solutions of different NaOH concentration with a fixed concentration of H2O2 (1.0 mol/L); CVs (b) and CAs (c) of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and different concentrations of H2O2; CAs (d) of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and 0.5 mol/L H2O2 at different applied potentials
图5
MnO2/rGO@Ni foam电极在1.0 mol/L H2O2和X mol/L NaOH (X=1~4) 溶液中的循环伏安对比图(a); 在3.0 mol/L NaOH和X mol/L H2O2 (X=0.6, 0.8, 1.0, 1.2) 溶液中的循环伏安(b)和计时电流(c)对比图; 在1.0 mol/L H2O2和3 mol/L NaOH溶液中不同电位时的计时电流图(d)
Figure5.
CVs (a) of the MnO2/rGO@Ni foam electrode in solutions of different NaOH concentration with a fixed concentration of H2O2 (1.0 mol/L); CVs (b) and CAs (c) of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and different concentrations of H2O2; CAs (d) of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and 0.5 mol/L H2O2 at different applied potentials
式中v电极反应速度(mol/s); S电极的表面积(cm2); c反应物浓度(mol/L); t反应时间(s); n一个反应粒子所需要的电子数; F法拉第常数(C/mol).
从上式中可以看出, 在电极电位不变的情况下, 电流密度随反应物浓度的增大而增大, 即速率也随H2O2浓度的增大而增大.但是当过氧化氢浓度大于1.0 mol/L时, 反应速率随H2O2浓度的增大反而减小, 这是由于H2O2本身极易分解, NaOH虽有抑制H2O2分解的作用, 但是当其浓度较高时, 在电解液中仍然不能稳定存在, 会分解产生O2.此时, 随着H2O2浓度增大, 分解产生O2的速率也随之增大, 产生的O2不能及时逸出, 造成电极表面的气体积累, 阻隔H2O2与催化剂的接触, H2O2直接电还原速率下降. H2O2分解是不被期望的副反应, 不但浪费燃料, 而且在组成电池时会增加电池内部气压, 造成电池变形, 甚至引起爆炸, 造成安全隐患.因此选择合适的H2O2浓度非常重要, 在本实验中的后续电化学测试中, 都选用过氧化氢浓度为1.0 mol/L进行测试对比分析.从图 5(c)的CA曲线中可以看出, 电极在不同H2O2溶液中均表现出良好的稳定性, 且反映出与CV曲线相同的规律.当H2O2浓度为1.2 mol/L, CA曲线出现了小范围的抖动, 这是由于H2O2分解产生的气泡对曲线的测量产生了扰动. 图 5(d)为电极在3 mol/L NaOH和1.0 mol/L H2O2溶液中不同电位条件下的CA曲线, 随着电位的负移, 电流密度呈现出明显的增大趋势.这是由于过电位增大也就意味着反应的推动力增大, 由tafel方程可知, 过电位越大, 电流密度也就越大.同样, 从图 5(d)中可以看出, 电极在不同电位条件下均表现出良好的稳定性.
图 6为MnO2@Ni foam和MnO2/rGO@Ni foam电极在电位为-0.6 V时在3 mol/L NaOH+X mol/L H2O2 (X=0, 1) 溶液中的电化学阻抗谱图.从图中可以看出, 当不添加H2O2时, 两种电极的电化学阻抗谱图均呈一条直线, 表明此时电极表面没有电化学反应发生.当加入H2O2后, 两种电极的电化学阻抗谱则都呈现出一个半圆的形状, 这是由于溶液中的众多H2O2迁移到电极表面(固-液界面)得到两个电子被还原为OH-, 这个半圆的出现对应于H2O2的电还原反应. 图 6中的插图为两种电极上H2O2的电还原反应的等效电路.由图中绿色方框标记的区域的放大图可以看出, 添加rGO后, 电极和电解液的欧姆阻抗(RS)从1.287 Ω减小到0.913 Ω.表明rGO的的添加提高了电极的导电性, 电极导电性的提高为电极催化性能的提高也做出了一定贡献.另外, 电化学阻抗谱图中半圆的直径代表了电荷转移电阻, 其大小能够反映出电极反应动力学的快慢.从图中可以明显地看出, 加入rGO后, 半圆的直径显著减小, 电荷转移电阻从10.84 Ω减小到4.97 Ω, 表明rGO的加入加速了电极反应的进行, 使得电极的催化性能得到了提高.
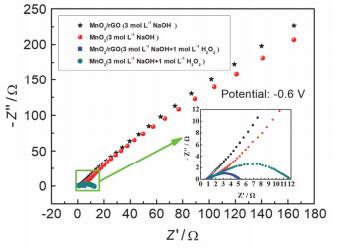 图6
MnO2@Ni foam和MnO2/rGO@Ni foam电极在3 mol/L NaOH+X mol/L H2O2 (X=0, 1) 溶液中的电化学阻抗谱图.插图为绿色方框区域的放大图(测试电位: -0.6 V)
Figure6.
Electrochemical impedance spectra of MnO2@Ni foam and MnO2/rGO@Ni foam electrodes in solutions of 3 mol/L NaOH+X mol/L H2O2 (X=0, 1) at -0.6 V. The insert is the enlargement of the region marked by green rectangle
图6
MnO2@Ni foam和MnO2/rGO@Ni foam电极在3 mol/L NaOH+X mol/L H2O2 (X=0, 1) 溶液中的电化学阻抗谱图.插图为绿色方框区域的放大图(测试电位: -0.6 V)
Figure6.
Electrochemical impedance spectra of MnO2@Ni foam and MnO2/rGO@Ni foam electrodes in solutions of 3 mol/L NaOH+X mol/L H2O2 (X=0, 1) at -0.6 V. The insert is the enlargement of the region marked by green rectangle
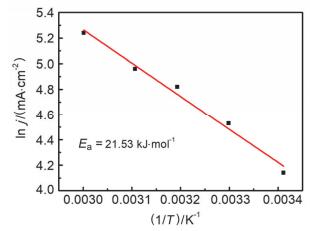
为了探究反应温度对MnO2/rGO@Ni foam电极催化性能的影响, 对电极在不同温度条件下的极化曲线进行了测量和分析, 测试的电解液仍为3 mol/L NaOH和1.0 mol/L H2O2, 结果如下图 7所示.将5个温度(293, 303, 313, 323, 333 K)条件下极化曲线的塔菲尔区进行外推, 得到与过电位为0的水平线的交点即可得到不同温度条件下的交换电流密度值. 图 7(f)显示了不同温度条件下的交换电流密度值, 可以看出, 随着温度的升高, 交换电流密度逐渐增大, 分别为62.95, 92.68, 123.59, 142.23, 188.80 mA/cm2, 这是由于随着温度的升高, 反应物在体系中的传质速率增大, 进而使得交换电流密度增大.结合不同温度条件下的交换电流密度值和阿伦尼乌斯公式即可求得H2O2在MnO2/rGO@Ni foam电极上直接电还原反应的活化能. 图 8为交换电流密度的自然对数ln(j0)与反应温度的倒数(1/T)的关系曲线图.式(2) 为阿伦尼乌斯公式:
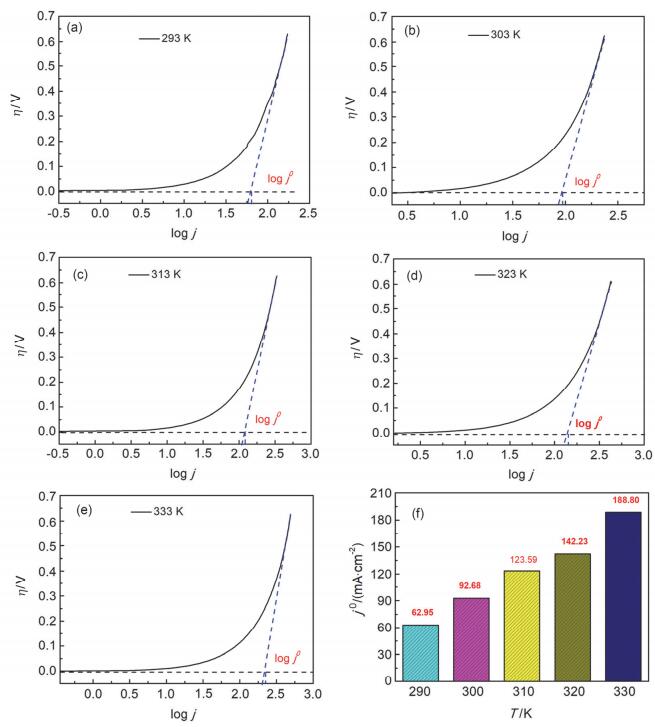 图7
MnO2/rGO@Ni foam电极在3 mol/L NaOH和1.0 mol/L H2O2溶液中不同温度下的极化曲线(a) 293, (b) 303, (c) 313, (d) 323, (e) 333 K和不同温度下的交换电流密度柱状图(f)
Figure7.
Polarization curves of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and 1.0 mol/L H2O2 at five temperatures (a) 293, (b) 303, (c) 313, (d) 323, (e) 333 K and histogram (f) of exchange current densities j0 (mA·cm-2) under different temperatures
图7
MnO2/rGO@Ni foam电极在3 mol/L NaOH和1.0 mol/L H2O2溶液中不同温度下的极化曲线(a) 293, (b) 303, (c) 313, (d) 323, (e) 333 K和不同温度下的交换电流密度柱状图(f)
Figure7.
Polarization curves of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and 1.0 mol/L H2O2 at five temperatures (a) 293, (b) 303, (c) 313, (d) 323, (e) 333 K and histogram (f) of exchange current densities j0 (mA·cm-2) under different temperatures
式中: j测量电流密度mA/cm2; T反应温度(K); Ea表观活化能(kJ/mol); R气体常数[8.314 J·(mol·K)-1].
经过计算可得, H2O2在MnO2/rGO@Ni foam电极上直接电还原反应的活化能为21.53 kJ·mol-1, 明显低于文献中报道的数值[22, 23], 表明MnO2/rGO@Ni foam电极对H2O2的电还原反应具有优异的催化性能.
3 结论
综上所述, 本论文以rGO为添加剂, 采用一步水热法制备了rGO@Ni foam新型导电集流体.并通过再一步水热法将MnO2纳米片均匀生长在rGO@Ni foam基体表面制备得到了MnO2/rGO@Ni foam电极.通过各项电化学测试结果可知, MnO2/rGO@Ni foam电极对H2O2的电还原反应表现出了良好的催化性能.其中, rGO的添加可以增大电极的比表面积, 并能提供更多的电子转移通道, 使得电极的催化性能和稳定性较MnO2@Ni foam电极均得到了大幅度的提升.在3 mol/L NaOH和1.0 mol/L H2O2溶液中, 电位为-0.8 V时, MnO2/rGO@Ni foam电极上H2O2的还原电流密度可以达到240 mA/cm2, 电极反应活化能为21.53 kJ/mol, 充分证明制备的MnO2/rGO@Ni foam是一种非常具有发展前景的电极材料.
4 实验部分
MnO2/rGO@Ni foam电极的制备过程如下图 9所示.本实验中使用的氧化石墨烯(GO)是由改进的Hummers法制备得到[24].将得到的氧化石墨烯配置成浓度为1 mg/mL的溶液待用.
首先, 对泡沫镍进行前处理.将裁剪后的泡沫镍分别置于丙酮和6 mol/L的盐酸溶液中超声处理15 min, 然后用去离子水清洗并干燥.量取15 mL GO分散液稀释至40 mL, 与处理好的泡沫镍一起转移至100 mL的反应釜中160 ℃反应16 h.反应结束后, 待反应釜冷却至室温即可得到rGO修饰泡沫镍基体(rGO@Ni foam).接着称取0.2528 g高锰酸钾配置成40 mL溶液, 并将其与上一步得到的rGO@Ni foam基体一同转移至100 mL反应釜中120 ℃反应12 h即可得到MnO2/rGO@Ni foam.在该过程中, 反应釜内发生的反应如公式(3) 所示
MnO2/rGO@Ni foam电极对H2O2电还原反应催化性能的测试在三电极体系中进行.其中, 工作电极为MnO2/rGO@Ni foam电极, 参比电极为饱和银-氯化银电极(Ag/AgCl, KCl), 辅助电极为碳棒.测试的电解液为NaOH和H2O2的混合溶液.
-
-
[1]
陈鑫, 鄢慧君, 夏定国, 化学学报, 2017, 75, 189. doi: 10.3969/j.issn.0253-2409.2017.02.008Chen, X.; Yan, H.; Xia, D. Acta Chim. Sinica 2017, 75, 189. doi: 10.3969/j.issn.0253-2409.2017.02.008
-
[2]
Li, J.; Zhang, X.; Pan, B. Chin. J. Chem. 2016, 34, 1021. doi: 10.1002/cjoc.v34.10
-
[3]
Sun, L. M.; Cao, D. X.; Wang, G. L.; Lu, Y. Z.; Zhang, M. L. Acta Phys. Chim. Sin. 2008, 24, 323. http://en.cnki.com.cn/Article_en/CJFDTOTAL-WLHX200802027.htm
-
[4]
Ma, J.; Choudhury, N. A.; Sahai, Y. Renew. Sust. Energ. Rev. 2010, 14, 183. doi: 10.1016/j.rser.2009.08.002
-
[5]
田永梅, 雷婷, 王贵领, 曹殿学, 高等学校化学学报, 2011, 32, 2382. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=gdxh201110029&dbname=CJFD&dbcode=CJFQTian, Y. M.; Lei, T.; Wang, G. L.; Cao, D. X. Chem. J. Chin. Univ. 2011, 32, 2382. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=gdxh201110029&dbname=CJFD&dbcode=CJFQ
-
[6]
程魁, 杨帆, 闫鹏, 曹殿学, 殷金玲, 王贵领, 高等学校化学学报, 2014, 35, 110. doi: 10.7503/cjcu20130504Cheng, K.; Yang, F.; Yan, P.; Cao, D. X.; Yin, J. L.; Wang, G. L. Chem. J. Chin. Univ. 2014, 35, 110. doi: 10.7503/cjcu20130504
-
[7]
Li, Z. P.; Liu, B. H.; Arai, K.; Suda, S. J. Electrochem. Soc. 2003, 150, A868. doi: 10.1149/1.1576767
-
[8]
Sun, L. M.; Cao, D. X.; Wang, G. L. J. Appl. Electrochem. 2008, 38, 1415. doi: 10.1007/s10800-008-9581-8
-
[9]
Flätgen, G.; Wasle, S.; Lübke, M.; Eickes, C.; Radhakrishnan, G.; Doblhofer, K.; Ertl, G. Electrochim. Acta 1999, 44, 4499. doi: 10.1016/S0013-4686(99)00184-X
-
[10]
Gerlache, M.; Senturk, Z.; Quarin, G.; Kauffmann, J. M. Electroanal. 1997, 9, 1088. doi: 10.1002/(ISSN)1521-4109
-
[11]
Luo, Y. F.; Li, H. Z.; Chen, T. T.; Ge, C. W.; Tang, Y. W.; Chen, Y.; Lu, T. H. Electrochim. Acta 2013, 87, 839. doi: 10.1016/j.electacta.2012.09.018
-
[12]
Yang, F.; Cheng, K.; Wu, T. H.; Zhang, Y.; Yin, J. L.; Wang, G. L.; Cao, D. X. RSC Adv. 2013, 3, 5483. doi: 10.1039/c3ra23415k
-
[13]
王贵领, 郝世阳, 陆天虹, 曹殿学, 尹翠蕾, 高等学校化学学报, 2010, 31, 2264. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=gdxh201011028&dbname=CJFD&dbcode=CJFQWang, G. L.; Hao, S. Y.; Lu, T. H.; Cao, D. X.; Yin, C. L. Chem. J. Chin. Univ. 2010, 31, 2264. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=gdxh201011028&dbname=CJFD&dbcode=CJFQ
-
[14]
Wang, G. L.; Cao, D. X.; Yin, C. L.; Gao, Y. Y.; Yin, J. L.; Cheng, L. Chem. Mater. 2009, 21, 5112. doi: 10.1021/cm901928b
-
[15]
Cheng, F.; Shen, J.; Ji, W.; Tao, Z.; Chen, J. ACS Appl. Mater. Inter. 2009, 1, 460. doi: 10.1021/am800131v
-
[16]
Ma, Y.; Wang, R.; Wang, H.; Key, J.; Ji, S. J. Power Sources 2015, 280, 526. doi: 10.1016/j.jpowsour.2015.01.139
-
[17]
Roche, I.; Chaînet, E.; Chatenet, M.; Vondrák, J. J. Phys. Chem. C 2007, 111, 1434. doi: 10.1021/jp0647986
-
[18]
闫鹏, 张栋铭, 程魁, 徐阳, 李莹莹, 叶克, 曹殿学, 王贵领, 高等学校化学学报, 2015, 36, 1801. http://www.cjcu.jlu.edu.cn/CN/abstract/abstract25816.shtmlYan, P.; Zhang, D. M.; Cheng, K.; Xu, Y.; Li, Y. Y.; Ye, K.; Cao, D. X.; Wang, G. L. Chem. J. Chin. Univ. 2015, 36, 1801. http://www.cjcu.jlu.edu.cn/CN/abstract/abstract25816.shtml
-
[19]
Quan, Q.; Lin, X.; Zhang, N.; Xu, Y. J. Nanoscale 2017, 9, 2398. doi: 10.1039/C6NR09439B
-
[20]
Han, C.; Zhang, N.; Xu, Y. J. Nano Today 2016, 11, 351. doi: 10.1016/j.nantod.2016.05.008
-
[21]
Yang, M. Q.; Zhang, N.; Wang, Y.; Xu, Y. J. J. Catal. 2017, 346, 21. doi: 10.1016/j.jcat.2016.11.012
-
[22]
Hu, C.; Bai, Z.; Yang, L.; Lv, J.; Wang, K.; Guo, Y.; Cao, Y.; Zhou, J. Electrochim. Acta 2010, 55, 6036. doi: 10.1016/j.electacta.2010.05.063
-
[23]
Cao, D.; Sun, L.; Wang, G.; Lv, Y.; Zhang, M. J. Electroanal. Chem. 2008, 621, 31. doi: 10.1016/j.jelechem.2008.04.007
-
[24]
Marcano, D. C.; Kosynkin, D. V.; Berlin, J. M.; Sinitskii, A.; Sun, Z.; Slesarev, A.; Alemany, L. B.; Lu, W.; Tour, J. M. ACS Nano 2010, 4, 4806. doi: 10.1021/nn1006368
-
[1]
-
图 5 MnO2/rGO@Ni foam电极在1.0 mol/L H2O2和X mol/L NaOH (X=1~4) 溶液中的循环伏安对比图(a); 在3.0 mol/L NaOH和X mol/L H2O2 (X=0.6, 0.8, 1.0, 1.2) 溶液中的循环伏安(b)和计时电流(c)对比图; 在1.0 mol/L H2O2和3 mol/L NaOH溶液中不同电位时的计时电流图(d)
Figure 5 CVs (a) of the MnO2/rGO@Ni foam electrode in solutions of different NaOH concentration with a fixed concentration of H2O2 (1.0 mol/L); CVs (b) and CAs (c) of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and different concentrations of H2O2; CAs (d) of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and 0.5 mol/L H2O2 at different applied potentials
图 6 MnO2@Ni foam和MnO2/rGO@Ni foam电极在3 mol/L NaOH+X mol/L H2O2 (X=0, 1) 溶液中的电化学阻抗谱图.插图为绿色方框区域的放大图(测试电位: -0.6 V)
Figure 6 Electrochemical impedance spectra of MnO2@Ni foam and MnO2/rGO@Ni foam electrodes in solutions of 3 mol/L NaOH+X mol/L H2O2 (X=0, 1) at -0.6 V. The insert is the enlargement of the region marked by green rectangle
图 7 MnO2/rGO@Ni foam电极在3 mol/L NaOH和1.0 mol/L H2O2溶液中不同温度下的极化曲线(a) 293, (b) 303, (c) 313, (d) 323, (e) 333 K和不同温度下的交换电流密度柱状图(f)
Figure 7 Polarization curves of the MnO2/rGO@Ni foam electrode in 3 mol/L NaOH and 1.0 mol/L H2O2 at five temperatures (a) 293, (b) 303, (c) 313, (d) 323, (e) 333 K and histogram (f) of exchange current densities j0 (mA·cm-2) under different temperatures
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 16
- 文章访问数: 3082
- HTML全文浏览量: 677





 下载:
下载:








 下载:
下载:

