 图 1
小分子化合物的合成路线
Figure 1.
Synthesis of Zinc(Ⅱ)-salen complex (ZSC)
图 1
小分子化合物的合成路线
Figure 1.
Synthesis of Zinc(Ⅱ)-salen complex (ZSC)

Citation: Wang Yafen, Zhang Xiong, Liu Chaoxing, Zhou Xiang. Induction Stabilization and Fluorescence-based Switch-on Detection of G-Quadruplex by Zinc (Ⅱ)-salen Complex[J]. Acta Chimica Sinica, 2017, 75(7): 692-698. doi: 10.6023/A17040162

锌配体化合物选择性诱导、稳定、荧光检测G-四联体
English
Induction Stabilization and Fluorescence-based Switch-on Detection of G-Quadruplex by Zinc (Ⅱ)-salen Complex
-
Key words:
- Zinc (Ⅱ)-salen complex
- / selectivity
- / G-quadruplex
- / fluorescence
- / stability
-
1 引言
高选择性的荧光打开检测(Fluorescence-based Switch-on Detection)核酸是表观遗传学中很重要的研究领域之一.荧光信号从无到有, 可以非常有效地降低检测背景, 从而实现对目标物的高灵敏性的定性和定量分析[1].对于单个修饰碱基而言, 比如醛基修饰嘧啶的检测, 可以通过设计合成有机小分子化合物与目标检测物发生共价反应从而实现荧光的打开检测[2, 3].然而, 针对不同的核酸二级结构, 比如G-四联体, 则需要通过控制微观环境的亲疏水性、氢键、静电作用等实现对目标核酸的识别与调控[4]. G-四联体在人体端粒, 核糖核苷酸, 肝癌病毒, 埃博拉病毒中均有发现[5~8].检测识别调控G-四联体对人类延长寿命, 疾病诊断治疗具有重大的意义[9].在端粒的富G序列中容易形成G-四联体.通过设计合成具有特异性靶向原癌基因启动子区域的G-四联体序列的G-四联体稳定剂, 可以非常有效地调控癌基因的表达, 进而实现对癌症或肿瘤的有效治疗[10~12].传统G-四联体的稳定剂可以分为三类.一是显著地增加G-四联体的稳定性, 本身不具备荧光检测作用.比如喹啉衍生物, 卟啉衍生物, 吡啶酰胺衍生物, 钌配体衍生物, 镍配体衍生物等[13~19].二是荧光标记G-四联体.化合物本身既具有荧光, 又能够实现对G-四联体的荧光标记.比如PDP-CY5, L1BOD-7OTD等[20~22].这类小分子的合成设计分为稳定G-四联体的部分和荧光标记部分.三是荧光打开检测G-四联体, 硫黄素T, 咪唑衍生物(IZCM-1), 苯并噻唑类衍生物等[23~26].这类小分子往往设计比较巧妙, 既可以选择性作用于G-四联体, 又可以发生荧光响应, 具有很广泛的应用前景.比如用来检测蛋白酪氨酸激酶7 (PTK7)[27]和通过构建G-四联体与探针体系进行更多识别和检测等的运用[28~31].
本文主要在我们课题组前期工作的基础上, 通过精心的设计筛选, 首次报道一个具有诱导稳定并且荧光打开G-四联体的锌的配体化合物Zinc(Ⅱ)-salen complex (ZSC).并且通过运用荧光检测器和圆二色谱等仪器详细研究其与不同构型的G-四联体之间的相互作用.
2 结果与讨论
2.1 化合物的合成
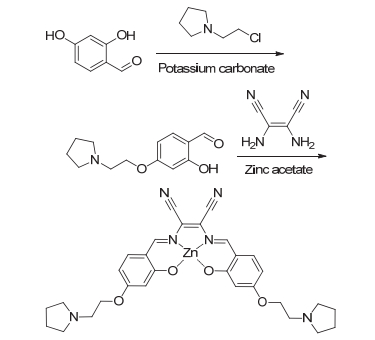
我们先将2, 4-二羟基苯甲醛与N-(2-氯乙基)吡咯烷盐酸盐在碱性条件下反应生成2-羟基-4-(2-吡咯烷基)乙氧基苯甲醛; 然后通过2, 3-二氨基-2-丁烯二腈与其形成席夫碱, 再加入醋酸锌配位形成最终产物(图 1).该反应设计简单, 步骤少, 反应产率高.
2.2 不同序列荧光响应
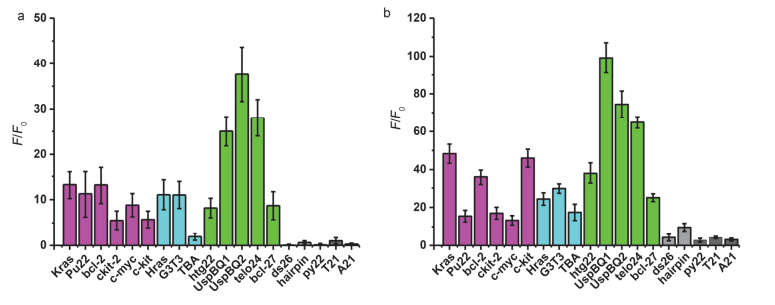
为了验证化合物ZSC的荧光性质, 我们将化合物和已经报道在K+存在的情况下会形成G-四联体的脱氧核糖核苷酸序列和不会形成G-四联体的核酸序列(单链、双链以及具有发卡结构的DNA)[26, 32]进行孵育, 通过荧光强度的变化进行探索.首先我们尝试了反应缓冲液中有100 mmol/L K+存在的情况下荧光强度的变化, 将相同浓度的不同DNA序列和5 μmol/L的ZSC在37 ℃条件下孵育30 min后进行荧光光谱的测试.如图 2a所示, 当化合物遇到具有G-四联体结构的DNA后荧光显著增强, 而在体系中加入单链、双链或者发卡结构的DNA时荧光变化小.值得注意的是, 混合型的G-四联体荧光强度变化最为显著.得到这一结果后, 我们将反应体系换成无K+的状态, 从图 2b可以看到, 在没有K+的时候, 化合物和G-四联体孵育后荧光增强的倍数比有K+时更显著, 而其他的DNA序列荧光增强依然不明显.我们猜测是因为ZSC和K+与G-四联体作用有一个竞争过程, 当有K+存在时, ZSC只有部分可以作用于G-四联体的平面, 在相同浓度的DNA下, 没有K+时ZSC可以自由的作用于G-四联体的平面, 从而荧光增强的更多.从这个结果初步判断ZSC具有诱导G-四联体形成的功能.进一步的验证我们将通过圆二色谱进行证实.
2.3 ZSC与混合型G-四联体DNA的相互作用的研究
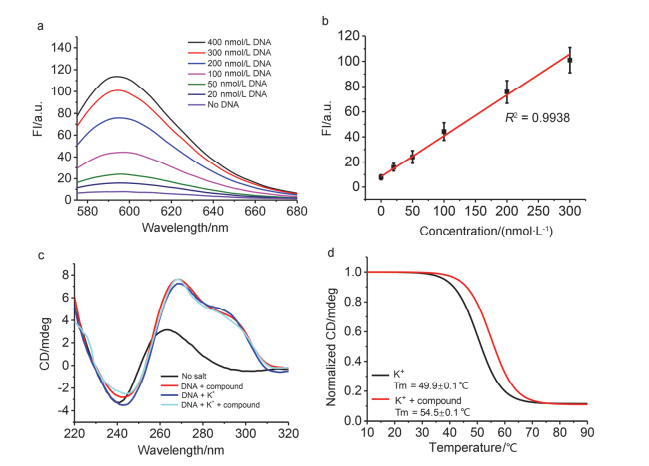
图 2的结果表明UspBQ1与化合物ZSC作用后荧光强度显著增强, 而荧光的强度是否与DNA的浓度呈正相关对于定量是很关键的, 因此不同浓度的UspBQ1与化合物ZSC进行了孵育, 图 3a和图 3b结果表明随着DNA浓度的增强荧光强度是依次增高的.这对G-四联体的定量提供了一定的基础.为了进一步验证化合物ZSC是否可以诱导G-四联体的形成, 我们利用圆二色谱做了进一步的研究.圆二色谱是表征核酸二级结构的有效方式.通过CD光谱可以有效地判断G-四联体是属于平行结构、反平行结构、混合型结构或者是Z-型结构[33].在100 mmol/L K+存在的情况下, UspBQ1在266 nm处和290 nm处分别出现了一个正的尖峰和宽峰, 这些是混合型G-四联体的特征峰, 在ZSC的存在下UspBQ1同样地出现了混合型G-四联体的特征峰.当K+和ZSC同时存在时光谱图也没有发生变化(图 3c). ZSC是否可以稳定G-四联体也是至关重要的, 从图 3d可以看到, 当化合物ZSC加入到体系后, UspBQ1的熔解温度(TM)上升了4.6 ℃.这一结果表明化合物ZSC不仅能够诱导G-四联体的形成而且可以稳定G-四联体.同时, 我们还将化合物与另一条混合型G-四联体进行作用.同样地我们发现, 化合物ZSC可以有效地诱导UspBQ2形成混合型G-四联体.并且DNA的浓度与荧光有一个很好的线性关系(补充数据图S1).为了研究小分子与G-四联体的结合情况, 我们通过Job’S Plot实验探讨化合物和G-四联体的最佳结合配比.配制一系列不同比例浓度的ZSC与DNA体系进行荧光光谱的测定.通过分析可以看到当ZSC与DNA的物质的量浓度比为1:1时, 荧光强度最强.从实验数据上看, 化合物ZCS与G-四联体是1:1 (物质的量浓度比)结合的(支持信息图S3).
2.4 ZSC与平行G-四联体DNA的相互作用的研究
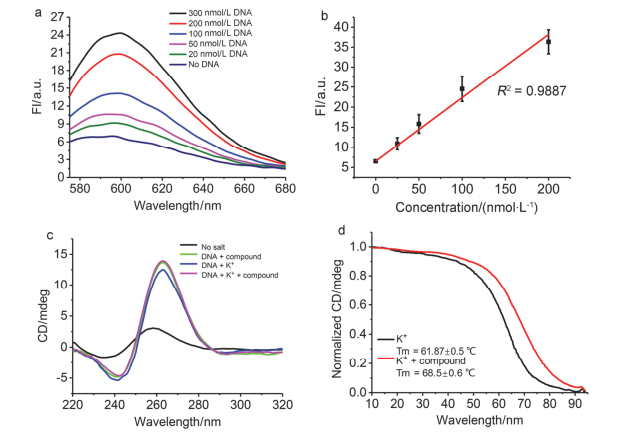
原癌基因启动子ckit含有可以形成平行G-四联体的DNA序列, 它的生物学功能可能与癌症息息相关[34].我们将一种平行的G-四联体ckit序列与化合物ZSC进行了研究.首先对荧光强度与ckit的浓度的关系做了一系列实验, 从图 4a和图 4b可以看到体系的荧光强度是随着ckit的浓度增加而增强.其次为了了解化合物ZSC对ckit的结构是否有影响, 在圆二色谱的测定实验中, K+和ZSC分别加入ckit里, 结果表明在这两种不同条件下, CD光谱呈现了两组特征峰——240 nm处一个负峰和265 nm处一个正峰, 与此同时当K+和化合物ZSC同时存在时特征峰也没有发生变化(图 4c).最后熔解温度测量实验表明ZSC可以使ckit的TM值升高6.7 ℃. (图 4d).同时, 我们也对同样形成平行G-四联体的Pu22核苷酸序列进行了研究.结果表明, ZSC确实可以对其有明显的荧光响应, 荧光强度与G-四联体的浓度有一个很好的线性关系.并且, 其诱导Pu22形成的G-四联体结构与K+存在时一样具有相同的光谱性质(支持信息图S2).
2.5 ZSC与Z型G-四联体DNA的相互作用的研究
Phan教授[35]在2015年报道了左手DNA也称为Z型的G-四联体的存在.但是研究小分子化合物与Z型G-四联体之间的相互作用, 以及调节DNA从Z-型结构到B-型的构型转换的报道是非常少的[36, 37].我们选择了Z型G-四联体(ZG4) 进行了研究.从图 5a和5b可以看到, ZSC对ZG4也有很好的荧光响应.在K+的条件下, CD光谱在276 nm处和249 nm处分别出现了一个负峰和一个正峰, 这是Z型G4的特征峰.值得注意的是当体系为ZSC时, CD光谱的峰发生了显著的变化出现了平行结构G-四联体的特征峰——265 nm的正峰和240 nm的负峰(图 5c).当在有K+的体系里再加入ZSC后CD光谱的特征峰由Z型的特征峰变成了平行的特征峰(图 5d), 这为DNA的构型转换提供了一定的思路.
3 结论
我们通过简单的两步反应, 合成了具有诱导稳定荧光打开检测G-四联体的锌配体化合物.并且通过荧光检测发现其对G-四联体, 特别是混合型G-四联体有一个很强的荧光响应.化合物与G-四联体之间的固有的荧光性质使得将其用于定量检测G-四联体成为可能.我们还将其作用于Z型G四联体, 发现其可以将Z型G四联体变成平行结构的G四联体, 并且对其也有很好的荧光线性.这为未来研究DNA不同的二级结构转变提供了一个新思路.
4 实验部分
4.1 主要试剂及仪器
脱氧核糖核酸序列均购买自武汉金开瑞生物工程有限公司(DNA序列见支持信息Table S1).化学试剂均采购自北京伊诺凯科技有限公司.荧光仪器为PerkinElmer LS 55 (PerkinElmer, USA).圆二色谱信号搜集自Jasco-810 spectropolarimeter (Jasco, Easton, MD, USA).
4.2 不同的DNA序列与ZSC孵育后的荧光性质的检测
向20 μL 1 mol/L K+的Tris-HCl (100 mmol/L, pH=7.2) 缓冲液里加入100 μmol/L的DNA (1 μL), 再加入10 μL 200 μmol/L的化合物ZSC, 加入169 μL的超纯水补齐到200 μL, 37 ℃孵育30 min后进行荧光光谱的测试.选择激发波长为540 nm, 激发狭缝是15 nm, 发射狭缝为20 nm, 扫描速度为500 nm/min, 从光谱图可以看到当富G序列与化合物ZSC孵育后在590 nm处有一个最大的发射信号.另外一组是在没有K+的条件下进行的.向20 μL的Tris-HCl (100 mmol/L, pH=7.2) 缓冲液里加入100 μmol/L的DNA (1 μL), 再加入10 μL 200 μmol/L的化合物ZSC, 加入169 μL的超纯水补齐到200 μL, 37 ℃孵育30 min后进行荧光光谱的测试.参数的设置参考上面所述.
4.3 不同浓度的G-四联体与化合物ZSC作用后荧光强度的研究
向20 μL的Tris-HCl (100 mmol/L, pH=7.2) 缓冲液里加入不同量的DNA, 再加入10 μL 200 μmol/L的化合物ZSC, 加入一定体积的超纯水补齐到200 μL, 37 ℃孵育30 min后进行荧光光谱的测试.参数的设置参考上面所述.
4.4 化合物ZSC与G-四联体DNA相互作用的CD光谱
配制200 μL没有K+和化合物ZSC的如下反应体系: 20 μL 100 μmol/L的DNA, 20 μL 100 mmol/L Tris-HCl (pH=7.2) 和160 μL的超纯水.或者将Tris-HCl缓冲液换成含有1 mol/L K+的Tris-HCl (100 mmol/L, pH=7.2) 的条件.含有化合物ZSC的反应体系如下: 20 μL 100 μmol/L的DNA, 10 μL 200 μmol/L的化合物ZSC, 20 μL 100 mmol/L Tris-HCl (pH=7.2) 和150 μL的超纯水.含有化合物和K+的体系如下: 20 μL 100 μmol/L的DNA, 10 μL 200 μmol/L的化合物ZSC, 20 μL 1 mol/L K+ Tris-HCl (100 mmol/L, pH=7.2) 和150 μL的超纯水.所有体系37 ℃孵育30 min后用Jasco-810 spectropolarimeter获取CD光谱.
4.5 G-四联体DNA熔解温度的测定
向240 μL的超纯水里加入30 μL 100 μmol/L的DNA, 30 μL的1 mol/L K+的Tris-HCl缓冲液, 37 ℃孵育30 min.含有化合物的体系略有不同, 300 μL的体系里含有225 μL的超纯水, 30 μL 100 μmol/L的DNA, 30 μL 1 mol/L K+的Tris-HCl (pH=7.2) 缓冲液和15 μL 200 μmol/L的化合物ZSC.同样的37 ℃孵育30 min.用Jasco-810 spectropolarimeter进行熔解温度的测定.
4.6 2-羟基-4-(2-吡咯烷基)乙氧基苯甲醛的合成与纯化
在装有搅拌磁子250 mL三口烧瓶中加入2, 4-二羟基苯甲醛(2.76 g, 20 mmol), N-(2-氯乙基)吡咯烷盐酸盐(3.40 g, 20 mmol)和碳酸钾(5.56 g, 40 mmol), 在氩气的氛围中加入150 mL丙酮, 60 ℃加热搅拌回流20 h.反应结束后, 水泵减压蒸馏除去丙酮.然后先往里加入200 mL水, 再往里分三次, 每次加入200 mL乙酸乙酯萃取分液, 合并有机相, 减压蒸馏得到粗产物.最后用硅胶柱色谱, 淋洗剂选用V(CH2Cl2):V(CHOH)=30:1~20:1的混合液, 进行梯度淋洗.收集产物, 真空干燥, 得到3.24 g灰白色固体(产率为68.8%). 1H NMR (300 MHz, DMSO-d6) δ: 9.99 (s, 1H), 7.59 (d, J=8.6 Hz, 1H), 6.54 (d, J=8.5 Hz, 1H), 6.47 (s, 1H), 4.10 (t, J=5.1 Hz, 2H), 2.79~2.78 (m, 2H), 2.51~2.50 (m, 4H), 1.66~1.65 (m, 4H); 13C NMR (75 MHz, DMSO-d6) δ: 191.38, 165.48, 163.51, 132.51, 116.55, 108.03, 101.63, 67.40, 54.30, 23.45. HRMS calcd for C13H18NO3+ [M+H]+ 236.12812, found 236.12787.
4.7 锌配体化合物(ZSC)合成与纯化
在装有搅拌磁子的50 mL圆底烧瓶中分别加入2-羟基-4-(2-吡咯烷基)乙氧基苯甲醛(285 mg, 1.2 mmol)和2, 3-二氨基-2-丁烯二腈(65 mg, 0.6 mmol).然后加入10 mL甲醇, 60 ℃避光环境中搅拌20 min; 再往反应体系中加入二水合醋酸锌(132 mg, 0.6 mmol), 此时溶液立即由橘黄色变为血红色, 继续反应2 h, 通过薄层色谱[V(CH2Cl2):V(CH3OH):V(Et3N)=54:3:1作为展开剂]来监测原料完全反应完毕.反应结束后, 将有机溶剂甲醇减压蒸馏除去, 通过硅胶柱层析分离提纯产物[淋洗剂为V(CH2Cl2):V(CH3OH):V(Et3N)=65:3:1].收集纯品, 真空干燥, 得245 mg红色固体粉末(产率为67.7%). 1H NMR (300 MHz, DMSO-d6) δ: 8.35 (s, 2H), 7.46~7.15 (m, 2H), 6.23~6.22 (m, 4H), 4.12~4.11 (m, 4H), 2.98~2.72 (m, 4H), 2.71~2.34 (m, 8H), 1.99~1.54 (m, 8H); 13C NMR (75 MHz, DMSO-d6) δ: 176.89, 166.50, 161.21, 138.27, 120.96, 114.69, 112.40, 107.56, 105.05, 67.07, 54.35, 23.50. HRMS calcd for C30H33N6O4Zn+ [M+H]+ 605.18493, found 605.18161.
-
-
[1]
Bhasikuttan, A. C.; Mohanty, J. Chem. Commun. 2015, 51, 7581. doi: 10.1039/C4CC10030A
-
[2]
Liu, C.; Chen, Y.; Wang, Y.; Wu, F.; Zhang, X.; Yang, W.; Wang, J.; Chen, Y.; He, Z.; Zou, G.; Wang, S.; Zhou, X. Nano Res. 2017, DOI: 10.1007/s12274-017-1445-2.
-
[3]
Liu, C.; Wang, Y.; Zhang, X.; Wu, F.; Yang, W.; Zou, G.; Yao, Q.; Wang, J.; Chen, Y.; Wang, S.; Zhou, X. Chem. Sci. 2017, DOI: 10.1039/C7SC00637C.
-
[4]
田沺, 肖珩, 翁小成, 王少儒, 周翔, 中国科学:化学, 2013, 42, 1700. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htmTian, T.; Xiao, H.; Weng, X.; Wang, S.; Zhou, X. Sci. Sin. Chim. 2013, 42, 1700(in Chinese). http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htm
-
[5]
Biffi, G.; Tannahill, D.; McCafferty, J.; Balasubramanian, S. Nat. Chem. 2013, 5, 182. doi: 10.1038/nchem.1548
-
[6]
Chen, S. B.; Hu, M. H.; Liu, G. C.; Wang, J.; Ou, T. M.; Gu, L. Q.; Huang, Z. S.; Tan, J. H. J. Am. Chem. Soc. 2016, 138, 10382. doi: 10.1021/jacs.6b04799
-
[7]
Wang, S.; Min, Y.; Wang, J.; Liu, C.; Fu, B.; Wu, F., Wu, L; Qiao, Z.; Song, Y; Xu, G.; Wu, Z.; Huang, G.; Peng, N.; Huang, R.; Mao, W.; Peng, S.; Chen, Y.; Zhu, Y.; Tian, T.; Zhang, X.; Zhou, X. Sci. Adv. 2016, 2, e1501535 doi: 10.1126/sciadv.1501535
-
[8]
Wang, S.; Zhang, Q.; Wang, J.; Ge, X.; Song, Y.; Wang, Y.; Li, X.; Fu, B.; Xu, G.; Shu, B.; Gong, P.; Zhang, B.; Tian, T.; Zhou, X. Cell Chem. Biol. 2016, 23, 1113. doi: 10.1016/j.chembiol.2016.07.019
-
[9]
郑小辉, 穆舸, 谭彩萍, 曹乾, 毛宗万, 中国科学:化学2014, 44, 484. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htmZheng, X. H; Mu, G.; Tan, C. P.; Cao, G.; Mao, Z. W. Sci. Sin. Chim. 2014, 44, 484(in Chinese). http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htm
-
[10]
Lin, S.; Xu, M.; Yuan, G. Chin. Chem. Lett. 2012, 23, 329. doi: 10.1016/j.cclet.2011.11.002
-
[11]
Yan, J.; Guan, Y. Progr. Anatom. Sci. 2015, 21, 419.
-
[12]
郑小辉, 刘海英, 夏立新, 毛宗万, 中国药理学通报, 2016, 32, 751. doi: 10.3969/j.issn.1001-1978.2016.06.003Zheng, X.; Liu, H.; Xia, L.; Mao, Z. Chin. Pharmacol. Bull. 2016, 32, 751(in Chinese). doi: 10.3969/j.issn.1001-1978.2016.06.003
-
[13]
Müller, S.; Kumari, S.; Rodriguez, R.; Balasubramanian, S. Nat. Chem. 2010, 2, 1095. doi: 10.1038/nchem.842
-
[14]
张弛, 吴伟彬, 卢宇靖, 古练权, 黄志纾, 化学学报, 2008, 66, 953. doi: 10.3321/j.issn:0567-7351.2008.08.020Zhang, C.; Wu, W.; Lu, Y.; Gu, L.; Huang, Z. S. Acta Chim. Sinica 2008, 66, 953(in Chinese). doi: 10.3321/j.issn:0567-7351.2008.08.020
-
[15]
Zheng, K.; Zhang, D.; Zhang, L.; Hao, Y.; Zhou, X.; Tan, Z. J. Am. Chem. Soc. 2011, 133, 1475. doi: 10.1021/ja108972e
-
[16]
欧植泽, 句宝龙, 高云燕, 王子超, 黄干, 钱一梦, 物理化学学报, 2015, 31, 2386. doi: 10.3866/PKU.WHXB201510137Ou, Z. Z.; Ju, B. L.; Gao, Y. Y.; Wang, Z. C.; Huang, G.; Qian, Y. M. Acta Phys.-Chim. Sin. 2015, 31, 2386(in Chinese). doi: 10.3866/PKU.WHXB201510137
-
[17]
孟晨鹏, 王舜, 张克军, 金辉乐, 陈锡安, 胡茂林, 熊静, 化学学报, 2011, 69, 1173. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract340091.shtmlMeng, C.; Wang, S.; Zhang, K.; Jin, H.; Chen, X.; Hu, M.; Xiong, J. Acta Chim. Sinica 2011, 69, 1173(in Chinese). http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract340091.shtml
-
[18]
Reed, J. E.; Arnal, A. A.; Neidle, S.; Vilar, R. J. Am. Chem. Soc. 2006, 128, 5992. doi: 10.1021/ja058509n
-
[19]
Xu, L.; Wu, W.; Ding, J.; Feng, S.; Xing, X.; Deng, M.; Zhou, X. RSC Adv. 2012, 2, 894. doi: 10.1039/C1RA00851J
-
[20]
Yu, L.; Gai, W.; Yang, Q.; Xiang, J.; Sun, H.; Li, Q.; Wang, L.; Guan, A.; Tang, Y. Chin. Chem. Lett. 2015, 26, 705. doi: 10.1016/j.cclet.2015.02.002
-
[21]
Wu, F.; Liu, C.; Chen, Y.; Yang, S.; Xu, J.; Huang, R.; Wang, X.; Li, M.; Liu, W.; Mao, W.; Zhou, X. Sens. Actuators, B 2016, 236, 268. doi: 10.1016/j.snb.2016.05.162
-
[22]
Tera, M.; Iida, K.; Ikebukuro, K.; Seimiya, H.; Shin-ya, K.; Nagasawa, K. Org. Biomol. Chem. 2010, 8, 2749. doi: 10.1039/c002117b
-
[23]
Chen, Y.; Yan, S.; Yuan, L.; Zhou, Y.; Song, Y.; Xiao, H.; Weng, X.; Zhou, X. Org. Chem. Front. 2014, 1, 267. doi: 10.1039/c3qo00048f
-
[24]
Xu, S.; Li, Q.; Xiang, J.; Yang, Q.; Sun, H.; Guan, A.; Wang, L.; Liu, Y.; Yu, L.; Shi, Y.; Chen, H.; Tang, Y. Nucleic Acids Res. 2015, 43, 9575.
-
[25]
Mohanty, J.; Barooah, N.; Dhamodharan, V.; Harikrishna, S.; Pradeepkumar, P. I.; Bhasikuttan, A. C. J. Am. Chem. Soc. 2013, 135, 367. doi: 10.1021/ja309588h
-
[26]
Chen, S. B.; Wu, W. B.; Hu, M. H.; Ou, T. M.; Gu, L. Q.; Tan, J. H.; Huang, Z. S. Chem. Commun. 2014, 50, 12173. doi: 10.1039/C4CC05394J
-
[27]
Lin, S.; Gao, W.; Tian, Z.; Yang, C.; Lu, L.; Mergny, J.; Leung, C.; Ma, D. Chem. Sci. 2015, 6, 4284. doi: 10.1039/C5SC01320H
-
[28]
Ji, X.; Yao, C.; Wan, Y.; Song, H.; Xin, P.; Cui, H.; Zheng, C.; Deng, S. Chin. J. Chem. 2016, 34, 331. doi: 10.1002/cjoc.v34.3
-
[29]
Liu, X.; Yang, Y.; Hua, X.; Feng, X.; Su, S.; Huang, Y.; Fan, Q.; Wang, L.; Huang, W. Chin. J. Chem. 2015, 33, 981. doi: 10.1002/cjoc.v33.8
-
[30]
邵昱, 李闯, 周旭, 陈平, 杨忠强, 李志波, 刘冬生, 化学学报, 2015, 73, 815. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345059.shtmlShao, Y.; Li, C.; Zhou, X.; Chen, P.; Yang, Z.; Li, Z.; Liu, D. Acta Chim. Sinica 2015, 73, 815(in Chinese). http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345059.shtml
-
[31]
刘兴奋, 王亚腾, 黄艳琴, 冯晓苗, 范曲立, 黄维, 化学学报, 2016, 74, 664. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345652.shtmlLiu, X.; Wang, Y.; Huang, Y.; Feng, X.; Fan, Q.; Huang, W. Acta Chim. Sinica 2016, 74, 664(in Chinese). http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345652.shtml
-
[32]
周江, 袁谷, 化学学报, 2007, 65, 1728. doi: 10.3321/j.issn:0567-7351.2007.16.035Zhou, J.; Yuan, G. Acta Chim. Sinica 2007, 65, 1728(in Chinese). doi: 10.3321/j.issn:0567-7351.2007.16.035
-
[33]
魏强, 屈锋, 龚芮, 生物化学与生物物理进展, 2015, 42, 624. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htmWei, Q.; Qu, F.; Gong, R. Prog. Biochem. Biophys. 2015, 42, 624(in Chinese). http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htm
-
[34]
Rankin, S.; Reszka, A. P.; Huppert, J.; Zloh, M.; Parkinson, G. N.; Todd, A. K.; Ladame, S.; Balasubramanian, S.; Neidle, S. J. Am. Chem. Soc. 2005, 127, 10584. doi: 10.1021/ja050823u
-
[35]
Chung, W. J.; Heddi, B.; Schmitt, E.; Lim, K. W.; Mechulam, Y.; Phan, A. T. Proc. Natl. Acad. Sci. U. S. A. 2015, 112, 2729. doi: 10.1073/pnas.1418718112
-
[36]
Zhao, A.; Zhao, C.; Ren, J.; Qu, X. Chem. Commun. 2016, 52, 1365. doi: 10.1039/C5CC08401F
-
[37]
Fu, B.; Huang, J.; Chen, Y.; Wang, Y.; Xue, T.; Xu, G.; Wang, S.; Zhou, X. Chem. Commun. 2016, 52, 10052. doi: 10.1039/C6CC04866H
-
[1]
-
图 1 小分子化合物的合成路线
Figure 1 Synthesis of Zinc(Ⅱ)-salen complex (ZSC)
Step 1: 2, 4-dihydroxybenzaldehyde (2.76 g, 20 mmol), 1-(2-chloroethyl)-pyrrolidine hydrochloride (3.40 g, 20 mmol) and potassium carbonate (5.56 g, 40 mmol) were dissolved in 150 mL acetone. After reflux for 20 h in Ar atmosphere, the product was dried in vacuum, then extraction by ethyl acetate (200 mL) three times. Finally, the product 2-hydroxy-4-(2-(pyrrolidin-1-yl)ethoxy)benzaldehyde was purified by silica gel column chromatography using eluent CH2Cl2/MeOH (V/V=30:1~20:1) to yield 3.24 g (68.8%) as a pale solid. Step 2: 2-hydroxy-4-(2-(pyrrolidin-1-yl)ethoxy)benzaldehyde (285 mg, 1.2 mmol) and diaminomaleonitrile (65 mg, 0.6 mmol) were dissolved into 10 mL methanol. After 20 min stirring at 60 ℃ in dark atmosphere, the Zinc acetate dehydrate (132 mg, 0.6 mmol) was added in the solution for further 2 h reaction time. The final product Zinc(Ⅱ)-salen Complex (ZSC) was obtained by silica gel column chromatography using eluent CH2Cl2/MeOH/Et3N (V/V/V=65:3:1) to yield 245 mg (67.7%) as a red powder.
图 2 不同构型的DNA序列与化合物ZSC的荧光响应
Figure 2 Fluorescence spectra of different configuration ODNs after incubation with ZSC
a. The mixture of 1 μL DNA (100 μmol/L) and 10 μL ZSC (200 μmol/L) were incubated in 100 mmol/L K+ Tris-HCl (10 mmol/L, pH 7.2) buffer at 37 ℃ for 30 min. b. The mixture of 1 μL DNA (100 μmol/L) and 10 μL ZSC (200 μmol/L) were incubated in 10 mmol/L Tris-HCl (pH 7.2) buffer at 37 ℃ for 30 min
图 3 混合型G-四联体(UspBQ1) 的荧光线性图和CD分析
Figure 3 Fluorescence intensity and CD analysis of hybrid-type G-quadruplex UspBQ1
a. The fluorescence spectra of UspBQ1 in different concentration incubated with 10 μmol/L ZSC under the condition of 10 mmol/L Tris-HCl (pH 7.2) at 37 ℃ for 30 min. b. Analysis of data about fluorescence intensity dependence on different DNA concentration shown in (a). c. CD spectra of UspBQ1 under different condition. d. The melting curves of UspBQ1 under the condition of 100 mmol/L K+ and100 mmol/L K+ with 10 μmol/L ZSC respectively
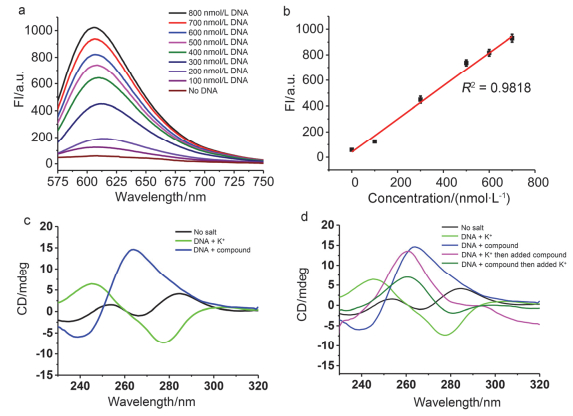
图 4 平行G-四联体(UspBQ1) 的荧光强度图和CD分析
Figure 4 Fluorescence intensity and CD analysis of parallel G-quadruplex ckit
a. The fluorescence spectra of ckit in different concentration incubated with 10 μmol/L ZSC under the condition of 10 mmol/L Tris-HCl (pH 7.2) at 37 ℃ for 30 min. b. Analysis of data about fluorescence intensity dependence on different DNA concentration shown in (a). c. CD spectra of ckit under different condition. d. The melting curves of ckit under the condition of 100 mmol/L K+and100 mmol/L K+with 10 μmol/L ZSC respectively
图 5 Z型G-四联体(ZG4) 的荧光强度图和CD分析
Figure 5 Fluorescence intensity and CD analysis of Z-G-quadruplex (ZG4)
a. The fluorescence spectra of ZG4 in different concentration incubated with 10 μmol/L ZSC under the condition of 10 mmol/L Tris-HCl (pH 7.2) at 37 ℃ for 30 min. b. Analysis of data about fluorescence intensity dependence on different DNA concentration shown in (a). c and d. CD spectra of ZG4 under different conditions
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 4
- 文章访问数: 2078
- HTML全文浏览量: 228


 下载:
下载:




 下载:
下载:

