 图 1
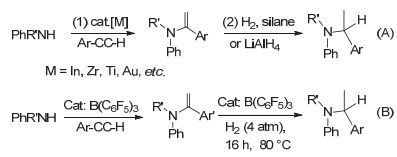
炔烃与芳胺的氢胺化/还原反应
Figure 1.
Reductive hydroamination of phenylacetylenes with amines
图 1
炔烃与芳胺的氢胺化/还原反应
Figure 1.
Reductive hydroamination of phenylacetylenes with amines

Citation: Zhang Luwen, Wen Zhiguo, Borzov Maxim, Nie Wanli. Research of B(C6F5)3/Aromatic Ammonium Chloride Systems Catalyzed Hydroamination/Reduction Reaction[J]. Acta Chimica Sinica, 2017, 75(8): 819-823. doi: 10.6023/A17040142

芳香胺盐酸盐/硼烷体系催化的氢胺化/还原反应研究
English
Research of B(C6F5)3/Aromatic Ammonium Chloride Systems Catalyzed Hydroamination/Reduction Reaction
-
1 引言
氢胺化反应(Hydroamination)通常是将N—H键加成到碳碳π键用来制备各种含C—N键仲胺或叔胺化合物的反应.由于其原子利用率为100%, 因此氢胺化反应在有机合成中也是一类非常重要的反应[1~3].目前有关氢胺化反应的文献报道, 较多集中在炔烃与苯胺类的两步法催化氢胺化/还原反应(Hydroamination/reduction)的研究.如图 1(A)所示, 其中所涉及的催化剂多为过渡金属、稀土金属及主族元素等配合物[4~6], 还原剂一般为氢气、氢化硅烷或四氢铝锂等.近些年, 以大位阻路易斯酸B (C6F5)3与大位阻有机碱(如Ph3P, t-Bu3P or TMP等)所组成的受限路易斯酸碱对(FLPs)为代表的非金属催化剂对小分子的活化及催化反应研究备受关注[7~13].但有关芳香胺类FLPs的应用研究却极少涉及. 2013年, 加拿大科学家Stephan课题组发表了一篇关于利用B (C6F5)3作为催化剂, 催化苯胺与炔烃氢胺化反应的文章.该文利用苯胺/B (C6F5)3体系对H2的活化特点, 首次实现了非金属催化的炔烃的氢胺化/还原的一锅两步合成方法[14], 如图 1(B)所示. 2015年, Stephan课题组同样利用B (C6F5)3作为催化剂, 氢气作为还原剂, 实现了分子内的一锅两步法氢胺化/还原制备含氮杂环类化合物[15], 但是该类反应需要较高的反应温度和压力.
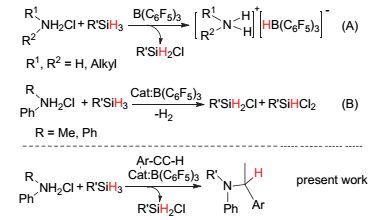
我们课题组最近报道了一种研究受限路易斯酸碱对化学的新方法, 以有机胺盐酸盐代替常规FLPs体系中的烷基胺路易斯碱, 与三(五氟苯基)硼B (C6F5)3所组成的新的“路易斯酸/胺盐”反应体系, 在以氢化硅烷替代氢气作为氢源时, 可制备各种取代的烷基胺类“硼氢化烷胺盐”, 如图 2(A)所示.该“硼氢化胺盐[R2NH2]+[H-B (C6F5)3]-”被认为是还原反应的活性中间体.研究表明“路易斯酸/胺盐”体系在对醛酮、炔烃、亚胺以及二氧化碳等的还原反应中均表现出了独特的反应活性[16~18].
由于“硼氢化芳胺盐”的不稳定性, 即使是在低温下也易释放出氢气的特点, 限制了其应用范围.虽然2014年我们以氢化硅烷作为还原剂, 以芳香胺盐酸盐作为氯代试剂, BCF作为催化剂, 首次实现了在温和条件下非金属催化的氢化硅烷的氯代, 如图 2(B)所示[19].但该反应并没有将“硼氢化芳胺盐”所释放出的氢气作为氢源利用.
本文则是以氢化硅烷作为氢源给体, B (C6F5)3为催化剂, 利用原位产生的“硼氢化芳胺盐”易于释放出“H2”特点, 实现了在温和反应条件下芳胺盐酸盐与炔烃的一步法氢胺化/还原反应.
2 结果与讨论
2.1 芳香胺盐酸盐/BCF体系与炔烃的反应研究
芳香胺盐酸盐可通过向二苯基胺或苯基甲基胺的二氯甲烷溶液中通入干燥的HCl气体来制备.
表 1反应所示是在B (C6F5)3催化下, 不同硅烷还原二苯胺盐酸盐与炔烃的氢胺化/还原反应.芳香胺盐酸盐通常不溶于氘代氯仿中, 加入B (C6F5)3后会缓慢溶解.硅烷一般应过量并且稀释后慢慢滴加, 随着硅烷加入会观察到明显的气体产生.一般情况下50 ℃过夜可使反应进行完全.通常我们认为硅烷的反应活性一般为: PhSiH3>Ph2SiH2>Ph3SiH>Et3SiH.但从表 1中的数据可以看出, 在本反应中, 反应的产率却与硅烷活性相反, 三取代的三乙基硅烷Et3SiH和三苯基硅烷Ph3SiH表现出较单取代的苯硅烷更高的反应活性.而三乙氧基硅烷参与的反应活性最低.当炔烃苯基上带有吸电子取代基时较带有给电子取代基炔烃具有较高的反应活性.

Entry Alkyne Silane Yield/% 1 C6H4-CCH Et3SiH 3a 62.6[20] 2 P-CH3-C6H5-CCH Et3SiH 3b 58.6[20] 3 p-F-C6H4-CCH Et3SiH 3c 100.0 4 C6H4-CCH Ph3SiH 3a 70.1 5 P-CH3-C6H5-CCH Ph3SiH 3b 37.6 6 p-F-C6H4-CCH Ph3SiH 3c 82.9 7 p-F-C6H4-CCH Ph2SiH3 3c 60.0 8 p-F-C6H4-CCH PhSiH3 3c 38.7 9 p-F-C6H4-CCH (EtO)3SiH 3c 19.3 a NMR Yield; Molar ratio of alkyne to silane=1:3. 表 2中所列出的数据是在苯硅烷的作用下, 不同芳胺与对氟苯乙炔的氢胺化/还原反应.从图中数据可以看出, 当二芳胺的苯环上对位带有强吸电子取代基Br时, 反应几乎定量进行(如3d、3e); 相反, 当芳胺氮上取代有烷基时, 反应产率明显降低(如3f、3g).化合物3h较低的产率说明端基芳炔上的取代基比芳胺上取代基对反应的影响更显著.
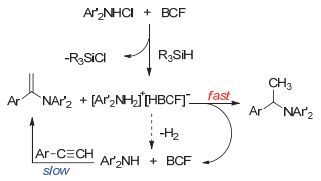
对于该反应的反应机理研究, 我们提出了如图 3所示的催化氢胺化/还原反应过程.在B (C6F5)3催化下, 硅烷与催化剂B (C6F5)3及胺盐首先反应形成活性中间体“硼氢化芳胺盐[Ar2NH2]+[H-B (C6F5)3]-”, 少量的硼氢化芳胺盐分解产生的游离胺Ar2NH在B (C6F5)3催化下与炔烃反应生成亚胺.这一中间产物亚胺可被活性“硼氢化芳胺盐”还原再释放出游离的胺Ar2NH及B (C6F5)3使得催化循环可以继续.
而决定B (C6F5)3催化下, 硅烷参与的氢胺化/还原反应产率的主要因素是所形成的活性中间体“硼氢化芳胺盐”的分解速度.由于炔烃的氢胺化反应较亚胺中间体的还原反应速度慢的特点, 活性较高的硅烷与B (C6F5)3及胺盐形成中间体“[R2NH2]+[H-B (C6F5)3]-”的速度较快, 受限于较慢的氢胺化反应及不稳定的硼氢化芳胺盐分解的特点, 因此还原产物产率不高.而活性较低的三取代硅烷, 由于形成硼氢化芳胺盐的速度较慢, 分解也就较慢, 中间体亚胺的还原较充分, 因此产率也较高.总之, 对于活性较高的硅烷参与的反应, 通过稀释或缓慢加入硅烷的方法来控制硼氢化芳胺盐的产生速率, 可有效地提高氢胺化/还原反应的产率.
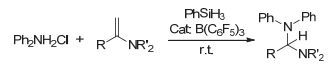
为了对反应机理的合理性进行验证, 我们设计了如图 4所示的实验: B (C6F5)3催化下的芳香胺盐酸盐与烯胺的还原反应.实验证明, 原位产生的“硼氢化芳胺盐”可在温和条件下将烯胺还原为胺.
3 结论
本文是我们课题组所报道的一系列有关以有机胺盐酸盐代替常规FLPs体系中的路易斯碱, 组成的新的“路易斯酸/胺盐”反应体系, 来研究FLPs化学的工作之一.首次实现了原位产生的“硼氢化芳胺盐”在炔烃的氢胺化及还原中的应用.该反应进一步扩展了有机芳胺盐体系的应用领域.尽管以硅烷代替氢气总会不可避免硅烷副产物的形成, 但是以有机胺盐酸盐代替常规FLPs体系中的路易斯碱, 所组成的新的“路易斯酸/胺盐”反应体系已显示出的独特反应活性和特征, 促使我们有必要继续对这一新的研究方法进行深入的探索研究.
4 实验部分
实验所有操作都是在无水无氧条件下进行的, 所有反应溶剂及氘代试剂均是在氮气保护下经过干燥除水处理.
4.1 芳香胺盐酸盐的制备
分别将5.0 mL或者5.0 g的芳香胺和10.0 mL CH2Cl2加入Schlenk瓶中, 搅拌下通入干燥的HCl气体, 室温搅拌反应5 h.在反应过程中大部分的盐酸盐会沉淀析出, 过滤, CH2Cl2洗涤3次, 真空抽滤干燥过夜可得到较纯净的盐酸盐.用此方法制备二苯胺盐酸盐、双(4-溴苯基)胺盐酸盐、N-甲基-2氟苯胺盐酸盐、4-溴-N-苯基胺盐酸盐.
4.2 N-(1-(4-fluorophenyl) ethyl)-N-(phenyl) benzen-amine (3c)的制备
在氮气保护下, 将205.0 mg (1.0 mmol)二苯胺盐酸盐置于反应瓶中, 然后加入41.0 mg (0.1 mmol)三(五氟苯基)硼于反应瓶中, 用9.0 mL氯仿溶解, 再加入120.0 mg (1.0 mmol)对氟苯乙炔, 最后缓慢加入氯仿稀释10倍的180.0 mg (1.5 mmol)三乙基硅烷, 50 ℃下反应24 h.硅胶过柱提纯分离[洗脱液为V(石油醚):V(乙酸乙酯)=6:1], 分离产率为51.5%. 1H NMR (400 MHz, CDCl3, 298 K) δ: 1.49 (d, J=7.01 Hz, 3H, CH3-CH), 5.29 (q, J=6.95 Hz, 1H, CH3CH), 6.83 (d, J=8.52 Hz, 4H, o-Ph), 7.01~6.92 (m, 4H, p-Ph/F-Ph), 7.20 (t, J=7.33 Hz, 4H, m-Ph), 7.34~7.17 (m, 2H, F-Ph); 13C{1H}NMR (100 MHz, CDCl3, 298 K) δ: 19.11, 56.75, 114.96, 115.21, 128.54, 128.62, 122.97 (o-Ph), 121.75 (p-Ph), 129.02 (m-Ph), 139.45 (d, 4JF-C=2.92 Hz), 146.74, 160.45/160.91 (d, 1JF-C=245.14 Hz); GC-MS (EI) m/z: 291.16 (M+). 19F {1H}NMR (376 MHz, CDCl3, 298 K) δ: -116.23.
4.3 4-Bromo-N-(1-(4-fluorophenyl) ethyl)-N-(p-bromophenyl) benzenamine (3d)的制备
在氮气保护下, 将361.5 mg (1.0 mmol)双(4-溴苯基)胺盐酸盐置于反应瓶中, 然后加入41.0 mg (0.1 mmol)三(五氟苯基)硼于反应瓶中, 用9.0 mL氯仿溶解, 再加入120.0 mg (1.0 mmol)对氟苯乙炔, 最后缓慢加入氯仿稀释10倍的180.1 mg (1.5 mmol)三乙基硅烷, 50 ℃下反应24 h.硅胶过柱提纯[洗脱液为V(石油醚):V(乙酸乙酯)=6:1], 分离产率为46.5%. 1H NMR (400 MHz, CDCl3, 298 K) δ: 1.44 (d, 3H, 1JCH=127.6 Hz, 3JHH=7.1 Hz, CH3), 5.19 (q, 1H, 3JHH=7.1 Hz, CH3CH), 6.67, 7.27 (d, 8H, 3JAX=8.9 Hz, H2, 6 and H3, 5 in 4-BrC6H4, respectively), 6.94~7.24 (m, 4H, 4-FC6H4); 13C{1H}NMR (100 MHz, CDCl3, 298 K) δ: 19.11 (s, CH3), 56.99 (s, CH3CH), 114.98 (s, CBr), 115.28 (d, 2JFC=21.3 Hz, 4-F-C6H4), 124.59, 132.08 (s, 4-BrC6H4), 128.46 (d, 3JFC=8.0 Hz, 4-F-C6H4), 138.47 (d, 4JFC=3.4 Hz, 4-FC6H4), 145.46 (s, 4-BrC6H4), 161.76 (d, 1JFC=245.7 Hz, CF); 19F NMR (376 MHz, CDCl3, 298 K) δ: -115.07 (tt, 3JFH=8.3 Hz, 4JFH=5.5 Hz).
4.4 N-(1-(4-fluorophenyl) ethyl)-N-(p-bromophenyl) benzenamine (3e)的制备
在氮气保护下, 将285.0 mg (1.0 mmol) 4-溴-N-苯基胺盐酸盐置于反应瓶中, 然后加入41.0 mg (0.1 mmol)三(五氟苯基)硼于反应瓶中, 用9.0 mL氯仿溶解, 再加入119.8 mg (1.0 mmol)对氟苯乙炔, 最后缓慢加入氯仿稀释10倍的180.2 mg (1.5 mmol)三乙基硅烷, 50 ℃下反应24 h.硅胶过柱提纯[洗脱液为V(石油醚):V(乙酸乙酯)=6:1], 分离产率为40.4%. 1H NMR (400 MHz, CDCl3, 298 K) δ: 1.46 (d, 3H, 1JCH=127.6 Hz, 3JHH=7.0 Hz, CH3), 5.22 (q, 1H, 1JCH=136.0 Hz, 3JHH=7.0 Hz, CH3CH), 6.60 (d, 3JAX=9.1 Hz, 2H, 4-Br-C6H4), 7.21 (d, 3JAX=9.1 Hz, 2H, 4-BrC6H4), 6.94~7.26 (m, 4H, 3JAX~3JAF=8.8 Hz, 4JXF=5.4 Hz, 4-FC6H4), 6.90~7.23 (m, 5H, Ph); 13C {1H}NMR (100 MHz, CDCl3, 298 K) δ: 19.34 (s, CH3), 57.01 (s, CH3CH), 112.97 (s, CBr), 115.21 (d, 2JFC=21.3 Hz, 4-F-C6H4), 122.27, 131.77, 146.46 (all s, C2, 6, C3, 5 and C1 in 4-Br-C6H4, respectively), 129.29 (d, 3JFC=8.0 Hz, C2, 6 in 4-F-C6H4), 123.54, 125.28, 129.29, 145.82 (all s, C4, C2, 6, C3, 5, and C1 in Ph, respectively), 138.96 (d, 4JFC=3.4 Hz, C1 in 4-F-C6H4), 161.75 (d, 1JFC=245.2 Hz, CF); 19F NMR (376 MHz, CDCl3, 298 K) δ: -115.58 (tt, 3JFH=8.8 Hz, 4JFH=5.4 Hz).
4.5 2-Fluoro-N-(1-(4-fluorophenyl) ethyl)-N-(methyl)-benzenamine (3f)的制备
在氮气保护下, 将161.6 mg (1.0 mmol) N-甲基-2氟苯胺盐酸盐置于反应瓶中, 然后加入41.0 mg (0.1 mmol)三(五氟苯基)硼于反应瓶中, 用9.0 mL氯仿溶解, 再加入119.8 mg (1.0 mmol)对氟苯乙炔, 最后缓慢加入氯仿稀释10倍的179.8 mg (1.5 mmol)三乙基硅烷, 50 ℃下反应24 h.硅胶过柱提纯[洗脱液为V(石油醚):V(乙酸乙酯)=6:1], 分离产率为35.5%. 1H NMR (400 MHz, CDCl3, 298 K)δ: 1.43 (d, 1JCH=123.7 Hz, 3JHH=6.9 Hz, 3H, CHCH3), 2.49 (s, 3H, 1JCH=135.1 Hz, NCH3), 4.72 (q, 1H, 1JCH=137.4 Hz, 3JHH=6.9 Hz, CH3CH), 6.99~7.33 (m, 4H, 4-FC6H4), 6.89~7.03 (m, 2-FC6H4); 13C {1H}NMR (100 MHz, CDCl3, 298 K) δ: 15.90 (s, CHCH3), 33.31 (s, NCH3), 59.56 (d, 4JFC=5.5 Hz, CH3CH), 114.85 (d, 2JFC=21.3 Hz, C3, 5 in 4-F-C6H4), 116.20 (d, 2JFC=21.2 Hz, C3 in 2-F-C6H4), 121.56 (d, 3JFC=2.8 Hz, C4 in 2-F-C6H4), 122.01 (br. d, 3JFC=7.6 Hz, C6 in 2-F-C6H4), 124.25 (d, 4JFC=3.8 Hz, C5 in 2-F-C6H4), 129.00 (d, 3JFC=8.0 Hz, C3 in 2-F-C6H4), 137.97 (d, 4JFC=2.7 Hz, C1 in 4-F-C6H4), 139.94 (br. d, 2JFC=8.3 Hz, C1 in 2-F-C6H4), 156.25 (d, 1JFC=244.9 Hz, CF in 2-F-C6H4), 161.88 (d, 1JFC=244.8 Hz, CF in 4-F-C6H4); 19F {1H}NMR (376 MHz, CDCl3, 298 K) δ: -121.86 (m, 2-FC6H4); -116.12 (m, 4-FC6H4).
-
-
[1]
Müller, T. E.; Hultzsch, K. C.; Yus, M.; Foubelo, F.; Tada, M. Chem. Rev. 2008, 108, 3795. doi: 10.1021/cr0306788
-
[2]
Severin, R.; Doye, S. Chem. Soc. Rev. 2007, 36, 1407. doi: 10.1039/b600981f
-
[3]
Nishina, N.; Yamamoto, Y. Top. Organomet. Chem. 2013, 43, 115.
-
[4]
(a) Sun, Q.; Wang, Y.-R.; Yuan, D.; Yao, Y.-M.; Shen, Q. Organometallics 2014, 33, 994. (b) Liang, S.-Z.; Hammond, L.; Xu, B.; Hammond, G. B. Adv. Synth. Catal. 2016, 358(20), 3313. (c) Sakai, N.; Takahashi, N.; Ogiwara, Y. Eur. J. Org. Chem. 2014, 5078.
-
[5]
王剑, 崔冬梅, 有机化学, 2016, 36(6), 1163. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htmWang, J.; Cui, D.-M. Chin. J. Org. Chem. 2016, 36(6), 1163 http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htm
-
[6]
卞荣剑, 鲍晓光, 有机化学, 2017, 37(1), 190. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htmBian, R.-J.; Bao, X.-G. Chin. J. Org. Chem. 2017, 37(1), 190 http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htm
-
[7]
McCahill, J. S. J.; Welch, G. C.; Stephan, D. W. Angew. Chem., Int. Ed. 2007, 46, 4968. doi: 10.1002/(ISSN)1521-3773
-
[8]
Dureen, M. A.; Brown, C. C.; Stephan, D. W. Organometallics 2010, 29, 6594. doi: 10.1021/om1009044
-
[9]
Sajid, M.; Elmer, L.-M.; Rosorius, C.; Daniliuc, C. G.; Grimme, S.; Kehr, G.; Erker, G. Angew. Chem., Int. Ed. 2013, 52, 2243. doi: 10.1002/anie.201208750
-
[10]
Mçmming, C. M.; Otten, E.; Kehr, G.; Frçhlich, R.; Grimme, S.; Stephan, D. W.; Erker, G. Angew. Chem., Int. Ed. 2009, 48, 6643. doi: 10.1002/anie.v48:36
-
[11]
Cardenas, A. J. P.; Culotta, B. J.; Warren, T. H.; Grimme, S.; Stute, A.; Froehlich, R.; Kehr, G.; Erker, G. Angew. Chem., Int. Ed. 2011, 50, 7567. doi: 10.1002/anie.201101622
-
[12]
Otten, E.; Neu, R. C.; Stephan, D. W. J. Am. Chem. Soc. 2009, 131, 9918. doi: 10.1021/ja904377v
-
[13]
Sajid, M.; Klose, A.; Birkmann, B.; Liang, L.; Schirmer, B.; Wiegand, T.; Eckert, H.; Lough, A. J.; Froehlich, R.; Daniliuc, C. G.; Grimme, S.; Stephan, D. W.; Kehr, G.; Erker, G. Chem. Sci. 2013, 4, 213. doi: 10.1039/C2SC21161K
-
[14]
Mahdi, T.; Stephan, D. W. Angew. Chem., Int. Ed. 2013, 52, 12418. doi: 10.1002/anie.201307254
-
[15]
Mahdi, T.; Stephan, D. W. Chem. Eur. J. 2015, 21, 11134. doi: 10.1002/chem.v21.31
-
[16]
温志国, 田冲, Borzov Maxim, 聂万丽, 化学学报, 2016, 74, 498. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345525.shtmlWen, Z.-G.; Tian, C.; Borzov, M.; Nie, W.-L. Acta Chim. Sinica 2016, 74, 498. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345525.shtml
-
[17]
胡茜, 田冲, Borzov Maxim, 聂万丽, 化学学报, 2015, 73, 1025. doi: 10.3866/PKU.WHXB201504141Hu, X.; Tian, C.; Borzov, M.; Nie, W.-L. Acta Chim. Sinica 2015, 73, 1025. doi: 10.3866/PKU.WHXB201504141
-
[18]
Nie, W.-L.; Sun, G.-F.; Tian, C.; Borzov, M. V. Z. Naturforsch. 2016, 71(10) b, 1029.
-
[19]
田冲, 姜亚, Borzov Maxim, 聂万丽, 化学学报, 2015, 73, 1203. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345179.shtmlTian, C.; Jiang, Y.; Borzov, M.; Nie, W.-L. Acta Chim. Sinica 2015, 73, 1203. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345179.shtml
-
[20]
Li, L.; Huang, G.; Chen, Z.; Liu, W.; Wang, X.; Chen, Y.; Yang, L.; Li, W.; Li, Y. Eur. J. Org. Chem. 2012, 28, 5564.
-
[1]
-
表 1 反应条件的优化a
Table 1. Optimization of the reaction conditionsa

Entry Alkyne Silane Yield/% 1 C6H4-CCH Et3SiH 3a 62.6[20] 2 P-CH3-C6H5-CCH Et3SiH 3b 58.6[20] 3 p-F-C6H4-CCH Et3SiH 3c 100.0 4 C6H4-CCH Ph3SiH 3a 70.1 5 P-CH3-C6H5-CCH Ph3SiH 3b 37.6 6 p-F-C6H4-CCH Ph3SiH 3c 82.9 7 p-F-C6H4-CCH Ph2SiH3 3c 60.0 8 p-F-C6H4-CCH PhSiH3 3c 38.7 9 p-F-C6H4-CCH (EtO)3SiH 3c 19.3 a NMR Yield; Molar ratio of alkyne to silane=1:3. 表 2 芳香胺盐酸盐和炔烃的氢胺化/还原反应a
Table 2. Reductive hydroamination of phenylacetylenes with ammoniumsa

-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 7
- 文章访问数: 2575
- HTML全文浏览量: 689


 下载:
下载:



 下载:
下载:

