
Citation: Zhou Lixiang. Biomineralization: a Pivotal Process in Developing a Novel Passive Treatment System for Acid Mine Drainage[J]. Acta Chimica Sinica, 2017, 75(6): 552-559. doi: 10.6023/A17020058

生物矿化:构建酸性矿山废水新型被动处理系统的新方法
-
关键词:
- 酸性矿山废水
- / 生物矿化
- / 重金属
- / 嗜酸性氧化亚铁硫杆菌
- / 施氏矿物
English
Biomineralization: a Pivotal Process in Developing a Novel Passive Treatment System for Acid Mine Drainage
-
Key words:
- acid mine drainage
- / biomineralization
- / heavy metal
- / Acidithiobacillus ferrooxidans
- / schwertmannite
-
1 引言
生物矿化是生物介入下的矿物晶体形成过程.在生物体系中, 细胞、菌体或其胞外聚合物不但为矿物生长提供了合适的矿化位置, 而且还能通过生物的直接或间接作用在多组分的体系中进一步调控晶体的定向组装, 形成特定的矿物相和特殊的形貌[1~4].生物矿化是自然界普遍存在的现象, 例如, 海洋生物中贝类、人和动物体内的结石、骨骼及牙齿的形成; 植物体内的草酸钙、硅石的沉积等等[1~4].在生物湿法冶金、酸性矿山废水(Acid mine drainage, AMD)、污泥生物沥浸(Sludge bioleaching)等极端酸性环境中, 也发现生物成因羟基硫酸铁矿物(如红棕色的施氏矿物)的形成[5~9].但如何有意识地去调控生物矿化尤其是微生物介导下的生物矿化过程并将之用于水处理上报道很少.
本文总结了国内外在AMD处理领域中所取得的进展和存在的不足, 利用AMD中存在的生物矿化现象, 提出了有意识地调控和强化这些生物矿物形成以构建AMD新型被动处理系统的新思想:即在嗜酸性氧化亚铁硫杆菌Acidithiobacillus ferrooxidans(以下简称“A.f菌”)促进下将AMD中溶解性铁和硫酸根在酸性条件下就地原位自然形成生物矿物, 并利用共沉淀作用和吸附作用同步去除水中部分重(类)金属, 出水进一步经过石灰沟渠中和达标排放, 生物矿物(可作为涂料、砷吸附剂、异相类Fenton反应的催化剂等环境材料)则可定期或不定期回收利用.这不但高效处理了含重金属的酸性矿山废水, 而且还在处理过程中获得了有价值的资源.是一种融合了物理法、化学法和生物法的第四种废水处理新方法-生物矿化法.本文还基于上述新方法, 展示了对模拟AMD处理的初步效果, 在此基础上提出了未来需要进一步关注和解决的科学问题.这为创建和发展生物矿化法废水处理新方法新原理奠定了基础, 也可为研究者运用生物矿化现象解决环境问题提供一些参考和思路.
2 酸性矿山废水危害及其处理现状
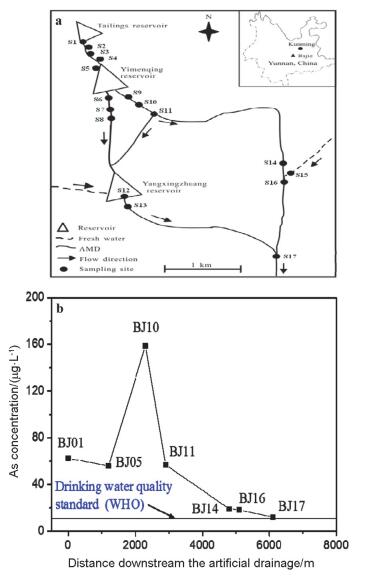
酸性矿山废水是指矿山(包括许多金属矿山和煤矿)开采中废矿石、尾矿堆所含硫化矿物(如黄铁矿FeS2, 砷黄铁矿AsFeS2, 黄铜矿CuFeS2等)在化能自养型硫杆菌(如A.f 菌)促进下, 发生氧化所产生pH<5的排水[10].极端酸性(pH常在2.0~3.5), 含丰富的SO42-(常在2000~6000 mg•L-1), Fe3+和Fe2+(多数在500~4500 mg•L-1)并同时溶解有大量有毒(类)金属元素(如As, Cd, Cu, Pb, Ni等)是AMD的重要特征[11, 12]. 表 1为本课题组对两个典型的AMD水质分析测试结果.通常离开采点越近, AMD的pH越低, 有毒金属的浓度也越高, AMD流经的溪流或沟渠因底部沉积物颜色而呈现赭黄或红色(图 1).

酸性矿山废水对矿区周边水土环境污染所造成的严重后果在我国湖南、广东、云南、广西、江西、安徽、贵州、湖北、山西等地有广泛报道[13~15].例如, 因矿区开采以及选冶过程中产生的酸性重金属废水导致湘江和湘江流域内4000万人口的饮用水安全受到威胁, 大量农田不能耕种, 有相当地域的鱼类、粮食、蔬菜不能食用, “镉大米”问题最为突出[13].对广东大宝山矿区的调查也表明, 因AMD导致重(类)金属污染使当地居民患癌症的风险指数高出安全值的100多倍[16].
除有色金属矿山外, 众多煤矿的AMD危害也不容小视[17, 18].值得指出的是, AMD的产生及其环境影响不因矿山停止开采而很快消除, 一些废弃矿山数十年后AMD污染问题依然严重[17, 19, 20].同样, AMD污染在国外如英国、美国、德国、西班牙、澳大利亚、加拿大等也是相当普遍的区域环境问题[19~22].由于矿山环境的复杂性, 采用传统的覆土回填采矿点, 以及包括使用缓释杀菌剂、钝化剂(利用化学药剂在硫化矿物表面形成保护膜)等在内的措施[14, 23, 24], 虽在一定时间内可减少硫化矿物氧化产生AMD, 但要长时间从源头上完全防控AMD的产生仍十分困难, 因此, AMD污染迄今都一直是世界性的难题, 备受各国高度关注.
目前我国金属非金属矿山近10万座, 其中小型矿山的比例高达95%.与大中型矿山不同, 小型矿山采矿点分散, 基础差、环保投资少, AMD污染在这些矿山特别严重, 成为该区重金属污染的“元凶”.对于这类矿山废水国际上虽有采用硫酸盐还原菌(SRB)介导的人工湿地或渗透性反应墙(PRB)的方法来处理的研究报道, 但因SRB菌最适pH是中性, 当AMD的pH<5时效果往往较差.迄今, 国内外实际投入运行的这种处理系统非常少见[25, 26].国际上主流技术主要采用以石灰中和(中和酸度, 沉淀重金属)为主的石灰石沟渠“被动处理系统”处理[27~29].被动处理系统的优点在于无需机械搅拌或鼓风充氧故几乎没有能耗、无需添加药剂、不需构建大型的反应器, 因此维护简单、运行费用低廉, 特别适合小型矿山AMD处理[30].
然而, 国内外实践都发现这种石灰中和被动处理系统, 仍存在许多问题, 突出的是:
(1) AMD通过石灰沟渠时, AMD中Fe3+易生成Fe(OH)3絮状沉淀, 而包覆在石灰石等介质表面, 一方面阻止了石灰石与AMD进一步的中和反应, 导致石灰需求量大增或重(类)金属(特别是As)去除率低, 降低了处理效能, 另一方面, 产生的大量Fe(OH)3絮状沉淀和废石膏(CaSO4)等沉渣会堵塞过滤介质, 减少水力导度, 随时间的延长, 系统将逐渐变差直至崩溃, 大大缩短了该系统的使用寿命[31]; (2) 直接石灰中和会导致大量的毒渣(指有毒金属的氢氧化物或砷酸钙等与废石膏的混合物)产生[32], 由于AMD中铁和硫酸根浓度较之有毒金属浓度高好几个数量级, 因此, 毒渣中有毒金属(主要是有色金属和类金属As等)品位低, 无法利用, 安全处置难度大; (3) AMD中的溶解性Fe仍有部分以Fe2+存在[11], 它完全沉淀所需pH(一般在pH 8.5以上)要比Fe3+(pH3.5左右即可生成相应沉淀)高得多, 因此, 在常规的石灰沟渠处理系统中会导致排水中亚铁高而影响水质.无疑, AMD中高浓度的可溶性铁(Fe3+和Fe2+)和硫酸根正是制约石灰石的渗透沟渠系统良好运行的根本原因.
因此, 若能在AMD本身较低pH的酸性环境下, 原位去除AMD中的溶解性铁和消减部分硫酸根, 再进入石灰沟渠被动处理系统, 既可有效去除有毒金属, 又能从根本上解决上述传统石灰石沟渠被动处理系统存在的弊端, 使其真正发挥出简便而有效消减AMD污染的功效.
3 AMD环境中生物矿化现象及其重要启示
通常金属离子在极端酸性条件下活性最高, 是很难沉淀的.如何在极端酸性的AMD环境中就地去除溶解性铁、大部分硫酸根甚至有毒金属As, 为后期石灰中和系统有效沉淀去除其余重金属离子并使石灰沟渠被动处理系统持续高效运行? AMD自然环境中生物矿化现象为我们提供了一个全新的思路.
研究发现, 在这种含较多溶解性Fe、SO42-以及存在A.f菌的AMD流经的路径中, 往往能观测到颜色从黄橙色到红棕色的一系列含铁沉积物的生成[11, 33, 34], 且在这些沉积物中含有大量的As, 使水中As在AMD流经的路径中出现自然钝化现象[11, 35], 如图 2所示.
研究揭示, 在这些环境中铁沉积物主要为结晶度相对较差的施威特曼石(Schwertmannite), 典型分子式[Fe8O8(OH)6SO4]或结晶度好的黄铁矾[Jarosite, (K、Na、NH4、H3O)Fe3(OH)6(SO4)2], 它们二者均为羟基硫酸铁矿物, 少数也见有针铁矿(Goethite, α-FeOOH)的存在, 但在源头或离AMD产生点很近的极端酸性环境中, 却很少见有铁的氢氧化物或水铁矿(Ferrihydrite, 5Fe2O3• 9H2O)的存在[33].显然, 在这种富铁富硫酸根和有微生物A.f菌存在的极端酸性的天然环境中很容易形成羟基硫酸铁矿物.
然而, 在非生物环境中天然的施氏矿物和黄铁矾在自然界中却非常稀少.尽管黄铁矾和施氏矿物也可采用化学方法合成, 但这些反应过程需高温高压、加热或/并使用化学氧化剂等极端条件[36~38], 在常温常压的非生物环境下这些羟基硫酸铁矿物形成则很难.在极端酸性并富含SO42-条件下, 在微生物促进下, S会优先与Fe结合, 形成羟基硫酸铁矿物, 而不会生成Fe(OH)3或水铁矿[39, 40].其反应式可表述为:
其中M+=K+, NH4+, Na+, H3O+等
形成黄铁矾(包括黄钾铁矾、黄铵铁矾、黄钠铁矾、黄草铁矾等)的条件与形成施氏矿物的略有不同, 前者所需要的pH (1.8~3.0) 比后者(pH 2.5~3.5) 更低, 且需要较多的一价阳离子(主要为K+, NH4+, Na+, H3O+等)[41, 42].
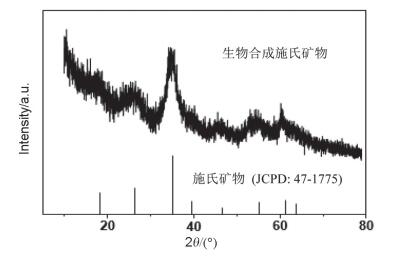
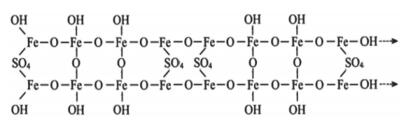
结晶度较差的施氏矿物外观呈“海胆”状, 棕红色, 颜色鲜艳(见图 3), XRD图谱上有典型的8个宽峰(图 4).其结构类似四方纤铁矿β-FeOOH (akagannite), 晶格构造沿C轴方向呈管状, 直径约0.5 nm, 与砷酸盐、亚砷酸盐、铬酸盐等(类)金属含氧阴离子的直径相当(见图 5)[7, 43].因此, 它对As有相当大的专性吸持作用, 使AMD中As得到自然钝化或作为除砷材料[7, 44].
近10年来不但在我国许多AMD或受AMD影响的自然环境中发现施氏矿物等的存在, 而且进一步证实在A.f菌的推动下, 在类似AMD的极端酸性环境中, Fe2+能在数小时内形成这些矿物, 并发现菌密度、起始亚铁浓度、一价阳离子种类及其与亚铁的比例、亚铁氧化速率、溶液pH、反应时间等共同决定了矿物类型、生成量及其速率[42, 44, 46].这些矿物通过共沉淀或吸附作用可部分去除有毒金属, 特别是As, 在最佳条件下最大吸持量可达到120~140 mg•g-1[37, 44].上述发现, 为我们在极端酸性的AMD环境中, 发展一种强化和调控生物矿化现象有效去除溶解性铁(Fe2+, Fe3+)和SO42-及部分有毒金属的新方法提供了重要启示.
值得注意的是, A.f菌促进AMD中Fe2+转化为黄铁矾的速度以及转化率, 虽然要远比其形成施氏矿物快或高得多, 但却需要外源投入高浓度的一价阳离子尤其是K+(体系中至少含500 mg•L-1以上. K+是成矾能力最强的元素, 是NH4+的75倍, 是Na+的200倍)[41, 42], 这在AMD实际废水被动处理中因成本高昂也难于操作控制, 明显不可行.而且结晶度好的黄钾铁矾类在酸性条件下对As的吸持能力也要远低于施氏矿物.因此, 发展一种强化生物成因施氏矿物高效快速形成的方法则显得更为重要.
然而我们发现, A.f菌促进AMD中施氏矿物的形成, 虽不需要投加K+, 但矿化效率却很低:仅30%左右的Fe2+转化成矿(施氏矿物), 剩余的大部分Fe2+是被A.f菌氧化后以Fe3+形式存在溶液中.若AMD中溶解性铁完全以Fe3+形式存在, 则根本不能形成施氏矿物(成矿率为0)[47, 48].这为高效去除AMD中溶解性铁、硫酸盐和部分As增添了极大困难.如何使水中溶解性铁能从0%的沉淀率提高到80%以上甚至100%?是一项富有挑战性的课题.
4 AMD中施氏矿物生物成矿机制及采用嗜酸性铁还原菌等措施定向调控其生成以构筑AMD水处理系统的科学设想
我们发现在常温常压下, Fe3+水解形成施氏矿物(反应式2) 在热力学上是不能自发进行的, 因为其反应自由能∆rG°298为正值(∆rG°298=6.275 kJ•mol-1).而在A.f菌参与下的Fe2+氧化成Fe3+(即反应式1), 其∆rG°298为-44.32 kJ•mol-1[49].显然在Fe2+→Fe3+→ Fe8O8(OH)6SO4(施氏矿物)的偶联反应中(即反应式1+反应式2), 其∆rG°298为(-44.32)+6.275=-38.045 kJ•mol-1, 很明显, 此时反应能在常温常压下完全自发进行.因此, 在常温常压的酸性条件下A.f菌能促进次生施氏矿物形成的重要原因是A.f菌氧化Fe2+会释放出能量, 克服了后续Fe3+水解成矿的能垒, 二者(生物氧化和Fe3+水解成矿)偶联使总的反应自由能∆rG°298为负值(-38.045 kJ•mol-1), 因此容易自发进行.这是为什么Fe3+在常温常压下不能形成施式矿物的反应, 只要在A.f菌参与下, 通过促进Fe2+氧化成Fe3+却容易生成的重要原因.
至于为什么在酸性富硫酸盐的AMD反应体系中, 虽然Fe2+能在数小时的时间内完全氧化成Fe3+, 但其中仍有70%左右的Fe3+不能沉淀生成施氏矿物?我们推测其原因在于A.f菌氧化Fe2+成Fe3+的速度远高于Fe3+水解成矿的速度, Fe2+氧化释放出能量不能被完全同步利用于Fe3+水解成矿, 因此, 剩余的未能生物矿化的Fe3+无法获得能量成矿[47].另一方面, 根据生物矿化结晶学原理, 生物矿化最主要的形式是溶液结晶过程, 界面能最小化是结晶也就是生物矿化的最初驱动力.在过饱和的亚稳相中, 新相一旦成核就能自发长大, 这是因为新相的长大是系统吉布斯自由能降低的过程[1].但制造一个过饱和溶液是不足以诱导溶液中自发均相成核发生[50].只有当溶液的过饱和度超过了一个临界值, 结晶或沉淀才能观测到.试验证明, 在成核初期阶段, 当晶体尺寸小于临界尺寸(γ*)时, 随着晶体生长, 总吉布斯自由能升高, 当达到或超过γ*时, 则随着晶体生长, 总吉布斯自由能急剧下降[1, 51].外观表现为在成核初期晶体形成极慢, 只要超过一定临界大小后则晶体生长较快的现象.因此, 在实践中人为地加入固相杂质(如石膏粉末、石英砂等)和晶种(如施氏矿物、黄钾铁矾等), 可以不同程度地降低乃至消除临界现象的产生, 促进矿物的快速形成, 这在我们前期研究中已得到证实[52, 53].
根据上述分析, 溶液中残余的Fe3+之所以不能进一步生物矿化是由于缺乏产生能量的反应与之相耦联, 也可能缺乏足够的晶核.因此, 我们有理由认为, 若将溶液中残余的Fe3+还原成Fe2+, 再通过与生物氧化(可释放能量)与生物矿化(需要能量)相耦联, 多次还原-氧化耦合循环, 再辅助以晶种的介入, 则能实现高效生物矿化的目的.近年来, 本课题组分离到一株嗜酸性铁还原菌Acidiphilium sp. JZ-6, 它与隐藏嗜酸菌模式菌株Acidiphilium Cryptum的16SRNA相似度高达99.93%.其重要特征在于它是兼性厌氧菌, 在一般缺氧时(溶液静止即可, 无需严格厌氧)对Fe3+还原能力最强, 这为其上述高效生物矿化设想的实现提供了科学支撑.
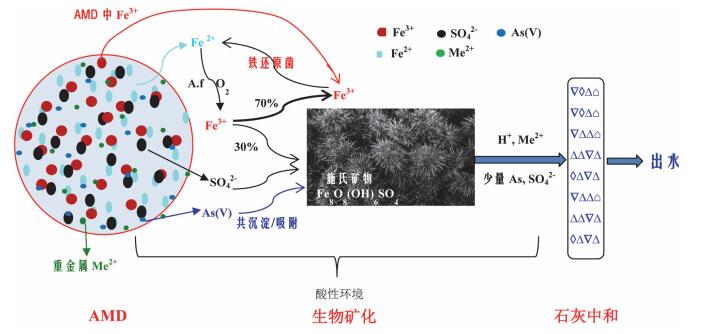
为此, 可构成这样一个以生物矿化为核心的AMD处理的新方法, 其原理为利用A.f菌将AMD中Fe2+全部氧化为Fe3+, 其中部分Fe3+(大约30%左右)与SO42-利用亚铁生物氧化释放出的能量合成施氏矿物; 剩余未成矿的Fe3+(大约70%)连同AMD中本身存在的Fe3+全部生物还原成Fe2+, 继而再通过A.f菌氧化成矿, 再还原, 再氧化……多次循环, 实现AMD中溶解性铁和部分SO42-高效生物矿化目标.在生物矿化过程中, AMD中有毒金属特别是As部分可通过共沉淀或吸附去除, 大部分其他金属阳离子和少量在生物矿化中未去除的As则在其后的石灰沟渠中和系统时可完全沉淀, 出水达标.由于前端生物矿化过程消减了影响石灰中和系统的溶解性铁和SO42-, 因此该新方法可有望解决传统中和系统效率低、寿命短、毒渣量大、水质难达标的弊端.该AMD处理的原理如图 6所示.
5 基于定向调控面向实际工程应用的“生物矿化-石灰石沟渠”AMD新型被动处理系统构建方法及其效果
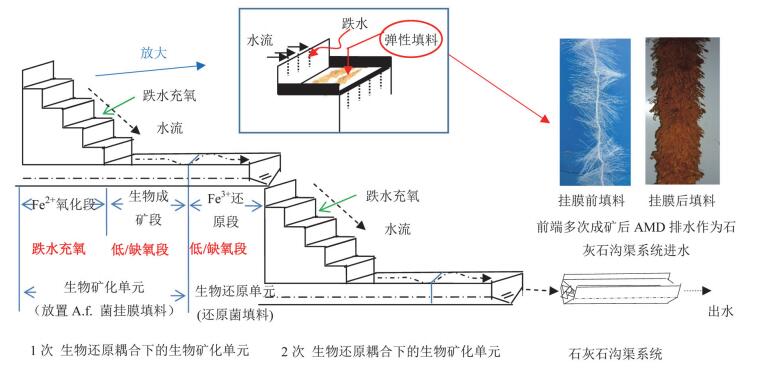
我们发现, Fe2+生物氧化形成Fe3+虽是一个需氧的过程(野外实践中可利用地形高差进行跌水充氧), 但生物成因羟基硫酸铁矿物的形成与“生长”, 却完全可在低氧或缺氧下进行[54].因此, 紧靠其后, 采用软性填料和缓释碳源(如作物秸秆)负载嗜酸性铁还原菌, 即可继续在缺氧条件下有效还原没有生物矿化的Fe3+, 其后再重复放置A.f菌的载体并跌水充氧, 将还原获得的Fe2+进一步氧化并形成矿物晶核, 在低氧或缺氧段继续成矿或生长.如此, 负载有A.f菌的载体与负载有嗜酸性铁还原菌的载体交替放置, 重复多次, 利用跌水充氧构筑AMD中A.f氧化菌工作环境和利用AMD水平流时的水深及与缓释碳源作用时构建缺氧环境, 使AMD中A.f氧化菌与嗜酸性铁还原菌耦合高效转化溶解性铁和硫酸根成施氏矿物的原理, 即可成功构建出高效生物矿化单元(即在底部填充有少量填料用以交替负载A.f菌或嗜酸性铁还原菌的沟渠).与后端传统石灰沟渠整合, 可形成高效且几乎零能耗的AMD新型被动处理系统(图 7).使AMD流经这种新型的系统时, 其中Fe2+在生物矿化单元被全部生物氧化成Fe3+, 在微生物促进下部分Fe3+、SO42-转化成施氏矿物并通过其共沉淀和吸附作用消减AMD中的部分有毒金属特别是类金属As[21, 55].剩余未成矿的Fe3+包括AMD中原有的Fe3+在嗜酸性铁还原菌作用下被还原为Fe2+, 再经过氧化、成矿过程转化为施氏矿物.这样在生物矿化单元中多次氧化与还原耦合成矿, 使AMD中溶解性铁的转化率大幅提高.经过该生物矿化单元后的出水, 再进入常规的AMD石灰石沟渠被动处理系统, 则可高效净化AMD, 从根本上克服传统石灰沟渠被动处理系统的弊端.生物矿化单元中在填料上生长和形成的施氏矿物(见图 7)还可被定期回收.
表 2列出了采用直接石灰中和以及采用生物矿化后再石灰中和处理模拟的AMD的结果.结果显示, 采用新型处理方法较之常规的石灰中和AMD处理法, 水质容易达标.而且还具备如下优点: ① 通过A.f菌氧化和残余Fe3+的生物还原协同作用, 可在低pH条件下预先去除AMD中85%左右的溶解性铁(Fe2+和Fe3+)和78%左右的SO42-以及70%左右的有毒金属As, 为后端的石灰沟渠被动处理系统减负; ② 同时在该阶段还可从弹性填料上方便回收施氏矿物, 产率可达约4 g•L-1.施氏矿物是一类在低pH下生物形成的外观色彩鲜艳(棕红色)的铁基矿物, 且遮盖性好, 因而也是非常珍贵的天然能抵抗酸雨腐蚀的无机颜料.又由于它具有不规则的孔道结构加之结晶度差, 比表面积大(100~200 m2•g-1), 可作为非常理想的砷高效吸附剂[43, 44, 56].因此, 在处理AMD的同时, 还可不断收获有用的环境材料; ③ 经生物矿化后, AMD中溶解性铁和硫酸根因生成施氏矿物已大幅度消减, 进入石灰中和阶段时使以往常见的Fe(OH)3絮状沉淀和生成大量CaSO4堵塞过水通道现象得到消除, 有望大大延长AMD石灰石沟渠被动处理系统寿命; ④ 石灰需求量减少82%, 毒渣(即石灰中和渣)产生量减少91%, 产生的这些少量“毒渣”可作为“次生”金属矿开采和冶炼, 因为这些毒渣中有色金属的品位可提高10多倍, 达到金属冶炼对原料品位的要求.最近有学者提出的建设一座(批)面向2030~2040年的中国污水处理概念厂就是要求不仅能净化水质, 而且能够成为有价资源的生产厂[57].因此, 在净化污(废)水的同时, 获得有用资源, 将是未来污(废)水处理的重要发展态势[58].
 表 2
模拟AMD仅用石灰中和(常规处理)和用生物矿化-石灰中和(新型处理)处理的效果
Table 2.
The water quality of lime neutralization-treated AMD with and without biomineralization pretreatment
表 2
模拟AMD仅用石灰中和(常规处理)和用生物矿化-石灰中和(新型处理)处理的效果
Table 2.
The water quality of lime neutralization-treated AMD with and without biomineralization pretreatment

6 研究展望
构建高效的“生物矿化-石灰中和”AMD新型被动处理系统, 还有许多科学问题需要进一步研究:
6.1 生物矿物“生长”原理与作用机制.
包括需要研究(1) AMD生物矿化的溶液化学.例如, 溶液结晶饱和度因素(Fe2+, Fe3+, SO42-浓度及其pH)及Fe2+/Fe3+比例对A.f菌促进生物矿化的影响(包括铁沉淀率和矿物量、类型、形貌等); (2) 生物矿化过程中A.f菌的作用.除氧化作用外, 起诱导矿物形成和晶体生长的晶核作用或模版作用有多大?是菌体本身的作用还是分泌的胞外聚合物EPS的作用, 或是二者兼而有之? (3) 新生态矿物本身的作用以及与微生物的相互关系.如, A. f菌促进下形成新生态施氏矿物“晶核”的临界尺寸及成核后“晶核”大小对后续矿物晶体“生长”的影响.新生态矿物与微生物是什么样的相对位置(包裹微生物?还是微生物不断在矿物表面生长?还是微生物与矿物形成层状结构?)?表面矿物不断生长的过程对成矿效率或速率有何影响?
6.2 生物矿化高效调控方法及对有毒金属同步去除的机理
需要研究A.f菌(铁氧化菌)和铁还原菌负载在载体和缓释碳源上“生长”机制; 铁还原菌与铁氧化菌协同成矿机制及影响因素(包括填料上矿物的收集频率、收集比例对菌密度及活性的短期影响、恢复周期和对成矿的影响等); 负载在弹性填料上“生长”的施氏矿物对AMD中有毒重(类)金属(重点关注As)的吸附特征和形成过程中对有毒金属的共沉淀作用大小及影响因素; 进入施氏矿物的重(类)金属在AMD环境中的稳定性以及形成的施氏矿物本身的稳定性等.此外, 还需深入研究铁氧化菌与铁还原菌如何高效协同, 特别是如何保障铁氧化成矿单元和残余Fe3+生物还原单元的最佳pH保持基本不变的方法, 这涉及到铁还原单元中缓释碳源种类的选择及各单元水力持留时间的选择等问题.
6.3 实际环境下新型被动处理系统构建及运行效果评估
需要研究在实际环境下, 如何通过设置生物成矿单元的跌水级数与跌水高度、水层深度、填料和缓释碳源种类与填充度、沟渠水流路径等来保证或控制生物矿化各单元的溶氧、菌密度及活性、水力持留时间等.以及研究末端石灰石沟渠长度、石灰石填充度、孔隙度、截面积大小与形状.最终需要评估整个“生物矿化-石灰石沟渠”新型被动系统处理AMD的效果及较长期运行的稳定性等.
通过对上述这些问题尤其是废水中生物矿化的深入研究, 不但对研发出适合小型矿山的AMD污染控制的被动处理系统意义重大, 同样对在大中型矿山构建生物矿化-石灰中和的主动处理系统有重要价值[59], 生物矿化法也可望为污水净化提供一种新方法.
-
-
[1]
崔福斋, 生物矿化, 清华大学出版社, 北京, 2007, pp. 1~85.Cui, F. Z. Biomineralization, Tsinghua University Press, Beijing, 2007, pp. 1~85.
-
[2]
姚菊明, 魏克民, 励丽, 孔祥东, 祝永强, 林凤, 化学学报, 2007, 65, 635. doi: 10.3321/j.issn:1001-4861.2007.04.012Yao, J.-M.; Wei, K.-M.; Li, L.; Kong, X.-D.; Zhu, Y.-Q.; Lin, F. Acta Chim. Sinica 2007, 65, 635. doi: 10.3321/j.issn:1001-4861.2007.04.012
-
[3]
张生, 杨如娥, 欧阳健明, 化学学报, 2011, 69, 284. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract339727.shtmlZhang, S.; Yang, R.; Ouyang, J. Acta Chim. Sinica 2011, 69, 284. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract339727.shtml
-
[4]
王荔军, 王运华, 张福锁, 杨文胜, 李铁津, 化学学报, 2002, 60, 1144. doi: 10.3321/j.issn:0567-7351.2002.06.035Wang, L.-J.; Wang, Y.-H.; Zhang, F.-S.; Yang, W.-S.; Li, T.-J. Acta Chim. Sinica 2002, 60, 1144. doi: 10.3321/j.issn:0567-7351.2002.06.035
-
[5]
Yu, R.-L.; Zhong, D.-L.; Miao, L.; Wu, F.-D.; Qiu, G.-Z.; Gu, G.-H. Trans. Nonferrous Met. Soc. China 2011, 21, 1634. doi: 10.1016/S1003-6326(11)60907-2
-
[6]
梁长利, 夏金兰, 杨益, 聂珍媛, 邱冠周, 中国有色金属学报, 2012, 22, 265.Liang, C.-L.; Xia, J.-L.; Yang, Y.; Nie, Z.-Y.; Qiu, G.-Z. Chin. J. Nonferrous Met. 2012, 22, 265.
-
[7]
Bigham, J. M.; Schwertmann, U.; Murad, E.; Carlson, L. Geochim. Cosmochim. Acta 1990, 54, 2743. doi: 10.1016/0016-7037(90)90009-A
-
[8]
Bigham, J. M.; Carlson, L.; Murad, E. Mineral Mag. 1994, 58, 641. doi: 10.1180/minmag
-
[9]
Liao, Y. H.; Zhou, L. X.; Bai, S. Y.; Liang, J. R.; Wang, S. M. Appl. Geochem. 2009, 24, 1739. doi: 10.1016/j.apgeochem.2009.05.003
-
[10]
Singer, P. C.; Stumm, W. Science 1970, 167, 1121. doi: 10.1126/science.167.3921.1121
-
[11]
España, J. S.; Pamo, E. L.; Santofimia, E.; Aduvire, O.; Reyes, L.; Barettino, D. Appl. Geochem. 2005, 20, 1320. doi: 10.1016/j.apgeochem.2005.01.011
-
[12]
Myers, T. J. Hydrol. 2016, 533, 277. doi: 10.1016/j.jhydrol.2015.12.020
-
[13]
贺广华, 曹昌, 中国经济周刊, 2009, 16, 16.He, G. H.; Cao, C. China Economic Weekly 2009, 16, 16.
-
[14]
党志, 矿区污染源头控制, 科学出版社, 北京, 2015, pp. 5~9.Dang, Z. Source Control of Mine Pollution, Science Press, Beijing, 2015, pp. 5~9.
-
[15]
Liao, J. B.; Wen, Z. W.; Ru, X.; Chen, J. D.; Wu, H. Z.; Wei, C. H. Ecotox. Environ. Safe. 2016, 124, 460. doi: 10.1016/j.ecoenv.2015.11.023
-
[16]
Chen, M.; Lu, G.; Guo, C.; Yang, C.; Wu, J.; Huang, W.; Yee, N.; Dang, Z. Chemosphere 2015, 119, 734. doi: 10.1016/j.chemosphere.2014.07.094
-
[17]
Gammons, C. H.; Duaime, T. E.; Parker, S. R.; Poulson, S. R.; Kennelly, P. Chem. Geol. 2010, 269, 100. doi: 10.1016/j.chemgeo.2009.05.026
-
[18]
Qureshi, A.; Maurice, C.; Öhlander, B. J. Geochem. Explor. 2016, 160, 44. doi: 10.1016/j.gexplo.2015.10.014
-
[19]
VanGeen, A.; Adkins, J. F.; Boyle, E. A.; Nelson, C. H.; Palanques, A. Geology 1997, 25, 291. doi: 10.1130/0091-7613(1997)025<0291:AYROWC>2.3.CO;2
-
[20]
Maicaneanu, A.; Bedelean, H.; Ardelean, M.; Burca, S.; Stance, M. Chemosphere 2013, 93, 1400. doi: 10.1016/j.chemosphere.2013.07.003
-
[21]
Papassiopi, N.; Zaharia, C.; Xenidis, A.; Adam, K.; Liakopoulos, A.; Romaidis, I. Miner. Eng. 2014, 64, 78. doi: 10.1016/j.mineng.2014.04.002
-
[22]
Caraballo, M. A.; Macías, F.; Nieto, J. M.; Ayora, C. Sci. Total Environ. 2016, 539, 427. doi: 10.1016/j.scitotenv.2015.08.156
-
[23]
Johnson, D. B.; Hallberg, K. B. Sci. Total Environ. 2005, 338, 3. doi: 10.1016/j.scitotenv.2004.09.002
-
[24]
Akcil, A.; Koldas, S. J. Clean. Prod. 2006, 14, 1139. doi: 10.1016/j.jclepro.2004.09.006
-
[25]
Gibert, O.; J. De Pablo, J.; Cortina, J. L.; Ayora, C. Rev. Environ. Sci. Biotech. 2002, 1, 327. doi: 10.1023/A:1023227616422
-
[26]
Sánchez-Andrea, I.; Sanz, J. L.; Bijmans, M. F. M.; Stams, A. J. M. J. Hazard. Mater. 2014, 269, 98. doi: 10.1016/j.jhazmat.2013.12.032
-
[27]
Kalin, M.; Fyson, A.; Wheeler, W. N. Sci. Total Environ. 2006, 366, 395. doi: 10.1016/j.scitotenv.2005.11.015
-
[28]
Shim, M. J.; Choi, B. Y.; Lee, G.; Hwang, Y. H.; Yang, J. S.; O'Loughlin, E. J.; Kwon, M. J. J. Geochem. Explor. 2015, 159, 234. doi: 10.1016/j.gexplo.2015.09.015
-
[29]
Iakovleva, E.; Makila, E.; Salonen, J.; Sitarz, M.; Wang, S. B.; Sillanpaa, M. Ecol. Eng. 2015, 81, 30. doi: 10.1016/j.ecoleng.2015.04.046
-
[30]
Kleinmann, R. L. P.; Hedin, R. S. Pollut. Eng. 1993, 25, 20.
-
[31]
Santomartino, S.; Webb, J. A. Appl. Geochem. 2007, 22, 2344. doi: 10.1016/j.apgeochem.2007.04.020
-
[32]
杨中超, 朱利军, 刘锐平, 曲久辉, 环境工程学报, 2014, 8, 2205. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=hjjz201406011&dbname=CJFD&dbcode=CJFQYang, Z.; Zhu, L.; Liu, R.; Qu, J. Chin. J. Environ. Eng. 2014, 8, 2205. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=hjjz201406011&dbname=CJFD&dbcode=CJFQ
-
[33]
Schwertmann, U; Bigham, J. M.; Murad, E. Eur. J. Mineral. 1995, 7, 547. doi: 10.1127/ejm/7/3/0547
-
[34]
谢越, 博士论文, 南京农业大学, 南京, 2010.Xie, Y. Ph. D. Dissertation, Nanjing Agricultural University, Nanjing, 2010 (in Chinese).
-
[35]
Fukushi, K.; Sasaki, M.; Sato, T.; Yanase, N.; Amano, H.; Ikeda, H. Appl. Geochem. 2003, 18, 1267. doi: 10.1016/S0883-2927(03)00011-8
-
[36]
Loan, M.; Richmond, W. R.; Parkinson, G. M. J. Cryst. Growth. 2005, 275, 1875. doi: 10.1016/j.jcrysgro.2004.11.276
-
[37]
李浙英, 梁剑茹, 柏双友, 周立祥, 环境科学学报, 2011, 31, 460. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=hjxx201103002&dbname=CJFD&dbcode=CJFQLi, Z. Y.; Liang, J. R.; Bai, S. Y.; Zhou, L. X. Acta Scientiae Circumstantiae 2011, 31, 460. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=hjxx201103002&dbname=CJFD&dbcode=CJFQ
-
[38]
Liu, F. W.; Zhou, J.; Zhang, S. S.; Liu, L. L.; Zhou, L. X.; Fan, W. H. PLoS ONE 2015, 10, e0138891. doi: 10.1371/journal.pone.0138891
-
[39]
Bigham, J. M.; Schwertmann, U.; Pfab, G. Appl. Geochem. 1996, 11, 845. doi: 10.1016/S0883-2927(96)00052-2
-
[40]
Jambor, J. L.; Dutrizac, J. E. Chem. Rev. 1998, 98, 2549. doi: 10.1021/cr970105t
-
[41]
Gramp, J. P.; Jones, F. S.; Bigham, J. M.; Tuovinen, O. H. Hydrometallurgy 2008, 94, 29. doi: 10.1016/j.hydromet.2008.05.019
-
[42]
Bai, S. Y.; Xu, Z. H.; Wang, M.; Liao, Y. H.; Liang, J. R; Zheng, C. C.; Zhou, L. X. Mater. Sci. Eng. C 2012, 32, 2323. doi: 10.1016/j.msec.2012.07.003
-
[43]
Regenspurg, S.; Peiffer, S. Appl. Geochem. 2005, 20, 1226. doi: 10.1016/j.apgeochem.2004.12.002
-
[44]
Liao, Y. H.; Liang, J. R.; Zhou, L. X. Chemosphere 2011, 83, 295. doi: 10.1016/j.chemosphere.2010.12.060
-
[45]
Barham, R. J. Mater. Res. 1997, 12, 2751 doi: 10.1557/JMR.1997.0366
-
[46]
Liao, Y. H.; Zhou, L. X.; Liang, J. R.; Xiong, H. X. Mater. Sci. Eng. C 2009, 29, 211. doi: 10.1016/j.msec.2008.06.011
-
[47]
柏双友, 博士论文, 南京农业大学, 南京, 2012.Bai, S. Y. Ph. D. Dissertation, Nanjing Agricultural University, Nanjing, 2012.
-
[48]
王宁, 博士论文, 南京农业大学, 南京, 2016.Wang, N. Ph. D. Dissertation, Nanjing Agricultural University, Nanjing, 2016.
-
[49]
Majzlan, J.; Navrotsky, A.; Schwertmann, U. Geochim. Cosmochim. Acta 2004, 68, 1049. doi: 10.1016/S0016-7037(03)00371-5
-
[50]
Hohenberg, P. C.; Halperin, B. I. Rev. Mod. Phys. 1977, 49, 435. doi: 10.1103/RevModPhys.49.435
-
[51]
Tang, R. K.; Wang, L. J.; Orme, C. A.; Bonstein, T.; Bush, P. J.; Nancollas, G. H. Angrew. Chem., Int. Ed. 2004, 43, 2697. doi: 10.1002/(ISSN)1521-3773
-
[52]
Wang, M.; Zhou, L. X. Hydrometallurgy 2012, 125, 152. http://www.sciencedirect.com/science/article/pii/S0304386X12001351
-
[53]
Liu, F. W.; Zhou, J.; Zhou, L. X.; Zhang, S. S.; Liu, L. L.; Wang, M. J. Hazard. Mater. 2015, 299, 404. doi: 10.1016/j.jhazmat.2015.06.035
-
[54]
Hou, Q. J.; Fang, D.; Liang, J. R.; Zhou, L. X. Plos One 2015, 10, e0120966. doi: 10.1371/journal.pone.0120966
-
[55]
Ahoranta, S. H.; Kokko, M. E.; Papirio, S.; Özkaya, B.; Puhakka, J. S. J. Hazard. Mater. 2016, 306, 124. doi: 10.1016/j.jhazmat.2015.12.012
-
[56]
Xie, Y.; Zhou, L. X. Pedosphere 2013, 23, 402. doi: 10.1016/S1002-0160(13)60032-6
-
[57]
曲久辉, 王凯军, 王洪臣, 柯兵, 俞汉青, 中国环境报, 2014, 1, 7.Qu, J. H.; Wang, K. J.; Wang, H. C.; Yu, G.; Ke, B.; Yu, H. Q. China Environ. News 2014, 1, 7.
-
[58]
黄霞, 给水排水, 2013, 39, 1. doi: 10.3969/j.issn.1002-8471.2013.02.001Huang, X. Water Wastewater Eng. 2013, 39, 1. doi: 10.3969/j.issn.1002-8471.2013.02.001
-
[59]
周立祥, 地学前缘, 2008, 15, 74. doi: 10.3321/j.issn:1005-2321.2008.05.008Zhou, L. X. Earth Science Frontiers 2008, 15, 74. doi: 10.3321/j.issn:1005-2321.2008.05.008
-
[1]
-
表 1 两个典型的酸性矿山废水水质
Table 1. The water quality of two typical AMD

表 2 模拟AMD仅用石灰中和(常规处理)和用生物矿化-石灰中和(新型处理)处理的效果
Table 2. The water quality of lime neutralization-treated AMD with and without biomineralization pretreatment

-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 29
- 文章访问数: 3806
- HTML全文浏览量: 634




 下载:
下载:






 下载:
下载:

