 图 1
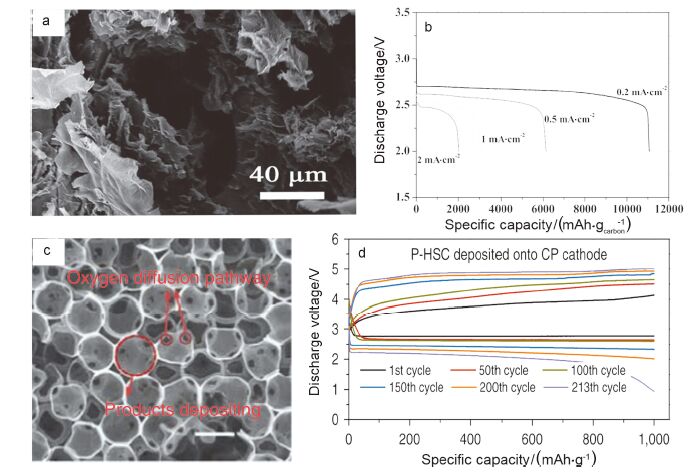
(a)石墨烯空气电极的SEM图像, (b)石墨烯空气电极的倍率性能, (c)碳球壳空气电极的SEM图像和(d)碳球壳空气电极的循环性能[41, 39]
Figure 1.
(a) SEM image of the graphene electrode, (b) rate performance of the graphene electrode, (c) SEM image of the hollow spherical carbon electrode and (d) cycling performance of the hollow spherical carbon electrode[41, 39]
图 1
(a)石墨烯空气电极的SEM图像, (b)石墨烯空气电极的倍率性能, (c)碳球壳空气电极的SEM图像和(d)碳球壳空气电极的循环性能[41, 39]
Figure 1.
(a) SEM image of the graphene electrode, (b) rate performance of the graphene electrode, (c) SEM image of the hollow spherical carbon electrode and (d) cycling performance of the hollow spherical carbon electrode[41, 39]

Citation: Liu Qingchao, Ma Shiyu, Xu Jijing, Li Zhongjun, Zhang Xinbo. Design and Preparation of Advanced Materials for Lithium-Air Batteries[J]. Acta Chimica Sinica, 2017, 75(2): 137-146. doi: 10.6023/A16070326

锂-空气二次电池关键材料与器件的设计与制备
English
Design and Preparation of Advanced Materials for Lithium-Air Batteries
-
Key words:
- lithium-air battery
- / energy density
- / energy storage devices
- / electrode
- / electrochemical performance
-
1 引言
锂-空气二次电池具有远高于传统锂离子电池的理论能量密度以及对环境较友好等特点, 这一概念一经提出便受到了科研界的广泛关注, 被认为是最具应用前景的新一代化学电源. 锂-空气二次电池采用金属锂片作为负极, 电解液中的锂离子与正极中来自空气的氧气发生电化学反应: 2Li++2e-+O2→Li2O2[1~3], 电池在反应过程中可直接利用空气中的氧气, 但实现所设计的理想反应过程, 仍面临诸多重大的挑战.
锂-空气二次电池目前仍处于其发展的初期阶段, 许多关键的科学技术问题还有待解决. 具体主要包括以下几个方面: (1)锂-空气二次电池的氧还原(ORR)和氧析出(OER)过程的过电位偏高, 严重制约了电池充放电效率的提升. 为解决这一问题, 研究者们开发了一系列的锂-空气二次电池用催化剂, 这些催化剂包括贵金属、金属氧化物、金属氮化物以及贵金属合金等[4~14], 其中贵金属钌及其氧化物因其相对其它贵金属较为廉价, 且催化性能优异, 在锂-空气二次电池催化剂领域得到广泛研究[15~21]. 较为典型的为Wang[15, 16]以及Zhou[18, 20, 21]课题组, 他们使用钌及其氧化物作为空气电极催化剂使电池的充放电效率得到大幅度的提升, 为锂-空气二次电池的商业化应用奠定了基础. (2)锂-空气二次电池的电极稳定性, 包括物理稳定性以及化学稳定性等仍有待提升[22]. Bruce课题组[23]发现, 目前广泛使用的碳材料作为锂-空气二次电池正极材料并不稳定, 在电压高于3.5 V时会发生分解, 且碳为疏水性质时分解更为严重; 另外, IBM实验室[24]同样证明了电池放电产物Li2O2会和碳材料反应在其界面生成Li2CO3, 造成电极腐蚀; Nazar课题组[25]发现, 制备空气正极广泛使用的有机粘结剂PVDF在电池反应过程中会发生分解, 使电池内部副反应加剧, 极大地影响电池的电化学性能. 电极材料的不稳定以及粘结剂的分解会造成电极的化学不稳定性. 另外, 粘结剂的分解同样会造成电极结构坍塌, 电极结构的物理稳定性变差, 不利于电池反应的传质, 同样影响电池的电化学性能. 为解决上述问题, 一系列关于电极材料的开发以及电极结构的设计等方面的工作也相继开展起来. 其中包括使用非碳空气电极[21, 22, 26, 27]、构筑自支撑结构电极等[28], 虽然这些方法在一定程度上提高了电极的稳定性, 但电极对电池的作用机制以及电极与电池之间的构效关系还有待进一步研究. (3)由于锂-空气二次电池在一个开放的体系中运行, 空气中的H2O和CO2进入电池内部与金属锂负极发生反应, 造成负极腐蚀粉化. Shui等[29]通过同步辐射X光衍射和三维显微成像技术对锂片在电池循环过程中的变化进行了分析, 发现在电池循环过程中锂片表面有副产物LiOH生成, 并且随着电池的运行, LiOH在锂片的比重逐渐增加, 直到金属锂被完全消耗掉. 金属锂负极的腐蚀与粉化将会严重影响电池内部的离子导电性与电子导电性. 近些年在锂-空气二次电池负极的研究中, 通过对锂负极表面进行修饰[30]、使用合适的电解质[31]以及用含锂化合物进行取代[32]等方式来减缓负极所带来的不利影响, 但这些方法还不能从根本上解决这一问题, 需要开拓新的思路以及开发具有高比容量且电位较低的金属锂合金可能会很好的 解决该问题. (4)锂-空气二次电池还处于研发初级阶段, 研究人员更多的是关注电极材料对电池容量以及能量的贡献, 很少考虑电池作为一个整体对电池性能的影响以及将来电池如何商业化应用等问题. 针对以上问题并结合本课题组所做的工作, 在这里以我们所研究的成果为主线, 系统的对空气正极材料的开发以及结构设计、负极的修饰保护和柔性电池的组装等进行阐述, 并对该领域的未来发展趋势进行介绍, 以期能较好的说明锂-空气二次电池电极材料的设计与合成规律, 并清晰的展示我们的工作思路和研究成果.
2 空气正极材料的开发与结构设计
空气正极材料包括基底材料与催化剂材料, 基于锂空气电池的作用机理, 空气正极基底材料一般具有优良的导电性与良好的稳定性, 由于具有优良的导电性和一定的催化活性, 商业碳材料作为基底材料在锂空气电池领域得到广泛的应用, 如KB碳和Super P, Vulcan carbon等可直接用作锂空电池的正极基底材料[33~35]. 此外, 还有各种具有丰富微观结构的碳材料, 如石墨烯、碳纳米管、碳纳米纤维、碳纳米球壳等[36~39]. 由于它们具有良好的孔径结构以及较高的比表面积, 增强了电池反应物的传质促进反应的动力学过程; 优良的孔径结构以及高比表面积为放电产物Li2O2的沉积提供了存储空间, 从而提高了电池的充放电容量. 所以设计合理的孔道结构以及提高材料比表面积是碳材料设计中的一个重要出发点[22, 39]. 此外, 为了进一步提高碳材料的催化活性, 负载和掺杂对ORR或OER有良好催化活性的催化剂是一种非常有效的途径. 同时, 还有两个不容忽视的问题就是如上所述的碳正极不稳定和有机粘结剂分解, 开发和构筑非碳自支撑空气正极将会很好解决这一问题. 为此, 我们展开了电极孔道设计、高效催化剂的开发以及非碳自支撑空气正极的构筑等一系列的工作.
2.1 碳材料的孔径设计
在锂-空电池反应中通常认为正极材料孔径的大小分布在2~50 nm左右较为合适, 此外孔径结构还需要有一定的稳定性, 如果没有良好机械强度, 在充放电过程中, 孔道结构便很容易被破坏, 导致不可逆的崩塌[40]. 基于上面的设计要点, 我们课题组在控制碳材料孔道方面主要开展了两项工作.
首先, 我们使用氧化石墨烯凝胶作为碳源, 采取简单的溶胶凝胶法, 将分级多孔碳材料直接生长在泡沫镍上, 得到自支撑结构的氧化石墨烯空气正极[41], 如图 1a. 在反应中, 氧化石墨烯不仅是一个碳源, 同时也为凝胶的3D结构提供了框架. 从电镜图片可以看出, 我们所制得的这种分级多孔碳材料中含有10 nm左右的介孔和20到100 nm左右的中孔和大孔结构, 介孔为催化反应提供催化位点, 而中孔和大孔则为放电产物的沉积以及电池反应物的传质提供了空间. 当将其直接作为锂-空气二次电池空气正极时, 得到了令人满意的电化学性能. 在电流密度为0.2 mA·cm-2时, 电池容量可达11060 mAh·g-1; 即使在电流密度2 mA·cm-2时, 电池依然有超过2000 mAh·g-1的放电容量(图 1b). 在该工作的基础上, 我们采用SiO2模板方法得到相互连通的均匀碳球壳[39], 如图 1c. 在这里我们可以根据放电产物的形态调控碳球壳的大小, 缓解电极的体积效应; 另外, 从图中可以看出, 碳球壳之间是相互连通的, 这为反应物的传质提供了传输通道, 电池的容量、倍率性能以及循环稳定性等都得到较大的提升. 此外, 通过贵金属Pd的修饰, 使电池的电化学性能又得到了进一步的提升, 电池在限制容量为1000 mAh·g-1的情况下稳定循环超过200次(图 1d). 催化剂对电池性能的影响以及作用机制后面内容会进行介绍, 这里我们主要关注碳电极在结构和孔道上的设计.
 图 1
(a)石墨烯空气电极的SEM图像, (b)石墨烯空气电极的倍率性能, (c)碳球壳空气电极的SEM图像和(d)碳球壳空气电极的循环性能[41, 39]
Figure 1.
(a) SEM image of the graphene electrode, (b) rate performance of the graphene electrode, (c) SEM image of the hollow spherical carbon electrode and (d) cycling performance of the hollow spherical carbon electrode[41, 39]
图 1
(a)石墨烯空气电极的SEM图像, (b)石墨烯空气电极的倍率性能, (c)碳球壳空气电极的SEM图像和(d)碳球壳空气电极的循环性能[41, 39]
Figure 1.
(a) SEM image of the graphene electrode, (b) rate performance of the graphene electrode, (c) SEM image of the hollow spherical carbon electrode and (d) cycling performance of the hollow spherical carbon electrode[41, 39]
2.2 催化剂在碳材料上的负载
碳材料本身对ORR及OER的催化效果有限, 导致充放电电位在很大程度上偏离平衡时的理论电位值(2.96 V), 极大地降低了电池的充放电效率, 这一问题严重制约了锂空气电池的发展. 催化剂的加入会在很大程度上缓解这一难题, 目前锂-空气二次电池广泛使用的催化剂包括金属氧化物、金属氮化物、贵金属氧化物以及贵金属合金等[4~14]. 我们课题组主要研究了过渡金属氧化物(MnO2、Co3O4)[42~46]以及钙钛矿结构的复合氧化物LaFeO3 (LFO)[47]和La0.75Sr0.25MnO3 (LSMO)[48], 在这里我们重点对钙钛矿结构氧化物以及过渡金属氧化物Co3O4进行介绍.
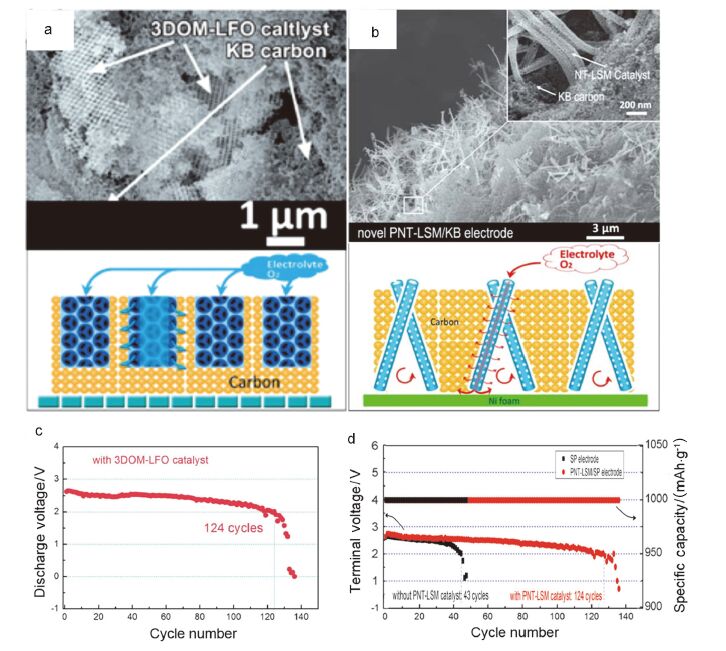
首先, 我们分别采用模板法和静电纺丝方法分别合成了反蛋白石结构的LFO以及中空多孔纳米管结构的LSMO[47, 48]. 催化剂的加入一方面提高电池的反应动力学, 另一方面对电极的结构也进行调控. 图 2a和2b分别为商业KB碳电极加入LFO和LSMO扫描电镜图片, 从图中可以看出, 相比纯碳电极催化剂的加入使电极结构变的较为“疏松”, 这些“疏松”的孔道为电池反应
提供了空间, 促进传质, 同时也缓解了由电池放电产物所产生的体积效应, 对提高电池的循环稳定性有利. 图 2c和2d分别为电极加入LFO和LSMO催化剂后电池的循环性能图, 可以看出相比纯商业碳材料, 电池的循环稳定性都得到大幅度的提升. 循环性能的提升一方面得益于催化剂本身对电极的催化活性, 另一方面也源自催化剂对电极结构的调控.
如上所述, 催化剂的加入一方面促进了电池反应动力学, 提高了电池充放电效率; 另一方面也对电极的结构进行了调控, 缓解了放电产物的体积效应, 有利于传质促进了循环. 所合成的催化剂虽然在很大程度上提高了电池的电化学性能, 但是催化剂对电池的作用机制还需进一步研究. 基于此问题, 我们采用简单的水热-热处理方法合成了高比表面积且具有海胆形貌的Co3O4纳米线 (Co3O4 NWs)[45]. 在这里不仅研究了其对电池反应的动力学以及对电极结构的调控, 更研究了催化剂对电池放电产物形态的影响. 从该工作可以看出, 电极加入催化剂之后, 在同等电流以及放电容量的情况下, 电池放电产物Li2O2的尺寸明显变小, 而小尺寸Li2O2一方面缓解了电极的体积效应, 对提高电池的循环稳定性有利; 另一方面, 小尺寸Li2O2有利于电子传输, 对电池充电有利[49]. 在此基础上, 我们也研究了催化剂对放电产物结晶性的影响, 发现Li2O2在加入催化剂电极上的结晶性要明显弱于使用纯Super P电极, 文献已经报道, 弱结晶性或者非晶态Li2O2在充电过程中更容易分解, 对提高电池充放电效率是有利的[50, 51]. 关于催化剂是如何诱导放电产物生成弱结晶态或者非结晶态这一现象还有待进一步研究. 得益于以上优势, 催化剂的加入使得电池的电化学性能得到很大的提升.
2.3 非碳材料正极的开发和应用
上述一系列工作虽然在很大程度上提高了电池的放电容量、充放电效率、倍率性能以及循环稳定性等电化学性能, 但上述体系还是基于碳基活性材料展开的研究, 上面也已经提到, 碳材料在锂-空气二次电池体系中是不稳定的, 一方面在高电位下自身会发生分解, 另外碳自身会和Li2O2发生反应生成碳酸盐[23, 24], 这一系列的副反应会恶化电池的电化学性能, 使电池过早失效. 如何利用碳优良导电性这一优点同时又避免或者减缓碳分解这一问题呢? 基于此, 我们开展了一系列碳基底材料的复合改性方面的工作, 这里重点介绍两项工作.
首先, 我们采用电化学沉积的方法将Co3O4纳米片 (Co3O4 NSs)电沉积到导电性良好的碳布(CT)基底上, 然后再采用浸渍方法将Ru纳米颗粒修饰在表面得到Co3O4 NSs/Ru空气电极[46]. 图 3a和3b分别为CT基底在包覆前以及包覆后的扫描电镜图片, 图 3c为3b的放大图. 从图中可以看出, Co3O4 NSs/Ru包覆后在很大程度上避免了碳纤维的裸露, 由于该电极的主要活性物质和催化剂为Co3O4 NSs(或者Co3O4 NSs/Ru), 减缓了由碳带来的一系列副反应, 对提高电极的稳定性有利; 另外由于活性物质和催化剂为具有较高活性的Co3O4 NSs(或者Co3O4 NSs/Ru), 对电极的电化学性能的提升也是有利的. 为了验证该电极的电化学性能, 我们分别将CT和Co3O4 NSs/Ru作为空气电极组装电池测试它们的电化学性能. 从图 3d和3e可以看到电池使用Co3O4NSs/Ru电极无论在电池充放电效率还是循环稳定性等方面都远优于使用CT电极的电池; 此外, 使用Co3O4 NSs/Ru电极的电池也有较好倍率性能, 即使在电流为1000 mA·g-1的情况下首次放电依然有将近2000 mAh· g-1的容量.
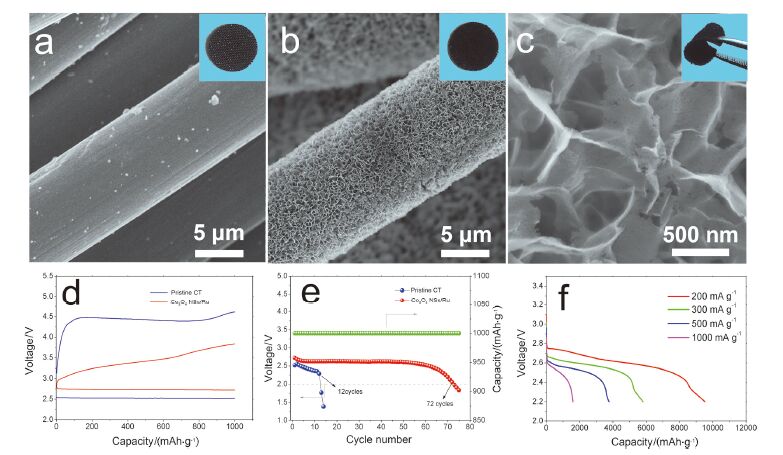 图 3
(a) CT电极的SEM图像, (b, c) Co3O4 NSs/Ru电极的SEM图像, (d)电池使用不同电极的在限制容量1000 mAh·g-1时首次充放电曲线, (e)电池使用不同电极在限制容量1000 mAh·g-1时的循环性能和(f)电池使用Co3O4 NSs/Ru电极的倍率性能[46]
Figure 3.
(a) SEM image of the CT cathode, (b, c) SEM image of the Co3O4 NSs/Ru cathode, (d) first discharge-charge curves of Li-O2 cells with two different cathodes, (e) cycling performance of Li-O2 cells with two different cathodes and (f) rate performance of Li-O2 cells with Co3O4 NSs/Ru cathode[46]
图 3
(a) CT电极的SEM图像, (b, c) Co3O4 NSs/Ru电极的SEM图像, (d)电池使用不同电极的在限制容量1000 mAh·g-1时首次充放电曲线, (e)电池使用不同电极在限制容量1000 mAh·g-1时的循环性能和(f)电池使用Co3O4 NSs/Ru电极的倍率性能[46]
Figure 3.
(a) SEM image of the CT cathode, (b, c) SEM image of the Co3O4 NSs/Ru cathode, (d) first discharge-charge curves of Li-O2 cells with two different cathodes, (e) cycling performance of Li-O2 cells with two different cathodes and (f) rate performance of Li-O2 cells with Co3O4 NSs/Ru cathode[46]
为了进一步对非碳空气电极进行研究, 我们采用简单的水热-热处理的方法将TiO2 纳米棒阵列(TiO2 NAs)均匀的包覆在CT表面得到TiO2 NAs/CT电极[52], 合成示意图如图 4a所示. 图 4b和4c为不同放大倍率下的TiO2 NAs/CT电极形貌图片, 可以看出, 碳纤维布表面被一层TiO2 NAs均匀覆盖, TiO2纳米棒垂直生长CT表面且纳米棒之间的空隙为电池反应提供了足够的空间, 在循环过程中对电极结构的稳定性有利. 在这里我们对碳纤维多层包覆的目的一方面是提高活性物质TiO2的载量, 另外一个重要原因是对CT进行包覆, 减缓或者避免在电池反应过程中碳的分解. 为了验证TiO2 NAs对CT的包覆程度我们对TiO2 NAs/CT电极做了Raman分析, 如图 4d, 从图谱上我们可以明显的看到TiO2的特征峰, 而碳的特征峰D峰(1336 cm-1)与G峰(1597 cm-1)几乎消失[53], 说明TiO2 NAs对CT有一个很好的覆盖. 为了进一步验证使用该电极对电池副反应的抑制效果, 我们采用气相色谱(GC)对电池使用不同电极(TiO2 NAs/CT电极和CT电极)充电所产生的气体进行分析. 由于首次放电的主要产物为Li2O2, 所以在后续的充电过程中电池释放出来的气体主要为氧气(图 4e); 同样我们也对电池使用不同电极在充电过程中所产生的CO2气体进行了检测, 从图 4f中可以明显的看出使用CT电极在充电过程中产生的CO2气体明显多于使用TiO2 NAs/CT电极的电池(图 4f). 此外, 我们也对氧气及二氧化碳等气体做了标准校正曲线, 定量的对电池在充电过程中所释放出来的氧气和二氧化碳进行了分析计算. 基于以上优势, 使用TiO2 NAs/CT电极的电池获得了高达356次的循环寿命(图 4g). 一个意外的收获是, 由于正极活性物质为耐酸碱性良好的TiO2, 而电池在充放电过程中所产生的主要副产物为碳酸盐和羧酸盐, 这些都是易溶于酸的物质, 我们把多次循环后的正极取出, 经过简单的酸洗除去其表面的副产物的沉积物后, 发现正极又可进行重复使用, 其结构没有发生变化, 其作为空气电极的性能也几乎没有改变, 这也为我们提高电极的利用率提供了一个新的思路.
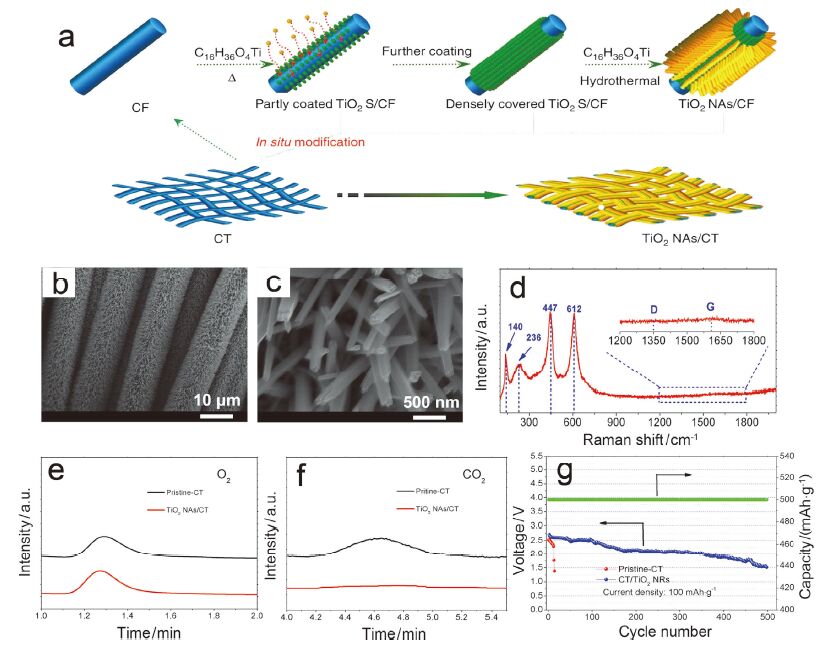 图 4
(a) TiO2 NAs/CT电极的合成示意图, (b, c) TiO2 NAs/CT电极的SEM图像, (d) TiO2 NAs/CT电极的Raman图谱, (e, f)电池使用CT电极TiO2 NAs/CT电极在充电过程中所释放出氧气和二氧化碳气体的GC曲线和(g)电池使用不同电极在限制容量500 mAh·g-1时的循环性能[52]
Figure 4.
(a) Schematic representations for the design and preparation of the TiO2 NAs/CT, (b, c) SEM images of the TiO2 NAs/CT cathode, (d) Raman spectra of the TiO2 NAs/CT cathode, (e, f) GC signals of O2 and CO2 released after charging the Li-air cells with CT and TiO2 NAs/CT cathode and (g) cycling performance of Li-O2 cells with two different cathodes, respectively[52]
图 4
(a) TiO2 NAs/CT电极的合成示意图, (b, c) TiO2 NAs/CT电极的SEM图像, (d) TiO2 NAs/CT电极的Raman图谱, (e, f)电池使用CT电极TiO2 NAs/CT电极在充电过程中所释放出氧气和二氧化碳气体的GC曲线和(g)电池使用不同电极在限制容量500 mAh·g-1时的循环性能[52]
Figure 4.
(a) Schematic representations for the design and preparation of the TiO2 NAs/CT, (b, c) SEM images of the TiO2 NAs/CT cathode, (d) Raman spectra of the TiO2 NAs/CT cathode, (e, f) GC signals of O2 and CO2 released after charging the Li-air cells with CT and TiO2 NAs/CT cathode and (g) cycling performance of Li-O2 cells with two different cathodes, respectively[52]
2.4 自支撑空气正极的开发和应用
如前所述, 在空气正极的制备过程中通常采用的有机粘结剂(PVDF、PTFE等)在电池反应过程中不稳定, 易发生分解[25]. 粘结剂分解产生的副产物对电池的反应不利, 使电池反应更为复杂; 另外, 依靠粘结剂粘合的活性物质会随着粘结剂的分解而坍塌, 对电极的结构稳定性不利[22]. 关于这一类问题, 我们组也开展了相关的研究. 如2.1节中, 采用溶胶凝胶法将氧化石墨烯直接生长在泡沫镍骨架上[41]、采用电泳方法将合成碳球壳模板的SiO2球嵌入碳纸内部[39], 在2.3节中采用电化学沉积和水热等 方法分别将Co3O4 NSs和TiO2 NAs沉积生长到碳纤维布表面等一系列方法获得自支撑电极[44, 46, 52]. 本节针对相关工作的其中三个进行简要介绍: 电沉积法得到的Co3O4 NSs-碳纸(Co3O4 NSs/CP)电极; 电沉积法得到Co3O4 NSs/Ru-碳布(Co3O4 NSs/Ru/CT)电极; 水热-热处理方法得到的TiO2 NAs/CT电极. 在这里我们重点介绍自支撑这一结构对电池性能的影响.
图 5分别为三种电极的电镜图片以及电池的循环性能, 从扫描电镜图中可以看出自支撑结构电极有着共同的特点, 即一维或者二维纳米结构的活性物质均垂直于集流体基底且活性物质之间存在大量孔道, 如2.1节中所述这些孔道可为电池的反应产物提供足够的寄宿空间, 缓解电极的体积效应, 另外这些孔道为电池反应物的传输提供足够多的通道, 有利于传质. 作为自支撑结构的空气电极, 在其制作过程中避免了粘结剂的使用, 也就从根本上避免了使用粘结剂所带来的一系列问题. 另外一个重要的特点就是在自支撑电极结构中, 活性物质和集流体是直接连接的, 有利于电子传输, 对提高电极的导电性有利. 基于以上优势, 使用自支撑电极的电池电化学性能尤其是循环稳定性等得到很大提升(图 5c, 5f, 5i).
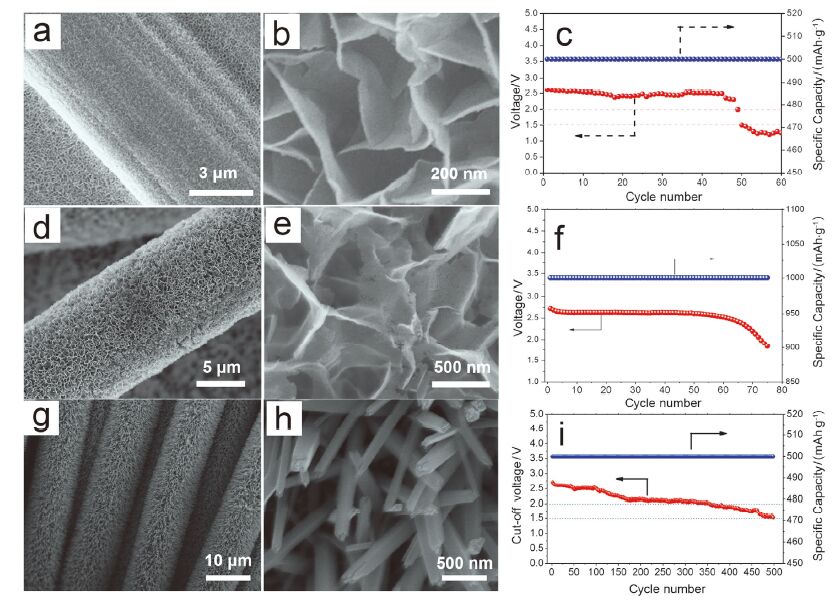 图 5
(a, b) Co3O4 NSs/CP电极的SEM图像, (d, e) Co3O4 NSs/Ru/CT电极的SEM图像, (g, h) TiO2 NAs/CT电极的SEM图像和(c, f, i)电池使用Co3O4 NSs-碳纸电极、Co3O4 NSs/Ru-碳布电极以及TiO2 NAs/CT电极的循环性能[44, 46, 52]
Figure 5.
(a, b) SEM images of the Co3O4 NSs/CP cathode, (d, e) SEM images of the Co3O4 NSs/Ru/CT cathode, (g, h) SEM images of the TiO2 NAs/CT cathode and (c, f, i) cycling performance of Li-O2 cells with three different cathodes, respectively[44, 46, 52]
图 5
(a, b) Co3O4 NSs/CP电极的SEM图像, (d, e) Co3O4 NSs/Ru/CT电极的SEM图像, (g, h) TiO2 NAs/CT电极的SEM图像和(c, f, i)电池使用Co3O4 NSs-碳纸电极、Co3O4 NSs/Ru-碳布电极以及TiO2 NAs/CT电极的循环性能[44, 46, 52]
Figure 5.
(a, b) SEM images of the Co3O4 NSs/CP cathode, (d, e) SEM images of the Co3O4 NSs/Ru/CT cathode, (g, h) SEM images of the TiO2 NAs/CT cathode and (c, f, i) cycling performance of Li-O2 cells with three different cathodes, respectively[44, 46, 52]
3 金属锂负极的保护
在锂-空气二次电池的研究中, 负极的开发与保护也是至关重要的. 在负极材料中, 金属锂具有较高的比能量(3860 mAh·g-1)以及较低的电位值(-3.04 V vs. SHE), 是所有材料中最适合做锂-空气二次电池负极的材料. 但正如上面所介绍的, 金属锂作为锂-空气二次电池负极较以往锂离子电池有着更大的挑战, 不仅要考虑电池内部副反应对其的影响, 还要考虑外部环境如CO2、水蒸汽等对其的腐蚀. 针对这一问题, 我们采用电化学方法预先在金属锂片表面沉积SEI膜[54], 这里用的成膜剂为锂离子电池常用的氟代碳酸乙烯酯(FEC)[55]. 实验证明这种方法能很有效地对负极锂片进行保护.
图 6a和6b分别为锂片表面成膜的示意图以及机理图[56]. 根据FEC本身的物理化学性质并结合分析结果, 推测出锂片表面膜的成分主要为Li2CO3, LiF, 多烯和C-F化合物等. 为了验证锂片表面预先成膜处理之后对电池性能的影响, 我们分别对纯锂片(PLM)和经FEC处理的锂片(F-TLM)的腐蚀情况进行追踪观察, 并将它们作为锂-空气二次电池负极进行循环测试. 首先对PLM和F-TLM在作为负极之前进行形貌观察, 可以看出, 经过电化学处理之后F-TLM表面( 图6f)要明显比PLM表面平整(图 6c). 为了追踪锂片的腐蚀状况并尽可能地避免正极以及电解液对其的影响, 采用定期更换正极和电解液的方法[29], 该工作采用每循环10次进行一次正极和电解液的更换. 图 6d和6g分别为电池循环60次(正极和电解液更换5次)后PLM和F-TLM的扫描电镜图片, 虽然F-TLM在所难免的有一定的腐蚀, 但是相比PLM其腐蚀情况要减缓很多, 说明预先在锂片表面形成的一层保护膜有效的减缓了电池内部成分以及外界CO2、水蒸汽等对其的腐蚀. 对电池使用PLM和F-TLM作为负极进行电池循环测试, 发现经过预先处理的负极在限制容量为1000 mAh·g-1的情况下能稳定循环超过100次(图 6h), 远大于使用PLM电极的31次(图 6e).
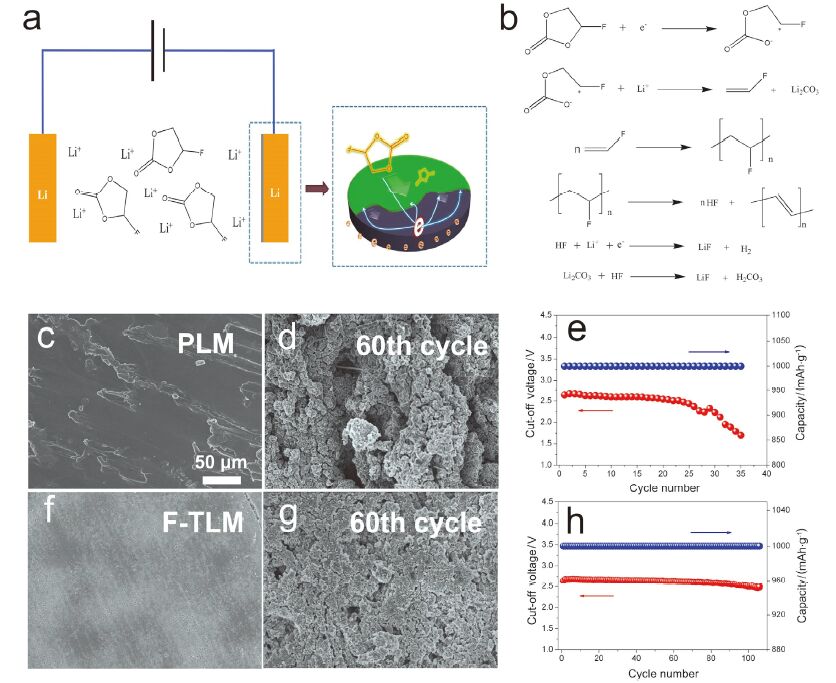 图 6
(a, b) F-TLM负极的合成示意图以及机理图, (c, d) PLM电极原始形貌以及循环60次后的形貌图片, (f, g) F-TLM电极原始形貌以及循环60次后的形貌图片和(e, h)电池使用PLM和F-TLM电极的循环性能[54]
Figure 6.
(a, b) Schematic illustration and mechanism of the formation of F-TLM anode, (c, d) SEM images of the pristine and 60th cycle of PLM anode, (f, g) SEM images of the pristine and 60th cycle of F-TLM anode and (e, h) cycling performance of Li-O2 cells with PLM and F-TLM anode, respectively[54]
图 6
(a, b) F-TLM负极的合成示意图以及机理图, (c, d) PLM电极原始形貌以及循环60次后的形貌图片, (f, g) F-TLM电极原始形貌以及循环60次后的形貌图片和(e, h)电池使用PLM和F-TLM电极的循环性能[54]
Figure 6.
(a, b) Schematic illustration and mechanism of the formation of F-TLM anode, (c, d) SEM images of the pristine and 60th cycle of PLM anode, (f, g) SEM images of the pristine and 60th cycle of F-TLM anode and (e, h) cycling performance of Li-O2 cells with PLM and F-TLM anode, respectively[54]
4 新型锂空气电池的设计与组装
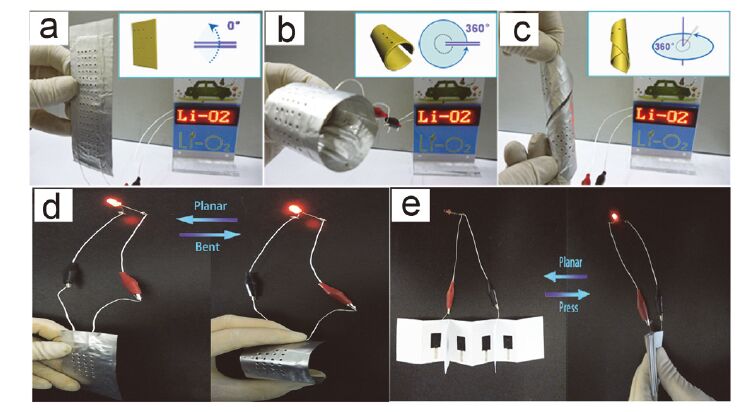
如上所述, 锂-空气二次电池还处于发展的初期, 对其的研究还是基于扣式电池和模具电池, 这些组装方式均用到笨重的不锈钢外包装, 这在很大程度上牺牲了电池的能量密度. 如何实现锂-空气二次电池高能量密度以及如何将其广泛应用, 是我们研究锂-空气二次电池必须要面临的一个问题. 针对这一问题, 结合锂离子电池的相关经验, 课题组也尝试开展了一系列关于开发柔性锂-空气二次电池的工作. 首先我们组装了最常见的二维平面柔性锂-空气二次电池[52, 57], 如图 7. 作为柔性锂-空气二次电池, 其抗弯曲 以及抗扭转能力也是要考虑的, 如图 7a~7c我们将组装的柔性电池进行弯曲和扭转测试, 发现电池在受弯折和扭曲的情况下对其电化学性能几乎没有影响. 另外, 在组装平面柔性锂-空气二次电池方面, 受中国书法启发, 我们制备出柔性纸质电极[57], 并用其组装了柔性锂-空气二次电池如图 7d, 这种电池仍然展现出了良好的耐弯折性能. 值得注意的是, 我们采用纸电极成功组装了纸电池组(四电池并联), 在该电池中, 电池集流体、隔膜以及外包装全部采用纸(图 7e), 无论在质量能量密度还是在体积能量密度上都较传统锂-空气二次电池有较大的提升, 这也为我们开发新型空气电极以及组装柔性锂-空气二次电池提供了新的思路.
为使柔性锂-空气二次电池用途更为广泛, 在上述工作基础上, 对柔性锂-空气二次电池的组装进行了改进, 组装了一维线性锂-空气二次电池[58], 如图 8. 同样对组装的线性锂-空气二次电池进行弯曲和扭曲测试, 发现在各种情况下电池都能正常运行(图 8a), 且电池的放电容量几乎没有变化(图 8b). 为了检测电池抗弯折疲劳能力, 将电池分别弯折1000、2000、3000、4000次后进行充放电测试, 其充放电过电位也几乎没有变化(图 8c).
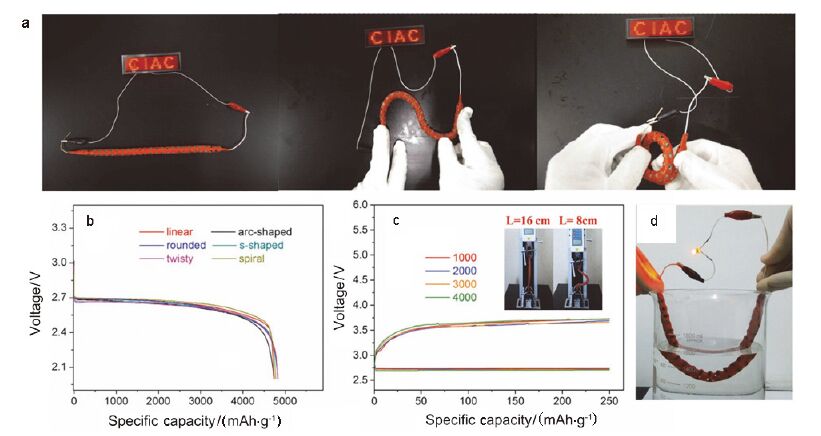 图 8
(a)线性锂空气电池在不同弯曲和扭曲情况下正常工作, (b)线性锂空气电池在不同弯曲和扭曲情况下的放电容量, (c)线性锂空气电池在弯曲不同次数之后充放电曲线和(d)线性锂空气电池在水中正常工作[58]
Figure 8.
(a) Cable-type Li-O2 batteries work normally under different bending and twisting conditions, (b) discharge capacity of cable-type Li-O2 batteries with different bending and twisting conditions, (c) discharge-charge curves of cable-type Li-O2 batteries after a certain cycles and (d) cable-type Li-O2 battery work normally immersed in water[58]
图 8
(a)线性锂空气电池在不同弯曲和扭曲情况下正常工作, (b)线性锂空气电池在不同弯曲和扭曲情况下的放电容量, (c)线性锂空气电池在弯曲不同次数之后充放电曲线和(d)线性锂空气电池在水中正常工作[58]
Figure 8.
(a) Cable-type Li-O2 batteries work normally under different bending and twisting conditions, (b) discharge capacity of cable-type Li-O2 batteries with different bending and twisting conditions, (c) discharge-charge curves of cable-type Li-O2 batteries after a certain cycles and (d) cable-type Li-O2 battery work normally immersed in water[58]
较以往电池不同的是, 在该线性柔性锂-空气二次电池的组装中采用了聚合物凝胶电解质, 这种电解质有很好的疏水性质, 且该电解质采用原位的合成方法直接在锂负极表面合成, 对锂负极有很好的包覆, 在很大程度上避免了空气或者电池反应过程中水对负极的腐蚀, 为此我们做了电池的浸水实验, 如图 8d, 发现电池依然能够安全稳定的工作, 这对提高电池的安全性有着重大意义.
5 总结与展望
本文主要对课题组近年来在锂-空气二次电池电极材料领域的研究成果进行了较为科学和清晰的归纳介绍. 从构效关系角度展现了锂-空气二次电池电极材料的多种物理化学性能与结构设计之间的关系, 通过一系列研究成果介绍阐明了课题组的研究思路, 同时又为锂-空气二次电池电极材料的选择、设计与应用提供了许多新颖的想法.
当然, 锂-空气二次电池的发展还处于基础研究阶段, 包括正极材料的结构与设计、负极的保护以及电池结构的设计等一系列科学和技术上的问题亟待解决:
(1) 开发多孔、高效、稳定且与电解液相匹配的空气电极来提高电池的催化性能及充放电效率. 由于碳材料的不稳定性, 开发轻质、多孔、稳定且具有良好导电性及优良的催化活性的金属或者合金作为正极材料来提高电极的结构稳定性及化学稳定性, 当然, 在电极表面可以进一步沉积少量贵金属来提高电极的导电性及催化活性, 从而提高电池整体的电化学性能.
(2) 在负极锂片表面原位合成具有高稳定性的聚合物电解质膜, 减缓空气或者电解液中的水分及二氧化碳对锂片的腐蚀, 从而提高锂片的利用率以及电池的循环寿命; 但是开发高容量、低电位的锂合金或者化合物可能是解决负极的最终方案.
(3) 开发和组装新型结构的锂-空气二次电池来提高电池整体的能量密度, 为其商业化应用提供参考. 在这里要从电池的结构、外包装材料以及电芯材料进行综合考虑, 在不影响电池性能的情况下, 减少或者避免过多电池部件的使用. 当然为了更广泛的拓展其在各个领域中的应用, 开发和组装各种类型以及柔性锂-空气二次电池也是该领域发展的一个重要方向.
除了电极材料的影响, 电解液的选择、电解液添加剂等因素对锂-空气二次电池性能也有十分重要的影响[59, 60]. 尤其是近年来出现的采用加入正极液相催化剂的方法, 即通过添加微量可溶于正极体系的物质, 如TTF, LiI, FePc, TEMPO, DBBQ等[61~65], 使其作为氧化还原中间体或产物Li2O2成核及生长的形貌调控剂, 来改变反应过程和反应位点, 从而极大地提升了电池整体的电化学性能. 这种新方法的出现, 为锂-空气二次电池的改良开辟了一种全新的途径, 受到越来越广泛的关注. 同时不可否认的是, 电极材料本身作为电池反应发生的场所和电池的重要组成部分, 其性能的提升和深入的研究仍然在锂-空气二次电池研究中占有重要一席. 我们相信, 开发更为稳定、高效的电极与更适宜的液相添加剂是锂-空气二次电池商业化应用的重要前提.
-
-
[1]
Bruce, P. G.; Freunberger, S. A.; Hardwick, L. J.; Tarascon, J. M. Nat. Mater. 2012, 11, 19.
-
[2]
Luntz, A. C.; Mccloskey, B. D. Chem. Rev. 2014, 114, 11721.
-
[3]
Wang, Z. L.; Xu, D.; Xu, J. J.; Zhang, X. B. Chem. Soc. Rev. 2013, 43, 7746.
-
[4]
Cheng, F.-Y.; Chen, J. Acta Chim. Sinica 2013, 71, 473. (程方益, 陈军, 化学学报, 2013, 71, 473.)
-
[5]
Ryu, W. H.; Yoon, T. H.; Song, S. H.; Jeon, S.; Park, Y. J.; Kim, I. D. Nano Lett. 2013, 13, 4190. doi: 10.1021/nl401868q
-
[6]
Oh, S. H.; Black, R.; Pomerantseva, E.; Lee, J. H.; Nazar, L. F. Nat. Chem. 2012, 4, 1004. doi: 10.1021/nl401868q
-
[7]
Zhao, Y. L.; Xu, L.; Mai, L. Q.; Han, C. H.; An, Q. Y.; Xu, X.; Liu, X.; Zhang, Q. J. Proc. Natl. Acad. Sci. USA 2012, 109, 19569. doi: 10.1073/pnas.1210315109
-
[8]
Zhang, Z. A.; Zhou, G.; Chen, W.; Lai, Y. Q.; Li, J. ECS Electrochem. Lett. 2014, 3, A8.
-
[9]
Cao, Y.; Wei, Z. K.; He, J.; Zang, J.; Zhang, Q.; Zheng, M. S.; Dong, Q. F. Energy Environ. Sci. 2012, 5,9765. doi: 10.1039/c2ee23475k
-
[10]
Li, F. J.; Ohnishi, R.; Yamada, Y.; Kubota, J.; Domen, K.; Yamada, A.; Zhou, H. S. Chem. Commun. 2013, 49, 1175. doi: 10.1039/c2cc37042e
-
[11]
Dong, S. M.; Chen, X.; Zhang, K. J.; Gu, L.; Zhang, L. X.; Zhou, X. H.; Li, L. F.; Liu, Z. H.; Han, P. X.; Xu, H. X.; Yao, J. H.; Zhang, C. J.; Zhang, X. Y.; Shang, C. Q.; Cui, G. L.; Chen, L. Q. Chem. Commun. 2011, 47, 11291. doi: 10.1039/c1cc14427h
-
[12]
Mccloskey, B. D.; Scheffler, R.; Speidel, A.; Bethune, D. S.; Shelby, R. M.; Luntz, A. C. J. Am. Chem. Soc. 2011, 133, 18038. doi: 10.1021/ja207229n
-
[13]
Lu, Y. C.; Gasteiger, H. A.; Yang, S. H. J. Am. Chem. Soc. 2011, 133, 19048. doi: 10.1021/ja208608s
-
[14]
Yu, X. W.; Ye, S. Y. J. Power Sources 2007, 172, 133. doi: 10.1016/j.jpowsour.2007.07.049
-
[15]
Sun, B.; Munroe, P.; Wang, G. X. Sci. Rep. 2013, 3, 2247.
-
[16]
Sun, B.; Chen, S.; Liu, H.; Wang, G. Adv. Funct. Mater. 2015, 25, 4436. doi: 10.1002/adfm.v25.28
-
[17]
Jung, H. G.; Jeong, Y. S.; Park, J. B.; Sun, Y. K.; Scrosati, B.; Lee, Y. J. ACS Nano 2013, 7, 3532. doi: 10.1021/nn400477d
-
[18]
Li, F. J.; Chen, Y.; Tang, D. M.; Jian, Z. L.; Liu, C.; Golberg, D.; Yamada; Zhou, H. S. Energy Environ. Sci. 2014, 7, 1648. doi: 10.1039/c3ee44043e
-
[19]
Yilmaz, E.; Yogi, C.; Yamanaka, K.; Ohta, T.; Byon, H. R. Nano Lett. 2013, 13, 4679. doi: 10.1021/nl4020952
-
[20]
Li, F. J.; Tang, D. M.; Chen, Y.; Golberg, D.; Kitaura, H.; Zhang, T.; Yamada, A.; Zhou, H. S. Nano Lett. 2013, 13, 4702. doi: 10.1021/nl402213h
-
[21]
Jian, Z. L.; Liu, P.; Li, F. J.; He, P.; Guo, X. W.; Chen, M. W.; Zhou, H. S. Angew. Chem., Int. Ed. 2014, 53, 442. doi: 10.1002/anie.v53.2
-
[22]
Chang, Z. W.; Xu, J. J.; Liu, Q. C.; Li, L.; Zhang, X. B. Adv. Energy Mater. 2015, 22, 1500633.
-
[23]
Thotiyl, M. M. O.; Freunberger, S. A.; Peng, Z. Q.; Bruce, P. G. J. Am. Chem. Soc. 2013, 135, 494. doi: 10.1021/ja310258x
-
[24]
Mccloskey, B. D.; Speidel, A.; Scheffler, R.; Miller, D. C.; Viswanathan, V.; Hummelshoj, J. S.; Norskov, J. K.; Luntz, A. C. J. Phys. Chem. Lett. 2012, 3, 997. doi: 10.1021/jz300243r
-
[25]
Black, R.; Oh, S. H.; Lee, J. H.; Yim, T.; Adams, B.; Nazar, L. F. J. Am. Chem. Soc. 2012, 134, 2902. doi: 10.1021/ja2111543
-
[26]
Thotiyl, M. M. O.; Freunberger, S. A.; Peng, Z. Q.; Chen, Y. H.; Liu, Z.; Bruce, P. G. Nat. Mater. 2013, 12, 1049.
-
[27]
Riaz, A.; Jung, K. N.; Chang, W.; Lee, S. B.; Lim, T. H.; Park, S. J.; Song, R. H.; Yoon, S.; Shin, K. H.; Lee, J. W. Chem. Commun. 2013, 49, 5984. doi: 10.1039/c3cc42794c
-
[28]
Cui, Y. M.; Wen, Z. Y.; Liu, Y. Energy Environ. Sci. 2011, 4, 4727.
-
[29]
Shui, J. L.; Okasinski, J. S.; Kenesei, P.; Dobbs, H. A.; Zhao, D.; Almer, J. D.; Liu, D. J. Nat. Commun. 2013, 4, 2255.
-
[30]
Kang, S. J.; Mori, T.; Suk, J.; Kim, D. W.; Kang, Y. K.; Wilcke, W.; Kim, H. C. J. Mater. Chem. A 2014, 2, 9970. doi: 10.1039/c4ta01314j
-
[31]
Walker, W.; Giordani, V.; Uddin, J.; Bryantsev, V. S.; Chase, G. V.; Addison, D. A. J. Am. Chem. Soc. 2013, 135, 2076. doi: 10.1021/ja311518s
-
[32]
Hassoun, J.; Jung, H. G.; Lee, D. J.; Park, J. B.; Amine, K.; Sun, Y. K.; Scrosati, B. Nano Lett. 2012, 12, 5775. doi: 10.1021/nl303087j
-
[33]
Yang, X. H.; He, P.; Xia, Y. Y. Electrochem. Commun. 2009, 11, 1127. doi: 10.1016/j.elecom.2009.03.029
-
[34]
Mirzaeian, M.; Hall, P. J. Electrochim. Acta 2009, 54, 7444. doi: 10.1016/j.electacta.2009.07.079
-
[35]
Nakanishi, S.; Mizuno, F.; Nobuhara, K.; Abe, T.; Iba, H. Carbon 2012, 50, 4794. doi: 10.1021/nl203332e
-
[36]
Xiao, J.; Mei, D. H.; Li, X. L.; Xu, W.; Wang, D. Y.; Graff, G. L.; Bennett, W. D.; Nie, Z. M.; Saraf, L. V.; Aksay, I. A.; Liu, J.; Zhang, J. G. Nano Lett. 2011, 11, 5071.
-
[37]
Lim, H. D.; Park, K. Y.; Song, H.; Jang, E. Y.; Gwon, H.; Kim, J.; Kim, Y. H.; Lima, M. D.; Robles, R. O.; Lepro, X.; Baughman, R. H.; Kang, K. Adv. Mater. 2013, 25, 1348.
-
[38]
Cui, Y. M.; Wen, Z. Y.; Liang, X.; Lu, Y.; Jin, J.; Wu, M. F.; Wu, X.W. Energy Environ. Sci. 2012, 5, 7893. doi: 10.1039/c2ee21638h
-
[39]
Xu, J. J.; Wang, Z. L.; Xu, D.; Zhang, L. L.; Zhang, X. B. Nat. Commun. 2013, 4, 2438.
-
[40]
Shao, Y. Y.; Ding, F.; Xiao, J.; Zhang, J.; Xu, W.; Park, S.; Zhang, J. G.; Wang, Y.; Liu, J. Adv. Funct. Mater. 2013, 23, 987. doi: 10.1002/adfm.v23.8
-
[41]
Wang, Z. L.; Xu, D.; Xu, J. J.; Zhang, L. L.; Zhang, X. B. Adv. Funct. Mater. 2012, 22, 3699. doi: 10.1002/adfm.v22.17
-
[42]
Zhang, L. L.; Zhang, X. B.; Wang, Z. L.; Xu, J. J.; Xu, D.; Wang, L. M. Chem. Commun. 2012, 48, 7598. doi: 10.1039/c2cc33933a
-
[43]
Zhang, L. L.; Wang, Z. L.; Xu, D.; Xu, J. J.; Zhang, X. B.; Wang, L. M. Chin. Sci. Bull. 2012, 57, 4210. doi: 10.1007/s11434-012-5013-6
-
[44]
Liu, Q. C.; Xu, J. J.; Chang, Z. W.; Zhang, X. B. J. Mater. Chem. A 2013, 2, 6081.
-
[45]
Liu, Q. C.; Jiang, Y. S.; Xu, J. J.; Xu, D.; Chang, Z. W.; Yin, Y. B.; Liu, W. Q.; Zhang, X. B. Nano Res. 2015, 8, 576. doi: 10.1007/s12274-014-0689-3
-
[46]
Liu, Q. C.; Xu, J. J.; Chang, Z. W.; Yin, Y. B.; Yang, X. Y.; Liu, T.; Jiang, Y. S.; Yan, J. M.; Zhang, X. B. Part. Part. Syst. Charact. 2016, 33, 500. doi: 10.1002/ppsc.v33.8
-
[47]
Xu, J. J.; Wang, Z. L.; Xu, D.; Meng, F. Z.; Zhang, X. B. Energy Environ. Sci. 2014, 7, 2213. doi: 10.1039/c3ee42934b
-
[48]
Xu, J. J.; Xu, D.; Wang, Z. L.; Wang, H. G.; Zhang, L. L.; Zhang, X. B. Angew. Chem., Int. Ed. 2013, 52, 3887. doi: 10.1002/anie.v52.14
-
[49]
Huang, X.; Yu, H.; Tan, H. T.; Zhu, J. X.; Zhang, W. Y.; Wang, C. Y.; Zhang, J.; Wang, Y. X.; Lv, Y. B.; Zeng, Z.; Liu, D. Y.; Ding, J.; Zhang, Q. C.; Srinivasan, M.; Ajayan, P. M.; Hng, H. H.; Yan, Q. Y. Adv. Funct. Mater. 2014, 24, 6516. doi: 10.1002/adfm.v24.41
-
[50]
Tian, F.; Radin, M. D.; Siegel, D. J. Chem. Mater. 2014, 26, 2952. doi: 10.1021/cm5007372
-
[51]
Geng, W. T.; He, B. L.; Ohno, T. J. Phys. Chem. C 2013, 117, 25222. doi: 10.1021/jp405315k
-
[52]
Liu, Q. C.; Xu, J. J.; Xu, D.; Zhang, X. B. Nat. Commun. 2015, 6, 7892. doi: 10.1038/ncomms8892
-
[53]
Lipomi, D. J.; Tee, B. C. K.; Vosgueritchian, M.; Bao, Z. N. Adv. Mater. 2011, 23, 1771. doi: 10.1002/adma.201004426
-
[54]
Liu, Q. C.; Xu, J. J.; Yuan, S.; Chang, Z. W.; Xu, D.; Yin, Y. B.; Li, L.; Zhong, H. X.; Jiang, Y. S.; Yan, J. M.; Zhang, X. B. Adv. Mater. 2015, 27, 5241. doi: 10.1002/adma.201501490
-
[55]
Cheng, X. L.; Hu, M.; Huang, R.; Jiang, J. S. ACS Appl. Mater. Interfaces 2014, 6, 19176. doi: 10.1021/am504971h
-
[56]
Nakai, H.; Kubota, T.; Kita, A.; Kawashima, A. J. Electrochem. Soc. 2011, 158, A798.
-
[57]
Liu, Q. C.; Li, L.; Xu, J. J.; Chang, Z. W.; Xu, D.; Yin, Y. B.; Yang, X. Y.; Liu, T.; Jiang, Y. S.; Yan, J. M.; Zhang, X. B. Adv. Mater. 2015, 27, 8095. doi: 10.1002/adma.201503025
-
[58]
Liu, T.; Liu, Q. C.; Xu, J. J.; Zhang, X. B. Small 2016, 12, 3101. doi: 10.1002/smll.v12.23
-
[59]
Gu, D.-M.; Wang, Y.; Gu, S.; Zhang, C.-M.; Yang, D.-D. Acta Chim. Sinica 2013, 71, 1354. (顾大明, 王余, 顾硕, 张传明, 杨丹丹, 化学学报, 2013, 71, 1354.)
-
[60]
Jiang, J.; Liu, X.; Zhao, S.; He, P.; Zhou, H. Acta Chim. Sinica 2014, 72, 417. (蒋颉, 刘晓飞, 赵世勇, 何平, 周豪慎, 化学学报, 2014, 72, 417.)
-
[61]
Chen, Y. H.; Freunberger, S. A.; Peng, Z. Q.; Fontaine, O.; Bruce, P. G. Nat. Chem. 2013, 5, 489. doi: 10.1038/nchem.1646
-
[62]
Lim, H. D.; Song, H.; Kim, J.; Gwon, H.; Bae, Y.; Park, K. Y.; Hong, J.; Kim, H.; Kim, T.; Kim, Y. H.; Lepro, X.; Ovalle-robles, R.; Baughman, R. H.; Kang, K. Angew. Chem., Int. Ed. 2014, 53, 3926. doi: 10.1002/anie.201400711
-
[63]
Sun, D.; Shen, Y.; Zhang, W.; Yu, L.; Yi, Z. Q.; Yin, W.; Wang, D.; Huang, Y. H.; Wang, J.; Wang, D. L.; Goodenough, J. B. J. Am. Chem. Soc. 2014, 136, 8941. doi: 10.1021/ja501877e
-
[64]
Bergner, B. J.; Schürmann, A.; Peppler, K.; Garsuch, A.; Janek, J. J. Am. Chem. Soc. 2014, 136, 15054. doi: 10.1021/ja508400m
-
[65]
Gao, X.; Chen, Y.; Johnson, L.; Bruce, P. G. Nat. Mater. 2016, 15, 882. doi: 10.1038/nmat4629
-
[1]
-
图 1 (a)石墨烯空气电极的SEM图像, (b)石墨烯空气电极的倍率性能, (c)碳球壳空气电极的SEM图像和(d)碳球壳空气电极的循环性能[41, 39]
Figure 1 (a) SEM image of the graphene electrode, (b) rate performance of the graphene electrode, (c) SEM image of the hollow spherical carbon electrode and (d) cycling performance of the hollow spherical carbon electrode[41, 39]
图 3 (a) CT电极的SEM图像, (b, c) Co3O4 NSs/Ru电极的SEM图像, (d)电池使用不同电极的在限制容量1000 mAh·g-1时首次充放电曲线, (e)电池使用不同电极在限制容量1000 mAh·g-1时的循环性能和(f)电池使用Co3O4 NSs/Ru电极的倍率性能[46]
Figure 3 (a) SEM image of the CT cathode, (b, c) SEM image of the Co3O4 NSs/Ru cathode, (d) first discharge-charge curves of Li-O2 cells with two different cathodes, (e) cycling performance of Li-O2 cells with two different cathodes and (f) rate performance of Li-O2 cells with Co3O4 NSs/Ru cathode[46]
图 4 (a) TiO2 NAs/CT电极的合成示意图, (b, c) TiO2 NAs/CT电极的SEM图像, (d) TiO2 NAs/CT电极的Raman图谱, (e, f)电池使用CT电极TiO2 NAs/CT电极在充电过程中所释放出氧气和二氧化碳气体的GC曲线和(g)电池使用不同电极在限制容量500 mAh·g-1时的循环性能[52]
Figure 4 (a) Schematic representations for the design and preparation of the TiO2 NAs/CT, (b, c) SEM images of the TiO2 NAs/CT cathode, (d) Raman spectra of the TiO2 NAs/CT cathode, (e, f) GC signals of O2 and CO2 released after charging the Li-air cells with CT and TiO2 NAs/CT cathode and (g) cycling performance of Li-O2 cells with two different cathodes, respectively[52]
图 5 (a, b) Co3O4 NSs/CP电极的SEM图像, (d, e) Co3O4 NSs/Ru/CT电极的SEM图像, (g, h) TiO2 NAs/CT电极的SEM图像和(c, f, i)电池使用Co3O4 NSs-碳纸电极、Co3O4 NSs/Ru-碳布电极以及TiO2 NAs/CT电极的循环性能[44, 46, 52]
Figure 5 (a, b) SEM images of the Co3O4 NSs/CP cathode, (d, e) SEM images of the Co3O4 NSs/Ru/CT cathode, (g, h) SEM images of the TiO2 NAs/CT cathode and (c, f, i) cycling performance of Li-O2 cells with three different cathodes, respectively[44, 46, 52]
图 6 (a, b) F-TLM负极的合成示意图以及机理图, (c, d) PLM电极原始形貌以及循环60次后的形貌图片, (f, g) F-TLM电极原始形貌以及循环60次后的形貌图片和(e, h)电池使用PLM和F-TLM电极的循环性能[54]
Figure 6 (a, b) Schematic illustration and mechanism of the formation of F-TLM anode, (c, d) SEM images of the pristine and 60th cycle of PLM anode, (f, g) SEM images of the pristine and 60th cycle of F-TLM anode and (e, h) cycling performance of Li-O2 cells with PLM and F-TLM anode, respectively[54]
图 8 (a)线性锂空气电池在不同弯曲和扭曲情况下正常工作, (b)线性锂空气电池在不同弯曲和扭曲情况下的放电容量, (c)线性锂空气电池在弯曲不同次数之后充放电曲线和(d)线性锂空气电池在水中正常工作[58]
Figure 8 (a) Cable-type Li-O2 batteries work normally under different bending and twisting conditions, (b) discharge capacity of cable-type Li-O2 batteries with different bending and twisting conditions, (c) discharge-charge curves of cable-type Li-O2 batteries after a certain cycles and (d) cable-type Li-O2 battery work normally immersed in water[58]
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 23
- 文章访问数: 5773
- HTML全文浏览量: 1232


 下载:
下载:







 下载:
下载:

