 Scheme1.
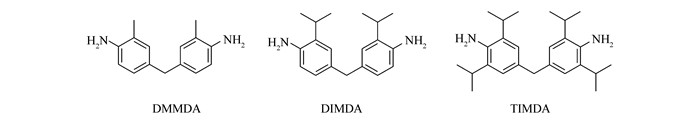
Chemical structures of DMMDA, DIMDA, TIMDA
Scheme1.
Chemical structures of DMMDA, DIMDA, TIMDA

Citation: BI Weihui, MAO Hongchao, ZHANG Suobo. Synthesis, Characterization and Gas Transport Properties of Polynaphthalimides Membranes[J]. Chinese Journal of Applied Chemistry, 2017, 34(11): 1265-1272. doi: 10.11944/j.issn.1000-0518.2017.11.170042

聚萘酰亚胺膜的制备及其气体分离性能
English
Synthesis, Characterization and Gas Transport Properties of Polynaphthalimides Membranes
-
Key words:
- naphthalene dianhydride
- / polynaphthalimides
- / gas separation
- / membrane material
-
气体分离膜技术是当代新型高效气体分离技术, 具有低能耗、操作方便、不污染环境等突出优点,目前已经在天然气纯化、空气分离提纯、燃烧废气中CO2回收及空气除湿等方面得到应用[1]。气体分离膜材料是气体分离膜技术的核心, 其性能会直接影响膜的制备、分离性能和长期使用性能。聚酰亚胺是主链上具有酰亚胺环的一类聚合物,具有良好的热稳定性、机械强度、良好的成膜性及结构的多样性等优点,成为制备气体分离膜的理想材料[2]。通过对现有聚酰亚胺材料的气体分离性能进行分析研究发现,聚酰亚胺自身结构所具有的高刚性、大自由体积的特点是其具有良好气体分离表现的重要保证[3-4]。因此,研究开发具有高刚性的聚酰亚胺膜材料成为气体分离膜研究领域的一个重要研究方向。
含六元环结构的聚萘酰亚胺一般是由商品化的萘二酐与二胺聚合得到的,与含五元环结构的聚酰亚胺相比,具有更为优异的水解稳定性、耐溶剂性能及热稳定性[5-7]。尤其是考虑到自身结构的高刚性,聚萘酰亚胺如果作为膜材料可能具有突出的气体分离性能。然而,目前尚无商品化的聚萘酰亚胺出现,这主要是由于聚萘酰亚胺具有的刚性结构及较强的分子间相互作用,使其在大部分有机溶剂中难以溶解[8]。另外,不同于五元环聚酰亚胺,其聚合过程并不经过易溶的聚酰胺酸阶段,而只能在高温下一步得到聚萘酰亚胺[9-10]。这样,其较差的溶解性往往导致聚萘酰亚胺相对分子质量较低,难以具有较好的机械性能。针对这一问题,人们尝试通过向聚合单体中引入一些特殊的结构来提高聚萘酰亚胺材料的溶解性。Wang等[11]合成一种含酚酞Cardo结构的芳香二胺,通过与萘二酐的聚合得到可溶解的聚萘酰亚胺,表现良好的热稳定性。Hsiao等[12]利用含三氟甲基的二胺与萘二酐聚合,制备了一系列可溶解于有机溶剂的聚萘酰亚胺,明确了三氟甲基基团在改善聚合物溶解性方面的作用。然而,相对于聚酰亚胺在气体分离性能方面的研究,聚萘酰亚胺在该领域的研究却极少[13]。
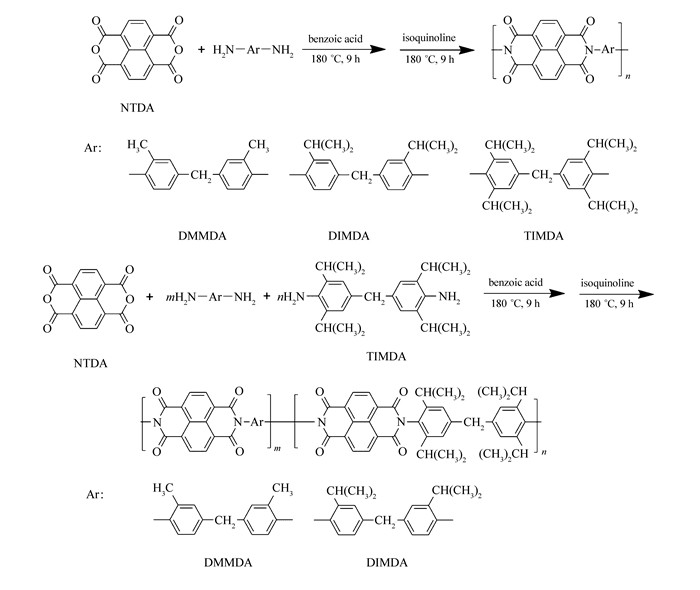
在研究聚酰亚胺的结构与气体分离性能的过程中,发现引入取代基的大小与位置对材料的气体分离性质均有显著的影响[14]。取代基位于二胺邻位即C—N键邻位的聚酰亚胺一般表现较好的气体分离性能。这主要是由于取代基的位阻效应使聚酰亚胺的苯环与酰亚胺环两者不能同处一个平面,从而同时提高了聚酰亚胺的主链刚性和自由体积[15]。由此,我们考虑将这样的邻位取代基引入到聚萘酰亚胺中,一方面,这些在C—N键邻位的取代基可能会破坏聚合物共平面结构,减弱分子间的作用力,从而提高聚萘酰亚胺在有机溶剂中的溶解性[16];另一方面,萘酰亚胺与C—N键邻位的取代基所形成的刚性扭曲结构可能使聚萘酰亚胺具有突出的气体分离表现。基于以上考虑,我们设计并合成了3种邻位具有脂肪族取代基的芳香二胺(Scheme 1),并将其与萘二酐聚合得到了一系列可溶解于有机溶剂的聚萘酰亚胺均聚物及共聚物(Scheme 2)。在此基础上,我们深入讨论了邻位取代基大小、摩尔分数对聚萘酰亚胺的溶解性、热稳定性以及气体分离性能的影响。
1 实验部分
1.1 仪器和试剂
Bruker AV300 MHz或400MHz型核磁谱仪(德国布鲁克公司);Elemental Analyzer MOD-1106型元素分析仪(意大利卡拉尔巴公司);Bio-Rad FTS-80型红外光谱仪(美国伯乐公司);1834型Ubbelohde毛细管粘度计(测试溶液为聚合物的质量分数为0.5%的N-甲基吡咯烷酮溶液, 测试温度(30±0.1) ℃,上海思尔达科学仪器有限公司); Perkin-Elemer TGA-2型热失重分析仪(样品重10~30 mg,升温速率10 ℃/min,美国铂金-埃尔默公司);Instron-1211型静态力学测试仪(拉伸速率5 mm/min,每张膜取3个样品,取3次测试结果的平均值,美国英斯特朗公司); Rheometric Scientific DMTAV型动态热机械性能分析仪(测试样品厚50 μm左右,测试频率1 Hz,恒定拉力,空气中升温速率3 ℃/min,美国流变科技公司);Siemensp44-Circle X型射线衍射仪(铜靶,测试温度25 ℃,德国西门子公司)。
N-甲基吡咯烷酮(NMP)用CaH2干燥8 h, 减压蒸馏,4A分子筛保存。1, 4, 5, 8-萘四甲酸酐(NTDA)从国药集团化学试剂有限公司购买,化学纯,通过高温升华的方法提纯。苯甲酸及异喹啉由北京化工公司提供直接使用。其它的试剂为分析纯,购置于北京化工厂,未经特殊提纯。
1.2 单体的合成
1.2.1 3, 3′-二甲基-4, 4′-亚甲基联苯二胺(DMMDA)
参照文献[17]方法,将邻甲基苯胺(24 g)放入250 mL三口瓶中,在N2气保护下,加入水(34 mL)和浓盐酸(17 mL),而后在30 ℃条件下,搅拌20 min,然后加入DMAP(4-二甲氨基吡啶)(0.16 g)和多聚甲醛(3 g),再继续搅拌30 min后,将体系升温至90 ℃, 反应4 h,停止加热,并冷却至室温,用KOH调节体系的pH值至中性,白色固体析出,过滤白色固体并干燥,再用以乙醇为溶剂对粗产品进行重结晶。熔点154~156 ℃,产率为58%。1H NMR(CDCl3-d6), δ:6.85~6.93(m, 4H),6.63~6.68(d, 2H),3.60~4.0(s, 4H),2.12~2.20(s, 6H)。
1.2.2 3, 3′-二异丙基-4, 4′-亚甲基联苯二胺(DIMDA)
参照文献[17]方法,将邻甲基苯胺(27 g)放入250 mL三口瓶中,在N2气保护下加入水(34 mL)和浓盐酸(17 mL),30 ℃,搅拌20 min,加入DMAP(0.16 g)和多聚甲醛(3 g),搅拌30 min,升温至90 ℃, 反应4 h,停止加热,并冷却至室温,用KOH调节体系的pH值至中性,体系呈粘稠状。向体系中加入水,而后用CH2Cl2萃取,收集有机相用MgSO4干燥。在经过滤后蒸出CH2Cl2得到深红棕色液体。用柱层析法分离粗产品(洗脱剂V(石油醚):V(乙酸乙酯)=6:1)。产品为深红棕色液体,产率44%。1H NMR(CDCl3-d6), δ:6.85~6.87(d, 2H),6.62~6.69(dd, 2H),6.47~6.53(dd, 2H),3.60~4.0(s, 4H),2.86~2.98(m, 2H),1.05~1.15(d, 12H)。
1.2.3 3, 3′, 5, 5′-四异丙基-4, 4′-亚甲基联苯二胺(TIMDA)
参照文献[17]方法,制备方法同DMMDA,熔点57~59 ℃,产率67%。1H NMR(CDCl3-d6), δ:6.70~6.77(s, 4H),2.88~3.02(m, 4H),1.03~1.12(d, 24H)。
1.3 聚合物的合成
均聚物的合成路径如下:在配有机械搅拌,N2气入口及冷凝管的三口瓶中加入10 mmol二胺及萘二酐,20 mmol苯甲酸,180 ℃,反应9 h, 而后加入20 mmol异喹啉再反应9 h, 冷却后得到黄色粘稠透明溶液,倒入乙醇溶液中,浸泡24 h, 过滤,120 ℃,干燥,得到黄色固体。二胺单体为DMMDA、DIMDA和TIMDA。
共聚物NTDA-DMMDA/TIMDA(9:1)(n(DMMDA):n(TIMDA)=9:1)合成路径如下:在配有机械搅拌,N2气入口及冷凝管的三口瓶中加入9 mmol DMMDA,1 mmol TIMDA以及10 mmol萘二酐,20 mmol苯甲酸,180 ℃,反应9 h, 加入20 mmol异喹啉,反应9 h, 冷却后得到黄色粘稠透明溶液,倒入乙醇溶液中,浸泡24 h, 过滤,120 ℃,干燥,得到黄色固体。其它共聚物合成方法类似,只是二胺单体摩尔比不同,分别为NTDA-DMMDA/TIMDA(8:2)(n(DMMDA):n(TIMDA)=8:2)、NTDA-DIMDA/TIMDA(9:1)(n(DIMDA):n(TIMDA)=9:1)和NTDA-DIMDA/TIMDA(8:2)(n(DIMDA):n(TIMDA)=8:2)。
1.4 膜的制备
将聚合物粉末溶解在NMP得到质量分数为7%的聚萘酰亚胺溶液,在干燥洁净的玻璃板上流延铺膜,80 ℃,干燥6 h, 挥发掉大部分溶剂,然后在真空烘箱150 ℃,加热12 h, 自然冷却至室温。将玻璃板放入水中,揭下薄膜,用滤纸擦干,而后至于甲醇中浸泡12 h, 置换掉残余的溶剂,擦干,放入真空烘箱中120 ℃,加热12 h, 备用。
1.5 气体分离性能测试
O2、N2、CH4和CO2的气体分离性能是在25 ℃一个标准大气压下测试的,用低真空法测定膜对气体的透过系数,其由下一公式计算得到:
式中,渗透系数P的单位为Barrer(1 Barrer=10-10 cm3[STP]·cm·cm-2·s-1·cm·Hg-1),pup是仪器上腔压力,dp/dt是稳定状态下下腔压强随时间变化系数,Vd为测试下腔体积(cm3),l为膜厚度(cm),R为气体常数,T为热力学温度(K),A为有效膜面积(cm2)。D为扩散系数(108cm2/s),S为溶解系数(10-2cm3[STP]·cm-3·cm-1·Hg-1)。
2 结果与讨论
2.1 聚萘酰亚胺的合成与表征
一般来说,六元二酐的反应活性往往低于五元二酐,这使它只能在较高的温度(>180 ℃)以及在催化剂存在的条件下才能与二胺反应。在反应过程中,酐与二胺首先反应生成异酰亚胺,如果在有机酸催化的条件下,得到的产物是反式异酰亚胺。相反,在无催化剂的条件下得到的是顺式异酰亚胺。只有反式异酰亚胺可以在有机碱的催化下进一步转化为酰亚胺结构,而顺式异酰亚胺则不能。因此,制备聚萘酰亚胺的较为理想的反应条件是在高温下先加入酸催化反应,反应一段时间后加入碱催化反应[10]。在本文中,基于萘二酐的聚萘酰亚胺都是在180 ℃条件下先加入苯甲酸做催化剂反应9 h, 而后加入异喹啉反应9 h制备得到的。在制备的三种均聚的聚萘酰亚胺中,NTDA-DMMDA与NTDA-DIMDA的粘度较高,分别为0.81和0.69 L/g(如表 1所示),但是其中NTDA-DMMDA难于溶解无法加工成膜。相比之下,NTDA-TIMDA的粘度仅为0.37 L/g,制备的膜机械性能很差。这主要是由于二胺单体空间位阻较大降低了其聚合反应活性,导致聚合物相对分子质量偏低造成的。基于以上原因,我们采用共聚的方法来制备可溶解于有机溶剂同时机械性能良好的聚萘酰亚胺,如Scheme 2所示。4种共聚的聚萘酰亚胺对数比粘度为0.57~0.71 L/g(如表 1所示),均可以制备成黄色透明,柔韧的薄膜。
 表 1
聚萘酰亚胺的粘度,热分解温度,玻璃化转变温度和机械性能对照
Table 1.
Inherent viscosity, decomposition temperature, glass-transition temperature(Tg) and mechanical property of polynaphthalimides.
表 1
聚萘酰亚胺的粘度,热分解温度,玻璃化转变温度和机械性能对照
Table 1.
Inherent viscosity, decomposition temperature, glass-transition temperature(Tg) and mechanical property of polynaphthalimides.
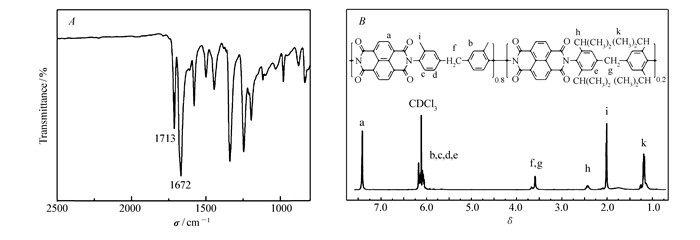
Polymer ηa/(dL·g-1) Tdb/℃ Tgc/℃ Tensile strength/MPa Young′s modulus/GPa Elongation at break/% N2 Air NTDA-DMMDA 0.81 501 484 — — — — NTDA-DMMDA/TIMDA(9:1) 0.71 472 438 391 76 2.2 6.6 NTDA-DMMDA/TIMDA(8:2) 0.73 460 428 388 54 1.5 7.7 NTDA-DIMDA 0.69 447 428 382 77 1.6 6.7 NTDA-DIMDA /TIMDA(9:1) 0.64 448 426 383 72 1.5 8.1 NTDA-DIMDA /TIMDA(8:2) 0.57 459 424 380 66 1.3 6.4 NTDA-TIMDA 0.37 451 419 — — — — a.inherent viscosity was measured at a concentration of 0.5 g/dL in NMP at 30 ℃; b.onset decomposition temperature in TGA at 10 ℃/min heating rate; c.measured by DMTA at 1 Hz and at a rate of 3 ℃/min. 聚合物的结构经FT-IR、1H NMR以及元素分析等技术手段进行了表征。聚萘酰亚胺的FT-IR谱图在1713(asym.C=O stretching)、1672 cm-1(asym.C=O stretching)处出现六元环聚萘酰亚胺特征吸收峰(如图 1A所示),这表明得到了六元环的聚萘酰亚胺。图 1B给出了聚合物NTDA-DMMDA/TIMDA(8:2)的1H核磁谱图,其峰位置及峰面积与聚合物推测值一致。
2.2 聚萘酰亚胺的溶解性
聚合物的溶解性的结果列于表 2中。均聚物中,NTDA-DMMDA只在高温中溶解于间甲酚中,NTDA-DIMDA则溶解于间甲酚及NMP中,而NTDA-TIMDA则可溶解于NMP、DMAc(N, N-二甲基乙酰胺)、DMF(N, N-二甲基甲酰胺)以及低沸点的CHCl3。较之相对应的均聚物,4种共聚物的溶解性有了较大程度的提高,如NTDA-DMMDA/TIMDA(8:2)不同于NTDA-DMMDA,可以溶解于NMP、DMAc等溶剂。总体上来说,聚酰亚胺中C—N键邻位取代基可以通过空间位阻效应减弱C—N键的旋转,破坏了共平面结构,减小分子链间的相互作用,改善聚萘酰亚胺的溶解性。
Polymer CHCl3 THF m-cresol NMP DMAc DMF NTDA-DMMDA - - ++ - - - NTDA-DMMDA/TIMDA(9:1) - - ++ ++ ++ + NTDA-DMMDA/TIMDA(8:2) ++ - ++ ++ ++ + NTDA-DIMDA ++ sw ++ ++ + - NTDA-DIMDA/TIMDA(9:1) ++ sw ++ ++ ++ + NTDA-DIMDA/TIMDA(8:2) ++ sw ++ ++ ++ + NTDA-TIMDA ++ - ++ ++ + ++ a.++:100 mg of polymer sample was totally soluble in 1 mL of solvent(10%); +:5%; sw:swelling; -:insoluable. 2.3 聚萘酰亚胺的热稳定性与机械性能
聚萘酰亚胺的热性能是通过动态热力学分析法和热失重分析法来表征的,其结果列于表 1中。整体上来说,聚合物中的萘酰亚胺结构使它们表现了良好的热稳定性及热氧化稳定性。3种均聚物中,热稳定性的顺序是NTDA-DMMDA>NTDA-DIMDA>NTDA-TIMDA,可见随着取代基的数量变多变大聚合物的热稳定性也变差。此外,4种共聚物也发现了类似的规律,即具有DMMDA的两种共聚物Td高于具有DIMDA两种共聚物的Td。这可能是由于聚合物中的脂肪族取代基会最先分解,所以聚合物中的脂肪族取代基越多其热稳定性越差。由于NTDA-DMMDA与NTDA-TIMDA无法加工成膜,所以没有得到其玻璃化转变温度数据。如表 1所示,这些聚萘酰亚胺的玻璃化转变温度在382~391 ℃之间,远高于商品化的聚酰亚胺(Uplex-R Tg=266 ℃,Matrimid 5218 Tg=330 ℃)[18],表明它们具有很好的耐热性。此外,基于DMMDA的两种共聚物要高于其它的聚萘酰亚胺。这可能是由于DIMDA的异丙基较之DMMDA内的甲基对聚萘酰亚胺有更强的增塑作用,从而降低了聚合物的玻璃化转变温度。
除NTDA-DMMDA及NTDA-TIMDA以外,其它制备的聚萘酰亚胺材料均具有较好的成膜性,它们均可以得到黄色、柔韧的薄膜。从表 1可以看到,这些聚萘酰亚胺材料的拉伸强度、杨氏模量和断裂伸长率分别在54~77 MPa、1.3~2.2 GPa及6.4%~8.1%之间。
2.4 聚萘酰亚胺的气体分离性能
表 3列出了25 ℃时所制备的聚萘酰亚胺均质膜对O2、N2、CO2和CH4 4种气体的透过系数PN2、PO2、PCO2和PCH4及理想分离系数αO2/N2、αCO2/CH4。由表 3中数据可以看出,聚萘酰亚胺中气体透过系数取决于聚合二胺的取代基,取代基越大数量越多则气体透过性能越好,这与Langsam等[19]对六氟二酐(6FDA)与带有不同取代基的二氨基苯甲烷所得到的聚酰亚胺的气体透过性能的研究所报道的规律类似。气体透过性最大的是NTDA-DIMDA/TIMDA(8:2)(PO2=24.9 barrer),而气体透过系数最小的是NTDA-DMMDA/TIMDA(9:1)(PO2=7.16 barrer),但均远高于商品化的Matrimid 5218(PO2=1.46 barrer)[20]。在聚合二胺相同的情况下,NTDA-DIMDA的气体透过性(PO2=19.2 barrer)也高于6FDA-DIMDA(PO2=8.2 barrer)。这说明萘酰亚胺高的刚性以及C—N键邻位取代基团的组合可以更为有效的提高材料的气体透过性能。
 表 3
聚萘酰亚胺膜的气体透过性及选择性
Table 3.
Pure gas permeabilities and selectivities of the polynaphthalimide membranes
表 3
聚萘酰亚胺膜的气体透过性及选择性
Table 3.
Pure gas permeabilities and selectivities of the polynaphthalimide membranes
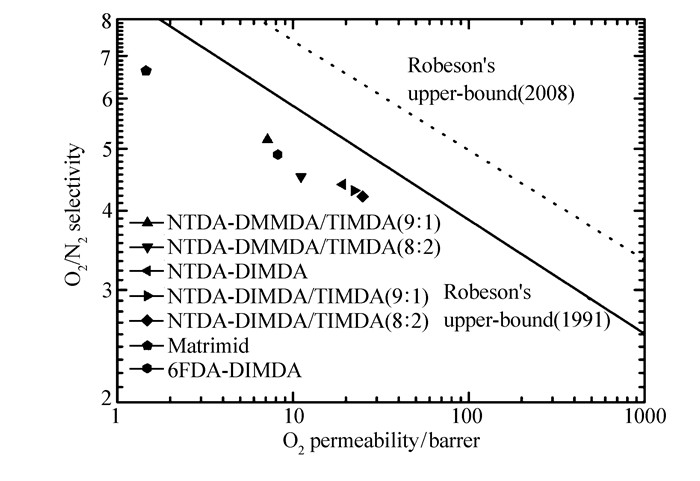
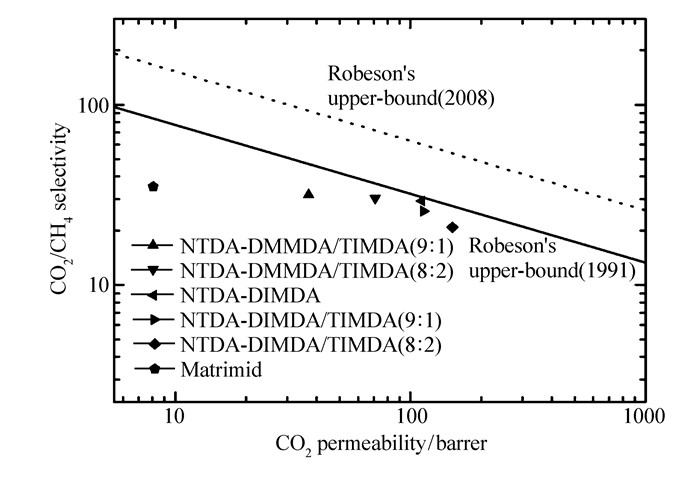
Polymer Permeabilities/barrera Selectivities(α) P(O2) P(N2) P(CO2) P(CH4) α(O2/N2) α(CO2/CH4) NTDA-DMMDA/TIMDA(9:1) 7.16 1.44 37.2 1.08 4.97 31.7 NTDA-DMMDA/TIMDA(8:2) 11.1 2.58 71 2.35 4.31 30.2 NTDA-DIMDA 19.2. 4.55 112 3.83 4.22 29.2 NTDA-DIMDA/TIMDA(9:1) 22.3 5.33 114 4.44 4.18 25.7 NTDA-DIMDA/TIMDA(8:2) 24.9 6.41 151 7.21 3.91 20.9 a.P is permeability coefficient; units:1 Barrer=10-10 cm3[STP]·cm·cm-2·s-1·cm·Hg-1. 为了直观的研究聚萘酰亚胺的气体分离性能,图 2及图 3分别为这些聚合物对O2/N2及CO2/CH4气体的分离性能与Robeson上限线进行的比较。聚合物的气体分离数据在图中越是靠近Robeson上限线,说明它们的气体分离性能越好。如图 2所示,尽管制备的聚萘酰亚胺气体分离数据均在O2/N2的Robeson上限线之下,但是整体上要好于6FDA-DIMDA,尤其是远远优于Matrimid 5218。在图 3中,聚萘酰亚胺对CO2/CH4气体分离表现整体上也好于Matrimid 5218,尤其是NTDA-DIMDA的数据已经位于1991 Robeson上限线上。这表明C—N键邻位含脂肪取代基的聚萘酰亚胺具有良好的气体分离性能,在天然气纯化等方面具有广阔的应用前景。
3 结论
本文利用邻位含脂肪族取代基的芳香二胺与萘二酐的聚合,制备了一系列可溶解于有机溶剂的聚萘酰亚胺。C—N键邻位取代基的引入一方面可以有效破坏聚合物共平面结构,减弱分子间作用力,改善了聚萘酰亚胺的溶解性;另一方面,在保证主链刚性的前提下提高了聚萘酰亚胺的自由体积,从而使聚萘酰亚胺表现高的气体分离性能。
-
-
[1]
Yampolskii Y. Polymeric Gas Separation Membranes[J]. Macromolecules, 2012, 45(8): 3298-3311. doi: 10.1021/ma300213b
-
[2]
Xiao Y C, Low B T, Hosseini S S. The Strategies of Molecular Architecture and Modification of Polyimide-based Membranes for CO2 Removal from Natural Gas-A Review[J]. Prog Polym Sci, 2009, 34(6): 561-590. doi: 10.1016/j.progpolymsci.2008.12.004
-
[3]
Robeson L M. Correlation of Separation Factor Versus Permeability for Polymeric Membranes[J]. J Membr Sci, 1991, 62(2): 165-185. doi: 10.1016/0376-7388(91)80060-J
-
[4]
Mao H C, Zhang S B. Synthesis, Characterization, and Gas Transport Properties of Novel Poly(amine imide)s Containing Tetraphenylmethane Pendant Groups[J]. J Mater Chem A, 2014, 2(25): 9835-9843. doi: 10.1039/C4TA00429A
-
[5]
Genies C, Mercire R, Sillion B. Stability Study of Sulfonated Phthalic and Naphthalenic Polyimide Structures in Aqueous Medium[J]. Polymer, 2001, 42(12): 5097-5105. doi: 10.1016/S0032-3861(00)00645-5
-
[6]
Yin Y, Suto Y, Sakabe T. Water Stability of Sulfonated Polyimide Membranes[J]. Macromolecules, 2006, 39(3): 1189-1198. doi: 10.1021/ma0523769
-
[7]
Urrehman S, Li P, Zhou H W. Thermally and Hydrolytically Stable Polyimides Containing Naphthalimide Units[J]. Polym Degrad Stab, 2012, 97(9): 1581-1588. doi: 10.1016/j.polymdegradstab.2012.06.035
-
[8]
Li W M, Zhang S B, Chen G. A New Class of High Tg and Organosoluble Polynaphthalimides[J]. Polymer, 2007, 48(11): 3082-3089. doi: 10.1016/j.polymer.2007.03.065
-
[9]
Sek D, Wanic A, Balcerzak E S. Investigation of Polyimides Containing Naphthalene Units.Ⅲ.Influence of Monomers Structure on Polymers Properties[J]. J Polym Sci Part A:Polym Chem, 1997, 35(3): 539-545. doi: 10.1002/(ISSN)1099-0518
-
[10]
Sek D, Wanic A. High-Temperature Polycondensation of Six Membered Dianhydrides with o-Substituted Aromatic Diamines 1.Model Compounds Investigation[J]. Polymer, 2000, 41(7): 2367-2372. doi: 10.1016/S0032-3861(99)00427-9
-
[11]
Yang C P, Su Y Y, Wang J M. Synthesis and Properties of Organosoluble Polynaphthalimides Based on 1, 4, 5, 8-Naphthalene Tetracarboxylic Dianhydride, 3, 3-Bis[4-(4-Aminophenoxy)phenyl]phthalide, and Various Romatic Diamines[J]. J Polym Sci Part A:Polym Chem, 2006, 44(2): 940-948. doi: 10.1002/(ISSN)1099-0518
-
[12]
Yang C P, Su Y Y, Guo W J. Synthesis and Properties of Novel Fluorinated Polynaphthalimides Derived from 1, 4, 5, 8-Naphthalenetetracarboxylic Dianhydride and Trifluoromethyl-Substituted Aromatic Bis(ether amine)s[J]. Eur Polym J, 2009, 45(3): 721-729. doi: 10.1016/j.eurpolymj.2008.12.013
-
[13]
Tanaka K, Islam M N, Kido M. Gas Permeation and Separation Properties of Sulfonated Polyimide Membranes[J]. Polymer, 2006, 47(12): 4370-4377. doi: 10.1016/j.polymer.2006.04.001
-
[14]
Du N Y, Park H B, Dal-Cin M M. Advances in High Permeability Polymeric Membrane Materials for CO2 Sepration[J]. Energy Environ Sci, 2012, 5(6): 7306-7322. doi: 10.1039/C1EE02668B
-
[15]
Al-Masri M, Kricheldorf H R, Fritsch D. New Polyimides for Gas Separation, 1.Polyimides Derived from Substituted Terphenylenes and 4, 4'-(Hexafluoroisopropylidene)diphthalic Anhydride[J]. Macromolecules, 1999, 32(23): 7853-7860. doi: 10.1021/ma9910742
-
[16]
Wang C Y, Chen W T, Chen Y Y. Synthesis and Properties of New Fluorene-based Polyimides Containing Trifluoromethyl and Isopropyl Substituents[J]. Mater Chem Phys, 2014, 144(3): 553-559. doi: 10.1016/j.matchemphys.2014.01.039
-
[17]
Lu Q H, Yin J, Xu H J. Preparation and Properties of Organo-Soluble Polyimides Based on 4, 4'-Diamino-3, 3-dimethyldiphenylmethane and Conventional Dianhydrides[J]. J Appl Polym Sci, 1999, 72(10): 1299-1304. doi: 10.1002/(ISSN)1097-4628
-
[18]
Tong Y J, Huang W X, Luo J. Synthesis and Properties of Armomatic Polyimides Derived from 2, 2, 3, 3-Biphenyltetracarboxylic Dianhydride[J]. J Polym Sci Part A:Polym Chem, 1997, 37(10): 1425-1432.
-
[19]
Grubb T L, Ulery V L, Smith T J. Highly Soluble Polyimides from Sterically Hindered Diamines[J]. Polymer, 1999, 40(15): 4279-4288. doi: 10.1016/S0032-3861(98)00663-6
-
[20]
Barbari T A, Koros W J, Paul D R. Polymeric Membranes Based on Bisphenol-A for Gas Separation[J]. J Membr Sci, 1989, 42(1): 69-86.
-
[21]
Robeson L M. The Upper Bound Revisited[J]. J Membr Sci, 2008, 320(1/2): 390-400.
-
[1]
-
表 1 聚萘酰亚胺的粘度,热分解温度,玻璃化转变温度和机械性能对照
Table 1. Inherent viscosity, decomposition temperature, glass-transition temperature(Tg) and mechanical property of polynaphthalimides.
Polymer ηa/(dL·g-1) Tdb/℃ Tgc/℃ Tensile strength/MPa Young′s modulus/GPa Elongation at break/% N2 Air NTDA-DMMDA 0.81 501 484 — — — — NTDA-DMMDA/TIMDA(9:1) 0.71 472 438 391 76 2.2 6.6 NTDA-DMMDA/TIMDA(8:2) 0.73 460 428 388 54 1.5 7.7 NTDA-DIMDA 0.69 447 428 382 77 1.6 6.7 NTDA-DIMDA /TIMDA(9:1) 0.64 448 426 383 72 1.5 8.1 NTDA-DIMDA /TIMDA(8:2) 0.57 459 424 380 66 1.3 6.4 NTDA-TIMDA 0.37 451 419 — — — — a.inherent viscosity was measured at a concentration of 0.5 g/dL in NMP at 30 ℃; b.onset decomposition temperature in TGA at 10 ℃/min heating rate; c.measured by DMTA at 1 Hz and at a rate of 3 ℃/min. 表 2 聚萘酰亚胺溶解性a
Table 2. Solubilitya of polynaphthalimides
Polymer CHCl3 THF m-cresol NMP DMAc DMF NTDA-DMMDA - - ++ - - - NTDA-DMMDA/TIMDA(9:1) - - ++ ++ ++ + NTDA-DMMDA/TIMDA(8:2) ++ - ++ ++ ++ + NTDA-DIMDA ++ sw ++ ++ + - NTDA-DIMDA/TIMDA(9:1) ++ sw ++ ++ ++ + NTDA-DIMDA/TIMDA(8:2) ++ sw ++ ++ ++ + NTDA-TIMDA ++ - ++ ++ + ++ a.++:100 mg of polymer sample was totally soluble in 1 mL of solvent(10%); +:5%; sw:swelling; -:insoluable. 表 3 聚萘酰亚胺膜的气体透过性及选择性
Table 3. Pure gas permeabilities and selectivities of the polynaphthalimide membranes
Polymer Permeabilities/barrera Selectivities(α) P(O2) P(N2) P(CO2) P(CH4) α(O2/N2) α(CO2/CH4) NTDA-DMMDA/TIMDA(9:1) 7.16 1.44 37.2 1.08 4.97 31.7 NTDA-DMMDA/TIMDA(8:2) 11.1 2.58 71 2.35 4.31 30.2 NTDA-DIMDA 19.2. 4.55 112 3.83 4.22 29.2 NTDA-DIMDA/TIMDA(9:1) 22.3 5.33 114 4.44 4.18 25.7 NTDA-DIMDA/TIMDA(8:2) 24.9 6.41 151 7.21 3.91 20.9 a.P is permeability coefficient; units:1 Barrer=10-10 cm3[STP]·cm·cm-2·s-1·cm·Hg-1. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 3
- 文章访问数: 906
- HTML全文浏览量: 177


 下载:
下载:




 下载:
下载:

