
Citation: WANG Yutong, FAN Weidong, XIAO Zhenyu, HUANG Zhaodi, XU Lin, ZHANH Liangliang, XING Lixue, DAI Fangna, SUN Daofeng. Solvent-Dependent Synthesis and Fluorescent Properties of Cu(Ⅱ) Metal-Organic Frameworks[J]. Chinese Journal of Applied Chemistry, 2017, 34(9): 1035-1045. doi: 10.11944/j.issn.1000-0518.2017.09.170180

溶剂控制的铜基金属-有机框架物的合成与荧光性能
English
Solvent-Dependent Synthesis and Fluorescent Properties of Cu(Ⅱ) Metal-Organic Frameworks
-
近年来,我国水土环境的污染越来越严重,其中以铅、铬、汞、镉等生物毒性明显的重金属离子对水体造成的污染危害更为深远。重金属离子不能被生物降解,相反却能在食物链的生物放大作用下,成百上千倍地富集,最后进入人体,可能在人体的某些器官中累积,造成慢性中毒。因此,对其进行有效地监测对于人类健康和环境保护均具有重要意义。众多的检测手段中,荧光识别法凭借其反应速度快、灵敏度高、简便易操作等优点成为重金属识别的重要手段之一。要准确高效地识别重金属离子,迫切地需要一种良好的、具有选择性识别的基物,科学家们将目光投向能有效捕获分析物的多孔金属-有机框架物(Metal Organic Frameworks, 简称MOFs)。2004年,Liu等[1]用合成的镧系MOFs识别Zn2+、Cd2+、Hg2+等金属阳离子,为MOF在荧光识别方面的应用开辟了新的研究方向。2011年,Kitagawa课题组[2]制备了基于MOFs材料的芳香类衍生物小分子传感器,使识别的领域扩大到有机物。2012年,Lin课题组[3]合成高灵敏识别手性氨基醇的MOFs,在敏感度和识别性能方面取得重大进展。2013年,Li课题组[4]成功制备了动态监测乙腈蒸汽的MOFs材料传感器,更是为实际应用奠定了基础。我们课题组[5]也成功制备了Eu-MOFs荧光pH传感器,进而扩大了MOFs材料荧光识别的领域。这些均为应用MOFs材料识别重金属离子提供了参考。
MOFs是由金属离子或金属簇单元通过配位作用与有机配体自组装而成的一类具有多维周期性网状结构的晶态材料,因此,也被称为多孔配位聚合物。多维网状结构的存在使其形成了各式各样的孔道,通过控制配体的大小及种类,可以对孔道的大小进行调控与修饰,形成多级的孔道。由于结合了金属离子和配体各自的优点,及其可控的孔道和种类各异的拓扑结构使其在分子磁性、药物分子的传递、温室气体的吸附与分离、能源气体的储存、荧光探针、空间限域内的不对称催化等领域具有巨大的应用潜力和前景[6-13]。目前,MOFs的合成已经不再是技术难题,但是MOFs组装的过程高度依赖于金属离子的配位模式、配体主链的柔韧性、金属与配体摩尔比率、生长体系酸碱度和不同的溶剂[14-18],因此,预测和控制框架的自组装过程仍然是科学家们面临的巨大挑战。
在这些因素中,溶剂对自组装过程具有较大影响,这一现象在沸石和分子筛的合成过程中也被观察到[19-21]。当使用相同的金属和有机配位以相同的比例组装MOFs时只要溶剂有稍微的变化,就可能会导致形成不同的框架结构。因此,研究相同材料的溶剂定向组装对于设计合成多功能性金属-有机框架物是非常重要的[22]。
本文主要通过溶剂调控的方法,应用5-丙酰胺基间苯二甲酸(H2PAIA)配体与三水合硝酸铜合成出两种结构及性质不同的金属-有机框架结构:配合物1的分子式为{[Cu(PAIA)(H2O)]·2H2O};配合物2的分子式为{[Cu3(PAIA)2(DMSO)(Pyridine)1.5]} (DMSO:二甲基亚砜;Pyridine:吡啶)。有趣的是,配合物1和2均可以作为荧光探针,实现对重金属离子的选择性识别,但由于其结构上的差异,配合物1能够同时识别Pb2+和Ag+离子,而配合物2只能识别Pb2+, 对Ag+无明显的信号响应。本研究工作为设计新型高敏荧光探针提供了实验参考。
1 实验部分
1.1 仪器和试剂
VERTEX-70型傅里叶变换红外光谱仪(德国布鲁克公司),采取KBr压片法;Vario ELⅢ型元素分析仪(德国Elementar公司);F-7000型荧光分光光度计(日本HITACHI);TGA/DSC-1型同步热分析仪(瑞士梅特勒-托利多公司),在N2气氛围(100 mL/min)中以10 K/min的加热速率从40 ℃升至900 ℃;ASAP2020型吸附仪(美国麦克公司);SuperNova型X射线单晶衍射仪(美国安捷伦);D8 ADVANCE型粉末X射线单晶衍射仪(PXRD, 德国布鲁克公司)。
硝酸铜(Cu(NO3)2·3H2O)、二甲亚砜(DMSO)、吡啶(Pyridine)及咪唑(Imidazole)均为分析纯试剂,购于萨恩化学技术(上海)有限公司,没有经过进一步纯化;实验用水均为去离子水。
1.2 晶体的合成
1.2.1 配合物{[Cu(PAIA)(H2O)]·2H2O}(1)的制备
用电子天平准确称取Cu(NO3)2·3H2O(10.0 mg, 0.041 mmol)、H2PAIA(10.0 mg, 0.042 mmol)和咪唑(3.0 mg, 0.042 mmol)放入10 mL的玻璃瓶中,用滴管滴加2 mL去离子水,将装有溶液的密封玻璃瓶放入恒温干燥箱中,设置反应时间和温度。第1阶段:用60 min升温至75 ℃;第2阶段:在75 ℃下恒温保持2000 min;第3阶段:从75 ℃经过100 min降温至30 ℃。取出得到蓝色透明块状晶体,产率为80%。元素分析测试值(理论值)/%:C 38.1(37.4), H 3.8(4.3), N 3.9(4.0)。
1.2.2 配合物{[Cu3(PAIA)2(DMSO)(Pyridine)1.5]}(2)的制备
配合物2的制备反应温度和时间与配合物1的一样,只是调整了溶剂。在10 mL的小玻璃瓶中加入准确称量的Cu(NO3)2·3H2O(5.0 mg,0.021 mmol)和H2PAIA(60.0 mg,0.253 mmol),滴加2 mL DMSO和H2O(体积比1:1) 混合溶剂,之后加入20 μL的吡啶,放入恒温干燥箱中生长,取出得到蓝色透明块状晶体,产率为85%。元素分析测试值(理论值)/%:C 46.8(46.1),H 4.1(3.7),N 5.5(5.6),S 4.4(4.2)。
2 结果与讨论
2.1 配合物晶体数据
两种配合物的单晶数据在X射线单晶衍射系统上收集。挑选合适大小的晶体粘在Loop环上,室温条件下用石墨单色化的钼靶Kα(λ=0.07107 nm)和铜靶Kα (λ=0.154184 nm)射线,以ω-2θ扫描方式收集晶体衍射数据,使用multiscan program SADABS进行吸收校正。晶体结构数据利用Olex2程序,通过使用Superflip程序解得,并用Shelxs程序以全矩阵经最小二乘法对F2进行不断修正后得到全部非氢原子坐标以及其各向异性参数。有机配体的H原子通过几何加氢法处理。通过PLATON/SQUEEZE程序去除无序溶剂分子,并计算得到孔隙率。配合物1和2的数据已存入剑桥晶体学数据中心(CCDC Number:1541107和1550251),晶体学数据见表 1。
Compound 1 2 Formula C11H15CuNO8 C29H28Cu2N3O11S Mr 352.78 754.69 Crystal system trigonal orthorhombic Space group R-3 Pbcm a/nm 1.883 85(8) 0.978 64(2) b/nm 1.883 85(8) 2.823 81(5) c/nm 2.242 61(8) 2.476 27(5) α /(°) 90 90 β/(°) 90 90 γ /(°) 120 90 V/nm3 6.892 5(6) 6.843 2(2) Z 18 8 Dc/(g·cm-3) 1.530 1.465 μ /mm-1 1.461 1.363 F(000) 3 258.0 3 088.0 θ range for data collection/(°) 6.176 to 49.984 3.286 to 50.19 Reflections collected 6 148 23 486 Temperature/K 293(2) 150 Data/restraints/parameters 2694/0/198 6271/17/434 Final R indexes [I≥2σ(I)] R1=0.058 0, wR2=0.173 8 R1=0.119 9, wR2=0.354 9 Final R indexes [all data] R1=0.077 9, wR2=0.192 5 R1=0.143 4, wR2=0.378 7 Largest diff. peak/hole/(e·nm-3) 1.51×10-3/-0.43 4.06×10-3/-2.40 a.R1=Σ(‖F0|-|Fc‖)/Σ|F0|; b.wR2=[Σw(|F0|2-|Fc|2)2/Σ(F02)2]1/2. 2.2 配合物结构分析
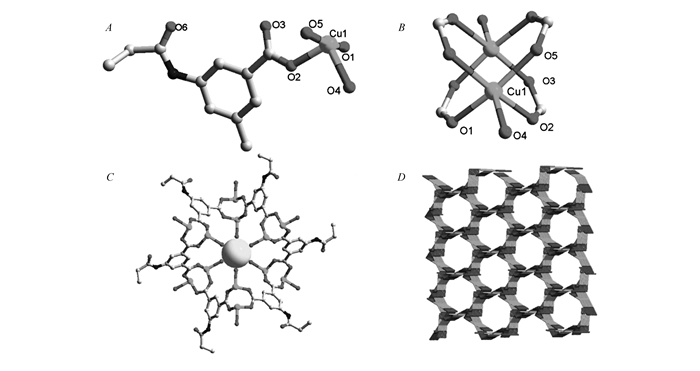
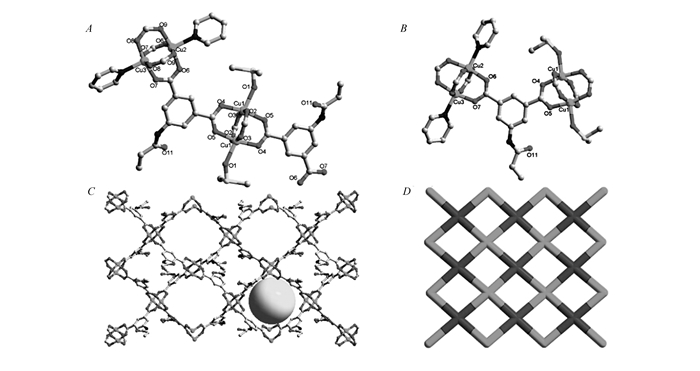
X射线单晶衍射分析表明,配合物1属于单斜晶系R-3空间群。如图 1A所示,其不对称单元包含一个Cu2+离子,一个PAIA2-配体,1个配位的H2O分子和2个游离的H2O分子。Cu2+离子采用五角锥体配位构型与来自4个不同PAIA2-配体的4个O原子和1个来自H2O分子的氧原子配位。两个相邻的Cu原子通过4个羧基连接起来形成典型的轮浆状次级结构单元(SBU),如图 1B所示,两个Cu原子之间的距离为0.2615 nm,Cu—Ocarboxylate平均键长为0.1964 nm,Cu—Owater键长为0.2139 nm。相邻的SBU通过PAIA2-配体彼此连接,形成了如图 1C所示的拥有一维孔道的复杂三维网络,其中孔道内切圆直径约为0.37 nm。为了方便了解其网络结构,我们通过拓扑的方法来简化配合物结构。这里我们将二连接配体抽象成一条连接线,而四联接的轮浆状SBU则可以抽象为一个四连接的节点。那么,配合物1就是一个4-c的三维NbO拓扑(图 1D),点符号为{64·82}。通过PLATON软件计算了配合物1的孔隙率,约为32.6%(计算晶胞孔隙率时,框架中所有的溶剂分子包括配位的水全部被移除)。
X射线单晶衍射分析表明,配合物2属于单斜晶系Pbcm空间群,如图 2A所示,其不对称单元包含1个Cu2+离子(Cu1)、2个一半的Cu2+离子(Cu2和Cu3)、2个PAIA2-配体、1个配位的DMSO分子和2个二分之一个吡啶分子。如图 2B所示,配合物2中相邻的Cu2+中心,通过羧酸的桥连,形成了和配合物1中相同的轮浆状SBU,但是不同于配合物1,在配合物2中存在两种不同的SBU:一种是两个相邻的Cu1被桥连(SBU-1),轴向由DMSO配位,其中Cu1—Cu1之间的距离为0.2651 nm,Cu—O平均键长为0.1967 nm,Cu—ODMSO键长为0.2196 nm;另一种是有相邻的Cu2和Cu3被桥连(SBU-2),轴向由吡啶分子配位,其中Cu2—Cu3之间的距离为0.2642 nm,Cu—O平均键长为0.1960 nm,Cu—N平均键长为0.217 nm。每个SBU-1通过4个PAIA2-配体连接了4个相同的SBU-2,同时,每个SBU-2通过4个PAIA2-配体连接了4个相同的SBU-1,最终形成了如图 2C所示的二维层状结构。同样,为了更方便地理解这个层状结构,我们利用拓扑的观点,将有机配体抽象成一条线,轮桨状的SBU抽象成四联接的节点,那么最终这个层状网络可以简化成sql拓扑,如图 2D所示,点符号为{44·62}。同时,通过PLATON软件计算配合物2每个晶胞的孔隙率为49.8%(计算晶胞孔隙率时,框架中所有的溶剂分子包括配位的水全部被移除)。
2.3 配合物1和2的基本性能表征
在室温条件下,对配合物1和2进行粉末X射线衍射表征,得到的PXRD谱图如图 3A所示。从图中可以看出,实测得到配合物1和2的粉末X射线衍射峰和由单晶数据模拟得到的粉末衍射峰完全一致,这表明由实验得到的配合物1和2晶体具有很高的相纯度。
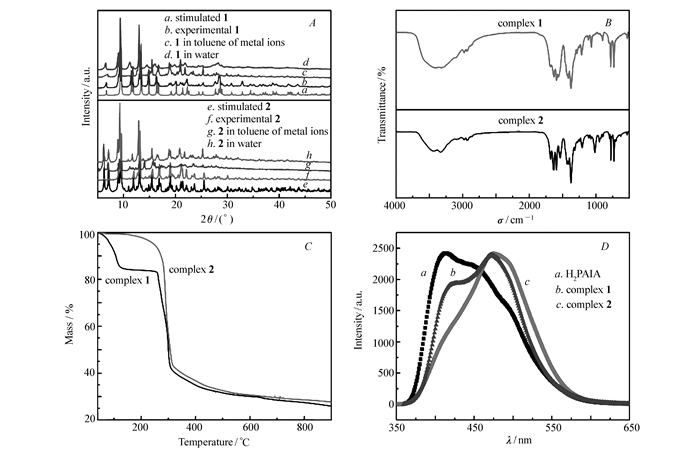 图3
配合物1和2的XRD对比图(金属离子包含Pb2+、Co2+、Cr3+、Al3+、Ag+、Fe3+、Cd2+、Ca2+、Ba2+、Mg2+)(A)、红外谱图(B)、热重分析图(C)及配合物与配体的固态荧光谱图(D)
Figure3.
XRD patterns(Metal ions include Pb2+, Co2+, Cr3+, Al3+, Ag+, Fe3+, Cd2+, Ca2+, Ba2+, Mg2+)(A), infrared spectra(B), TGA curves(C) of complexes 1 and 2, and the solid-state fluorescence spectra of two complexes and ligands(D)
图3
配合物1和2的XRD对比图(金属离子包含Pb2+、Co2+、Cr3+、Al3+、Ag+、Fe3+、Cd2+、Ca2+、Ba2+、Mg2+)(A)、红外谱图(B)、热重分析图(C)及配合物与配体的固态荧光谱图(D)
Figure3.
XRD patterns(Metal ions include Pb2+, Co2+, Cr3+, Al3+, Ag+, Fe3+, Cd2+, Ca2+, Ba2+, Mg2+)(A), infrared spectra(B), TGA curves(C) of complexes 1 and 2, and the solid-state fluorescence spectra of two complexes and ligands(D)
配合物1的红外光谱数据波数范围400~4000 cm-1。如图 3B所示,主要红外吸收峰(σ/cm-1)为:3410(s), 2980(m), 1635(s), 1592(s), 1423(s), 1374(s), 1218(m), 1069(m), 900(m), 775(s), 732(s), 533(m)。配合物2的红外光谱数与配合物1用的同一台仪器在相同的波数范围下采用相同方法测试得到,如图 3B所示,主要红外吸收峰(σ/cm-1)为:3435(w), 2937(m), 1685(w), 1635(s), 1592(s), 1529(w), 1423(s), 1374(s), 1205(m), 1012(w), 944(m), 782(s), 732(s), 533(m)。
配位化合物1和2的热重分析数据如图 3C所示:化合物1在120 ℃发生第1次失重,这主要对应配合物中游离水组分的丢失,第2次失重发生在300 ℃,对应配合物的分解;而化合物2由于不存在游离水分子,只有配位的DMSO和吡啶分子,因此只表现出1次失重,对应配合物的分解,同时伴随着配位溶剂分子的挥发。
室温下测试配合物1、配合物2和配体H2PAIA的固体荧光性能如图 3D所示。配体H2PAIA的主要发射峰出现在413 nm(λex=330 nm)。配合物1和2分别在473 nm(λex=330 nm)和475 nm(λex=330 nm)出现最大发射峰。与H2PAIA的最大发射峰相比,配合物1和2显示红移(分别为Δ=60 nm和62 nm)。
2.4 配合物1和2的荧光识别性能
为了进一步探究配合物1和2的荧光识别性能。我们将两种晶体研磨称取2.0 mg分别分散到3 mL共6种有机溶剂中(二甲基乙酰胺DMA、DMSO、乙醇、乙腈、甲苯、硝基苯),超声15 min后进行荧光测试。如图 4A所示,配合物1的荧光性能与溶剂的选择有很大关系。当配合物1分散在甲苯溶剂中时,荧光强度有明显的提高,相反,分散在硝基苯中有最弱发射峰。因此,接下来的测试我们选择在甲苯中进行。
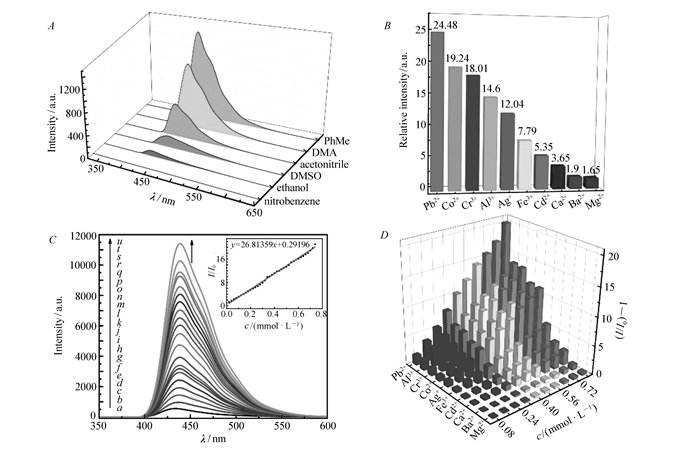 图4
分散在不同溶剂中的配合物1的荧光光谱(A); 不同离子对配合物1荧光增强倍数(B); 加入Pb2+离子(0~0.8 mmol/L)后的荧光光谱变化及I/I0值与Pb2+浓度关系图(C); 分析物的Stern-Volmer曲线(D)
Figure4.
The fluorescence spectra of complex 1 dispersed in different solvents(A); fluorescence enhancement ratio of complex ion pair complex 1(B); the change of fluorescence spectrum and the relationship between I/I0 and Pb2+ concentration after adding Pb2+ ions(0~0.8 mmol/L)(C); corresponding Stern-Volmer plots of analytes(D)
图4
分散在不同溶剂中的配合物1的荧光光谱(A); 不同离子对配合物1荧光增强倍数(B); 加入Pb2+离子(0~0.8 mmol/L)后的荧光光谱变化及I/I0值与Pb2+浓度关系图(C); 分析物的Stern-Volmer曲线(D)
Figure4.
The fluorescence spectra of complex 1 dispersed in different solvents(A); fluorescence enhancement ratio of complex ion pair complex 1(B); the change of fluorescence spectrum and the relationship between I/I0 and Pb2+ concentration after adding Pb2+ ions(0~0.8 mmol/L)(C); corresponding Stern-Volmer plots of analytes(D)
为了检测配合物1对金属离子的识别能力,将含有不同金属离子(Pb2+、Co2+、Cr3+、Al3+、Ag+、Fe3+、Cd2+、Ca2+、Ba2+、Mg2+)的甲苯溶液(1.0 mmol/L)中逐渐加入到含有配合物1的甲苯悬浊液中。如图 4B所示,大多数金属离子对配合物1均有一定的荧光增强效果,当Pb2+加到0.8 mmol/L时荧光增强达到24.48倍。而且其增强效果成线性增长(图 4C)。我们通过Stern-Volmer(SV)式:(I/I0)=KSV[A]+1计算其增强率,如图 4D所示。其它9种金属离子的增强效果及SV式在图 5中展现,从图中可以看出,所有的增强效果均能很好地拟合为一次函数。
配合物2的测试方法与配合物1相同,在不同溶剂中分散的荧光光谱如图 6A所示,可见在6种溶剂中硝基苯对配合物的荧光具有强烈的淬灭效果,而在甲苯中具有较高的荧光特性,因此我们将配合物2分散到甲苯溶液中进行测试。研究结果表明,10种金属离子对配合物2均有荧光增强效果,不同离子对荧光增强倍数如图 6B所示,Pb2+离子的增强效果最为明显,当浓度达到0.8 mmol/L时荧光增强达到17.05倍,其增强效果呈线性增长(图 6C)。我们通过SV式计算其增强率,如图 6D所示。其它9种金属离子的增强效果及SV式在图 7中展现,从图中可以看出,所有的增强效果都能很好地拟合为一次函数。
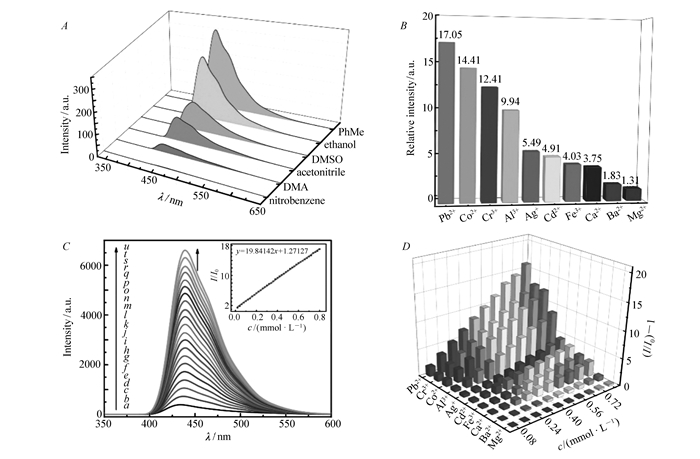 图6
分散在不同溶剂中的配合物2的荧光光谱(A); 不同离子对配合物2荧光增强倍数(B); 加入Pb2+离子(0~0.8 mmol/L)后的荧光光谱变化及I/I0值与Pb2+浓度关系图(C); 分析物的Stern-Volmer曲线(D)
Figure6.
The fluorescence spectra of complex 2 dispersed in different solvents(A); fluorescence enhancement ratio of complex ion pair complex 2(B); the change of fluorescence spectrum and the relationship between I/I0 and Pb2+ concentration after adding Pb2+ ions(0~0.8 mmol/L)(C); corresponding Stern-Volmer plots of analytes(D)
图6
分散在不同溶剂中的配合物2的荧光光谱(A); 不同离子对配合物2荧光增强倍数(B); 加入Pb2+离子(0~0.8 mmol/L)后的荧光光谱变化及I/I0值与Pb2+浓度关系图(C); 分析物的Stern-Volmer曲线(D)
Figure6.
The fluorescence spectra of complex 2 dispersed in different solvents(A); fluorescence enhancement ratio of complex ion pair complex 2(B); the change of fluorescence spectrum and the relationship between I/I0 and Pb2+ concentration after adding Pb2+ ions(0~0.8 mmol/L)(C); corresponding Stern-Volmer plots of analytes(D)
将配合物1和2进行对比可以看出,它们对Pb2+离子均有明显的识别能力,但配合物1的识别能力更强一些。对Ag+离子识别上,配合物1具有明显的识别能信号,而配合物2的识别能力却相对较弱。可能是金属离子与配合物的某种键合作用使得其荧光性能呈线性增长。
为了证明配合物1和2在含有各种金属离子浸泡的甲苯溶液中能维持结构的稳定,我们将测试完荧光识别后的晶体收集起来通过PXRD对比,发现晶体保持了很好的晶态和纯度(见图 3A)。
2.5 配合物疏水性能
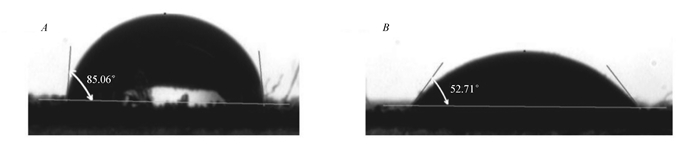
由图 3A的PXRD结果可以看出,水浸泡过后的配合为1和2均能维持结构的稳定,为了探究配合物1和2是否会因为结构的不同而导致其疏水性能的改变,在室温下我们测试了两种配合物的疏水能力,将配合物分别平铺到玻璃片上,在配合物上滴一滴去离子水,测量其疏水角,如图 8A和8B所示,配合物1的疏水角85.06°比配合物2的52.71°有显著的增加。实验证明配合物1有一定的疏水性能,而配合物2则是亲水的。结构的不同导致了其性质的差异,据此可为合成具有一定疏水性能的MOFs材料提供合成条件的参考,也为绿色合成水稳MOFs提供了新的思路。
3 结论
本文使用相同的原料,通过溶剂热反应在不同溶剂中合成了两例新型不同Cu-Paddlewheel结构的多孔金属有机框架物。对这些MOFs的合成和结构研究表明,溶剂的定向组装可以导致具有不同拓扑结构的多孔骨架材料,在荧光识别和疏水性能等方面有显著的多样性,尤其是在铅离子的识别上有着重要意义。不同于大部分MOFs材料的荧光淬灭现象,本文合成的两种配合物对重金属离子均产生荧光增强效果,为设计新型高敏荧光探针提供了新的优良材料。又基于溶剂定向组装的策略,可以通过在合成过程中改变反应溶剂来预期设计合成各种新型MOFs,调控结构的同时可以筛选出识别特定金属离子的优良金属-有机框架材料。
-
-
[1]
Liu W S, Jiao T Q, Li Y Z. Lanthanide Coordination Polymers and Their Ag+-Modulated Fluorescence[J]. J Am Chem Soc, 2004, 126(8): 2280-2281. doi: 10.1021/ja036635q
-
[2]
Takashima Y, Martínez V M, Furukawa S. Molecular Decoding Using Luminescence from an Entangled Porous Framework[J]. Nat Commun, 2011, 2(168): 1-8.
-
[3]
Wanderley M M, Wang C, Wu C D. A Chiral Porous Metal-Organic Framework for Highly Sensitive and Enantioselective Fluorescence Sensing of Amino Alcohols[J]. J Am Chem Soc, 2012, 134(22): 9050-9053. doi: 10.1021/ja302110d
-
[4]
Wang J H, Li M, Li D. A Dynamic, Luminescent and Entangled MOF as a Qualitative Sensor for Volatile Organic Solvents and a Quantitative Monitor for Acetonitrile Vapour[J]. Chem Sci, 2013, 4(4): 1793-1801. doi: 10.1039/c3sc00016h
-
[5]
Meng Q G, Xin X L, Zhang L L. A Multifunctional Eu MOF as a Fluorescent pH Sensor and Exhibiting Highly Solvent-Dependent Adsorption and Degradation of Rhodamine B[J]. J Mater Chem A, 2015, 3(47): 24016-24021. doi: 10.1039/C5TA04989J
-
[6]
Furukawa H, Cordova K E, O'Keeffe M. The Chemistry and Applications of Metal-Organic Frameworks[J]. Science, 2013, 44(45): 1230444.
-
[7]
Eddaoudi M, Kim J, Rosi N. Systematic Design of Pore Size and Functionality in Isoreticular MOFs and Their Application in Methane Storage[J]. Science, 2002, 295(5554): 469-72. doi: 10.1126/science.1067208
-
[8]
Yang J, Wang X Q, Wang R M. Syntheses, Crystal Structures, and Properties of Two 2-FoldInterpenetrating Metal-Organic Frameworks Based on a Trigonal Rigid Ligand[J]. Cryst Growth Des, 2014, 14(12): 6521-6527. doi: 10.1021/cg501425x
-
[9]
Zhao B, Chen X Y, Cheng P. Coordination Polymers Containing 1D Channels as Selective Luminescent Probes[J]. J Am Chem Soc, 2004, 126(47): 15394-15395. doi: 10.1021/ja047141b
-
[10]
Zhang M H, Xin X L, Xiao Z Y. A Multi-Aromatic Hydrocarbon Unit Induced Hydrophobic Metal Organic Framework for Efficient C2/C1 Hydrocarbon and Oil/Water Separation[J]. J Mater Chem A, 2017, 5(3): 1168-1175. doi: 10.1039/C6TA08368D
-
[11]
Xiao B, Wheatley P S, Zhao X B. High-Capacity Hydrogen and Nitric Oxide Adsorption and Storage in a Metal-Organic Framework[J]. J Am Chem Soc, 2007, 129(5): 1203-1209. doi: 10.1021/ja066098k
-
[12]
Rowsell J L C, Yaghi O M. Angew Strategies for Hydrogen Storage in Metal-Organic Framework[J]. Chem Int Ed, 2005, 44(30): 4670-4679. doi: 10.1002/(ISSN)1521-3773
-
[13]
Lan Y Q, Jiang H L, Li S L. Mesoporous Metal-Organic Frameworks with Size-tunable Cages:Selective CO2 Uptake, Encapsulation of Ln3+ Cations for Luminescence, and Column-Chromatographic Dye Separation[J]. Adv Mater, 2011, 23(43): 5015-5020. doi: 10.1002/adma.201102880
-
[14]
Lu X M, Li P Z, Wang X T. pH-Directed Assembly and Magnetic Properties of Two Polynuclear MnⅡ Complexes:(△, Λ)-{Mn3(phen)2(OOCCH3)6} and 1-D[J]. Polyhedron, 2008, 27(18): 3669-3673. doi: 10.1016/j.poly.2008.08.027
-
[15]
Tzeng B C, Yeh H T, Chang T Y. Novel Coordinated-Solvent Induced Assembly of Cd(Ⅱ) Coordination Polymers Containing 4, 4'-Dipyridylsulfide[J]. Cryst Growth Des, 2009, 9(6): 2552-2555. doi: 10.1021/cg900119a
-
[16]
Zou R Q, Amr I A F, Xu H W. Porous Metal-Organic Frameworks Containing Alkali-Bridged Two-Fold Interpenetration:Synthesis, Gas Adsorption, and Fluorescence Properties[J]. Cryst Growth Des, 2010, 10(3): 1301-1306. doi: 10.1021/cg901347p
-
[17]
Li C P, Du M. Role of Solvents in Coordination Supramolecular Systems[J]. Chem Commun, 2011, 47(21): 5958-5972. doi: 10.1039/c1cc10935a
-
[18]
Yin P X, Zhang J, Qin Y Y. Role of Molar-Ratio, Temperature and Solvent on the Zn/Cd 1, 2, 4-Triazolate System with Novel Topological Architectures[J]. CrystEngComm, 2011, 13(10): 3536-3544. doi: 10.1039/c0ce00762e
-
[19]
Beck J S, Vartuli J C, Kennedy G J. Molecular or Supramolecular Templating:Defining the Role of Surfactant Chemistry in the Formation of Microporous and Mesoporous Molecular Sieves[J]. Chem Mater, 1994, 6(10): 1816-1821. doi: 10.1021/cm00046a040
-
[20]
Egeblad K, Christensen C H, Kustova M. Templating Mesoporous Zeolites[J]. Chem Mater, 2008, 20(3): 946-960. doi: 10.1021/cm702224p
-
[21]
Yang X Y, Léonard A, Lemaire A. Self-formation Phenomenon to Hierarchically Structured Porous Materials:Design, Synthesis, Formation Mechanism and Applications[J]. Chem Commun, 2011, 47(10): 2763-2786. doi: 10.1039/c0cc03734f
-
[22]
Li P Z, Wang X J, Li Y X. Co(Ⅱ)-Tricarboxylate Metal-Organic Frameworks Constructed from Solvent-Directed Assembly for CO2 Adsorption[J]. Micropor Mesopor Mater, 2013, 176(10): 194-198.
-
[1]
-
图 3 配合物1和2的XRD对比图(金属离子包含Pb2+、Co2+、Cr3+、Al3+、Ag+、Fe3+、Cd2+、Ca2+、Ba2+、Mg2+)(A)、红外谱图(B)、热重分析图(C)及配合物与配体的固态荧光谱图(D)
Figure 3 XRD patterns(Metal ions include Pb2+, Co2+, Cr3+, Al3+, Ag+, Fe3+, Cd2+, Ca2+, Ba2+, Mg2+)(A), infrared spectra(B), TGA curves(C) of complexes 1 and 2, and the solid-state fluorescence spectra of two complexes and ligands(D)
图 4 分散在不同溶剂中的配合物1的荧光光谱(A); 不同离子对配合物1荧光增强倍数(B); 加入Pb2+离子(0~0.8 mmol/L)后的荧光光谱变化及I/I0值与Pb2+浓度关系图(C); 分析物的Stern-Volmer曲线(D)
Figure 4 The fluorescence spectra of complex 1 dispersed in different solvents(A); fluorescence enhancement ratio of complex ion pair complex 1(B); the change of fluorescence spectrum and the relationship between I/I0 and Pb2+ concentration after adding Pb2+ ions(0~0.8 mmol/L)(C); corresponding Stern-Volmer plots of analytes(D)
Volume of metal ion solution in C/μL:a.0; b.10; c.20; d.30; e.40; f.50; g.60; h.70; i.80; j.90; k.100; l.110; m.120; n.130; o.140; p.150; q.160; r.170; s.180; t.190; u.200
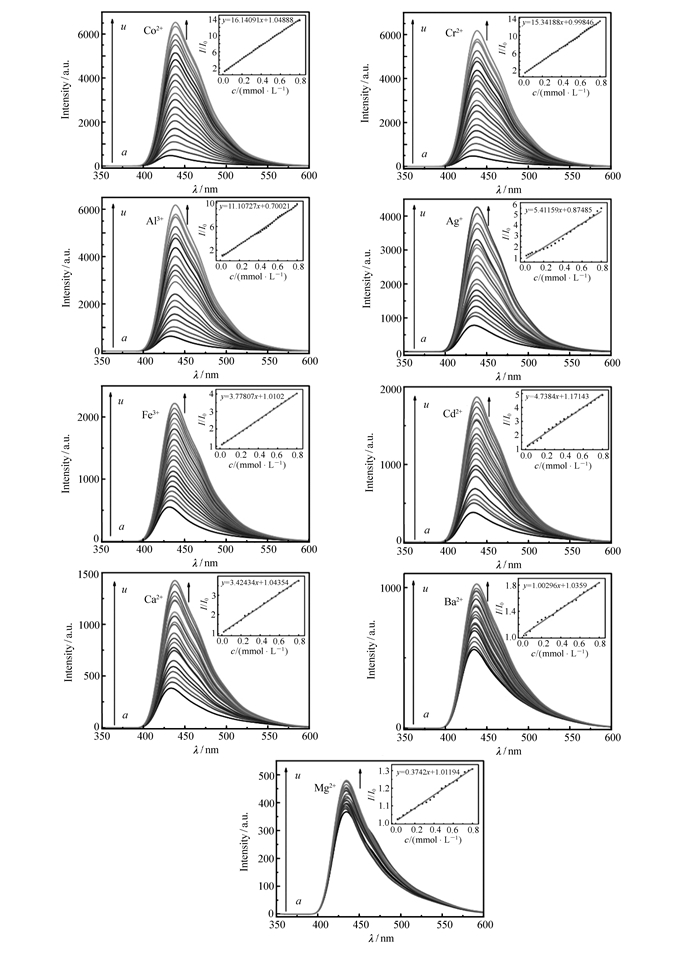
图 5 加入各种离子后的荧光光谱变化及I/I0值与离子浓度关系图
Figure 5 The change of fluorescence spectrum and the relationship between I/I0 and various metal ions concentration
Volume of metal ion solution/μL:a.0; b.10; c.20; d.30; e.40; f.50; g.60; h.70; i.80; j.90; k.100; l.110; m.120; n.130; o.140; p.150; q.160; r.170; s.180; t.190; u.200
图 6 分散在不同溶剂中的配合物2的荧光光谱(A); 不同离子对配合物2荧光增强倍数(B); 加入Pb2+离子(0~0.8 mmol/L)后的荧光光谱变化及I/I0值与Pb2+浓度关系图(C); 分析物的Stern-Volmer曲线(D)
Figure 6 The fluorescence spectra of complex 2 dispersed in different solvents(A); fluorescence enhancement ratio of complex ion pair complex 2(B); the change of fluorescence spectrum and the relationship between I/I0 and Pb2+ concentration after adding Pb2+ ions(0~0.8 mmol/L)(C); corresponding Stern-Volmer plots of analytes(D)
Volume of metal ion solution in C/μL:a.0; b.10; c.20; d.30; e.40; f.50; g.60; h.70; i.80; j.90; k.100; l.110; m.120; n.130; o.140; p.150; q.160; r.170; s.180; t.190; u.200
图 7 加入各种离子后的荧光光谱变化及I/I0值与离子浓度关系图
Figure 7 The change of fluorescence spectrum and the relationship between I/I0 and various metal ions concentration
Volume of metal ion solution/μL:a.0; b.10; c.20; d.30; e.40; f.50; g.60; h.70; i.80; j.90; k.100; l.110; m.120; n.130; o.140; p.150; q.160; r.170; s.180; t.190; u.200
表 1 配合物1和2的晶体学参数表
Table 1. Crytal data and structure refinement of complexes 1 and 2
Compound 1 2 Formula C11H15CuNO8 C29H28Cu2N3O11S Mr 352.78 754.69 Crystal system trigonal orthorhombic Space group R-3 Pbcm a/nm 1.883 85(8) 0.978 64(2) b/nm 1.883 85(8) 2.823 81(5) c/nm 2.242 61(8) 2.476 27(5) α /(°) 90 90 β/(°) 90 90 γ /(°) 120 90 V/nm3 6.892 5(6) 6.843 2(2) Z 18 8 Dc/(g·cm-3) 1.530 1.465 μ /mm-1 1.461 1.363 F(000) 3 258.0 3 088.0 θ range for data collection/(°) 6.176 to 49.984 3.286 to 50.19 Reflections collected 6 148 23 486 Temperature/K 293(2) 150 Data/restraints/parameters 2694/0/198 6271/17/434 Final R indexes [I≥2σ(I)] R1=0.058 0, wR2=0.173 8 R1=0.119 9, wR2=0.354 9 Final R indexes [all data] R1=0.077 9, wR2=0.192 5 R1=0.143 4, wR2=0.378 7 Largest diff. peak/hole/(e·nm-3) 1.51×10-3/-0.43 4.06×10-3/-2.40 a.R1=Σ(‖F0|-|Fc‖)/Σ|F0|; b.wR2=[Σw(|F0|2-|Fc|2)2/Σ(F02)2]1/2. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 27
- 文章访问数: 2389
- HTML全文浏览量: 422



 下载:
下载:







 下载:
下载:

