 图 1
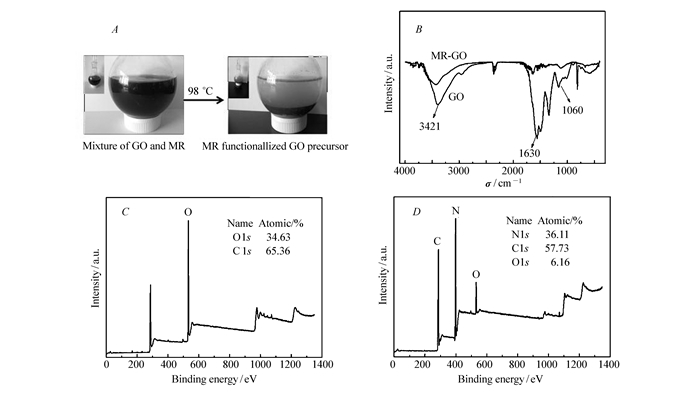
由MR和GO溶液制备功能化GO前驱体过程示意图(A);干燥的GO和MR-GO的红外光谱图(B);GO(C)及MR-GO(D)的XPS谱图
Figure 1.
Scheme of MR-GO synthesis(A); FTIR spectra of dry GO and MR-GO(B); XPS spectra of GO(C) and MR-GO(D)
图 1
由MR和GO溶液制备功能化GO前驱体过程示意图(A);干燥的GO和MR-GO的红外光谱图(B);GO(C)及MR-GO(D)的XPS谱图
Figure 1.
Scheme of MR-GO synthesis(A); FTIR spectra of dry GO and MR-GO(B); XPS spectra of GO(C) and MR-GO(D)

Citation: JIAO Liansheng, MENG Lingju, WU Tongshun, LI Fenghua, NIU Li. Synthesis and Properties of Lithium Vanadium Phosphates/Reduced Graphene Oxide Composite as Cathode Materials[J]. Chinese Journal of Applied Chemistry, 2017, 34(6): 712-722. doi: 10.11944/j.issn.1000-0518.2017.06.160357

磷酸钒锂/石墨烯复合正极材料的制备及表征
English
Synthesis and Properties of Lithium Vanadium Phosphates/Reduced Graphene Oxide Composite as Cathode Materials
-
Key words:
- lithium vanadium phosphate
- / graphene
- / electrode material
- / electrochemical performance
-
锂离子电池已广泛用于便携式电子设备中[1-2],同时由于其具有能量密度大、功率密度较高、使用寿命长等优点,也是混合动力汽车和纯电动汽车的重要驱动能源,在可再生能源存储中也将发挥重要作用[2-3]。锂离子电池正极材料方面,广泛研究的主要包括过渡金属氧化物正极材料如LiCoO2、LiMn2O4以及三元材料,但是这些材料均存在安全问题。由于其优异的热力学稳定性,锂过渡金属磷酸盐引起了广泛的研究兴趣[4-8]。其中研究最多的是LiFePO4,但是LiFePO4材料锂离子扩散系数小,工作电压低限制了其使用时的能量密度。相比之下,单斜结构的磷酸钒锂(Li3V2(PO4)3)具有较高的可逆容量和工作电压,锂离子扩散系数也比较大,是最具潜力的正极材料之一[9-13]。但是Li3V2(PO4)3的电子电导较低,这限制了它的实际应用[14-15]。碳包覆[16-20]、减小颗粒尺寸[21-22]以及金属离子掺杂[23-30]是主要的改性方法。金属离子掺杂虽然可以提高材料的电导率,改善了锂离子脱嵌环境,但是掺杂机理复杂,经常产生杂相,且难以避免金属离子在充放电过程中的溶解。因此采用碳包覆和减小颗粒尺寸是改善其性能的最为有效的方法。二维碳纳米材料石墨烯,由于具有极高的导电性和较高的比表面积,已经广泛用作锂离子电池材料的添加剂来改善材料的电化学性能[22, 31-33]。很多学者尝试用石墨烯来改善磷酸钒锂的电化学性能[21-22, 33-37],但是采用的方法涉及到微波、水热以及冷冻干燥等,过程比较繁琐且制备成本较高,同时石墨烯片层在后续热还原处理以及充放电过程中容易产生堆叠,影响了其性能的发挥。Choi等[38]利用三聚氰胺甲醛树脂(MR)中的羟基与石墨烯氧化物(GO)中的羟基或羧基发生沉淀反应,制备了堆叠程度较小的石墨烯用于超级电容器的研究,由于消除了石墨烯片层间的氢键作用,能够有效防止石墨烯片层的堆叠,材料展现了较好的电容性能。
本文首先通过三聚氰胺甲醛树脂(MR)中的羟基与石墨烯氧化物(GO)中的羧基发生的沉淀反应来制备功能化的氧化石墨烯前驱体,然后利用溶胶-凝胶及高温热处理方法制备Li3V2(PO4)3/石墨烯复合材料,功能化氧化石墨烯(MR-GO)的防堆叠性质在制备电极材料过程中能够有效保持,也可以使磷酸钒锂颗粒在石墨烯片层中更加均匀分布,可有效防止团聚现象的发生。利用此材料制备的电池电极,由于堆叠程度小的石墨烯网络提供了较好的导电环境以及锂离子较快的电荷传递速度等积极因素的共同作用,电极材料的电化学性能得到了较大改善。
1 实验部分
1.1 仪器和试剂
Bruker D8型X光衍射仪(XRD, 德国Bruker公司),操作条件为CuKα(0.15406 nm)、40 kV和30 mA,扫描范围20°~70°。XL 30 ESEM FEG型扫描电子显微镜(SEM.荷兰FEI公司),加速电压10 kV。Hitachi-600型透射电子显微镜(TEM, 日本Hitachi公司),加速电压100 kV。TGA50H型热重分析仪(TG, 日本岛津公司),升温速度10 ℃/min,温度范围30~750 ℃。Renishaw 2000型光谱仪(英国Renishaw公司),CCD检测器,激发线514.5 nm(氩离子激光器,50 mW)。VG ESCALAB MK II型光谱仪(XPS, 英国VG Scientific Ltd.公司),MgKα作为X射线源(hν=1253.6 eV),用C1s(284.6 eV)校正峰位置。CT-3008型多通道电池测试仪(深圳新威电子有限公司),CHI660D型电化学工作站(上海辰华仪器有限公司),测试幅值为5 mV,频率范围为100 KHz到0.01 Hz。石墨粉(<20 μm,Sigma-Aldrich),过硫酸钾(K2S2O8)、五氧化二磷(P2O5)、高锰酸钾(KMnO4)、硫酸(98%,H2SO4)、双氧水(30%,H2O2)、盐酸(37%,HCl)、三聚氰胺、甲醛水溶液(37%)、偏矾酸铵(NH4VO3)、草酸、磷酸二氢铵(NH4H2PO4)、碳酸锂(Li2CO3)、氮甲基吡咯烷酮(NMP)均为分析纯试剂,购于国药集团化学试剂有限公司(上海),使用前未经纯化。金属锂片、聚丙烯隔离膜(Celgard2400)、铝箔、聚偏氟乙烯(PVDF)购于合肥科晶材料技术有限公司,实验所用水均为Millipore系统纯化过的去离子水(≥18 MΩ·cm)。
1.2 GO、MR功能化GO前驱体制备
利用改进的Hummer法制备GO[39],透析7 d后得到浓度为4.0 g/L的GO溶液。然后按照文献[38]方法制备MR功能化GO前驱体。取20 mL GO溶液并超声分散30 min。在100 mL烧瓶中加入1.0 g三聚氰胺、1.77 mL甲醛水溶液以及15 mL去离子水,油浴加热到70 ℃直到溶液透明,再加入超声分散后的GO溶液,继续加热到98 ℃并保持3 h。此过程中MR中的羟基与GO片层上的羟基或羧基发生反应,消除了GO片层之间的氢键,从而形成MR功能化的GO沉淀物(见反应式(1))。
这样石墨烯片层的堆叠得到抑制,在后续的热处理过程中形貌也可得以保持。沉淀物用去离子水充分洗涤后在60 ℃下真空干燥24 h,得到MR功能化的GO前驱体MR-GO。
1.3 磷酸钒锂/石墨烯复合物的制备
磷酸钒锂/石墨烯复合物通过改进的溶胶-凝胶法制备。首先将NH4VO3、草酸、NH4H2PO4、Li2CO3按照化学计量比2:4:3:3.15分别称取0.6233、1.2360、0.8462和0.2854 g加到100 mL去离子水中,60 ℃下加热溶解直到形成透明溶液,草酸主要起络合作用。然后加入适量MR功能化的GO前驱体,继续加热到80 ℃,磁力搅拌得到均匀凝胶,GO前驱体的加入量由最后得到的复合物中碳含量确定,凝胶80 ℃下真空干燥12 h。干燥产物充分研磨后置于管式炉中350 ℃下预处理5 h,再在750 ℃下煅烧9 h,Ar和H2(体积比为94:6) 做保护气氛。作为比较,未功能化的GO经冷冻干燥后同样按照此步骤合成磷酸钒锂复合物。
1.4 磷酸钒锂/石墨烯电极的制备及电化学性能表征
将Li3V2(PO4)3活性材料、导电炭黑、PVDF按质量比80:10:10的比例用氮甲基吡咯烷酮(NMP)调制成适当粘度的浆料,再用涂膜器涂覆在铝箔上,70 ℃下干燥6 h后再120 ℃真空干燥12 h。涂好样品的铝箔辊压后冲制成直径12 mm的电极片待用,活性物质质量约为3~4 mg/cm。然后,在手套箱中(O2和H2O体积分数均低于1×10-6)组装成2032型纽扣电池,电解液是广州天赐高新材料股份有限公司生产的,组成为1.0 mol/L LiPF6/EC+DMC(EC:碳酸乙烯酯;DMC:碳酸二甲酯。体积比1:1)。Celgard2400聚丙烯膜做为隔离膜,金属锂片做为对电极。将扣式电池置于深圳Neware的CT-3008多通道电池测试仪上进行循环及倍率测试,电压测试范围根据实验分别为3.0~4.3 V和3.0~4.8 V。为了比较不同石墨烯前驱体合成的复合材料扣式电池内阻的大小,将电池循环1次后再充至4.0 V,静置后在电化学工作站进行交流阻抗谱测试。
2 结果与讨论
2.1 结构表征
图 1A是MR与GO溶液在98 ℃下反应制备MR-GO前驱体照片。图 1B是干燥的GO和MR-GO的红外吸收谱图。由图 1B可知,反应后3421 cm-1处对应于羟基的伸缩振动峰,1630 cm-1处氧化石墨烯吸收的水分子的—OH弯曲振动峰以及1060 cm-1处C—OH的振动峰的强度都大幅度减小,说明MR中的羟基已经与GO片层上的羟基或羧基发生反应,含氧官能团大量减少。图 1C和1D分别是GO和MR-GO的XPS谱图,GO样品中氧的相对原子百分含量为34.64%,而前驱体MR-GO中氧含量大幅下降,仅有6.16%。这进一步证明了MR中的羟基与GO片层上的羟基或羧基发生反应,从而部分地消除了GO片层之间的氢键,这与Choi等[38]的结论是一致的。
 图 1
由MR和GO溶液制备功能化GO前驱体过程示意图(A);干燥的GO和MR-GO的红外光谱图(B);GO(C)及MR-GO(D)的XPS谱图
Figure 1.
Scheme of MR-GO synthesis(A); FTIR spectra of dry GO and MR-GO(B); XPS spectra of GO(C) and MR-GO(D)
图 1
由MR和GO溶液制备功能化GO前驱体过程示意图(A);干燥的GO和MR-GO的红外光谱图(B);GO(C)及MR-GO(D)的XPS谱图
Figure 1.
Scheme of MR-GO synthesis(A); FTIR spectra of dry GO and MR-GO(B); XPS spectra of GO(C) and MR-GO(D)
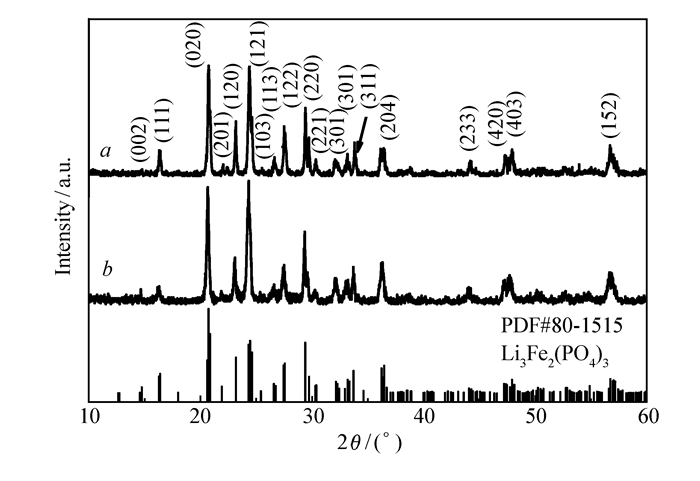
图 2是磷酸钒锂与MR-GO及GO分别复合后材料的XRD图谱。在20.7°、24.4°和29.4°的衍射峰(2θ)归属为单斜结构的Li3V2(PO4)3,与同为单斜结构的Li3Fe2(PO4)3(PDF#80-1515) 相同,空间群为P21/n,也与文献[9, 21-22]报道的一致。因此在实验条件下得到的两种材料是纯相结构的Li3V2(PO4)3,且没有出现碳材料的衍射峰,说明样品中的碳为无定形碳,这可以由拉曼光谱进一步证实。
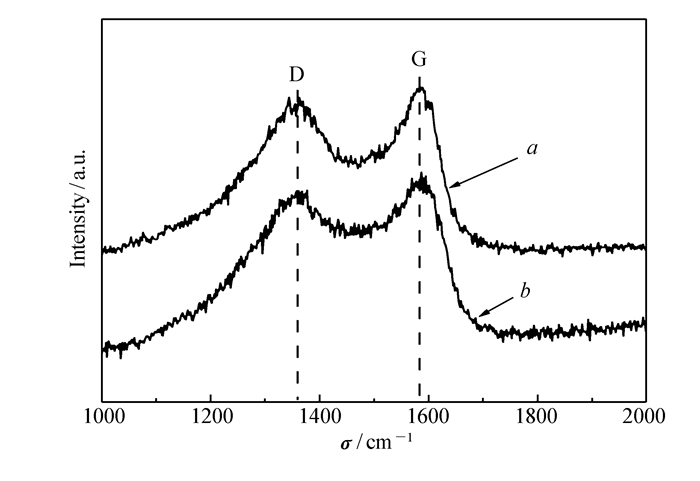
众所周知,因为碳材料有拉曼活性的E2g振动模式,有很强的拉曼散射,所以拉曼光谱普遍用于研究碳材料存在与否以及晶态。如图 3所示,位于1358 cm-1(D band, disordered)和1590 cm-1(G band, graphitic)的散射峰没有完全分开,说明两种复合材料中的碳是无定形的[40-41]。此外,750 ℃下产生的碳材料也通常是无定形的无序相。
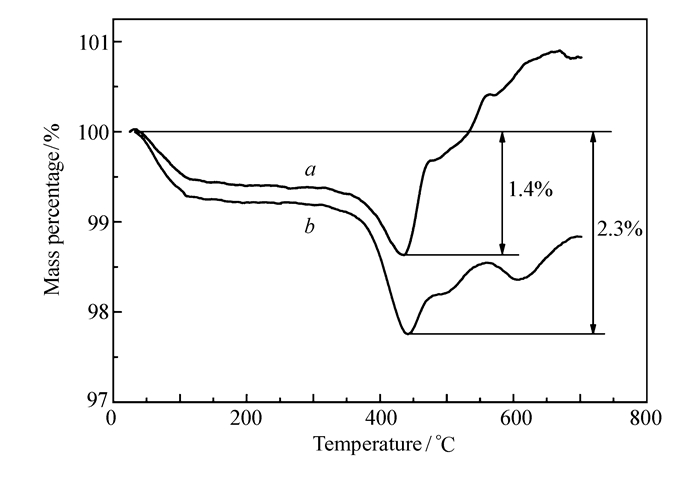
复合材料中的碳含量由热重分析得到,如图 4所示。根据芮等[16]的报道,在300~450 ℃温度范围内,复合材料的失重归因于碳氧化成(CO或CO2),450 ℃以上有个增重的过程,对应V(Ⅲ)在空气中的氧化。根据热重曲线的失重步骤,Li3V2(PO4)3/rGO和Li3V2(PO4)3/rMR-GO复合材料的碳质量分数分别为1.4%和2.3%,较低的含碳量可以有效提高活性材料的含量,这对提高能量密度是有利的,但是过低的碳含量也会导致功率密度的降低。在本文中综合考虑能量密度和功率密度以及循环性能,我们选择含量为2.3%的材料作为主要研究对象。而在生产中要结合实际的需要进行相应的优选。
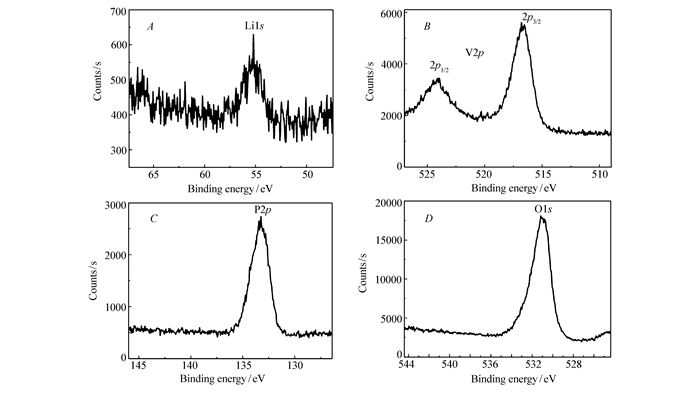
XPS测试结果(图 5)可以给出材料中组成元素及相应的价态信息。结合能55 eV处的峰强度虽然较弱,但是却很清晰,对应于Li的1s[42]。V2p芯能级谱中存在双峰,结合能为516.8和523.9 eV,分别对应V的2p3/2和2p1/2, 说明复合物中V3+是V元素的存在价态[43]。P2p只出现一个单峰,结合能为133.3 eV,说明P只有一种存在环境,即(PO4)3-基团[42]。此外,O1s峰结合能为531.1 eV,也证明了(PO4)3-基团的存在。
图 6A和6B是Li3V2(PO4)3/rMR-GO复合材料的SEM和TEM照片,图 6C和6D是Li3V2(PO4)3/rGO复合材料的SEM和TEM照片。可见,石墨烯功能化后,Li3V2(PO4)3颗粒在卷曲的石墨烯片中的分散更加均匀,这一方面可以极大改善材料的电子电导,同时也可以部分防止Li3V2(PO4)3颗粒的团聚。
图 7是Li3V2(PO4)3/rMR-GO复合材料的SEM-EDS元素分布图。由图 7可见,V、O、P等元素与C元素分布均匀,说明Li3V2(PO4)3均匀分布在石墨烯构成的三维导电网络之中,这与TEM结果相符合。这主要是因为实验过程中草酸作为络合剂,可以很容易地制备出均匀的前驱体。MR既可以实现GO的功能化防止其堆叠,又可以增加反应物之间的接触面积,这些均有助于均匀形貌的形成。而且这种形貌也增大了电解液与电极材料间的接触面积,在增加电子导电性的同时也缩短了锂离子的扩散路径,对材料的电化学性能有显著的影响。
2.2 电化学表征
将Li3V2(PO4)3/rGO和Li3V2(PO4)3/rMR-GO复合材料组装的电池在0.1 C下进行充放电测试,电压区间3.0~4.3 V(vs.Li+/Li)。图 8A和8B分别是电池的首次循环和第100次循环的充放电曲线比较,两种材料的首次曲线没有明显的区别,但100个循环后,Li3V2(PO4)3/rMR-GO复合材料仍能保持较好的充放电电压平台,比容量也优于普通的Li3V2(PO4)3/rGO材料。充电曲线上出现3.59、3.68和4.08 V三个电压平台,分别对应于LixV2(PO4)3从x=3.0到2.5,2.0以及1.0时锂离子的脱出和发生的相变过程。由于存在一个有序相Li2.5V2(PO4)3,第一个Li的脱出分两步进行,对应平台电压3.59和3.68 V。第二个Li的脱出一步完成,平台电压4.08 V,形成的Li1.0V2(PO4)3相保持了晶格的单斜结构对称性[14]。放电曲线上也有3个电压平台,分别是4.05、3.65和3.57 V,对应于LixV2(PO4)3从x=1.0到1.5,2.0以及3.0时2个锂离子的可逆嵌入和发生的相变过程,这与文献[22, 36-44]报道的一致。由充放电曲线得到的微分电容曲线可以更好地描述这一过程。
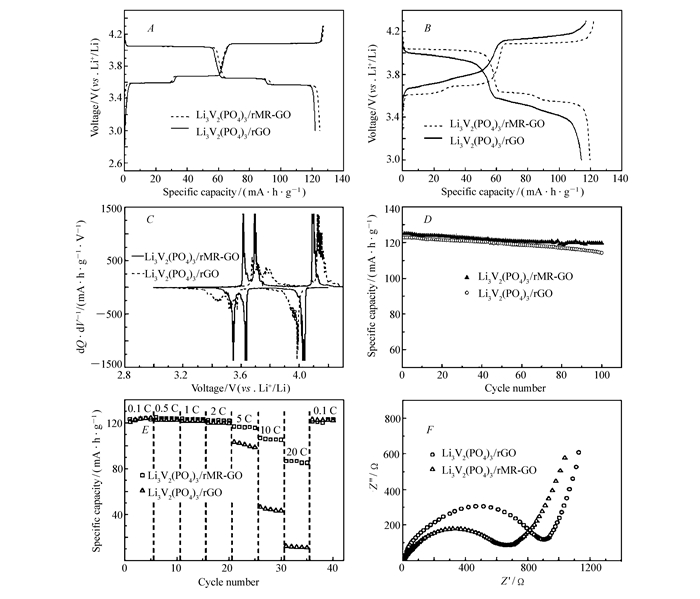 图 8
磷酸钒锂与不同石墨烯材料复合后材料的恒流充放电曲线比较第1次(A);第100次(B);第100次微分电容曲线比较(C);0.1 C循环性能比较(D);倍率性能比较(E);交流阻抗谱比较(F)
Figure 8.
Galvanostatic charge-discharge curves of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composites for the first cycle(A) and the 100th cycle(B) measured at 0.1C between the voltage limits of 3.0~4.3 V vs.Li+/Li; Differential capacity curves of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite for the 100th cycle(C); Cycling performances of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composites measured at 0.1 C between the voltage limits of 3.0~4.3 V vs.Li+/Li(D); Rate capability of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite at various discharge rates from 0.1 C to 20 C(E); Impedance measurements(Nyquist plot) of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite electrodes. All the measurements were performed after one cycle activation and once more charged to about 4.0 V(F)
图 8
磷酸钒锂与不同石墨烯材料复合后材料的恒流充放电曲线比较第1次(A);第100次(B);第100次微分电容曲线比较(C);0.1 C循环性能比较(D);倍率性能比较(E);交流阻抗谱比较(F)
Figure 8.
Galvanostatic charge-discharge curves of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composites for the first cycle(A) and the 100th cycle(B) measured at 0.1C between the voltage limits of 3.0~4.3 V vs.Li+/Li; Differential capacity curves of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite for the 100th cycle(C); Cycling performances of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composites measured at 0.1 C between the voltage limits of 3.0~4.3 V vs.Li+/Li(D); Rate capability of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite at various discharge rates from 0.1 C to 20 C(E); Impedance measurements(Nyquist plot) of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite electrodes. All the measurements were performed after one cycle activation and once more charged to about 4.0 V(F)
微分电容曲线也可用于锂电池材料的电化学性能研究[45],恒流充放电曲线上的电压平台对应于电容曲线上的尖峰。如图 8C是Li3V2(PO4)3/rMR-GO和Li3V2(PO4)3/rGO在0.1 C恒流充放电100次后的微分电容曲线,Li3V2(PO4)3/rGO样品的电压平台已不明显,峰峰电位差比较大说明极化程度大。相比之下,Li3V2(PO4)3/rMR-GO的充放电平台清晰且电压之差均小于0.07 V,说明经过100次循环后电池可逆性良好,电极材料极化程度小也说明电子和离子的传输速度比较快,这也得益于电池材料优良的结构设计。
0.1 C下的循环性能如图 8D所示,Li3V2(PO4)3/rMR-GO和Li3V2(PO4)3/rGO材料的首次放电(嵌锂)容量分别为127.4和126.8 mA·h/g。循环100次后Li3V2(PO4)3/rMR-GO的可逆容量为119.6 mA·h/g,容量保持率94%。相比之下,Li3V2(PO4)3/rGO的容量衰减较大,100次后容量为114.2 mA·h/g,容量保持率仅为90%。不同电流密度下的倍率性能如图 8E所示,在0.1、0.5、1、2、5、10和20 C下,Li3V2(PO4)3/rMR-GO的可逆容量分别为124.1、123.8、123.2、122.1、115.7、105.1和86.7 mA·h/g。特别是在5、10和20 C的高倍率下,Li3V2(PO4)3/rMR-GO的性能明显优于Li3V2(PO4)3/rGO,后者的可逆容量分别是100.9、44.4和11.5 mA·h/g。这可能是由于Li3V2(PO4)3颗粒在石墨烯网络中分散良好,电子电导较大,且石墨烯片层堆叠程度小,从而使得锂离子扩散路径缩短。为了进一步说明这一点,我们测试了扣式电池的电化学交流阻抗谱,如图 8F所示。电池先循环0.1 C循环1次,然后充电到4.0 V并恒压静置5 h后测试。两电池的阻抗谱都是由高频区的半圆和低频区的斜线组成,高频区的小截距表示溶液电阻,高频区的半圆是锂离子通过电极材料与电解质界面层的电荷传递电阻,低频区的斜线则代表锂离子在电极材料内扩散的Warburg阻抗。与Li3V2(PO4)3/rGO相比,Li3V2(PO4)3/rMR-GO的电荷传递电阻更小,表明堆叠程度小的石墨烯网络提供了较好的导电环境,改善了颗粒之间的电接触,锂离子的电荷传递速度较快,从而有利于改善材料的电化学性能。
此外,又考察了MR功能化GO前驱体的添加量对材料性能的影响。当前驱体与Li3V2(PO4)3质量比为0.3:1、0.45:1和0.6:1时,最终产物的碳质量分数分别为0.9%、2.3%和5.5%。相应的0.1 C电流密度下首次充放电曲线以及循环100次的性能比较如图 9所示。3个样品的首次容量分别为127.4、119.3和124.5 mA·h/g。质量比为0.3:1时的曲线极化较大,容量和循环性能也不理想。而质量比达到0.6:1时,极化虽然不大,但是容量较小。这可能是因为质量比较小时,Li3V2(PO4)3颗粒的碳包覆程度较低,样品的导电性较差。而质量比太大时,较高的含碳量使得有效的Li3V2(PO4)3活性物质量减少,降低了材料的容量。
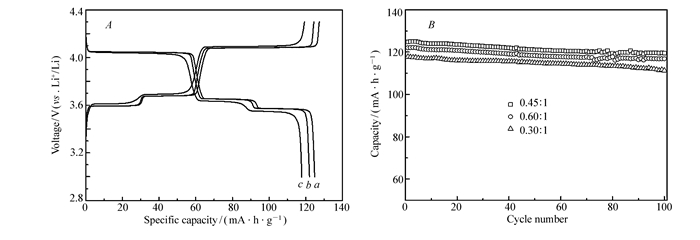 图 9
MR-GO前驱体与磷酸钒锂不同质量比0.1 C时首次充放电曲线(A);0.1 C循环性能比较(B)
Figure 9.
(A)Galvanostatic charge-discharge curves of Li3V2(PO4)3/rMR-GO composite for the first cycle (B)Cycling performance of Li3V2(PO4)3/rMR-GO composite measured at 0.1 C between the voltage limits of 3.0~4.3 V vs.Li+/Li at 0.45:1(a), 0.60:1(b) and 0.30:1(c) mass ratios of MR-GO precursor and Li3V2(PO4)3
图 9
MR-GO前驱体与磷酸钒锂不同质量比0.1 C时首次充放电曲线(A);0.1 C循环性能比较(B)
Figure 9.
(A)Galvanostatic charge-discharge curves of Li3V2(PO4)3/rMR-GO composite for the first cycle (B)Cycling performance of Li3V2(PO4)3/rMR-GO composite measured at 0.1 C between the voltage limits of 3.0~4.3 V vs.Li+/Li at 0.45:1(a), 0.60:1(b) and 0.30:1(c) mass ratios of MR-GO precursor and Li3V2(PO4)3
组装的扣式电池也在3.0~4.8 V的电压区间进行了循环和倍率性能测试(见图 10),由于堆叠程度小的石墨烯网络提供了较好的导电环境以及锂离子较快的电荷传递速度等积极因素的共同作用,使得Li3V2(PO4)3/rMR-GO复合材料的性能也优于Li3V2(PO4)3/rGO材料。与文献[37, 46-53]中报道的数据相比较,材料的综合电化学性能优异(见表 1)。但是相比于电压区间3.0~4.3 V的情况,循环过程中容量的衰减都比较大,这主要是因为在高电压下电解液的氧化导致电极/电解质界面层不稳定所致[9]。要防止此种现象,必须开发出合适的电解质溶液体系。
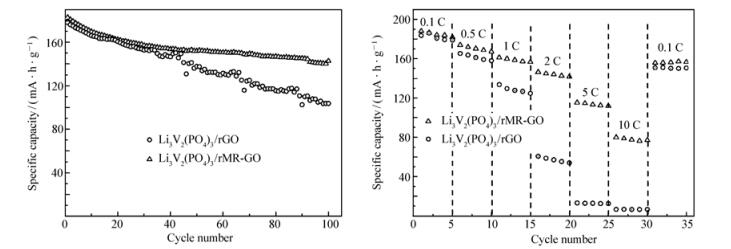 图 10
磷酸钒锂与不同石墨烯材料复合后材料的循环性能比较(A);倍率性能比较(B)。测试电压区间3~4.8 V
Figure 10.
Cycling performance of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite measured at 0.2 C between the voltage limits of 3.0~4.8 V vs.Li+/Li(A) and rate capability of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite at various discharge rates from 0.1 C to 10 C between the voltage limits of 3.0~4.8 V vs.Li+/Li(B)
图 10
磷酸钒锂与不同石墨烯材料复合后材料的循环性能比较(A);倍率性能比较(B)。测试电压区间3~4.8 V
Figure 10.
Cycling performance of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite measured at 0.2 C between the voltage limits of 3.0~4.8 V vs.Li+/Li(A) and rate capability of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite at various discharge rates from 0.1 C to 10 C between the voltage limits of 3.0~4.8 V vs.Li+/Li(B)
3 结论
利用三聚氰胺甲醛树脂与石墨烯氧化物发生的沉淀反应制备出功能化的石墨烯氧化物,继而通过改进的溶胶凝胶法制备Li3V2(PO4)3/rMR-GO复合材料,并利用此材料制备了电池电极,由于堆叠程度小的石墨烯导电网络的构建,改善了锂离子的传输环境,增大了锂离子的扩散速度和电子电导率,在常规电解质溶液允许的电压区间内,材料的循环性能和倍率性能均有较大程度的提高。在3.0~4.3 V的区间内20 C倍率仍有86 mA·h/g的可逆容量,0.1 C循环100次后容量为119.7 mA·h/g。在3.0~4.8 V的高电压区间内10 C倍率下可逆容量为80 mA·h/g,0.1 C循环100次后容量约为145.6 mA·h/g。如果开发出适合高电压的电解质溶液体系,则磷酸钒锂中的3个锂离子都可以实现可逆脱嵌,比容量将有显著的提高,继而可以提高电池整体的能量密度。
-
-
[1]
Bruce P G, Scrosati B, Tarascon J M. Nanomaterials for Rechargeable Lithium Batteries[J]. Angew Chem Int Ed, 2008, 47(16): 2930-2946. doi: 10.1002/(ISSN)1521-3773
-
[2]
Ji L, Lin Z, Alcoutlabi M. Recent Developments in Nanostructured Anode Materials for Rechargeable Lithium-Ion Batteries[J]. Energy Environ Sci, 2011, 4(8): 2682-2690. doi: 10.1039/c0ee00699h
-
[3]
Tarascon J M, Armand M. Issues and Challenges Facing Rechargeable Lithium Batteries[J]. Nature, 2001, 414(6861): 359-367. doi: 10.1038/35104644
-
[4]
Martha S K, Grinblat J, Haik O. LiMn0.8Fe0.2PO4:An Advanced Cathode Material for Rechargeable Lithium Batteries[J]. Angew Chem Int Ed, 2009, 48(45): 8559-8563. doi: 10.1002/anie.v48:45
-
[5]
Saıdi M Y, Barker J, Huang H. Electrochemical Properties of Lithium Vanadium Phosphate as a Cathode Material for Lithium-Ion Batteries[J]. Electrochem Solid-State Lett, 2002, 5(7): A149-A151. doi: 10.1149/1.1479295
-
[6]
Pan A, Liu J, Zhang J G. Nano-structured Li3V2(PO4)3/Carbon Composite for High-rate Lithium-Ion Batteries[J]. Electrochem Commun, 2010, 12(12): 1674-1677. doi: 10.1016/j.elecom.2010.09.014
-
[7]
Yin S C, Grondey H, Strobel P. Charge Ordering in Lithium Vanadium Phosphates:Electrode Materials for Lithium-Ion Batteries[J]. J Am Chem Soc, 2003, 125(2): 326-327. doi: 10.1021/ja028973h
-
[8]
Wu X B, Wu X H, Guo J H, et al. Polyanion Compounds as Cathode Materials for Li-Ion Batteries, in Rechargeable Batteries:Materials, Technologies and New Trends[M]. Springer International Publishing:Cham. 2015:93-134.
-
[9]
Huang H, Yin S C, Kerr T. Nanostructured Composites:A High Capacity, Fast Rate Li3V2(PO4)3/Carbon Cathode for Rechargeable Lithium Batteries[J]. Adv Mater, 2002, 14(21): 1525-1528. doi: 10.1002/1521-4095(20021104)14:21<1525::AID-ADMA1525>3.0.CO;2-3
-
[10]
Gaubicher J, Wurm C, Goward G. Rhombohedral Form of Li3V2(PO4)3 as a Cathode in Li-Ion Batteries[J]. Chem Mater, 2000, 12(11): 3240-3242. doi: 10.1021/cm000345g
-
[11]
Li Y, Bai W Q, Zhang Y D. Synthesis and Electrochemical Performance of Lithium Vanadium Phosphate and Lithium Vanadium Oxide Composite Cathode Material for Lithium Ion Batteries[J]. J Power Sources, 2015, 282: 100-108. doi: 10.1016/j.jpowsour.2015.02.051
-
[12]
B ckenfeld N, Balducci A. On the Use of Lithium Vanadium Phosphate in High Power Devices[J]. J Power Sources, 2013, 235: 265-273. doi: 10.1016/j.jpowsour.2013.02.019
-
[13]
Liu C, Massé R, Nan X. A Promising Cathode for Li-ion Batteries:Li3V2(PO4)3[J]. Energy Storage Mater, 2016, 4: 15-58. doi: 10.1016/j.ensm.2016.02.002
-
[14]
Yin S C, Grondey H, Strobel P. Electrochemical Property:Structure Relationships in Monoclinic Li3-yV2(PO4)3[J]. J Am Chem Soc, 2003, 125(34): 10402-10411. doi: 10.1021/ja034565h
-
[15]
Zheng J C, Li X H, Wang Z X. Li3V2(PO4)3/C Composite Material with Porous Structure and Nano-carbon Webs Synthesized Through Liquid Nitrogen Quenching[J]. Chem Lett, 2009, 38(8): 818-819. doi: 10.1246/cl.2009.818
-
[16]
Rui X H, Li C, Chen C H. Synthesis and Characterization of Carbon-coated Li3V2(PO4)3 Cathode Materials with Different Carbon Sources[J]. Electrochim Acta, 2009, 54(12): 3374-3380. doi: 10.1016/j.electacta.2009.01.011
-
[17]
Zhang J F, Wang X W, Zhang B. Multicore-shell Carbon-coated Lithium Manganese Phosphate and Lithium Vanadium Phosphate Composite Material with High Capacity and Cycling Performance for Lithium-Ion Battery[J]. Electrochim Acta, 2015, 169: 462-469. doi: 10.1016/j.electacta.2015.03.091
-
[18]
Liu Y, Wang S, Tao D. Electrochemical Characterization for Lithium Vanadium Phosphate with Different Calcination Temperatures Prepared by the Sol-gel Method[J]. Mater Charact, 2015, 107: 189-196. doi: 10.1016/j.matchar.2015.07.014
-
[19]
Wu Y, Zhao X, Song Z. Effect of Process Medium on the Synthesis of Carbon Coated Lithium Vanadium Phosphate Composite Using Rheological Phase Reaction Method[J]. J Power Sources, 2015, 274: 782-790. doi: 10.1016/j.jpowsour.2014.10.089
-
[20]
Yan H, Chen W, Wu X. Conducting Polyaniline-wrapped Lithium Vanadium Phosphate Nanocomposite as High-rate and Cycling Stability Cathode for Lithium-Ion Batteries[J]. Electrochim Acta, 2014, 146: 295-300. doi: 10.1016/j.electacta.2014.09.040
-
[21]
Pei B, Jiang Z, Zhang W. Nanostructured Li3V2(PO4)3 Cathode Supported on Reduced Graphene Oxide for Lithium-Ion Batteries[J]. J Power Sources, 2013, 239: 475-482. doi: 10.1016/j.jpowsour.2013.03.171
-
[22]
Cheng B, Zhang X D, Ma X H. Nano-Li3V2(PO4)3 Enwrapped into Reduced Graphene Oxide Sheets for Lithium-Ion Batteries[J]. J Power Sources, 2014, 265: 104-109. doi: 10.1016/j.jpowsour.2014.04.046
-
[23]
Mateyshina Y G, Uvarov N F. Electrochemical Behavior of Li3-xM'xV2-yM″y(PO4)3(M'=K, M″=Sc, Mg+Ti)/C Composite Cathode Material for Lithium-Ion Batteries[J]. J Power Sources, 2011, 196: 1494-1497. doi: 10.1016/j.jpowsour.2010.08.078
-
[24]
Sun H B, Zhang L L, Yang X L. Effect of Fe-Doping Followed by C+SiO2 Hybrid Layer Coating on Li3V2(PO4)3 Cathode Material for Lithium-Ion Batteries[J]. Ceram Int,, 2016, 42(15): 16557-16562. doi: 10.1016/j.ceramint.2016.07.075
-
[25]
Luo Y, He L H, Liu X H. Effect of Mg Doping on Electrochemical Performance of Li3V2(PO4)3/C Cathode Material for Lithium Ion Batteries[J]. Trans Nonferrous Met Soc China, 2015, 25(7): 2266-2271. doi: 10.1016/S1003-6326(15)63840-7
-
[26]
Liu L, Qiu Y, Mai Y. Influences of Neodymium Doping on Magnetic and Electrochemical Properties of Li3V2(PO4)3/C Synthesized Via a Sol-Gel Method[J]. J Power Sources, 2015, 295: 246-253. doi: 10.1016/j.jpowsour.2015.06.121
-
[27]
Liu L, Lei X, Tang H. Influences of La Doping on Magnetic and Electrochemical Properties of Li3V2(PO4)3/C Cathode Materials for Lithium-Ion Batteries[J]. Electrochim Acta, 2015, 151: 378-385. doi: 10.1016/j.electacta.2014.11.052
-
[28]
Yang X, Jun L, Jia H. Study on Structure and Electrochemical Performance of Tm3+-doped Monoclinic Li3V2(PO4)3/C Cathode Material for Lithium-Ion Batteries[J]. Electrochim Acta, 2014, 150: 62-67. doi: 10.1016/j.electacta.2014.10.133
-
[29]
Wang Y, Wang L, Hou Z. Effects of Nd-Doping on the Structure and Electrochemical Properties of Li3V2(PO4)3/C Synthesized Using a Microwave Solid-State Route[J]. Solid State Ionics, 2014, 261: 11-16. doi: 10.1016/j.ssi.2014.03.027
-
[30]
Yang Y, Xu W, Guo R. Synthesis and Electrochemical Properties of Zn-doped, Carbon Coated Lithium Vanadium Phosphate Cathode Materials for Lithium-Ion Batteries[J]. J Power Sources, 2014, 269: 15-23. doi: 10.1016/j.jpowsour.2014.07.005
-
[31]
Zhou X, Yin Y X, Wan L J. Facile Synthesis of Silicon Nanoparticles Inserted into Graphene Sheets as Improved Anode Materials for Lithium-Ion Batteries[J]. Chem Commun, 2012, 48(16): 2198-2200. doi: 10.1039/c2cc17061b
-
[32]
Guzman R C, Yang J, Cheng M C. Effects of Graphene and Carbon Coating Modifications on Electrochemical Performance of Silicon Nanoparticle/Graphene Composite Anode[J]. J Power Sources, 2014, 246: 335-345. doi: 10.1016/j.jpowsour.2013.07.100
-
[33]
Zhang L, Wang S, Cai D. Li3V2(PO4)3@C/Graphene Composite with Improved Cycling Performance as Cathode Material for Lithium-Ion Batteries[J]. Electrochim Acta, 2013, 91: 108-113. doi: 10.1016/j.electacta.2012.12.098
-
[34]
Sun D, Li J, Mai J. Application of Monoclinic Graphene-decorated Li3V2(PO4)3/C Nanocrystals as an Ultra-High-Rate Cathode for Lithium-Ion Batteries[J]. Ceram Int, 2016, 42(6): 7390-7396. doi: 10.1016/j.ceramint.2016.01.142
-
[35]
Cui K, Hu S, Li Y. Nitrogen-doped Graphene Nanosheets Decorated Li3V2(PO4)3/C Nanocrystals as High-Rate and Ultralong Cycle-Life Cathode for Lithium-Ion Batteries[J]. Electrochim Acta, 2016, 210: 45-52. doi: 10.1016/j.electacta.2016.05.099
-
[36]
Wang Z, Guo H, Yan P. In-situ Synthesis of Reduced Graphene Oxide Modified Lithium Vanadium Phosphate for High-Rate Lithium-Ion Batteries via Microwave Irradiation[J]. Electrochim Acta, 2015, 174: 26-32. doi: 10.1016/j.electacta.2015.05.154
-
[37]
Rai A K, Thi T V, Gim J. Li3V2(PO4)3/Graphene Nanocomposite as a High Performance Cathode Material for Lithium Ion Battery[J]. Ceram Int, 2015, 41(1, Part A): 389-396. doi: 10.1016/j.ceramint.2014.08.082
-
[38]
Lee J H, Park N, Kim B G. Restacking-Inhibited 3D Reduced Graphene Oxide for High Performance Supercapacitor Electrodes[J]. ACS Nano, 2013, 7(10): 9366-9374. doi: 10.1021/nn4040734
-
[39]
Gan S, Zhong L, Wu T. Spontaneous and Fast Growth of Large-area Graphene Nanofilms Facilitated by Oil/Water Interfaces[J]. Adv Mater, 2012, 24(29): 3958-3964. doi: 10.1002/adma.v24.29
-
[40]
Jung D S, Ryou M H, Sung Y J. Recycling Rice Husks for High-capacity Lithium Battery Anodes[J]. Proc Nat Acad Sci USA, 2013, 110(30): 12229-12234. doi: 10.1073/pnas.1305025110
-
[41]
Evanoff K, Magasinski A, Yang J. Nanosilicon-coated Graphene Granules as Anodes for Li-Ion Batteries[J]. Adv Energy Mater, 2011, 1(4): 495-498. doi: 10.1002/aenm.201100071
-
[42]
Dedryvère R, Maccario M, Croguennec L. X-Ray Photoelectron Spectroscopy Investigations of Carbon-coated LixFePO4 Materials[J]. Chem Mater, 2008, 20(22): 7164-7170. doi: 10.1021/cm801995p
-
[43]
Ren M, Zhou Z, Li Y. Preparation and Electrochemical Studies of Fe-doped Li3V2(PO4)3 Cathode Materials for Lithium-Ion Batteries[J]. J Power Sources, 2006, 162: 1357-1362. doi: 10.1016/j.jpowsour.2006.08.008
-
[44]
Rui X H, Li C, Liu J. The Li3V2(PO4)3/C Composites with High-rate Capability Prepared by a Maltose-based Sol-Gel Route[J]. Electrochim Acta, 2010, 55: 6761-6767. doi: 10.1016/j.electacta.2010.05.093
-
[45]
Hatzikraniotis E, Mitsas C L, Siapkas D I. Differential Capacity Analysis, a Tool to Examine the Performance of Graphites for Li-Ion Cells. In Materials for Lithium-Ion Batteries[M]. Julien, C., Stoynov, Z., Eds. Springer Netherlands:Dordrecht, 2000:529-534.
-
[46]
Xi Y, Zhang Y, Su Z. Microwave Synthesis of Li3V2(PO4)3/C as Positive-Electrode Materials for Rechargeable Lithium Batteries[J]. J Alloys Compd, 2015, 628(1): 396-400.
-
[47]
Kee Y, Dimov N, Kobayashi E. Structural and Electrochemical Properties of Fe-and Al-doped Li3V2(PO4)3 for All-Solid-State Symmetric Lithium Ion Batteries Prepared by Spray-Drying-Assisted Carbothermal Method[J]. Solid State Ionics, 2015, 272(1): 138-143.
-
[48]
赵蒙晰, 路中培, 陈林. Li3V2(PO4)3/碳纳米纤维复合材料的制备及其电化学性能研究[J]. 常熟理工学院学报, 2016,30,(2): 32-36. ZHAO Mengxi, LU Zhongpei, CHEN Lin. Electrospun Li3V2(PO4)3/Carbon Nanofiber as Cathode Materials for the High-performance Lithium-Ion Batteries[J]. J Changshu Inst Technol (Nat Sci), 2016, 30(2): 32-36.
-
[49]
张家恒, 陈玲, 莫有德. 锂离子电池Li3V(2-x)Alx(PO4)3正极材料合成及性能研究[J]. 广东化工, 2016,43,(12): 23-24. doi: 10.3969/j.issn.1007-1865.2016.12.011ZHANG Jiaheng, CHEN Ling, MO Youde. Synthesis and Properties of Li3V(2-x)Alx(PO4)3 Cathode Material for Lithium-Ion Battery[J]. Guangdong Chem, 2016, 43(12): 23-24. doi: 10.3969/j.issn.1007-1865.2016.12.011
-
[50]
Yin W M, Zhang T T, Zhu Q. Synthesis and Electrochemical Performance of Li(3-2x)MgxV2(PO4)3/C Composite Cathode Materials for Lithium-Ion Batteries[J]. Trans Nonferrous Met Soc China, 2015, 25(6): 1978-1985. doi: 10.1016/S1003-6326(15)63806-7
-
[51]
夏傲, 黄剑锋, 谈国强. 溶胶-凝胶法合成Li3V2(PO4)3/C复合材料及其合成活化能研究[J]. 陕西科技大学学报(自然科学版), 2015,33,(5): 56-59. XIA Ao, HUANG Jianfeng, TAN Guoqiang. Preparation and Synthesized Activation Energy of Li3V2(PO4)3/C Composites by Sol-Gel Method[J]. J Shanxi Univ Sci Tech (Nat Sci Ed), 2015, 33(5): 56-59.
-
[52]
Luo Y Z, He L H, Liu X H. Effect of Mg Doping on Electrochemical Performance of Li3V2(PO4)3/C Cathode Material for Lithium Ion Batteries[J]. Trans Nonferrous Met Soc China, 2015, 25(7): 2266-2271. doi: 10.1016/S1003-6326(15)63840-7
-
[53]
赖春艳, 魏娇娇, 王保峰. 锂离子电池正极材料Li3V2(PO4)3-MCNTs的合成及电化学性能[J]. 电源技术, 2015,39,(1): 34-36. LAI Chunyan, WEI Jiaojiao, WANG Baofeng. Research on Lithium-Ion Battery Cathode Material Li3V2(PO4)3/MCNTs Synthesis and Electrochemical Performance[J]. Chinese J Power Sources, 2015, 39(1): 34-36.
-
[1]
-
图 8 磷酸钒锂与不同石墨烯材料复合后材料的恒流充放电曲线比较第1次(A);第100次(B);第100次微分电容曲线比较(C);0.1 C循环性能比较(D);倍率性能比较(E);交流阻抗谱比较(F)
Figure 8 Galvanostatic charge-discharge curves of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composites for the first cycle(A) and the 100th cycle(B) measured at 0.1C between the voltage limits of 3.0~4.3 V vs.Li+/Li; Differential capacity curves of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite for the 100th cycle(C); Cycling performances of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composites measured at 0.1 C between the voltage limits of 3.0~4.3 V vs.Li+/Li(D); Rate capability of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite at various discharge rates from 0.1 C to 20 C(E); Impedance measurements(Nyquist plot) of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite electrodes. All the measurements were performed after one cycle activation and once more charged to about 4.0 V(F)
图 9 MR-GO前驱体与磷酸钒锂不同质量比0.1 C时首次充放电曲线(A);0.1 C循环性能比较(B)
Figure 9 (A)Galvanostatic charge-discharge curves of Li3V2(PO4)3/rMR-GO composite for the first cycle (B)Cycling performance of Li3V2(PO4)3/rMR-GO composite measured at 0.1 C between the voltage limits of 3.0~4.3 V vs.Li+/Li at 0.45:1(a), 0.60:1(b) and 0.30:1(c) mass ratios of MR-GO precursor and Li3V2(PO4)3
图 10 磷酸钒锂与不同石墨烯材料复合后材料的循环性能比较(A);倍率性能比较(B)。测试电压区间3~4.8 V
Figure 10 Cycling performance of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite measured at 0.2 C between the voltage limits of 3.0~4.8 V vs.Li+/Li(A) and rate capability of Li3V2(PO4)3/rMR-GO and Li3V2(PO4)3/rGO composite at various discharge rates from 0.1 C to 10 C between the voltage limits of 3.0~4.8 V vs.Li+/Li(B)
表 1 性能比较
Table 1. Comparison of electrochemical performances

-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 2
- 文章访问数: 857
- HTML全文浏览量: 119




 下载:
下载:









 下载:
下载:

