 图 1
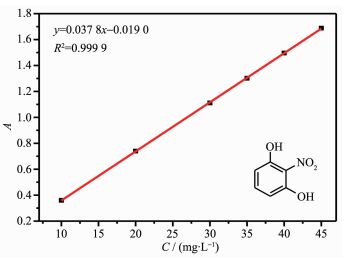
2-硝基-1, 3-苯二酚的标准曲线
Figure 1.
Standard curve for 2-nitroresorcinol
图 1
2-硝基-1, 3-苯二酚的标准曲线
Figure 1.
Standard curve for 2-nitroresorcinol

Citation: YANG Qing-Xiang, REN Shuang-Shuang, ZHAO Qian-Qian, CHEN Zhi-Jun. Synthesis of Magnetic UiO-66 Composites for the Adsorption of Nitro Phenol Organic Molecules in Water[J]. Chinese Journal of Inorganic Chemistry, 2017, 33(5): 843-852. doi: 10.11862/CJIC.2017.108

磁性UiO-66复合材料的合成及其对水体中硝基酚有机分子的吸附性能
-
关键词:
- 磁性UiO-66复合材料
- / 2-硝基-1, 3-苯二酚
- / 吸附性能
- / 静电引力
- / π-π作用
English
Synthesis of Magnetic UiO-66 Composites for the Adsorption of Nitro Phenol Organic Molecules in Water
-
金属-有机骨架材料 (metal-organic frameworks,MOFs) 是由金属离子与含羧酸或氮等多齿有机配体通过配位键自组装而成的具有高度周期性网络结构的一类新型多孔配位聚合物[1]。由于MOFs具有较大的比表面积、多孔结构和孔径较易调整等诸多优点,在气体存储、吸附分离[2]、催化[3]和传感等方面都表现出优异的性能。另外,MOFs材料的大比表面积和孔隙率,特别适用于水体中污染物的吸附,例如:芳香类污染物[4]。依靠液体分子与MOFs材料中骨架原子的相互作用力,以物理吸附的形式吸附在孔径中。目前大部分已报导的MOFs是由过渡金属离子和含有氧氮等的多齿有机配体构成[5]。其中,UiO-66是近几年来合成的一类新型MOF材料,化学式为Zr6O4(OH)4(CO2)12,是以Zr4+为金属以对苯二甲酸为配体制备得到的金属有机骨架材料[6]。它的骨架坍塌温度高于500 ℃[7],高的稳定性来源于高度对称的无机金属单元Zr6O4(OH)4,以及该Zr6八面体核与配体中羧基氧O的强相互作用。一个Zr6八面体核与12个对苯二甲酸配体配位,形成四面体和八面体两种类型的孔笼[8]。每个八面体笼的八个面上,均与一个四面体笼相连,它们的直径分别为1.1和0.8 nm,此连接方式在三维空间不断延伸,通过大小为0.5 nm×0.7 nm的窗口连接,从而提供了大的比表面积、大的孔和不饱和金属位点。
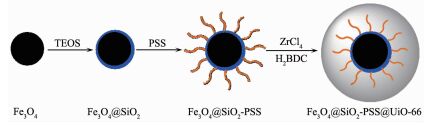
近年来,磁性纳米粒子因其具有高的比表面积、强的磁响应性,表面富含官能团易于功能化等优点而受到人们的广泛关注[9]。本论文通过层层组装法[10]设计合成了一种高比表面积、高吸附性能以及强磁响应性的磁性微纳米材料,将其作为吸附剂用于水中硝基酚有机污染物的去除研究。首先通过溶剂热法制备了Fe3O4纳米微球,然后再在Fe3O4表面包裹一层SiO2层,接着经物理超声法用聚苯乙烯磺酸钠 (PSS) 对其表面进行改性,得到Fe3O4@SiO2-PSS纳米微球。进一步以Fe3O4@SiO2-PSS为内核,在表面组装生长UiO-66壳层,制备核-壳结构的Fe3O4@SiO2-PSS@UiO-66复合材料,所得复合微球保持了磁核的磁性[9]。将制备的磁性复合材料应用于硝基酚化合物的吸附-分离性能研究,为水体有机污染物的处理提供了新思路和新方法。
1 实验部分
1.1 材料
三氯化铁 (FeCl3·6H2O),无水乙酸钠 (CH3COONa),无水乙醇 (C2H5OH),N,N-二甲基甲酰胺 (DMF) 和乙二醇 (C2H5OH) 均为分析纯,购于天津市风船化学试剂厂;氯化锆 (ZrCl4), 浓盐酸 (HCl),氨水 (NH3·H2O,质量分数为25%~28%),购于天津市科密欧试剂厂;聚苯乙烯磺酸钠 ((C8H7NaO3S)n),购于上海笛柏化学品技术有限公司;对苯二甲酸 (C8H4O6),硅酸四乙酯 (Si (OC2H5)4),购于天津市福晨化学试剂厂;去离子水自制。
1.2 材料的制备
1.3 样品的表征
高解析热场发射扫描电子显微镜 (FESEM,JSM-6490LV (JEOL,Japan)) 对磁性纳米粒子的形貌及粒径进行了表征。采用德国布鲁克D8-ADVANCB型X射线衍射仪对材料进行物相分析,工作电压40 kV, 管流30 mA, Cu靶Kα射线入射 (λ=0.154 18 nm), 2θ范围从5°到70°,步长0.04°。用Diamond TG/DTA综合热分析仪测定材料的热分解温度,以α-Al2O3为标样,其测量的温度范围是室温至800 ℃,测试条件是气体氛围,升温速率为10 ℃·min-1。用高分辨透射电子显微镜 (JEM-2100, 日本) 观察样品的分散情况和颗粒的形貌,加速电压100 kV。红外光谱分析采用Nicolet 5700型红外光谱仪,样品的结构及骨架振动采用KBr做支撑片,在400~4 000 cm-1范围内,记录样品的骨架振动红外吸收峰。N2吸附-脱附平衡测试 (BELSORP mini型,Japan) 的测试方法为:先在150 ℃、10-5 Pa下脱气处理10 h后转移到仪器进行测试。
1.4 吸附性能测试
1.2.2 Fe3O4纳米微粒的制备
取5.40 g FeCl3·6H2O溶解在40 mL的乙二醇中,形成透明的溶液,然后加入3.28 g无水乙酸钠,混合液超声混合,移入聚四氟乙烯反应釜内衬中,200 ℃,10 h,冷却至室温,在外加磁场的作用下进行磁分离,收集沉淀物,用水和乙醇洗涤数次,洗涤干净后,60 ℃真空干燥12 h,得到产物[11]。
1.2.3 Fe3O4@SiO2纳米微球的制备
取1.0 g Fe3O4,用200 mL盐酸水溶液 (0.1 mol·L-1) 处理,超声,水洗,洗涤之后将Fe3O4加入到320 mL乙醇,80 mL去离子水和5.0 mL的NH3·H2O的混合物中,超声混合均匀,再加入1 mL硅酸四乙酯 (TEOS),超声10 min,搅拌12 h,搅拌结束后磁分离,用乙醇和去离子水洗涤数次,真空60 ℃干燥12 h,得到产物。
1.2.1 UiO-66的合成
取0.053 g氯化锆和0.034 g对苯二甲酸 (H2BDC) 放入20 mL的聚四氟乙烯反应釜内衬中,加入18 mL的DMF[7],混合均匀,转移到烘箱中,120 ℃,24 h。
1.2.4 Fe3O4@SiO2-PSS@UiO-66的合成
取0.1 g Fe3O4@SiO2加入到溶解有0.9 g聚苯乙烯磺酸钠的500 mL水溶液中,超声20 min,水洗3次,得到Fe3O4@SiO2-PSS,再加入到溶解有0.164 g氯化锆和0.102 g H2BDC的54 mL的DMF中,混合均匀,转移到聚四氟乙烯反应釜内衬中,然后将其放入烘箱中,120 ℃,24 h,冷却到室温,磁分离。将固体作为上述步骤的Fe3O4@SiO2,重复上述实验2次,最后的产物磁分离后,反复用DMF洗,之后用甲醇清洗3遍,在60 ℃下真空干燥。
1.4.2 标准曲线的测定
分别配制10、20、30、35、40 mg·L-1的2-硝基-1,3-苯二酚,通过紫外-可见分光光度计 (λ=313 nm) 分别测量其吸光度。作空白校正后,以313 nm处吸光度为纵坐标,2-硝基-1,3-苯二酚的浓度 (mg·L-1) 为横坐标,绘制的标准曲线如图 1所示:
1.4.1 吸附试验
为了研究制备复合材料对硝基酚类有机分子的吸附性能,选用2-硝基-1,3-苯二酚作为吸附质,Fe3O4@SiO2-PSS@UiO-66作为吸附剂,充分吸附后用外磁场进行磁分离,取上清液采用紫外-可见分光光度计进行紫外光谱测定,在313 nm处测得2-硝基-1,3-苯二酚吸光度值,通过2-硝基-1,3-苯二酚吸光度值与浓度之间关系的线性方程将其转化为2-硝基-1,3-苯二酚的浓度,从而确定其单位吸附量[12]。
根据下面公式计算复合材料对2-硝基-1,3-苯二酚的单位吸附量:
其中qt为单位吸附量 (mg·g-1);C0和Ct分别为溶液中2-硝基-1,3-苯二酚的初始质量浓度和某时刻的质量浓度 (mg·L-1);V为2-硝基-1,3-苯二酚溶液体积 (L);m为复合材料的质量 (mg)。
2 结果与讨论
2.1 合成路线图
在这项工作中,我们设计将具有强磁响应性的磁性纳米微球Fe3O4作为复合材料的内核,并在其表面包覆SiO2层,合成改性磁性二氧化硅纳米微球。然后通过物理超声法把聚合物PSS结合到Fe3O4@SiO2复合材料的表面。最后通过静电相互作用,Fe3O4@SiO2-PSS表面的磺酸根离子先与带相反电荷的Zr4+结合,Zr4+再进一步跟配体H2BDC配位生长MOF层,形成稳定的化学组装结构。
2.2 XRD分析
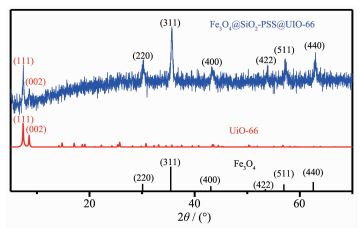
图 3为Fe3O4,UiO-66和Fe3O4@SiO2-PSS@UiO-66的XRD图。由图可见,复合材料在2θ=30.22°,35.68°,43.28°,53.68°,57.18°和62.76°处与标准卡上Fe3O4(PDF No.19-0629) 衍射峰相符,分别对应 (220),(311),(400),(422),(511) 和 (440) 晶面的特征衍射峰[13]。对比Fe3O4@SiO2-PSS@UiO-66的XRD衍射图,除去Fe3O4的衍射峰,剩下的衍射峰与UiO-66模拟峰位基本相符,分别为 (111),(002)。由XRD图分析可知,所制备的磁性多孔复合样品含有尖晶石结构的Fe3O4和UiO-66。
2.3 材料的形貌分析
从图 4(a)可知,合成的Fe3O4磁性纳米颗粒,形貌均一,尺寸大小为200 nm左右。由图 4(b)、(c)可知,磁性Fe3O4内核外层有明显的UiO-66包裹层,为立方体形状,厚度大于100 nm,随着UiO-66层的厚度的增大,单位质量的孔隙率增大,有利于硝基酚有机分子的吸附。
 图 4
TEM图: (a) Fe3O4, (b) Fe3O4@SiO2-PSS@UiO-66; SEM图: (c) Fe3O4@SiO2-PSS@UiO-66; (d) 磁分离的光学照片; 相机照片: (e) UiO-66, (f) Fe3O4@SiO2和 (g) Fe3O4@SiO2-PSS@UiO-66
Figure 4.
TEM images: (a) Fe3O4, (b) Fe3O4@SiO2-PSS@UiO-66; SEM images: (c) Fe3O4@SiO2-PSS@UiO-66; (d) Photo image of magnetic separation; Digital photographs: (e) UiO-66, (f) Fe3O4@SiO2 and (g) Fe3O4@SiO2-PSS@UiO-66
图 4
TEM图: (a) Fe3O4, (b) Fe3O4@SiO2-PSS@UiO-66; SEM图: (c) Fe3O4@SiO2-PSS@UiO-66; (d) 磁分离的光学照片; 相机照片: (e) UiO-66, (f) Fe3O4@SiO2和 (g) Fe3O4@SiO2-PSS@UiO-66
Figure 4.
TEM images: (a) Fe3O4, (b) Fe3O4@SiO2-PSS@UiO-66; SEM images: (c) Fe3O4@SiO2-PSS@UiO-66; (d) Photo image of magnetic separation; Digital photographs: (e) UiO-66, (f) Fe3O4@SiO2 and (g) Fe3O4@SiO2-PSS@UiO-66
2.4 材料的结合强度分析
为了检测磁性UiO-66复合材料在层层组装过程中,Fe3O4与UiO-66结合的强度,我们对该材料进行了超声2 h的处理,并用磁铁进行磁分离收集,随后对该复合材料的结合强度进行了分析检测。首先对该材料做了XRD检测分析,结果与图 3相同,都出现了Fe3O4和UiO-66的特征衍射峰,证明Fe3O4表面仍然存在UiO-66包覆层。随后又对该复合材料做了TEM和SEM分析。由图 5(a)、(b)可以看出,磁性内核外层UiO-66包裹层仍然比较厚且没有脱落,另外复合材料包覆情况与超声2 h前并无明显区别。由此证明Fe3O4与UiO-66之间结合作用强,可实现材料的层层包覆。
2.5 红外光谱 (FTIR) 分析
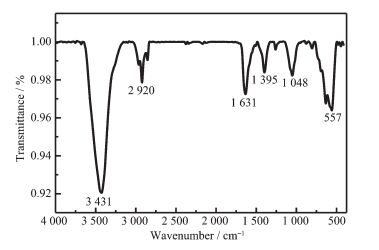
从图 6可以看出在3 431 cm-1处较强的吸收峰为O-H的伸缩振动所产生的吸峰,在2 920 cm-1处存在C-H的伸缩振动吸收峰,在1 631 cm-1处较强的吸收峰为-COO-反对称伸缩振动,在1 048和1 395 cm-1处较强的吸收峰为苯环结构的吸收峰,在557 cm-1处较强的吸收峰为Fe3O4的Fe-O特征吸收峰。在1 100~1 010 cm-1之间有一个宽峰,在800 cm-1附近的一个尖峰,这属于Si-O-Si键的对称振动峰。由红外光谱图可知,制备的磁性多孔材料已成功复合了Fe3O4和UiO-66。
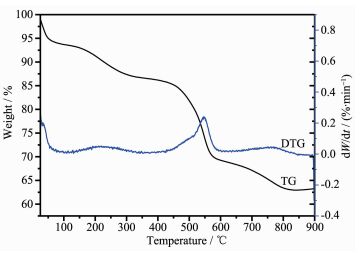
2.6 热重 (TG) 分析
从图 7可知,在整个温度范围内磁性多孔材料有3个质量减少台阶,分别为50~250 ℃,250~550 ℃和550~900 ℃。50~250 ℃之间的质量减少是由于水和小分子溶剂 (比如甲醇、DMF) 的分解引起的,约占总质量的7%;250~550 ℃质量减少27%,是由于配体与金属的配位键的断裂,导致了MOF骨架的缓慢坍塌;550 ℃之后,样品中的UiO-66已经完全分解。热重图谱证明了Fe3O4@SiO2-PSS@UiO-66有好的热稳定性。
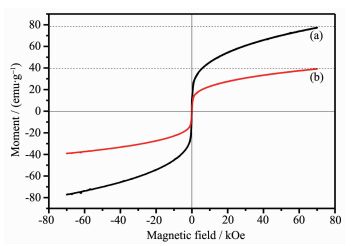
2.7 VSM分析
图 8为Fe3O4磁性粒子,Fe3O4@SiO2-PSS@UiO-66复合纳米粒子的磁滞回线,如图所示:磁性粒子Fe3O4的饱和磁化强度为78.80 emu·g-1,Fe3O4@SiO2-PSS@UiO-66的饱和磁化强度为39.07 emu·g-1。虽然Fe3O4@SiO2-PSS@UiO-66的磁性强度相比Fe3O4明显降低,但是Fe3O4@SiO2-PSS@UiO-66复合物还是很容易通过磁场收集和分离的。
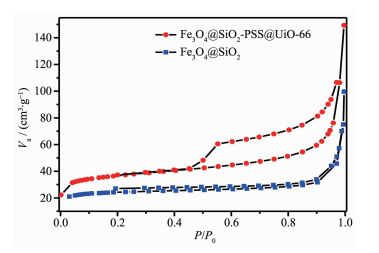
2.8 材料的N2吸脱附测试
N2吸附脱附等温线[14]是为了研究合成的Fe3O4 @SiO2-PSS@UiO-66的比表面积和孔容体积,结果如图 9所示。测试结果表明Fe3O4@SiO2-PSS@UiO-66吸脱附曲线属于第Ⅳ类等温线并出现明显的滞后环这表明材料具有介孔结构[15]。对比纯的UiO-66晶体,Fe3O4@SiO2-PSS@UiO-66的表面积和孔体积分别从891 m2·g-1和0.47 cm3·g-1减少到116 m2·g-1和0.21 cm3·g-1。主要是由于Fe3O4@SiO2存在大量的纳米孔结构,结果证明了UiO-66成功地包覆在了Fe3O4@SiO2-PSS表面。
2.9 样品的吸附性能
2.9.2 吸附时间对2-硝基-1,3-苯二酚的影响
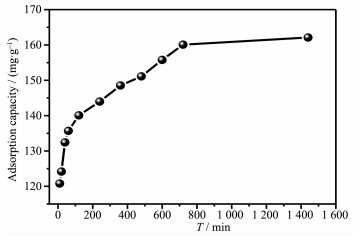
取11份初始浓度为400 mg·L-1的2-硝基-1,3-苯二酚溶液各5 mL,分别加入5 mg的磁性UiO-66复合材料,恒温振荡10 min,20 min,40 min,1 h,2 h,4 h,6 h,8 h,10 h,12 h和24 h的时间段,分别取样测试,通过外磁场分离,取上清液进行紫外吸收光谱分析,结果如图 11所示。从图 11中可以看出:在0~1 h内,随着时间的增加,吸附量迅速增加;在1~12 h内,单位吸附量的增长速率逐渐减小;吸附12 h后, 达到吸附平衡,最大吸附量为160.1 mg·g-1。
Sample BET surfuce area / (m2·g-1) Pore volume / (cm3·g-1) UiO-66[16] 891 0.47 Fe3O4@SiO2 61 0.1 Fe3O4@SiO2-PSS@UiO-66 116 0.21 表 1 Fe3O4@SiO2-PSS@UiO-66的比表面积和孔容体积
Table 1. Surface area and pore volumes of Fe3O4@SiO2-PSS@UiO-662.9.1 吸附机理
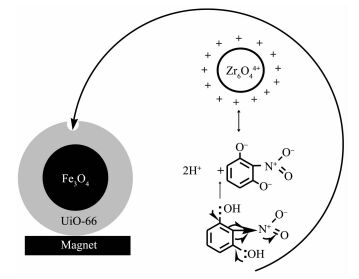
如图 10所示为磁性UiO-66复合材料对2-硝基-1,3-苯二酚的吸附机理。首先,2-硝基-1,3-苯二酚的分子尺寸为0.61 nm×0.49 nm,这与UiO-66笼的窗口尺寸大小相近,这为2-硝基-1,3-苯二酚分子进入到UiO-66孔道中提供了可能。其次,当2-硝基-1,3-苯二酚分子进入到UiO-66孔道中后,UiO-66中的Zr6O44+簇所带的正电荷与2-硝基-1,3-苯二酚 (-O-) 之间存在静电引力。另外,UiO-66和2-硝基-1,3-苯二酚之间苯环的π-π作用,也有利于磁性UiO-66复合材料对2-硝基-1,3-苯二酚的吸附。最后,我们设计将具有强磁响应性的Fe3O4纳米微球作为磁性UiO-66复合材料的内核,它能使表面的UiO-66壳层在吸附2-硝基-1,3-苯二酚之后,通过外磁场的作用,有效地从污水中分离出来。
2.9.6 吸附动力学研究[22]
从图 11可以看出在吸附开始的1 h以内,吸附量迅速增加,一方面由于吸附剂表面2-硝基-1,3-苯二酚与水溶液之间的浓度差,使溶液中的2-硝基-1,3-苯二酚快速移动到吸附剂的表面,从而使水中的2-硝基-1,3-苯二酚快速减少,另一方面在吸附前期吸附剂表面存在大量的吸附位点而导致吸附迅速。在1~12 h期间去除率缓慢增加直到达到平衡。在12~24 h内吸附基本上达到平衡。
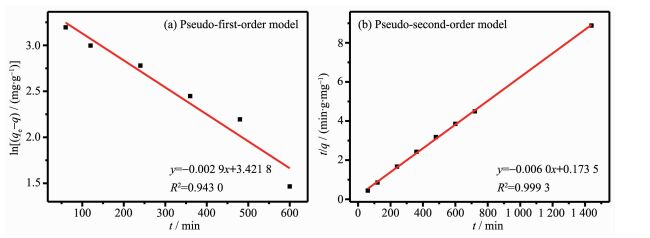
为了进一步探讨磁性复合纳米材料对2-硝基-1,3-苯二酚的吸附动力学特性,选用准一级动力学方程公式 (2) 和准二级动力学方程公式 (3) 对吸附动力学数据进行拟合。
式中,qe为平衡吸附量 (mg·g-1),qt为t时刻的吸附量 (mg·g-1),t为吸附时间 (min),k1为准一级反应速率常数 (min-1),k2为准二级反应速率常数 (g·mg-1·min-1)。
表 3为Fe3O4@SiO2-PSS@UiO-66吸附2-硝基-1,3-苯二酚数据采用准一级和准二级动力学模型得到的动力学参数,准二级动力学模型的线性相关系数R2>0.99,拟合度较高,而且理论平衡吸附量qe, cal与实验所得的平衡吸附量qe, exp有较好的吻合。如图 14(b)所示,二级动力学模型拟合的比较好,所以Fe3O4@SiO2-PSS@UiO-66对2-硝基-1,3-苯二酚的吸附符合准二级动力学模型。
 表 3
Fe3O4@SiO2-PSS@UiO-66吸附2-硝基-1, 3-苯二酚动力学的拟合结果
Table 3.
Fitting results of adsorption kinetics for 2-nitroresorcinolon Fe3O4@SiO2-PSS@UiO-66
表 3
Fe3O4@SiO2-PSS@UiO-66吸附2-硝基-1, 3-苯二酚动力学的拟合结果
Table 3.
Fitting results of adsorption kinetics for 2-nitroresorcinolon Fe3O4@SiO2-PSS@UiO-66
Kinetic parameter Pseudo-first-order kinetic Pseudo-second-order kinetic R2 0.943 0 0.999 3 qe, exp/(mg·g-1) 161.36 161.36 qe, cal/(mg·g-1) 30.62 125 表 3 Fe3O4@SiO2-PSS@UiO-66吸附2-硝基-1, 3-苯二酚动力学的拟合结果
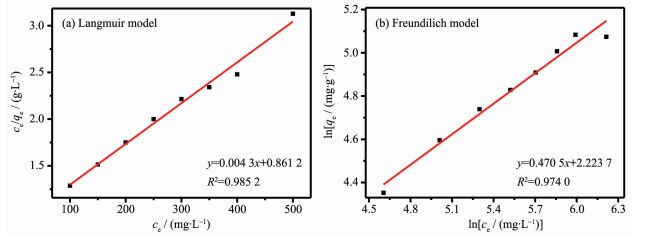
Table 3. Fitting results of adsorption kinetics for 2-nitroresorcinolon Fe3O4@SiO2-PSS@UiO-66为了研究Fe3O4@SiO2-PSS@UiO-66与2-硝基-1,3-苯二酚之间的相互作用机理和固液间平衡吸附的机制,通常采用Langmuir吸附等温线公式 (4) 和Freundlich吸附等温线公式 (5) 来对平衡的吸附数据进行拟合分析[23]。
上式中,Ce(mg·L-1) 是吸附质的平衡浓度;qe(mg·g-1) 是达到平衡状态时的吸附量;q(mg·g-1) 是单分子层的最大吸附量;b(L·mg-1) 是与吸附自由能有关的Langmuir常数;Kf(mg·g-1) 是Freundlich吸附常数。
表 4为Fe3O4@SiO2-PSS@UiO-66吸附2-硝基-1,3-苯二酚数据采用Langmuir模型和Freundlich模型拟合得到的参数,Langmuir模型的线性相关系数R2>0.98,拟合度较高。如图 15所示,Langmuir模型拟合的比较好, 所以Fe3O4@SiO2-PSS@UiO-66对2-硝基-1,3-苯二酚的吸附符合Langmuir模型。
Langmuir model Freundlich model q / (mg·g-1) b/ (L·mg-1) R2 Kf/ (mg·g-1) n R2 232.5 0.004 0.98 1.60 2.12 0.97 表 4 Langmuir模型和Freundlich模型的拟合结果
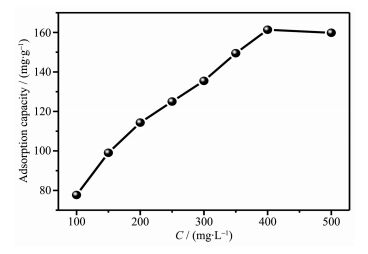
Table 4. Fitting results of Langmuir model and Freundlich model2.9.3 初始浓度对2-硝基-1,3-苯二酚的影响
分别配制9份不同浓度的2-硝基-1,3-苯二酚溶液5 mL,向其中加入5 mg的磁性UiO-66复合材料,然后恒温振荡器中振荡12 h,使磁性多孔材料充分吸附2-硝基-1,3-苯二酚,然后在外加磁场作用下,对其进行磁分离,充分分离磁性多孔材料和残留的2-硝基-1,3-苯二酚溶液,取上清液进行紫外吸收光谱分析,结果如图 12所示。从图 12可以看出:随着2-硝基-1,3-苯二酚的初始浓度的增加,在浓度达到400 mg·L-1之前,吸附量逐渐增大;而在浓度达到400 mg·L-1后,增长速率逐渐降低,最后趋于平衡。当2-硝基-1,3-苯二酚浓度达到400 mg·L-1,最大吸附量为161.4 mg·g-1。
2.9.5 吸附性能比较
表 2为文献中报道的不同吸附剂对酚类吸附性能的比较,由表可知,本工作合成的磁性UiO-66复合材料,在满足磁分离简便操作的同时,还能达到比较理想的吸附效果。
 表 2
不同吸附剂对酚类吸附容量的比较
Table 2.
Comparison of the adsorption capacity (mg·g-1) of phenols with other adsorbents
表 2
不同吸附剂对酚类吸附容量的比较
Table 2.
Comparison of the adsorption capacity (mg·g-1) of phenols with other adsorbents
Adsorbents Phenols Adsorption capacity / (mg • g-1) Reference Nano zeolite P-Nitrophenol 156.7 [17] Ui0-66-NH2 P-Nitrophenol 44.96 [18] Amino-MIL-53(Al) P-Nitrophenol 297.85 [19] Fe3O4@TpBD Bisphenol A 160.6 [20] MIL-53(Al)-F127 Bisphenol A 465 [21] Fe3O4@SiO2-PSS@UiO-66 2-Nitroresorcinol 161.36 Present work 表 2 不同吸附剂对酚类吸附容量的比较
Table 2. Comparison of the adsorption capacity (mg·g-1) of phenols with other adsorbents2.9.4 吸附剂的量对2-硝基-1,3-苯二酚的影响
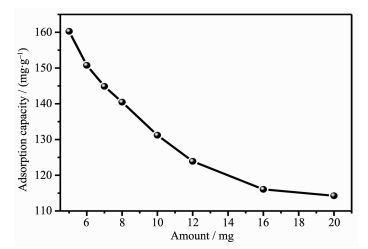
分别取7份浓度为400 mg·L-1的2-硝基-1,3-苯二酚溶液,然后分别加入5,6,7,8,10,12和16 mg磁性UiO-66复合材料,恒温振荡器中反应12 h,使磁性多孔材料充分吸附2-硝基-1,3-苯二酚,然后在外加磁场作用下,对其进行磁分离,充分分离磁性多孔材料和残留的2-硝基-1,3-苯二酚溶液,取上清液进行紫外吸收光谱分析,结果如图 13所示。从图 13中可以看出:随着吸附剂的量的增大,单位吸附量逐渐减小,并逐渐趋于稳定,当磁性UiO-66的用量为5 mg时,纳米粒子的吸附量最大,为160.3 mg·g-1。
3 结论
我们成功制备合成了以Fe3O4磁性纳米颗粒为内核,SiO2为包覆层,并通过物理超声法在其表面修饰了PSS,最后通过溶剂热法在Fe3O4@SiO2-PSS表面成功组装了立方多晶堆积的UiO-66壳层,制备了一种新型磁性纳米吸附材料Fe3O4@SiO2-PSS @UiO-66,并利用XRD,SEM,TEM,FTIR,TG,VSM和N2吸附-脱附对制备样品的物相结构形貌和磁性能进行了测试表征。结果表明:制备的磁性复合微球具有良好的超顺磁性,磁性核壳微球的比表面积和孔容分别为116 m2·g-1和0.21 cm3·g-1。另外,磁性UiO-66复合材料对2-硝基-1,3-苯二酚高的吸附性能可能是归功于UiO-66与2-硝基-1,3-苯二酚之间的静电作用以及二者之间苯环的π-π作用。并且Fe3O4@SiO2-PSS@UiO-66对2-硝基-1,3-苯二酚的吸附过程是以准二级动力学模型占主导,且最大吸附量达到了161.36 mg·g-1。
-
-
[1]
Zhu Q L, Xu Q. Chem. Soc. Rev., 2014, 43(16):5468-5512 doi: 10.1039/C3CS60472A
-
[2]
周奎, 姚宸.无机化学学报, 2015, 31(3):509-513 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20150312&flag=1Chaemchuen S, ZHOU Kui, YAO Chen, et al. Chinese J. Inorg. Chem., 2015, 31(3):509-513 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20150312&flag=1
-
[3]
Kuo C H, Yang T, Chou L Y, et al. J. Am. Chem. Soc., 2012, 134(35):14345-14348 doi: 10.1021/ja306869j
-
[4]
Hong S, Yoo J, Park N, et al. Chem. Commun., 2015, 51(3):E119-E124
-
[5]
金哲, 汤凯, 胡亚平.无机化学学报, 2015, 31(4):725-730 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20150414&flag=1JIN Zhe, TANG Kai, HU Ya-Ping, et al. Chinese J. Inorg. Chem., 2015, 31(4):725-730 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20150414&flag=1
-
[6]
戴田霖, 张艳梅, 储刚.无机化学学报, 2016, 32(4):609-616 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20160408&flag=1DAI Tian-Lin, ZHANG Yan-Mei, CHU Gang, et al. Chinese J. Inorg. Chem., 2016, 32(4):609-616 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20160408&flag=1
-
[7]
Cavka J H, Jakobsen S, Olsbye U, et al. J. Am. Chem. Soc., 2008, 130(42):13850-13851 doi: 10.1021/ja8057953
-
[8]
HUANG Yu-Ting (黄钰婷). Thesis for the Master of South China University of Technology(华南理工大学硕士论文). 2012.
-
[9]
SHAO Yan-Ming (邵彦明). Thesis for the Doctorate of Lanzhou University(兰州大学博士论文). 2016.
-
[10]
Zhang Y M, Dai T L, Zhang F, et al. Chem. J. Catal., 2016, 37(12):2106-2113 doi: 10.1016/S1872-2067(16)62562-7
-
[11]
GAO Dong-Lan (高冬兰). Thesis for the Master of Nanjing University of Science and Technology(南京理工大学硕士论文). 2013.
-
[12]
杨清香, 赵倩倩, 李银萍.轻工学报, 2016, 31(3):8-13YANG Qing-Xiang, ZHAO Qian-Qian, LI Yin-Ping, et al. J. Light Ind., 2016, 31(3):8-13
-
[13]
薛娟琴, 徐尚元, 朱倩文.无机化学学报, 2016, (09):1503-1511 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20160902&flag=1XUE Juan-Qin, XU Shang-Yuan, ZHU Qian-Wen, et al. Chinese J. Inorg. Chem., 2016, (09):1503-1511 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20160902&flag=1
-
[14]
Hu B, Huang L, He M, et al. J. Mater. Chem. A, 2015, 3(21):11587-11595 doi: 10.1039/C5TA01484K
-
[15]
Li Y, Sun J, Zhang L, et al. Appl. Surf. Sci., 2012, 258(8):3333-3339 doi: 10.1016/j.apsusc.2011.06.159
-
[16]
Ebrahim A M, Levasseur B, Bandosz T J. Langmuir, 2013, 29(1):168-174 doi: 10.1021/la302869m
-
[17]
Pham T-H, Lee B-K, Kim J. Process Saf. Environ. Prot., 2016, 104:314-322 doi: 10.1016/j.psep.2016.08.018
-
[18]
Lü G R, Liu J M, Xiong Z H, et al. J. Chem. Eng. Data, 2016, 61(11):3868-3876 doi: 10.1021/acs.jced.6b00581
-
[19]
Jia Z, Jiang M, Wu G. Chem. Eng. J., 2016, 307:283-290
-
[20]
Li Y, Yang C X, Yan X P. Chem. Commun., 2017, 53(16):2511 doi: 10.1039/C6CC10188G
-
[21]
Zhou M, Wu Y N, Qiao J, et al. J. Colloid Interface Sci., 2013, 405(9):157-163
-
[22]
龚文朋, 杜晓刚, 田超强.精细化工, 2016, 33(4):467-474GONG Wen-Peng, DU Xiao-Gang, TIAN Chao-Qiang, et al. Fine Chemicals, 2016, 33(4):467-474
-
[23]
李君, 王鲁香, 曹亚丽.无机化学学报, 2016, 32(9):1603-1610 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20160915&flag=1LI Jun, WANG Lu-Xiang, CAO Ya-Li, et al. Chinese J. Inorg. Chem., 2016, 32(9):1603-1610 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20160915&flag=1
-
[1]
-
图 4 TEM图: (a) Fe3O4, (b) Fe3O4@SiO2-PSS@UiO-66; SEM图: (c) Fe3O4@SiO2-PSS@UiO-66; (d) 磁分离的光学照片; 相机照片: (e) UiO-66, (f) Fe3O4@SiO2和 (g) Fe3O4@SiO2-PSS@UiO-66
Figure 4 TEM images: (a) Fe3O4, (b) Fe3O4@SiO2-PSS@UiO-66; SEM images: (c) Fe3O4@SiO2-PSS@UiO-66; (d) Photo image of magnetic separation; Digital photographs: (e) UiO-66, (f) Fe3O4@SiO2 and (g) Fe3O4@SiO2-PSS@UiO-66
表 1 Fe3O4@SiO2-PSS@UiO-66的比表面积和孔容体积
Table 1. Surface area and pore volumes of Fe3O4@SiO2-PSS@UiO-66
Sample BET surfuce area / (m2·g-1) Pore volume / (cm3·g-1) UiO-66[16] 891 0.47 Fe3O4@SiO2 61 0.1 Fe3O4@SiO2-PSS@UiO-66 116 0.21 表 2 不同吸附剂对酚类吸附容量的比较
Table 2. Comparison of the adsorption capacity (mg·g-1) of phenols with other adsorbents
表 3 Fe3O4@SiO2-PSS@UiO-66吸附2-硝基-1, 3-苯二酚动力学的拟合结果
Table 3. Fitting results of adsorption kinetics for 2-nitroresorcinolon Fe3O4@SiO2-PSS@UiO-66
Kinetic parameter Pseudo-first-order kinetic Pseudo-second-order kinetic R2 0.943 0 0.999 3 qe, exp/(mg·g-1) 161.36 161.36 qe, cal/(mg·g-1) 30.62 125 表 4 Langmuir模型和Freundlich模型的拟合结果
Table 4. Fitting results of Langmuir model and Freundlich model
Langmuir model Freundlich model q / (mg·g-1) b/ (L·mg-1) R2 Kf/ (mg·g-1) n R2 232.5 0.004 0.98 1.60 2.12 0.97 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 10
- 文章访问数: 1516
- HTML全文浏览量: 181



 下载:
下载:














 下载:
下载:

