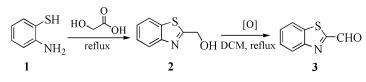
 图式1
苯并噻唑-2-甲醛的合成路线
图式1.
The synthetic route of benzothiazole-2-carbaldehyde
图式1
苯并噻唑-2-甲醛的合成路线
图式1.
The synthetic route of benzothiazole-2-carbaldehyde

Citation: Zhang Chao, Xu Dongdong, Wang Jingjing, Kang Congmin. An Improved Synthesis of Benzothiazole-2-carbaldehyde[J]. Chemistry, 2017, 80(8): 789-791.

苯并噻唑-2-甲醛合成方法的改进
English
An Improved Synthesis of Benzothiazole-2-carbaldehyde
-
Key words:
- Benzothiazol-2-yl methanol
- / Oxidation
- / Manganese dioxide
- / Benzothiazole-2-carbaldehyde
-
苯并噻唑类衍生物具有重要的药理活性或多种材料功能属性,在医药[1]、农药[2]、材料工程[3]等领域具有广泛的应用。对其修饰主要是在苯环上引入不同的取代基,或在2位引入不同的活性基团,其中2-位取代基对其活性影响最大,因此2-取代衍生物的合成是该类化合物合成研究中最受关注的部分[4]。苯并噻唑-2-甲醛以及取代苯并噻唑-2-甲醛具有反应活性很高的甲酰基,能进行多种化学反应,因而成为合成苯并噻唑类衍生物的重要中间体[5~8]。随着苯并噻唑-2-甲醛及其衍生物的应用日益广泛,其合成方法越来越受到人们的重视,其合成途径也仍在不断的探索。
最初,Taber等[9]用二氧化硒氧化2-甲基苯并噻唑来制备苯并噻唑-2-甲醛。近期,Zheng等[10]又以N, N-二甲基甲酰胺为溶剂,在130℃的密闭环境下,以氯化铜为催化剂,通入氧气反应36h氧化2-甲基苯并噻唑来制备苯并噻唑-2-甲醛。该方法操作不便利,反应时间过长,产率较低。Nagasawa等[11]将2-甲基苯并噻唑与碘和三氟乙酸在乙酸乙酯中70℃下搅拌8h,再在荧光照射下通入氧气反应20h来制备苯并噻唑-2甲醛。该方法反应时间长,反应条件较复杂,产率不高,不适合大规模生产。刘运奎等[12]以苯并噻唑和甲醇为原料,在氧化剂的作用下反应制得2-苯并噻唑二甲缩醛,然后在酸催化剂的作用下反应制得苯并噻唑-2-甲醛。该方法第一步制得2-苯并噻唑二甲缩醛反应的收率为30%~64%,收率偏低且不稳定,进而影响了最终产物苯并噻唑-2-甲醛的总收率。Wang等[13]通过使用2-羟甲基苯并噻唑与邻苯二甲酸二甲酯先进行酯化反应,然后再用硫代硫酸钠溶液将其还原成苯并噻唑-2-甲醛。此方法产率不高,副产物的后处理较困难。Campaigne等[14]通过以二氧化硒为氧化剂氧化2-羟甲基苯并噻唑来制备苯并噻唑-2-甲醛,这种方法容易引起副反应,且实际操作的产率很难提高,同样不适合大规模生产。
为了寻求更合理可行的苯并噻唑-2-甲醛及取代苯并噻唑-2-甲醛的制备方法,对2-羟甲基苯并噻唑氧化成苯并噻唑-2-甲醛的反应条件进行了探索优化。首先根据Elshihawy等[15]方法合成出2-羟甲基苯并噻唑,然后使用不同的氧化剂氧化生成苯并噻唑-2-甲醛(图式 1),最后对二氧化锰氧化的反应条件进行了优化。结果表明,使用二氧化锰作为氧化剂时,产率高、生产成本低、后处理简单,有良好的工业应用前景。
1 实验部分
1.1 仪器与试剂
X-4显微熔点测定仪(巩义市予华仪器有限责任公司);Bruker Advance 500MHz核磁共振谱仪(瑞士布鲁克公司,TMS为内标);Tensor 27红外光谱仪(德国布鲁克公司,KBr压片)。
邻氨基苯硫酚、羟基乙酸、邻碘苯甲酸(上海达瑞精细化学品有限公司);二氧化锰、溴酸钾(天津市广成化学试剂有限公司);吡啶(天津博迪化工股份有限公司);三氧化铬(天津市科密欧化学试剂开发中心);二氧化硒(成都市科龙化工试剂厂)。所用试剂均为分析纯级。
氯铬酸吡啶(PCC)的配制[16]:在搅拌下将100g CrO3迅速加入到184mL 6mol/L盐酸中,5min后将均相体系冷却至0℃,然后缓慢滴加79g吡啶。将反应体系重新冷却至0℃,得橙黄色固体,过滤,真空干燥1h,得181g PCC。
戴斯-马丁(Dess-Martin)氧化剂的配制[17]:(1) 在500mL烧瓶中加入20g溴酸钾、188mL 2mol/L硫酸,搅拌溶解,加热至60℃,在氮气保护下分3次加入邻碘苯甲酸20g,在30min内加完。维持65℃反应2.5h,然后冷却到2~3℃,抽滤,依次用300mL冰水、200mL乙醇和300mL冰水洗涤,得到白色固体22g。(2) 在250mL烧瓶中加入步骤(1) 得到的白色固体、40mL冰醋酸和80mL乙酸酐,氮气保护下搅拌反应。加热至85℃,完全溶解后继续反应2h,冷却至室温,析出白色晶体。抽滤,用30mL无水乙醚洗涤3次,真空干燥,得到Dess-Martin氧化剂25g。
1.2 2-羟甲基苯并噻唑(2) 的合成
100mL三口烧瓶中加入12.5g(0.10mol)邻氨基苯硫酚和11.4g(0.15mol)羟基乙酸,搅拌溶解,加热至回流反应5h。反应液冷却至70℃左右,加入30mL无水乙醇,再冷却至室温,加入100mL水,析出油状物,凝固后过滤,无水乙醇重结晶,干燥,得到淡黄色固体14.9g,产率90.2%。熔点:100~101 ℃(文献值101~102℃[14])。1H NMR (500MHz,DMSO-d6)δ:8.00 (d,J=7.9Hz,1H,ArH),7.84 (d,J=8.1Hz,1H,ArH),7.40(t,J=8.0Hz,1H,ArH),7.34 (t,J=8.0Hz,1H,ArH),6.19 (t,J=5.9Hz,1H,OH),4.78 (d,J=5.9Hz,2H,CH2)。
1.3 苯并噻唑-2-甲醛(3) 的合成
100mL的三口烧瓶中加入3.30g (0.02mol)2-羟甲基苯并噻唑、50mL二氯甲烷和适量氧化剂,回流反应一段时间,冷却至室温。真空抽滤,减压浓缩,干燥后无水乙醇重结晶,得到棕色固体。熔点:73~74 ℃(文献值75~77 ℃[9])。1H NMR (500 MHz,DMSO-d6)δ:10.11 (s,1H,CHO),8.27 (d,J=8.0Hz,1H,ArH),8.03 (d,J=8.0Hz,1H,ArH),7.71~7.62 (m,2H,ArH);IR (KBr) ν/cm-1:3057,2846,2354,1694,1485,1204,775。
2 结果与讨论
2.1 不同氧化剂对氧化反应的影响
首先用不同氧化剂对2-羟甲基苯并噻唑的氧化反应进行了研究。将3.30g (0.02mol)化合物2和0.04mol氧化剂在50mL二氯甲烷回流反应6h,结果如表 1所示。由实验结果可以看出,使用高锰酸钾氧化时,没有检测到2的氧化产物;使用PCC和Dess-Martin氧化时,产率分别为34.3%和42.1%;以二氧化锰作为氧化剂时,产率56.2%,相对较高。
氧化剂 溶剂 温度 产率/% PCC 二氯甲烷 回流 34.3 Dess-Martin 二氯甲烷 回流 42.1 KMnO4 二氯甲烷 回流 0 MnO2 二氯甲烷 回流 56.2 为了探索更优的由2氧化成3的工艺条件,进一步考察了氧化剂二氧化锰的用量、反应时间对产物收率的影响。
2.2 氧化剂用量对氧化反应的影响
探究二氧化锰用量对产率的影响。由表 2可见,氧化剂二氧化锰用量比较少时,产率较低;随着氧化剂量的增多,产率也随之增加。当2与氧化剂的摩尔比小于1:8时,产率随着氧化剂量的增加而速率变缓。考虑到实验成本和后处理问题,反应中2与二氧化锰较优的摩尔比为1:8。
2/MnO2(摩尔比) 1:2 1:4 1:6 1:8 1:10 1:12 产物质量/g 1.83 2.07 2.20 2.57 2.59 2.60 产率/% 56.20 63.50 67.60 78.90 79.30 79.60 反应条件:3.30g (0.02mol)化合物2,50mL二氯甲烷,回流反应6h 2.3 反应时间对氧化反应的影响
化合物2的加入量3.30g(0.02mol),以17.4g (0.16mol)二氧化锰为氧化剂,在50mL二氯甲烷回流反应,探究反应时间对产率的影响,结果见表 3。由表 3可见,反应时间较短时,产率较低;随着反应时间的延长,产率逐渐提高。当反应时间超过8h时,产率随时间变化的趋势变缓,最终确定较优的反应时间为8h。
反应时间/h 2 4 6 8 10 12 产物质量/g 1.07 2.07 2.57 2.94 2.96 2.94 产率/% 32.70 63.60 78.90 90.20 90.70 90.30 5 结论
按照现有文献的方法,先以邻氨基苯硫酚与羟基乙酸为原料,在无溶剂的条件下生成2-羟甲基苯并噻唑,然后2-羟甲基苯并噻唑再与多种氧化剂反应生成苯并噻唑-2-甲醛,通过比较发现,二氧化锰作为氧化剂时产率较高。最后探究了反应过程中氧化剂用量以及反应时间对产物收率的影响,确定较适宜的反应条件为:原料2-羟甲基苯并噻唑与氧化剂二氧化锰的摩尔比为1:8,在二氯甲烷中回流反应8h。此反应条件下产率可达90.2%。
由2-羟甲基苯并噻唑合成苯并噻唑-2-甲醛,这一合成路线条件温和,可操作性强,产率大幅度提高,成本低,有望应用于苯并噻唑-2-甲醛及其衍生物的大规模工业生产。
-
-
[1]
A A Weekes, A D Westwell. Curr. Med. Chem., 2010, 16(19):2430~2440. http://europepmc.org/abstract/MED/19601790
-
[2]
洪艳平, 宋宝安, 吴平等. 安徽农业科学, 2005, 33(7): 1254~1257. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=ahny200507062&dbname=CJFD&dbcode=CJFQ
-
[3]
G K Dutta, S Guha, S Patil. Org. Electron., 2010, 11(1):1~9. http://www.sciencedirect.com/science/article/pii/S1566119909002730
-
[4]
李焱, 王玉炉. 有机化学, 2006, (6): 878~884+744. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=yjhu200606023&dbname=CJFD&dbcode=CJFQ
-
[5]
O Labeeuw, N Levoin, X Billot et al. Bioorg. Med. Chem. Lett., 2016, 26(21):5263~5266. http://europepmc.org/abstract/MED/27692832
-
[6]
S S Chourasiya, D Kathuria, S S Nikam et al. J. Org. Chem., 2016, 81(17):7574~7583. http://europepmc.org/abstract/MED/27494613
-
[7]
Y Gao, H Liu, Q Liu et al. Tetrahed. Lett., 2016, 57(17):1852~1855.
-
[8]
D Goyard, B Konya, A S Chajistamatiou et al. Eur. J. Med. Chem., 2016, 108:444~454.
-
[9]
D Taber, N Picus, E I Becker et al. J. Am. Chem. Soc., 1955, 77:1010~1012. doi: 10.1021/ja01609a062
-
[10]
G Zheng, H Liu, M Wang. Chin. J. Chem., 2016, 34(5):519~523. http://d.wanfangdata.com.cn/Periodical/zghx-e201605015
-
[11]
Y Nagasawa, Y Tachikawa, E Yamaguchi et al. Adv. Synth. Catal., 2016, 358(2):178~182.
-
[12]
刘运奎, 江波, 徐振元. CN: 102977050A.
-
[13]
R Wang, C Chen, X Zhang et al. J. Med. Chem., 2015, 58(11):4713~4726. doi: 10.1021/acs.jmedchem.5b00470
-
[14]
E Campaigne, R L Thompson, J E Van Werth. J. Med. Pharm. Chem., 1959, 1:577~600.
-
[15]
H Elshihawy, M Hammad. Org Chem:Indian J., 2013, 9(2):41~57. http://europepmc.org/abstract/MED/26633023
-
[16]
潘高峰, 贺一君, 尹金玉. 广州化工, 2010, (2): 71~72+9. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=gzha201002026&dbname=CJFD&dbcode=CJFQ
-
[17]
胡辰飞, 汤啸, 李平等. 化学教育, 2014, (24): 23~25.
-
[1]
-
表 1 使用不同氧化剂时的产率
Table 1. The reaction yields for different oxidants
氧化剂 溶剂 温度 产率/% PCC 二氯甲烷 回流 34.3 Dess-Martin 二氯甲烷 回流 42.1 KMnO4 二氯甲烷 回流 0 MnO2 二氯甲烷 回流 56.2 表 2 氧化剂的用量对收率的影响
Table 2. Effect of the oxidant amount on the yield
2/MnO2(摩尔比) 1:2 1:4 1:6 1:8 1:10 1:12 产物质量/g 1.83 2.07 2.20 2.57 2.59 2.60 产率/% 56.20 63.50 67.60 78.90 79.30 79.60 反应条件:3.30g (0.02mol)化合物2,50mL二氯甲烷,回流反应6h 表 3 反应时间对收率的影响
Table 3. Effect of reaction time on the yields
反应时间/h 2 4 6 8 10 12 产物质量/g 1.07 2.07 2.57 2.94 2.96 2.94 产率/% 32.70 63.60 78.90 90.20 90.70 90.30 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0


 下载:
下载:
 下载:
下载:

