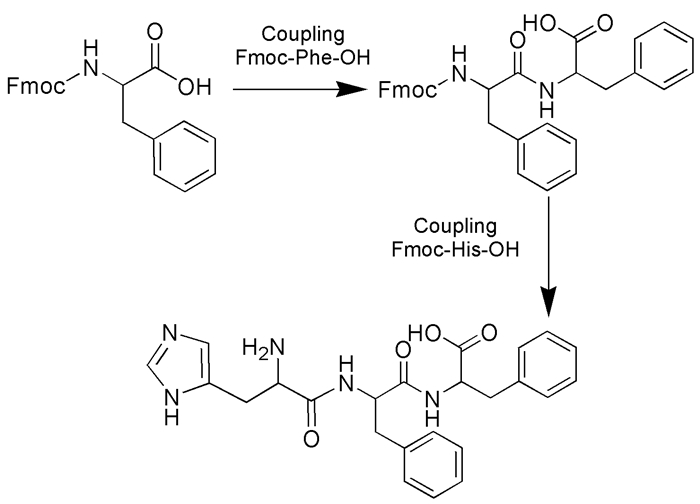
 图 图式1
HisFF的合成路线
Figure 图式1.
The synthetic route of HisFF
图 图式1
HisFF的合成路线
Figure 图式1.
The synthetic route of HisFF

Citation: Xue Peng, Zhang Shenghan, Zhang Yi, Wang Jide. Study on the Solid Phase Peptide Synthesis and Self-assembly Properties of Histidine-Diphenylalanine Molecule[J]. Chemistry, 2017, 80(3): 273-277.

固相合成法制备组氨酸-苯丙二肽分子及其自组装研究
English
Study on the Solid Phase Peptide Synthesis and Self-assembly Properties of Histidine-Diphenylalanine Molecule
-
Key words:
- Solid phase peptide synthesis
- / Diphenylalanine
- / Histidine
- / Gel
- / Self-assembly
-
超分子是一种可以构建不同形貌结构的优良组装模块。超分子凝胶因子由于能在特定条件下自组装成各种形状结构[1, 2],近年来受到广泛的关注,在生物材料[3]、传感和催化[4]、药物缓释[5]和光电子学[6]等众多领域具有潜在的应用价值。新型超分子凝胶因子的合成有望为新的软材料的制备创造条件。
2003年,Reches等[7, 8]发现阿尔茨海默病中Aβ淀粉样蛋白的核心片段苯丙二肽分子 (FF) 是一个良好的构建模块[7, 8],随后,相继出现大量以FF为核心的短肽修饰、形貌组装调控等方面的研究探索。FF分子易于修饰和控制,具有多重刺激响应性和良好生物相容性等特殊性质,广泛应用于纳米功能材料和生物传感等领域。不同功能性官能团的修饰赋予FF基短肽新的功能,其中,α氨基酸修饰FF的报道较为少见。本课题组先前选择带负电荷的脂肪族氨基酸天门冬氨酸 (Asp) 对FF进行修饰,在改善凝胶性能[9]和催化领域的应用[10]等方面取得了一定效果。将带有正电荷的杂环族组氨酸 (His) 引入体系,可为短肽的组装提供多种驱动力,有利于得到丰富多样的组装结构。
本文在组装性能优良的FF模块上,通过经典多肽固相合成法修饰组氨酸,合成组氨酸-苯丙氨酸二肽分子 (HisFF),并对HisFF的凝胶性能进行研究。同时,考察HisFF短肽分子在不同方法、不同溶剂条件下自组装的形貌,有利于研究超分子自组装的影响因素,调控出均一结构纳米材料。
1 实验部分
1.1 仪器与试剂
6210型质谱仪 (美国AGILENT公司);DRX 300核磁共振谱仪 (美国BRUKER公司);LC-300液相色谱仪 (美国Waters公司);UV-2450紫外可见分光光度计 (日本岛津公司);EQUINOX55傅里叶变换红外光谱仪 (德国BRUKER公司);902超低温冰箱 (美国THERMO公司);JEM-2010型扫描电镜 (SEM,日本JEOL公司);T20 TECNAI G2透射电镜 (TEM,美国FEI公司);PHSJ-4A酸度计 (上海雷磁公司)。
Fmoc-Phe-Wang Resin、Fmoc-Phe-OH (宁波康贝生化);六氟异丙醇 (HFIP)、二氮杂二环 (DBU)、苯并三氮唑-四甲基脲六氟磷酸酯 (HBTU)、三氟乙酸 (TFA)、乙二硫醇和苯甲硫醚 (阿拉丁试剂公司);N-甲基吗啡啉 (NMM)(安耐吉试剂公司);茚三酮 (国药沪试公司);乙酸乙酯 (EA)、N,N-二甲基甲酰胺 (DMF)、四氢呋喃 (THF)、甲苯、甲醇、乙腈等均为市售分析纯试剂。
1.2 HisFF固相合成方法
通过经典固相法合成HisFF (合成路线如图式1)。实验全程持续通入氮气保护,搅拌。合成步骤主要分为合成、裂解和纯化三部分。
1.3 HisFF凝胶制备与特性测试
1.4 HisFF形貌组装
称量1mg HisFF,加入10μL HFIP,超声溶解后,分别配制10mg/mL的丙酮、甲醇、乙醇、THF、EA和乙腈溶液及2mg/mL的乙腈溶液和50mg/mL的HFIP、二次水溶液。室温静置1h后,取10μL溶液滴加在硅片上,干燥后进行电镜分析。同样条件下,对比单一溶剂 (不加HFIP溶剂) 时组装的形貌。
1.2.2 树脂裂解
配置裂解液 (TFA 92.5%,乙二硫醇2.5%,苯甲硫醚2.5%,水2.5%;体积比),充分混合均匀,置于2~8℃环境下冷冻30min以上;向合成得到的树脂中加入配置好的裂解液 (10mL/g)。置于25℃下,于摇床中振荡反应2.5h,用砂芯漏斗 (3#) 过滤,弃去滤渣,滤液沉淀到乙酸乙酯中,离心后真空干燥,得到多肽粗品。
1.2.1 短肽的固相合成
称取0.6mmol Fmoc-Phe-Wang树脂 (取代度为0.75mmol/g) 加入固相合成管中,用50mL DMF溶胀3h,然后用DMF洗涤;加入50mL 20%的DBU/DMF溶液,30min后减压抽滤,除去反应液后用DMF洗涤;向合成管中加入18mmol Fmoc-Phe-OH、15mL DMF和17.1mmol HBTU,待彻底溶解后加入36mmol NMM,反应1h,取少量产物做茚三酮显色试验 (呈阴性则反应完成)。偶联成功后分别用DMF和MeOH洗涤。再重复偶联氨基酸,加入50mL 20% DBU/DMF溶液,30min后真空抽滤,向反应器中加入18mmol Fmoc-His-OH、15mL DMF和17.1mmol HBTU,待彻底溶解后加入36mmol NMM,反应1h后,再做茚三酮显色试验直到完成偶联。整个序列合成完成后,用DMF和MeOH洗涤,真空干燥后备用。
1.2.3 短肽纯化及结构确证
将多肽粗品用少量乙腈和水溶解,用0.45μm有机滤膜过滤,滤液进入制备型HPLC进行分离制备,收取目标峰。通过质谱确定产物的分子量 (质谱条件如下:离子源:ESI (+);扫描范围 (m/z):200~2000;毛细管电压:3500V;干燥温度:330℃;干燥气流速:9.0L/min;喷雾器压力:35.0psi),并用HPLC检测其化学纯度。得到上述多肽制备液后,将样品溶液置于冻干瓶中,在液氮中预冻10min后冷冻干燥24h,得到多肽粉末,取少量粉末做1H NMR分析测试。
1.3.2 最小胶凝浓度的测定
最小成胶浓度 (MGC) 是表征凝胶因子凝胶能力的重要指标[11, 12]。取适量HisFF短肽,加入50μL HFIP完全溶解,再混合1mL溶剂置于密封瓶中,超声诱导组装凝胶。所得到的稳定的凝胶时所需凝胶剂HisFF的最小浓度,即为该温度下该凝胶因子的MGC。
1.3.3 临界溶解温度的测定
选择MGC HisFF凝胶,从室温开始缓慢升温 (10℃/h),当观察到凝胶由固态胶体状缓慢变为溶液状态,保持温度,至凝胶完全变为溶液,此温度即为临界溶解温度。
1.3.1 HisFF凝胶制备
将HisFF配制成浓度为0.2mol/L的HFIP溶液。取50μL母液,然后用不同有机溶剂将溶液稀释至最终浓度为5mmol/L。超声5min得到有机凝胶。
2 结果与讨论
2.1 HisFF的合成与表征
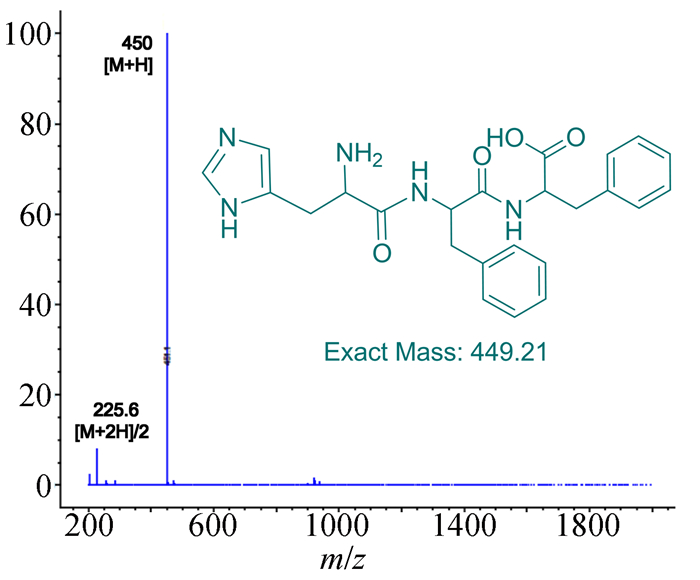
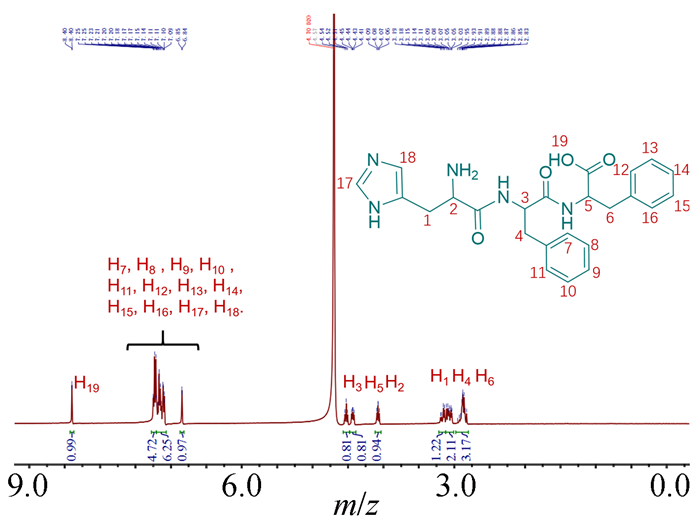
粗产品通过制备型HPLC进行提纯得后到纯品。在其质谱图 (图 1) 中,[M+1]+=450,可知被分析物的相对分子质量为449,与目标产物HisFF分子量符合。纯化后的产物进行1H NMR (溶剂D2O) 分析 (图 2),进一步确证其结构。
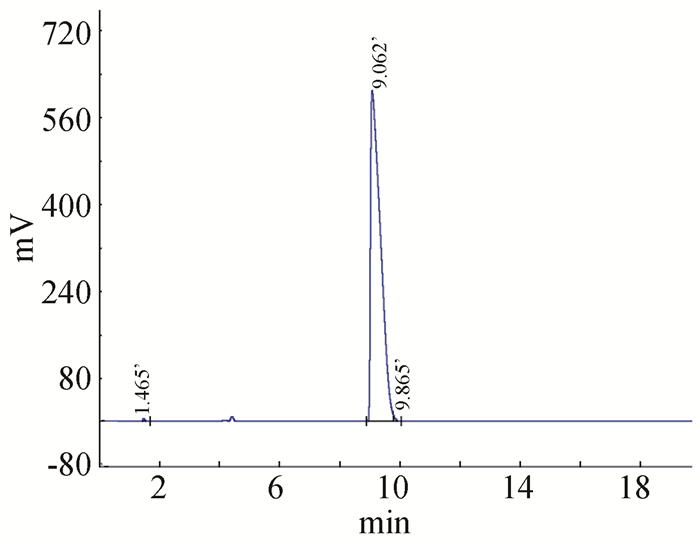
利用HPLC对经提纯后的产品进行纯度分析。由图 3可知,HisFF的保留时间为9.062min,纯度高达99.07%。
2.2 HisFF凝胶
HisFF凝胶因子在甲苯和氯仿溶剂中均可以形成无色透明的凝胶,其中甲苯凝胶具有较好的稳定性,而氯仿凝胶则较易坍塌。图 4为不同溶剂中成胶后的TEM照片,甲苯中,HisFF凝胶为纤维交缠的三维网状结构,而氯仿中HisFF凝胶则有明显的重叠,部分结构堆积重叠,使其较易坍塌,机械稳定性差。HisFF在单独的乙酸乙酯溶剂中,也可形成脆弱的乳白色凝胶,但在半小时内坍塌。薄弱且聚集的纤维结构,是导致凝胶机械强度较差的原因。由此可知,纤维强度和聚集形态影响凝胶的强度。
由图 5可知,室温下,在凝胶因子的甲苯溶液浓度≥5mg/mL时,体系呈现凝胶状态;浓度小于5mg/mL时,为溶胶状态。HisFF纤维横向交联形成的三维网络结构,最大程度地阻止溶剂的流动,从而成为胶状物。HisFF甲苯凝胶的临界成胶浓度为5mg/mL。
绝大部分超分子凝胶都表现出敏感的温度响应。这是由于温度升高,分子运动加快,使部分凝胶因子分子无法参与组装,分子间非共价键作用力无法作为主要驱动力来维持组装结构形貌。实验结果证明,HisFF甲苯凝胶是可逆温敏性凝胶,临界溶解温度为353K (图 6)。将HisFF甲苯溶胶置于室温环境下冷却,凝胶又能重新凝固为固态。
2.3 HisFF在不同溶剂中自组装
大量研究人员通过有机溶剂来调控多肽的自组装行为[11, 12]。传统的方法是用少量溶液溶解多肽分子,然后加入其他溶剂作为共溶剂来促进多肽分子组装。也有一些工作是利用纯有机溶剂诱导组装,通常情况下会得到不同的结构。例如,FF溶于HFIP后,用水稀释促进组装,可以得到纳米管或纳米线形貌[13, 14];而在纯水溶剂中,会组装成纳米纤维[15]。选择HisFF直接溶解在纯溶剂中和先用HFIP溶解再稀释两种方法,用多种有机溶剂诱导HisFF结构自组装形貌,结果发现,在相同浓度和静止时间下,部分溶剂对调控HisFF组装形貌影响较大。
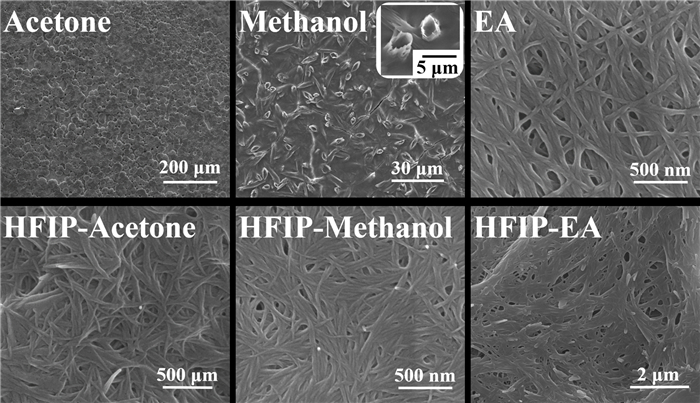
通过样品的SEM图 (图 7) 发现,浓度为10mg/mL的HisFF丙酮溶液,可组装成直径约为50nm的纳米球粒;而将HFIP溶解的HisFF再由丙酮稀释成同等浓度,会组装成较粗的纤维短棒。浓度为10mg/mL的HisFF甲醇溶液,可组装成直径约为4μm的微米管;而将HFIP溶解的HisFF再由甲醇稀释成同等浓度,微米管会变成纳米纤维。同样,浓度为10mg/mL的HisFF EA溶液,可组装成螺旋状纳米纤维;而将HFIP溶解的HisFF再由EA稀释成同等浓度,螺旋纳米纤维消失,网状的纳米纤维粘联在一起。
在THF中,10mg/mL的HisFF为可组装成直径约为50nm的纳米纤维;在乙醇中可组装成较细、密集的纳米纤维;在乙腈中,可组装成较粗的纳米短纤。而先将HisFF溶解在HFIP后,再由上述3种溶剂稀释至同浓度,其形貌没有明显变化。
HisFF的自组装是在大量氢键和π-π堆积等分子间弱相互作用力下协同完成的,它们引导HisFF的自组装,任何影响驱动力的因素的改变,都可能对组装的形貌结构产生影响。在制样方法及溶液浓度相同的情况下,HisFF水溶液随着静置时间的增加,其组装的形貌也有所不同。配制50mg/mL的HisFF水溶液,室温静置1h促进HisFF组装,大量氢键和苯环π-π堆积作用力为HisFF分子组装提供了驱动力,此时得到了团聚在一起的直径较细且相互交叉较少的纤维。随着孵化时间的增加,由于HisFF分子与水分子形成分子间氢键,促进其在水溶液中一直不断地完成自组装过程,产生的结构由简单到复杂,直到其内能趋于稳定,整个自组装过程比较缓慢。常温孵化一星期,大量细长纤维不断聚集,紧密排列组成粗纤维而析出。局部放大后可以看到粗纤维是由大量细小纤维紧密排列组成。组成网状粗纤维的孔隙较大,导致无法束缚水分子,未能形成凝胶 (图 9)。
3 结论
本文通过经典多肽固相合成法合成了HisFF有机凝胶因子,其可以在多种溶剂中形成凝胶,并且,该凝胶因子在不同溶剂、不同组装方法条件下,可以组装成不同的形貌。这一新型超分子凝胶因子的合成有望为新的软材料的制备创造条件。
-
-
[1]
P Terech, R G Weiss. Chem. Rev., 1997, 97(8):3133-3159. doi: 10.1021/cr9700282
-
[2]
J Raeburn, D J Adams. Chem. Commun., 2015, 51(25):5170-5180. doi: 10.1039/C4CC08626K
-
[3]
S G Zhang. Nat. Biotech., 2003, 21(10):1171-1178. doi: 10.1038/nbt874
-
[4]
Z F Sun, L Deng, H Gan et al. Biosens. Bioelectron., 2013, 39(1):215-219. doi: 10.1016/j.bios.2012.07.050
-
[5]
Z Z Zhang, T He, M Y Yuan et al. Chem. Commun., 2015, 51(87):15862-15865. doi: 10.1039/C5CC05195A
-
[6]
J H Kim, S Y Lim, D H Nam et al. Biosens. Bioelectron., 2011, 26(5):1860-1865. doi: 10.1016/j.bios.2010.01.026
-
[7]
M Reches, E Gazit. Science, 2003, 300(5619):625-627. doi: 10.1126/science.1082387
-
[8]
J Liu, P L He, J L Yan et al. Adv. Mater., 2008, 20(13):2508-2511. doi: 10.1002/adma.200703195
-
[9]
P Xue, H Q Wu, X J Wang et al. Sci. Rep., 2016, 6:25390. doi: 10.1038/srep25390
-
[10]
P Xue, Y N Wei, H Q Wu et al. Colloids Surf. A, 2016, 506:514-518. doi: 10.1016/j.colsurfa.2016.06.048
-
[11]
Y Jeong, K Hanabusa, H Masunaga et al. Langmuir, 2005, 21(2):586-594. doi: 10.1021/la047538t
-
[12]
M Suzuki, M Yumoto, H Shirai et al. Tetrahedron, 2008, 64(45):10395-10400. doi: 10.1016/j.tet.2008.08.061
-
[13]
Y Su, X H Yan, A H Wang et al. J. Mater. Chem., 2010, 20(32):6734-6740. doi: 10.1039/c0jm00110d
-
[14]
M C Du, P L Zhu, X H Yan et al. Chem. Eur. J., 2011, 17(15):4238-4245. doi: 10.1002/chem.201003021
-
[15]
J Kim, T H Han, Y Kim et al. Adv. Mater., 2010, 22(5):583-587. doi: 10.1002/adma.200901973
-
[1]
-
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0







 下载:
下载:









 下载:
下载:

