 图 1
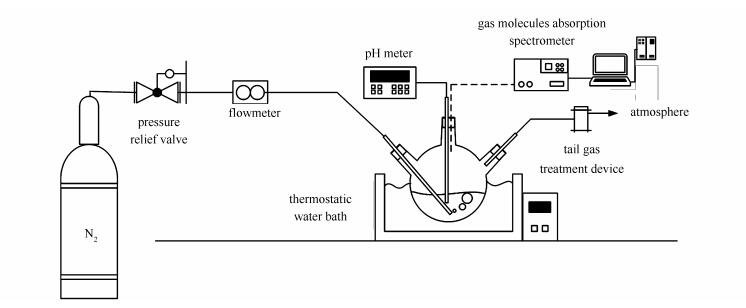
模拟实验装置示意图
Figure 1.
Schematic of the simulated device
图 1
模拟实验装置示意图
Figure 1.
Schematic of the simulated device

Citation: ZHAO Li, HE Qing-song, LIU Yu, WU Yang-wen, LU Qiang, LIU Song-tao, DONG Chang-qing. Mechanism of Hg2+ reduction in wet flue gas desulfurization liquors[J]. Journal of Fuel Chemistry and Technology, 2017, 45(6): 755-760.

湿法脱硫浆液中Hg2+的还原机制研究
English
Mechanism of Hg2+ reduction in wet flue gas desulfurization liquors
-
Key words:
- Hg2+ reduction
- / pH value
- / slurry temperature
- / ion concentration
- / wet desulfurization
-
燃煤电厂作为主要的汞排放源之一,因其排放量巨大,越来越受到人们的关注。2011年7月,中国环保部发布的《火电厂大气污染物排放标准》(GB13223—2011) 中规定,燃煤锅炉汞及其化合物的排放量低于0.03mg/m3[1],同时《火电厂石灰石-石膏湿法脱硫废水水质控制指标》(DL/T997—2006) 中规定,处理后脱硫废水中总汞含量低于0.05mg/L[2]。因此,降低火电厂汞的排放量迫在眉睫。
研究表明,选择性催化还原法(SCR)可将烟气中Hg0协同催化氧化为Hg2+,再通过湿法脱硫系统将Hg2+吸收[3-6]。根据中电联发布的2013年度火电厂烟气脱硫、脱硝、除尘产业信息,截至2013年底,已投运火电厂烟气脱硝机组容量约4.3×108kW,占中国现役火电机组容量的50%,其中,96%的机组采用SCR法脱硝[7]。随着相关环保政策的落实,这一数据将逐渐增大,也就意味着经脱硝系统氧化后湿法脱硫系统将吸收更多的Hg2+。然而,世界各国学者研究表明,烟气中的Hg2+被湿法脱硫系统吸收后会被再次还原为Hg0,导致脱汞效率降低,造成二次污染[8-15]。因此,本研究围绕上述问题展开,通过模拟真实湿法脱硫系统,研究Hg2+再释放机制,探讨影响汞再释放的主要因素,为湿法脱硫系统脱汞工艺及进一步筛选汞再释放抑制剂提供理论基础。
1 实验部分
模拟实验装置示意图见图 1。装置主要由模拟气体钢瓶、鼓泡反应器、尾气处理等部分构成。典型工况为:将预先配置的含有250mL 100μg/L Hg2+、100mmol/L Cl-溶液加入至500mL三口烧瓶中,保持水浴温度为55℃,加入一定量Na2SO3(溶液中SO32-=5mmol/L),迅速调剂溶液的pH值(溶液的pH值通过pH计实时监测,并通过添加缓冲液溶液控制溶液pH值)。控制质量流量计,维持N2流量为1.5L/min,N2作为载体并起到鼓泡搅拌的作用,其从液体表面经过时,将脱硫浆液中还原逸出的零价汞带入H2SO4/KMnO4吸收液后,排至大气。在实验中,Hg2+、Cl-、SO32-、Ca2+、Mg2+分别由HgCl2、Na2SO3、NaCl、CaCl2、MgCl2提供,缓冲溶液由邻苯二甲酸氢钾和混合磷酸盐配制而成。
本实验采用单一变量法,改变SO32-浓度、浆液温度、浆液pH值、Cl-浓度等主要因素,每隔一定时间用5mL移液管对反应液进行取样,稀释至50mL的容量瓶中,定容摇匀后,利用GMA3212(上海北裕分析仪器有限公司)检测样品中的Hg2+的含量。
2 结果与讨论
根据上述实验过程,于缓冲溶液中预先加入100μg/L Hg2+,考察温度、pH值及SO32-、Cl-、Ca2+、Mg2+浓度等因素对Hg2+在鼓泡反应器中被还原为Hg0的影响,通过气相分子吸收光谱仪测量Hg2+浓度,从而得出鼓泡反应器浆液中Hg2+浓度变化,确定其再释放特性。为了保证所考察因素对Hg2+还原影响的准确性和减小误差,研究首先进行了空白实验。即在温度55℃、pH值为5.5,通入1.50L/min N2的实验条件下,Hg2+初始浓度CHg2+, 0为95.1μg/L,实验持续时间120min后,Hg2+浓度基本未发生变化。
2.1 SO32-浓度对Hg2+还原性能的影响
湿法脱硫系统浆液中由于不断地吸收烟气中的SO2,浆液中会含有大量的S(IV),其浓度明显高于Hg2+浓度,许多研究表明,S(IV)是Hg2+还原成Hg0的主要还原剂[14-16]。在浆液S(IV)浓度明显高于Hg2+的条件下,汞主要以较为稳定Hg(SO3)22-形式存在,且在一定条件下,Hg(SO3)22-可分解生成HgSO3,HgSO3极不稳定,会分解释放Hg0。HgSO3的分解是液相二价汞还原的主要原因[16]。
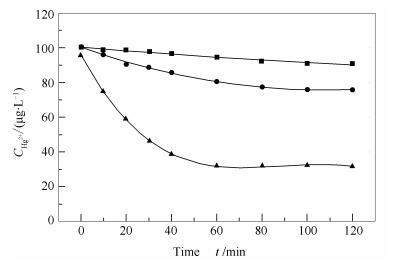
在温度55℃,pH值为5.5,考察SO32-的浓度对Hg2+还原性能的影响,具体见图 2。由图 2可知,随着溶液中SO32-浓度的增大,Hg2+的还原速率明显降低。当SO32-浓度分别为1和5mmol/L,在120min时,汞的还原率为66.5%和18.3%,SO32-浓度增大至10mmol/L时,Hg2+的还原被抑制。可见,Hg2+的还原速率随着溶液中SO32-浓度的增大而降低。这一结论与Sun等[17]和Heidel等[20]的研究结论一致,Sun等研究认为,Hg2+的还原与S(IV)存在明显的相关性,相关系数达0.96。这是由于起初SO32-浓度较低时,Hg2+与SO32-主要发生HgSO3的生成反应以及Hg2+被还原为Hg0、SO32-被氧化为SO42-的氧化还原反应,其反应机理如下:
在湿法脱硫系统中,上述反应被捕获的二价汞被还原为零价汞,而使汞元素被再释放。Carolinaa等[18]和Omine等[19]研究认为,氧浓度的变化对液相二价汞再释放的抑制作用源于氧对亚硫酸根的氧化,路径见式(3)。因此,增大脱硫浆液氧浓度可以导致上述式(2) 反应向左进行,从而抑制Hg0的再释放。
随着S(IV)的增加,即SO32-浓度的升高,HgSO3可以跟SO32-生成更稳定的Hg(SO3)22-络合产物,而使Hg2+的还原率下降[20],其反应机理为:
2.2 pH值对Hg2+还原性能的影响
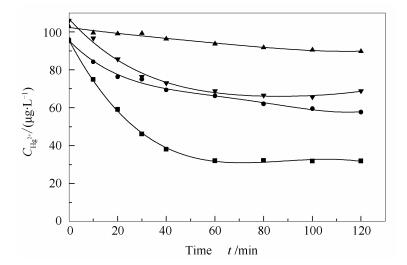
pH值能够显著影响Hg2+还原,是因为其会影响浆液中离子的电极电势和硫酸盐离子在溶液中的分布[21]。不同pH值对汞再释放的影响见图 3。在SO32-浓度为5mmol/L、55℃的实验条件下,随着pH值从3增加到5.5,Hg2+的还原率增加;但当pH值增加到7时,还原率又再次降低。即在pH值为5.5时,Hg2+的还原率最大,在120min时,Hg2+还原率达到66.5%。最小为pH值为3时,Hg2+的还原率仅为13.84%。结合2.1分析可知,在pH值为3时,溶液中SO32-主要以H2SO3分子存在,这不利于SO32-与溶液中Hg2+反应生成HgSO3,故Hg2+还原率较低;随着pH值升高至5.5,溶液中存在大量的SO32-且会促进式(6) 平衡向右进行,从而促使Hg2+的浓度降低;当pH值继续升高至7时,溶液中的OH-会与Hg2+反应,生成不易分解的Hg(OH)2,使式(7) 反应平衡右移,从而降低Hg2+的还原[22-24]。
这一研究结论也被Miretzky等[24]的实验验证,其研究表明,汞在pH值小于3时,主要以Hg2+和HgCl+的形式存在,在pH值为3-7以Hg(OH)+和Hg(OH)2形式存在,pH值的升高可以加速Hg2+向Hg(OH)+转化,进一步形成Hg(OH)2,转化过程也遵循式(7)。
2.3 温度对Hg2+还原性能的影响
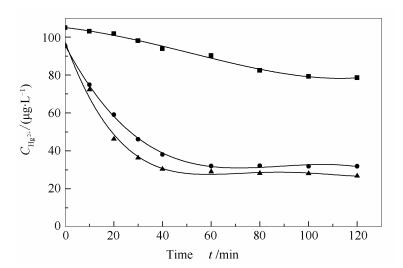
通常电厂烟气洗涤系统的运行温度在40-60℃,实验选择SO32-浓度为5mmol/L、pH值为5.5、温度为40-70℃时考察温度对Hg2+还原性能的影响。结果见图 4。
温度为40、55、70℃时,Hg2+在120min时的还原率分别为25.2%、66.5%、72.1%,即随着温度的升高,Hg2+的还原率逐渐增加,这表明, 温度对Hg2+的还原产生了显著影响,分析原因认为升高温度更有利于反应式(1)-(4) 的正向进行,而低温会使Hg2+的还原率降低[16]。这一结论也被许多实验研究验证,如Peng等[25]的研究认为,质子在气相中的扩散和HgSO3的分解都随着温度的升高而加速,高温不利于形成相对稳定的物质,如Hg(SO3)22-;此外,温度升高,Hg0的溶解度会降低[23]。Heidel等[20]研究也表明,浆液温度低于50℃时,Hg0的生成率明显降低。因此,温度对Hg0再释放有显著的影响,降低温度有利于汞的稳定存在。
2.4 Cl-浓度对Hg2+还原性能的影响
在湿法脱硫系统中,Cl-是最常见的离子之一,由于浆液的反复循环,其很容易累积较高的浓度,并与Hg2+形成

本研究在反应温度为55℃、pH值为5.5、SO32-为5mmol/L实验条件下,考察Cl-浓度对Hg2+还原性能的影响,具体见图 5。
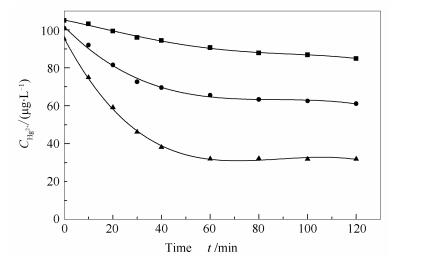
由图 5可知,随着Cl-浓度的升高,Hg2+的还原率逐渐降低。Cl-浓度为1、100、200mmol/L时,Hg2+在120min时的还原率分别为66.5%、39.5%、19.1%。这是由于Cl-的存在会与HgSO3形成更难分解的化合物

2.5 Ca2+和Mg2+浓度对Hg2+还原性能的影响
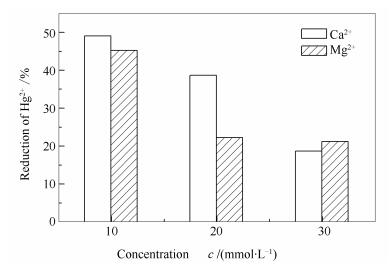
Ca2+和Mg2+作为脱硫浆液中含量最多的阳离子,研究其对Hg2+还原的影响具有重要的现实意义。本实验在SO32-浓度为5mmol/L、温度55℃、pH值为5.5的条件下,考察Ca2+、Mg2+离子浓度对Hg2+还原性能的影响,具体见图 6。
由图 6可知,Mg2+初始浓度分别为10、20、30mmol/L时,反应120min后,Hg2+的还原率分别为49.15%、38.78%、18.75%;Ca2+离子在此浓度和反应时间下,Hg2+的还原率分别为45.34%、22.34%、21.30%。分析原因认为,Ca2+、Mg2+主要是通过影响脱硫浆液中pH值、SO32-浓度等因素的变化,从而影响汞的还原速率。当浆液中含有Ca2+和Mg2+时,会优先与浆液中的SO32-反应生成CaSO3和MgSO3沉淀,溶液中SO32-的浓度下降,Hg2+的还原被抑制;另外,由于CaSO3的沉淀平衡常数小于MgSO3的平衡常数,会导致Ca2+对Hg2+的还原抑制程度强于Mg2+[29],在脱硫系统中,CaSO3会被进一步强制氧化生成CaSO4。
3 结论
pH值、温度以及SO32-、Cl-、Ca2+、Mg2+的浓度等因素对湿法脱硫系统中Hg2+的还原反应有显著影响。随着浆液中SO32-浓度的增加,高浓度的SO32-和HgSO3生成更稳定的Hg(SO3)22-络合产物,从而使Hg2+还原率降低。低pH值(pH=3) 和高pH值(pH=7) 对Hg2+还原有较好的抑制作用,在其他影响因素确定条件下,可通过调节电厂脱硫浆液中pH值控制Hg0的再释放。脱硫浆液在40-60℃条件下,温度越低越有利于抑制Hg2+的还原。Ca2+、Mg2+浓度的增加通过影响脱硫浆液中pH值、SO32-浓度等因素间接导致Hg2+的还原率下降,Cl-则通过与HgSO3反应生成稳定的络合物抑制Hg2+被还原。
-
-
[1]
GB13223-2011,火电厂大气污染物排放标准[S].GB13223-2011, Emission standard of air pollutants for thermal power plants[S].
-
[2]
DL/T997-2006, 火电厂石灰石-石膏湿法脱硫废水水质控制指标[S].DL/T997-2006, Discharge standard of wastewater from limestone-gypsum flue gas desulfurization system in fossil fuel power plants[S].
-
[3]
PAVLISH J H, SONDREAL E A, MANN M D, OLSON E S, GALBREATH K C, LAUDAL D L, BENSON S A. Status review of mercury control options for coal-fired power plants[J]. Fuel Process Technol, 2003, 82(2/3): 89-165.
-
[4]
钟丽萍, 曹晏, 李文英, 潘伟平, 谢克昌. 燃煤电厂污染控制单元对汞释放的控制作用[J]. 燃料化学学报, 2010,38,(6): 641-646. ZHONG Li-ping, CAO Yan, LI Wen-ying, PAN Wei-ping, XIE Ke-chang. Effect of the existing air pollutant control devices on mercury emission in coal-fired power plants[J]. J Fuel Chem Technol, 2010, 38(6): 641-646.
-
[5]
PUDASAINEE D, LEE S J, LEE S H, KIM J H, JANG H N, CHO S J, CHILSEO Y. Effect of selective catalytic reactor on oxidation and enhanced removal of mercury in coal-fired power plants[J]. Fuel, 2010, 89(4): 804-809. doi: 10.1016/j.fuel.2009.06.022
-
[6]
赵莉, 何青松, 李琳, 陆强, 董长青, 杨勇平. 改性SCR催化剂对Hg0催化氧化性能的研究[J]. 燃料化学学报, 2015,43,(5): 628-634. ZHAO Li, HE Qing-song, LI Lin, LU Qiang, DONG Chang-qing, YANG Yong-ping. Research on the catalytic oxidation of Hg0 by modified SCR catalysts[J]. J Fuel Chem Technol, 2015, 43(5): 628-634.
-
[7]
YANG J, YANG Q, SUN J, LIU Q C, ZHAO D, GAO W, LIU L. Effects of mercury oxidation on V2O5-WO3/TiO2 catalyst properties in NH3-SCR process[J]. Catal Commun, 2015, 59: 78-82. doi: 10.1016/j.catcom.2014.09.049
-
[8]
中电联节能环保分会. 中电联发布2013年度火电厂烟气脱硫、脱硝、除尘产业信息[EB/OL]. http: //www. cec. org. cn/huanbao/jienenghbfenhui/fenhuidongtai/fenhuixinwen/2014-05-06/121258.html, 2014. 05. 06.
-
[9]
LIU Y, WANG Q F, MEI R J, WANG H Q, WENG X L, WU Z B. Mercury re-emission in flue gas multi-pollutants simultaneous absorption system[J]. Environ Sci Technol, 2014, 48(23): 14025-14030. doi: 10.1021/es503837w
-
[10]
WANG Q F, LIU Y, WANG H Q, WENG X L, WU Z B. Mercury re-emission behaviors in magnesium-based wet FGD process:The effects of oxidation inhibitors[J]. Energy Fuels, 2015, 29(4): 2610-2615. doi: 10.1021/ef502833k
-
[11]
李志超, 段钰锋, 王运军, 黄治军, 孟素丽, 沈解忠. 300MW燃煤电厂ESP和WFGD对烟气汞的脱除特性[J]. 燃料化学学报, 2013,41,(4): 491-498. LI Zhi-chao, DUAN Yu-feng, WANG Yun-jun, HUANG Zhi-jun, MENG Su-li, SHEN Jie-zhong. Mercury removal by ESP and WFGD in a 300 MW coal-fired power plant[J]. J Fuel Chem Technol, 2013, 41(4): 491-498.
-
[12]
CHANG J C S, ZHAO Y X. Pilot plant testing of elemental mercury reemission from a wet scrubber[J]. Energy Fuels, 2007, 22(1): 338-342.
-
[13]
LOON L V, MADER E, SCOTT S L. Reduction of the aqueous mercuric ion by sulfite:UV spectrum of HgSO3 and its intramolecular redox reaction[J]. J Phys Chem A, 2000, 104(8): 1621-1626. doi: 10.1021/jp994268s
-
[14]
CHANG J C S, GHORISHI S B. Simulation and evaluation of elemental mercury concentration increase in flue gas across a wet scrubber[J]. Environ Sci Technol, 2003, 37(24): 5763-5766. doi: 10.1021/es034352s
-
[15]
VAN LOON L L, MADER E A, SCOTT S L. Sulfite stabilization and reduction of the aqueous mercuric ion:Kinetic determination of sequential formation constants[J]. J Phys Chem A, 2001, 105(13): 3190-3195. doi: 10.1021/jp003803h
-
[16]
SUN M Y, CHENG G H, LU R J, TANG T M, SBAIG H A, XU X H. Characterization of Hg0 re-emission and Hg2+ leaching potential from flue gas desulfurization (FGD) gypsum[J]. Fuel Process Technol, 2014, 118: 28-33. doi: 10.1016/j.fuproc.2013.08.002
-
[17]
CAROLINA A C, BRECHTEL K, SCHEFFKNECHT G, BRAß M. The effect of chlorine and oxygen concentrations on the removal of mercury at an FGD-batch reactor[J]. Fuel, 2009, 8(12): 2489-2494.
-
[18]
OMINE N, ROMERO C E, KIKKAWA H, WU S, ESWARAN S. Study of elemental mercury re-emission in a simulated wet scrubber[J]. Fuel, 2012, 91(1): 93-101. doi: 10.1016/j.fuel.2011.06.018
-
[19]
HEIDEL B, HILBER M, SCHEFFKNECHT G. Impact of additives for enhanced sulfur dioxide removal on re-emissions of mercury in wet flue gas desulfurization[J]. Appl Energy, 2014, 114: 485-491. doi: 10.1016/j.apenergy.2013.09.059
-
[20]
WO J J, ZHANG M, CHENG X Y, ZHONG X H, XU J, XU X H. Hg2+ reduction and re-emission from simulated wet flue gas desulfurization liquors[J]. J Hazard Mater, 2009, 172(2): 1106-1110.
-
[21]
陈传敏, 张建华, 俞立. 湿法烟气脱硫浆液中汞再释放特性研究[J]. 中国电机工程学报, 2011,31,(5): 48-51.
-
[22]
CHEN Chuan-min, ZHANG Jian-hua, YU Li. Study on the characteristics of mercury re-emission from wet flue gas desulfurization solution[J]. Proc CSEE, 2011, 31(5): 48-51.
-
[23]
MIRETZKY P, BISINOTI M C, JARDIM W F, ROCHA J C. Factors affecting Hg(Ⅱ) adsorption in soils from the Rio Negro Basin (Amazon), Quím[J]. Quím Nova, 2005, 28(3): 438-443. doi: 10.1590/S0100-40422005000300014
-
[24]
PENG B, LIU Z L, CHAI L Y, LIU H, YANG S, YANG B T, XIANG K S, LIU C. The effect of selenite on mercury re-emission in smelting flue gas scrubbing system[J]. Fuel, 2016, 168: 7-13. doi: 10.1016/j.fuel.2015.11.072
-
[25]
LIU Y, WANG Y J, WU Z B, ZHOU S Y, WANG H Q. A mechanism study of chloride and sulfate effects on Hg2+reduction in sulfite solution[J]. Fuel, 2011, 90(7): 2501-2507. doi: 10.1016/j.fuel.2011.02.036
-
[26]
OCHOA-GONZÁLEZ R, DÍAZ-SOMOANO M, MARTÍNEZ-TARAZONA M R. Effect of anion concentrations on Hg2+ reduction from simulated desulphurization aqueous solutions[J]. Chem Eng J, 2013, 214: 165-171. doi: 10.1016/j.cej.2012.09.037
-
[27]
王青峰. 湿法脱硫系统中氧化态汞的还原行为及脱硫石膏中汞的稳定性研究[D]. 杭州: 浙江大学, 2015.
-
[28]
成潇雅, 汤婷媚, 张萌, 钟晓航, 沃静静, 徐新华. 烟气脱硫液中Hg2+还原及稳定化初探[J]. 浙江大学学报(理学版), 2010,5,568-571. doi: 10.3785/j.issn.1008-9497.2010.05.020
-
[1]
-
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0


 下载:
下载:





 下载:
下载:

