 图 1
催化剂的XRD谱图
Figure 1.
XRD patterns of various CuO/Ce-Zr-RE-O2 catalysts
图 1
催化剂的XRD谱图
Figure 1.
XRD patterns of various CuO/Ce-Zr-RE-O2 catalysts

Citation: LU Xiao-lin, LIU Zi-kui, MA Su-fang, BAI Xue. Effect of Dy and Y doping on the catalytic performance of CuO/CeZrO2 for the preferential oxidation of CO in H2-rich stream[J]. Journal of Fuel Chemistry and Technology, 2016, 44(7): 870-875.

Dy和Y掺杂改性对CuO/CeZrO2催化剂在富氢气氛中CO优先氧化催化性能的影响
English
Effect of Dy and Y doping on the catalytic performance of CuO/CeZrO2 for the preferential oxidation of CO in H2-rich stream
-
Key words:
- CuO
- / CeZrO2 mixed oxide
- / preferential oxidation of CO
- / H2-rich stream
- / Dy2O3
- / Y2O3
-
质子交换膜燃料电池(PEMFC) 由于其高效、清洁、无污染等优点在未来能源系统中具有很好的应用前景[1, 2]。然而,由重整制得的并作为燃料电池最具前景的燃料--高效与接近零污染排放的氢气[3]中通常含有微量的CO,这会导致燃料电池的Pt电极中毒。CO选择性氧化是被认为用于去除富氢气体中CO最简单、最有效的方法之一[4]。
将贵金属元素(以Au、Pt、Rh、Pd等元素为活性组分) 负载到CeO2、La2O3、Fe2O3和TiO2(活性载体) 以及Al2O3、SiO2和MgO (惰性载体) 等金属氧化物上能够得到CO氧化活性与选择性较好的催化剂[5], 但贵金属价格昂贵、资源有限,难以普及。Liu等[6, 7]曾报道非贵金属铜、铈混合氧化物催化剂比负载型铂基和铜基催化剂具有更好的CO催化氧化活性。因而铜铈催化剂成为研究热点之一。
目前,CuO/CeO2催化剂在CO优先氧化反应中展现了良好的催化性能。Fornasiero等[8]发现,二氧化铈中掺杂阳离子如锆,由于形成铈锆复合固溶体,其中的高氧迁移率使载体中的氧空位增加,从而提高氧化还原性能。Wang等[9]对比研究了CuO/Ce0.8Zr0.2O2与CuO/CeO2两种催化剂性能,发现前者具有更好的热稳定性。Vidmar等[10]将Y、La、Pr、Nd、Sm等稀土元素掺杂到CuO/Ce1-xZrxO2催化剂体系中,形成的固溶体可以在较低的温度下使CeO2在表面与体相进行Ce4+/Ce3+之间的氧化还原转化,从而降低了固溶体的氧化还原温度,提高了催化剂的催化性能。
研究在CuO/Ce0.9Zr0.1O2催化剂中掺入不同含量的稀土元素Dy、Y,通过一系列表征手段考察了添加不同含量Dy、Y后的催化剂对CO优先氧化反应和抗CO2性能的影响,以及对催化剂稳定性的影响。
1 实验部分
1.1 催化剂的制备
通过水热浸渍法制备CuO/Ce-Zr-RE-O2催化剂,样品中Ce:Zr:RE=0.9-x:0.1:x(RE=Dy时,x=0、0.01、0.03、0.05,依次记为CZ、CZD1、CZD3、CZD5;RE=Y时, x=0.03、0.05、0.07,依次记为CZY3、CZY5、CZY7)。将一定量的模板剂十六烷基三甲基溴化氨(CTABr) 溶于蒸馏水中,在搅拌状态下滴加适量25%的氨水,将模板剂溶液的pH值调至11左右;将一定量的硝酸铈和硝酸氧锆溶于蒸馏水中,(制备添加稀土元素的催化剂时,需将稀土氧化物溶于硝酸中制成硝酸盐溶液,混合于铈锆混合液中) 制成0.1 mol/L的混合溶液,将混合溶液和25%的氨水同时逐滴加入模板剂溶液中,保持混合溶液的pH值在11左右,搅拌4 h,直到混合溶液成溶胶状,将其移入不锈钢晶化釜内,90 ℃下晶化48 h;抽滤,去离子水洗涤后,乙醇洗涤。将固体产物于90 ℃干燥12 h;最后在马弗炉中400 ℃焙烧4 h,制得Ce-Zr-RE-O2复合载体。将复合载体用一定量的硝酸铜溶液浸渍(其中, CuO的负载量为12%),室温下放置24 h,90 ℃干燥12 h,600 ℃下焙烧2 h,得到一系列催化剂。
1.2 催化剂的评价
1.3 催化剂的表征
H2-TPR测试是常压下在U型管反应器中进行,还原气是流量为30 mL/min的H2-Ar混合气体(含7% H2, 体积分数),催化剂的用量为50 mg。测试时打开混合气体,待色谱基线走平后,将程序升温仪调到50 ℃,温度稳定后,升温并采集数据,升温至800 ℃,速率为10 ℃/min。测试采用气相色谱在线分析,TCD检测。比表面积(ABET) 测试采用美国Micromeritics公司生产的ASAP2020型自动物理吸附仪进行,比表面积使用BET模型计算。X射线衍射(XRD) 实验采用D8 advance型X射线衍射仪,以Cu Kα光源(λ=0.154 nm),管电流为100 mA,管电压为40 kV,步长是0.04°,扫描速率为6(°)/min,20°-80°扫描。
1.2.1 催化剂的性能与稳定性评价
催化剂的性能与稳定性评价是常压下于固定床反应器中进行,载气为氮气。催化剂的用量是150 mg,用石英砂稀释,混合均匀后装入U型管中。测试用的混合气的体积组成为:1% CO + 1% O2+ 50% H2+ N2平衡,空速为40 000 mL/(g·h)。测试采用日本岛津气相色谱在线分析,TCD检测。稳定性测试待CO完全转化后每1 h测定一次,连续48 h。
1.2.2 催化剂的抗CO2性能
测试采用日本岛津气相色谱在线分析,TCD检测。催化剂的用量为150 mg,用石英砂稀释,混合均匀后装入U型管中。测试用的混合气的体积组成为:1%CO + 1% O2+ 50% H2+15% CO2+ N2平衡,空速为20 000 mL/(g·h)。由下式计算CO的转化率和对CO2的选择性:
2 结果与讨论
2.1 XRD和BET表征
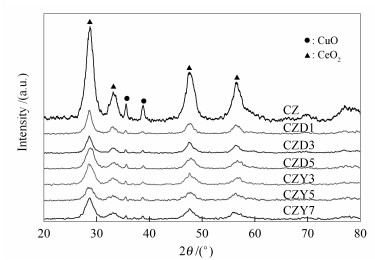
图 1为催化剂的XRD谱图。
由图 1可知,不同Dy2O3、Y2O3含量的Ce-Zr-RE催化剂在29°、33°、48°、57°时都表现出非常明显的CeO2衍射峰,分别对应CeO2的(111)、(200)、(220) 和(311) 晶面,是典型的萤石立方晶型结构。图 1中并未观察到明显的ZrO2、Dy2O3和Y2O3的衍射峰,原因可能由于Zr4+、Dy3+和Y3+进入Ce4+晶格,形成了Ce-Zr-Dy-O与Ce-Zr-Y-O固溶体,亦或以弥散的氧化物微细颗粒分散在催化剂中而无法被XRD检测到。当12%的CuO分别负载在CZ、CZD和CZY上时,CZD1和CZY3的晶相CuO特征衍射峰最弱,说明在铜铈锆催化剂中添加1%Dy2O3和3%Y2O3有利于活性组分CuO的分散。目前普遍认为,在CuO/Ce-Zr-O催化剂上CO氧化反应中,Cu簇中的Cu+物种为CO的吸附提供活性中心,CeO2提供氧源,反应在两种金属的界面进行。CuO在XRD谱图中的表现与催化性能测试相一致,CZD1和CZY3的活性最好,t50分别为82和81 ℃,100%转化时的温度均为115 ℃。
由Scherrer公式L=Kλ/B1/2cosθ计算出各CuO/Ce-Zr-RE-O2催化剂的晶粒粒径见表 1。由表 1可知,掺杂了稀土元素Dy后的催化剂比CZ催化剂的比表面积小,但孔径有所增大。一般来说,比表面积增大的同时会伴随着氧化物颗粒的粒径缩小,更多的活性中心暴露出来,这样有利于提高催化剂的活性[11]。然而,由表 1可知,比较掺杂了稀土元素Dy、Y后的催化剂与CZ催化剂以及CZD系列和CZY系列催化剂后发现,催化剂比表面积的大小并不是决定催化剂活性的最终因素[12]。催化剂CZ的比表面积达130.5 m2/g,但其t50为91 ℃,而比表面积相对较小的CZD1和CZD5催化剂, t50分别为82和83 ℃,Y2O3的掺杂量由3%增大到7%时,催化剂的比表面积是先逐渐增大然后陡然减小,但是根据催化性能测试可以发现,掺杂不同Y含量的催化性能要优于未掺杂的催化剂。这种现象可能是因为Ce4+ (0.097 nm,CN=8) 和Zr4+ (0.084 nm) 的离子半径比稀土元素Dy3+ (0.103 nm)、Y3+ (0.102 nm) 的离子半径小,当Dy3+、Y3+进入铈锆固溶体的晶格中后,在CeO2的结构保持不变的情况下,引起晶格膨胀。为了保持电价平衡,此时的固溶体必然形成一定程度的阴离子缺陷,由此产生的晶格应力和缺陷结构,增加了晶格氧的流动性,晶格离子的高流动性和氧扩散到催化剂面心立方晶格中的能力使固溶体的储氧能力增强,催化剂的催化活性也得到提高。又或者是由于加入稀土元素后有利于活性组分CuO在载体表层的分散,提高了相对单位密度的活性中心,有利于提高催化剂的催化性能。
 表 1
CuO/Ce-Zr-RE-O2催化剂的晶粒粒径、比表面积、孔径和孔容
Table 1.
Crystallite size, BET surface area, pore diameter and pore volume of various CuO/Ce-Zr-RE-O2 catalysts
表 1
CuO/Ce-Zr-RE-O2催化剂的晶粒粒径、比表面积、孔径和孔容
Table 1.
Crystallite size, BET surface area, pore diameter and pore volume of various CuO/Ce-Zr-RE-O2 catalysts
Sample 2 θ/(°) Interplanar spacing d/nm Crystallite size dCeO2(111) /nm ABET/(m2·g-1) Pore diameter d/nm Pore volume v/(cm3·g-1) CZ 28.94 0.308 3 8.51 130.5 6.31 0.265 CZD1 28.48 0.313 2 9.98 107.5 10.96 0.405 CZD3 28.64 0.311 4 10.18 99.4 8.35 0.288 CZD5 28.52 0.312 7 9.28 107.9 6.86 0.246 CZY3 28.93 0.308 0 8.53 127.1 5.64 0.256 CZY5 28.72 0.310 6 8.22 133.3 5.99 0.270 CZY7 28.88 0.308 9 9.11 119.3 8.10 0.330 dCeO2 (111) : calculated from Scherrer equation 表 1 CuO/Ce-Zr-RE-O2催化剂的晶粒粒径、比表面积、孔径和孔容
Table 1. Crystallite size, BET surface area, pore diameter and pore volume of various CuO/Ce-Zr-RE-O2 catalysts2.2 H2-TPR表征
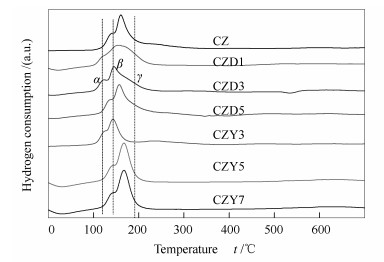
图 2为CZD和CZY系列催化剂的H2-TPR谱图。由图 2可知,各催化剂的CuO还原温度明显低于纯CuO的还原温度(约为390 ℃)[13],均在200-300 ℃且还原峰是双峰。这说明CuO在CZ、CZD和CZY催化剂中具有一定的分散度,而表面分散的氧化铜物种易于被还原,从而使CuO的还原温度降低,催化剂的催化性能得到提高。将催化剂CZ、CZD和CZY中CuO物种的还原状况相比较可以发现,掺杂了Dy2O3的催化剂以及Y2O3的掺杂量小于7%时还原温度都比较靠前,低于铜铈锆催化剂的还原温度。有文献报道[14],铜铈锆催化剂的H2-TPR谱图中有三个还原峰:第一个是低温还原峰α,它是与载体发生相互作用的CuO的还原;第二个是β峰,它是高分散CuO的还原峰;第三个是高温还原峰γ,它是大块氧化铜的还原。当Dy2O3的掺杂量到3%时,CZD3催化剂出现了三个CuO物种的还原峰。添加了Y2O3的各个催化剂都只有两个CuO物种的还原峰,可推测是α峰和β峰。实验中,CZD1和CZY3催化剂的还原峰最靠前,还原温度最低,说明CuO在该组分的催化剂上分散度最好,结合催化剂的催化性能可知,催化剂CZD1和CZY3的活性最好。CZY7催化剂的还原峰最落后,还原温度高于CZ催化剂,同时其催化性能也最差。由此可见,Y2O3的掺杂量不可过高,只有适当的掺杂,才能有利于氧化铜与介孔载体的相互作用,从而优化催化剂的活性选择性。在催化剂中掺杂离子半径较大的稀土,能够引起Ce-Zr-O固溶体晶格膨胀,提高晶格中氧离子的流动性和氧扩散能力,能够有效降低催化剂的还原温度。
2.3 催化剂的性能
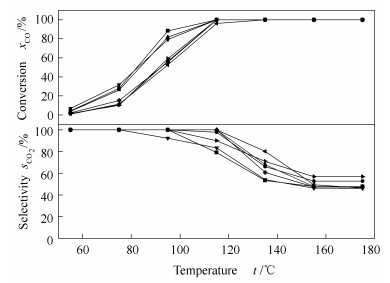
图 3为催化剂的CO优先氧化的活性与选择性。
由图 3可知,CZD1、CZD5以及CZY3、CZY5的活性与选择性明显优于其他催化剂。实验说明,在催化剂CZ中掺杂适量的稀土元素Dy与Y,明显提高了催化剂的催化性能。观察到所有的催化剂,其对CO2的选择性在115 ℃之前均高于80%,随着反应温度的升高选择性逐渐降低,且催化剂对于CO2选择性高时对应的CO转化率低,原因是氢竞争氧化的结果,高温利于氢氧化[15],催化剂在提高CO转化率的同时,也提高了H2到达活性中心并且发生反应的几率,从而使得催化剂的选择性下降[16]。另外在催化氧化反应中,活性组分的分散度、金属与载体间相互作用的大小是影响催化剂活性的主要因素[17]。只有催化剂中各元素达到一定比例,才能增强其间的相互作用力,使得CuO活性组分更好地分散,进而提高催化剂的催化活性,这个在XRD谱图中能够找到印证。
2.4 催化剂的抗CO2性能
图 4为催化剂的CO2活性与选择性。
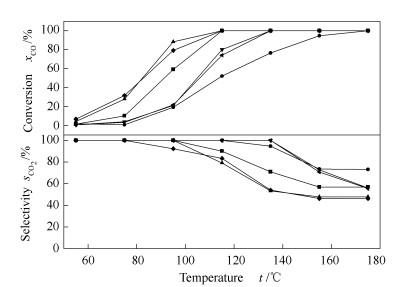 图 4
CO2对催化剂CO转化率和CO2选择性的影响
Figure 4.
Effect of CO2 on CO conversion and CO2 selectivity for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts (The reactions were carried out at atmospheric pressure in a N2-balanced stream containing 1% CO, 1% O2, 50% H2 and 15% CO2, with a GHSV of 20 000 mL/(gcat·h))
图 4
CO2对催化剂CO转化率和CO2选择性的影响
Figure 4.
Effect of CO2 on CO conversion and CO2 selectivity for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts (The reactions were carried out at atmospheric pressure in a N2-balanced stream containing 1% CO, 1% O2, 50% H2 and 15% CO2, with a GHSV of 20 000 mL/(gcat·h))
由图 4可知,当原料气中未加入CO2时,掺杂稀土元素后的催化剂活性明显优于未掺杂的催化剂。当原料气中加入15%的CO2时,掺杂1% Dy2O3催化剂的t50为105 ℃、t100为135 ℃优于未掺杂稀土元素的催化剂(t50为114 ℃、t100为175 ℃);掺杂3% Y2O3的催化剂的t50为106 ℃、t100为135 ℃同样优于未掺杂稀土元素的催化剂。由此可见,CO2的存在对催化剂的活性有抑制作用。原因可能是加入CO2时,CO2与H2发生逆水煤气反应[18],特别是在高温下易发生此反应。同时有文献报道[19],当反应气流中含有15%(体积分数) 的CO2时,CO氧化活性下降,可能是和CO在活性铜位点上与CO2的竞争吸附或在氧化铈载体上形成碳酸盐抑制氧气的流动性有关。由图 4还可知,当原料气中加入15%(体积分数) 的CO2时,未掺杂Dy、Y的催化剂选择性维持在100%时的温度升至115 ℃,掺杂Dy、Y的催化剂在135 ℃时的选择性仍为100%,可见稀土掺杂可以提高CZ催化剂的抗CO2性能。
2.5 催化剂的稳定性
图 5为CZ、CZD5和CZY5催化剂的稳定性。
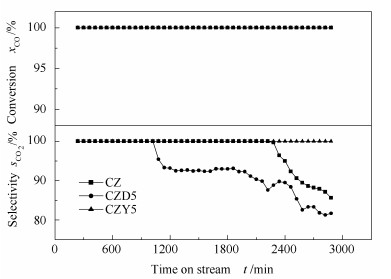 图 5
催化剂CZ、CZD5和CZY5的稳定性能
Figure 5.
Stability test of the CZ, CZD5 and CZY5 catalysts for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts (reactions were carried out at atmospheric pressure and 120 ℃ in a N2-balanced stream containing 1% CO, 1% O2 and 50% H2, with a GHSV of 40 000 mL/(gcat·h))
图 5
催化剂CZ、CZD5和CZY5的稳定性能
Figure 5.
Stability test of the CZ, CZD5 and CZY5 catalysts for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts (reactions were carried out at atmospheric pressure and 120 ℃ in a N2-balanced stream containing 1% CO, 1% O2 and 50% H2, with a GHSV of 40 000 mL/(gcat·h))
由图 5可知,三种催化剂的CO的转化率都为100%;其中,未添加稀土元素的催化剂其选择性在37 h之前一直保持在100%,之后选择性呈下降趋势,在48 h的时候降至85.6%。对于掺杂了5% Dy2O3的催化剂,其选择性在17 h的时候仍为100%,之后便逐渐下降,在48 h的时候降至81.65%。而掺杂了5% Y2O3的催化剂,经过48 h连续反应,CO的转化率和选择性一直为100%。据文献报道,在催化剂中掺杂稀土元素Y,可以明显增加催化剂的稳定性[20]。实验结果证实Y能提高催化剂的稳定性。
3 结论
通过水热-浸渍法制备了一系列具有萤石结构的CuO/Ce -Zr-RE-O2催化剂。性能测试显示, 适量稀土元素Dy、Y的掺杂,可增强CuO/CeZrO2催化剂的催化性能。Dy2O3的掺杂量为5%时,其CO完全转化时对应的CO2选择性是100%,此时的起燃温度t50为83 ℃,t100为115 ℃,温度操作窗口较宽(104-121.5 ℃),同其他Dy2O3掺杂量的催化剂对比其性能最佳;当Y2O3的掺杂量为5%时,其催化性能优于其他Y2O3掺杂量的催化剂,此时CO完全转化时对应的选择性为100%,t50为86 ℃,t100为115 ℃。在铜铈锆催化剂中添加适当离子半径较大的稀土元素Dy、Y,能够引起固溶体晶格膨胀,提高储氧能力。另外也有利于活性组分CuO在载体表层的分散,提高活性中心,降低催化剂的还原温度,使其具有良好的低温还原性能。同时亦可明显提高催化剂的抗CO2性能与稳定性。
-
-
[1]
SHARAF O Z, ORHAN M F. An overview of fuel cell technology. Fundamentals and applications[J]. Renewable Sustainable Energy Rev, 2014, 32: 810-853. doi: 10.1016/j.rser.2014.01.012
-
[2]
NASEF M M. Radiation-grafted membranes for polymer electrolyte fuel cells: Current trends and future directions[J]. Chem Rev, 2014, 114: 12278-12329. doi: 10.1021/cr4005499
-
[3]
AHLUWALIA R K, WANG X H. Fuel cell systems for transportation: Status and trends[J]. J Power Sources, 2008, 177(1): 167-176. doi: 10.1016/j.jpowsour.2007.10.026
-
[4]
王艳, 张文丽, 王奇, 王鹏展, 苏海全, 曾尚红. 富H2中优先氧化CO的CeO2/ CuO催化剂的研究进展[J]. 化学进展, 2011,30,(6): 1224-1229. WANG Yan, ZHANG Wen-li, WANG Qi, WANG Peng-zhan, SU Hai-quan, ZENG Shang-hong. Research progress of CeO2/CuO catalysts for preferential oxidation of CO in H2[J]. Prog Chem, 2011, 30(6): 1224-1229.
-
[5]
PILASOMBAT R, DALY H, GOGUET A, BREENA J P, BURCHA R, HARDACREA C, THOMPSETTB D. Investigation of the effect of the preparation method on the activity and stability of Au/CeZrO4 catalysts for the low temperature water gas shift reaction[J]. Catal Today, 2012, 180: 131-138. doi: 10.1016/j.cattod.2011.04.053
-
[6]
LIU W, FLYTZANL-STEPHANAPOULOS M. Total oxidation of carbon monoxide and methane over transition metal fluorite oxide composite catalysts: Ⅰ. Catalyst composition and activity[J]. J Catal, 1995, 153(2): 304-316. doi: 10.1006/jcat.1995.1132
-
[7]
LIU W, FLYTZANL-STEPHANAPOULOS M. Total oxidation of carbon monoxide and methane over transition metal fluorite oxide composite catalysts: Ⅱ. Catalyst characterization and reaction-kinetics[J]. J Catal, 1995, 153(2): 317-332. doi: 10.1006/jcat.1995.1133
-
[8]
FORNASIERO P, FONDA E, DI MONTE R, VLAIC G, KAŠPAR J, GRAZIANI M. Relationships between structural/textural properties and redox behavior in Ce0.6Zr0.4O2 mixed oxides[J]. J Catal, 1999, 187: 177-185. doi: 10.1006/jcat.1999.2589
-
[9]
WANG S P, WANG X Y, HUANG J. The catalytic activity for CO oxidation of CuO supported on Ce0.8Zr0.2O2 prepared via citrate method[J]. Catal Commun, 2007, 8: 231-236. doi: 10.1016/j.catcom.2006.06.006
-
[10]
VIDMAR P, FORNASIERO P, KASPAR J, GUBITOSA G, GRAZIANI M. Effects of trivalent dopants on the redox properties of Ce0.6Zr0.4O2 mixed oxide[J]. J Catal, 1997, 171(1): 160-168. doi: 10.1006/jcat.1997.1784
-
[11]
周仁贤, 丁云杰, 蒋晓源, 郑晓明. 掺杂ZrO2的Pt/Al2O3表面氧性质及一氧化碳氧化性能研究[J]. 分子催化, 1996,10,(3): 226-230. ZHOU Ren-xian, DING Yun-jie, JIANG Xiao-yuan, ZHENG Xiao-ming. Surface oxygen properties of Pt/Al2O3 doped ZrO2 and study on CO oxidation[J]. J Mol Catal, 1996, 10(3): 226-230.
-
[12]
朱鹏飞.高性能铜铈催化剂的制备及铜铈之间相互作用的研究[D].杭州:浙江大学, 2008.ZHU Peng-fei. Study on the preparation of high performance copper cerium catalyst and the interaction between copper and cerium[D]. Hangzhou: Zhejiang University, 2008.
-
[13]
郑修成, 张晓丽, 王淑荣, 于丽华, 王向宇, 吴世华. 不同CuO/CeO2催化剂上CO低温氧化反应[J]. 催化学报, 2005,26,(11): 971-976. ZHENG Xiu-cheng, ZHANG Xiao-li, WANG Shu-rong, YU Li-hua, WANG Xiang-yu, WU Shi-hua. Low temperature oxidation of CO over different CuO/CeO2 catalysts[J]. Chin J Catal, 2005, 26(11): 971-976.
-
[14]
WANG S P. An investigation of catalytic activity for CO oxidation of CuO/CexZr1-xO2 catalysts[J]. Catal Lett, 2008, 121(1): 70-76.
-
[15]
樊祺源, 白雪, 曾尚红. 表面活性剂模板法制备CeO2/ CuO催化剂用于富氢气氛中CO优先氧化[J]. 燃料化学学报, 2014,42,(5): 603-608. FAN Qi-yuan, BAI Xue, ZENG Shang-hong. CeO2/ CuO catalysts prepared by surfactant template method for CO preferential oxidation in hydrogen rich atmosphere[J]. J Fuel Chem Technol, 2014, 42(5): 603-608.
-
[16]
邹汉波, 董新法, 林维明. 非金属催化剂上CO选择性氧化反应的研究[J]. 天然气化工, 2004,29,(6): 10-13. ZOU Han-bo, DONG Xin-fa, LIN Wei-ming. Study on selective oxidation of CO over Non metallic catalyst[J]. Nat Gas Ind, 2004, 29(6): 10-13.
-
[17]
SEDMAK G, HOEVAR S, LEVEC J. Kinetics of selective CO oxidation in excess of H2 over the nanostructured Cu0.1Ce0.9O2-y catalyst[J]. J Catal, 2003, 213(2): 135-150. doi: 10.1016/S0021-9517(02)00019-2
-
[18]
邵建军, 朱锡, 申文杰. Co3O4/CeO2的氧化还原性能及反应条件对其CO氧化活性的影响[J]. 燃料化学学报, 2012,40,(1): 75-79. SHAO Jian-jun, ZHU Xi, SHEN Wen-jie. Redox properties of Co3O4/CeO2 and the effect of reaction conditions on the CO oxidation[J]. J Fuel Chem Technol, 2012, 40(1): 75-79.
-
[19]
BENEDETTO A D, LANDIB G, LISI L, RUSSO G. Role of CO2 on CO preferential oxidation over CuO/CeO2 catalyst[J]. Appl Catal B: Environ, 2013, 142: 169-177.
-
[20]
张利峰, 李金麟. La、Y改性的CuO-CeO2催化剂上富氢气体中一氧化碳的选择氧化[J]. 天津化工, 2009,23,(2): 29-31. ZHANG Li-feng, LI Jin-lin. La and Y modified CuO-CeO2 catalysts on selective oxidation of carbon monoxide in hydrogen rich gases[J]. Tianjin Chem Ind, 2009, 23(2): 29-31.
-
[1]
-
图 3 CO转化率和CO2选择性随温度的变化
Figure 3 CO conversion and CO2 selectivity along with temperature for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts
(the reactions were carried out at atmospheric pressure in a N2-balanced stream containing 1% CO, 1% O2 and 50% H2, with a GHSV of 40 000 mL/(gcat·h)) ■: CZD1; ●: CZD3; ▲: CZD5; ▼: CZY3; ◆: CZY5; ◀: CZY7; ▶: CZ
图 4 CO2对催化剂CO转化率和CO2选择性的影响
Figure 4 Effect of CO2 on CO conversion and CO2 selectivity for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts (The reactions were carried out at atmospheric pressure in a N2-balanced stream containing 1% CO, 1% O2, 50% H2 and 15% CO2, with a GHSV of 20 000 mL/(gcat·h))
■: A-without CO2; ●: A-adding CO2; ▲: B-without CO2; ▼: B-adding CO2; ◆: C-without CO2; ◀: C-adding CO2; A=CZ; B=CZD1; C=CZY3
图 5 催化剂CZ、CZD5和CZY5的稳定性能
Figure 5 Stability test of the CZ, CZD5 and CZY5 catalysts for the preferential oxidation of CO in H2-rich stream over various CuO/Ce-Zr-RE-O2 catalysts (reactions were carried out at atmospheric pressure and 120 ℃ in a N2-balanced stream containing 1% CO, 1% O2 and 50% H2, with a GHSV of 40 000 mL/(gcat·h))
表 1 CuO/Ce-Zr-RE-O2催化剂的晶粒粒径、比表面积、孔径和孔容
Table 1. Crystallite size, BET surface area, pore diameter and pore volume of various CuO/Ce-Zr-RE-O2 catalysts
Sample 2 θ/(°) Interplanar spacing d/nm Crystallite size dCeO2(111) /nm ABET/(m2·g-1) Pore diameter d/nm Pore volume v/(cm3·g-1) CZ 28.94 0.308 3 8.51 130.5 6.31 0.265 CZD1 28.48 0.313 2 9.98 107.5 10.96 0.405 CZD3 28.64 0.311 4 10.18 99.4 8.35 0.288 CZD5 28.52 0.312 7 9.28 107.9 6.86 0.246 CZY3 28.93 0.308 0 8.53 127.1 5.64 0.256 CZY5 28.72 0.310 6 8.22 133.3 5.99 0.270 CZY7 28.88 0.308 9 9.11 119.3 8.10 0.330 dCeO2 (111) : calculated from Scherrer equation -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0


 下载:
下载:




 下载:
下载:

