
Citation: ZHANG Li-qiang, LI Kai, ZHU Xi-feng. Two-step pyrolysis characteristics of bean stalks[J]. Journal of Fuel Chemistry and Technology, 2016, 44(5): 534-539.

豆类秸秆两级热解特性研究
English
Two-step pyrolysis characteristics of bean stalks
-
Key words:
- two-step pyrolysis
- / selective pyrolysis
- / Py-GC/MS
- / soybean stalk
-
利用生物质生产生物能源和生物基化学品具有良好的环境和经济效益,是当前生物质能发展的主要趋势之一[1]。采用选择性热解可以实现生物质向某些特定产物的转化[2],用于选择性热解的方法主要有催化热解、分级热解、原料预处理以及热解温度和热解时间的优化等。如Carlson等[3]利用分子筛ZSM-5催化热解生物质衍生物获得了芳香族化合物;李凯等[4]发现低温条件下热解产物种类相对单一,便于产物的分离和提纯。对于分级热解,世界各国学者也已经开展了一些相关的研究,如常胜等[5]对杉木进行了催化分级热解,提出第一级热解温度为300 ℃时热解主要以有机抽提物为主,且ZSM-5降低了第二级热解产物中乙酸的含量;Hammer等[6]利用HZSM-5催化剂进行两级热解,得到了富含糖类和木质素衍生物的高品质生物油;Huang等[7]利用自制装置进行了两级催化热解,在500 ℃催化热解条件下得到了碳氢化合物含量较高的生物油。目前,利用催化剂进行分级热解的研究较多,但是将催化剂运用到大规模生物质热解中的技术工艺相对复杂,所以,如果能够直接利用分级热解实现生物质选择性热解,将会为生物质的规模利用提供更有效的途径。
木质纤维素类生物质主要由纤维素、半纤维素和木质素组成,已有研究结果表明,半纤维素的热解温度为236-330 ℃,纤维素的热解温度为332-383 ℃,木质素的热解温度为250-630 ℃[8],而且各组分的热解产物也有所不同[9]。如果能够直接利用各组分热解温度的差异,通过分级热解提高某些产物的含量或者实现高附加值产物的富集,将会为生物质利用提供新的有效途径。基于木质纤维素类生物质的组成特点,研究以资源量丰富的豆类秸秆为原料[10],利用Py-GC/MS进行两级热解实验,研究两级热解对于生物质热解产物的影响,考察并获得了实现选择性热解的条件。
1 实验部分
1.1 实验原料
实验原料为黄豆秆,来自河南永城。黄豆秆经破碎后筛分至80-100目,并于50 ℃条件下烘干。表 1为黄豆秆的元素分析、工业分析和组分分析结果,元素分析采用Elementary Vario EL-Ⅲ型元素分析仪进行测定;工业分析按照中国国家标准《固体生物质燃料工业分析方法》GB/T 28731-2012进行测定;组分分析按照国家有关标准进行,如抽提物按GB/T2677.6-1994测定、木质素按GB/T 2677.8-1994测定、综纤维素按GB/T 2677.10-1995测定、纤维素按硝酸-乙醇法测定、半纤维素由综纤维素减去纤维素得到。
 表 1
黄豆秆的元素分析、工业分析和组分分析(收到基)
Table 1.
Ultimate, proximate and component analysis of soybean stalk (as received)
表 1
黄豆秆的元素分析、工业分析和组分分析(收到基)
Table 1.
Ultimate, proximate and component analysis of soybean stalk (as received)
Ultimate analysis Proximate analysis Component analysis composition war /% composition war /% composition war /% C 42.63 M 78.26 cellulose 41.44 H 6.28 V 2.90 hemicellulose 20.96 Oa 45.14 FC 14.66 lignin 16.10 N 1.44 A 4.18 extractives 9.95 S 0.33 a: by difference 表 1 黄豆秆的元素分析、工业分析和组分分析(收到基)
Table 1. Ultimate, proximate and component analysis of soybean stalk (as received)1.2 实验方法
Py-GC/MS由CDS5250型热裂解仪(Py, CDS, USA) 和Trace DSQⅡ型气相色谱-质谱联用仪(GC/MS, Thermo Electron, USA) 组成,配置TG-5MS毛细管柱(60 m×0.25 mm×0.25 μm, Thermo Electron, USA)。实验时,称取约0.5 mg黄豆秆样品装入一端装有石英棉的石英管中,并在其另一端装入石英棉,防止样品被吹出石英管,最后将石英管放入热裂解仪中。热裂解仪中通入纯度为99.999%的氦气作为载气,样品经过高温裂解后,由GC/MS对其热解气进行在线分析。分流比为1:40,热解气传输管线温度为250 ℃,进样口温度为280 ℃。色谱柱升温程序:初始温度为40 ℃并保持2 min,然后以3 ℃/min的升温速率升温至180 ℃并保持2 min,最后再以15 ℃/min的升温速率升温至280 ℃并保持3 min。电子轰击离子源温度为280 ℃,电子能量为70 eV。采用标准NIST谱库对热解气中有机成分进行定性分析。
在进行两级热解实验时,首先将热裂解仪以20 ℃/ms的升温速率升至第一级热解温度(t1,分别为250、300、350、400、450、500和550 ℃),保持20 s,试样停留在热裂解仪中,待GC/MS对第一级热解气检测完成后,再将热裂解仪以20 ℃/ms升温速率升至第二级热解温度(t2),统一设置为650 ℃,保持20 s,继续对第一级热解剩余物进行热解,并对生成的第二级热解气进行检测。另外,将热裂解仪以20 ℃/ms的升温速率直接升至650 ℃进行一次热解,并保持40 s,然后对其热解气进行检测,以此作为对照实验。每次实验重复三次,以确保实验数据的可重复性,并将产物的相对峰面积和归一化后的绝对峰面积求平均值用于实验结果分析。
另外,由于生物质原料是热的不良导体,故实际热解温度会低于其设定值,而随着时间的延长,温度差会逐渐减小[11]。生物质快速热解形成的热解气包括永久性气体、可冷凝的挥发性有机产物以及不可挥发的低聚物等,而GC/MS只能分析可冷凝的挥发性有机产物。由于与Py联用时GC/MS不能对产物进行在线定量分析,所以要通过比较绝对峰面积值的大小来反映产物产率的高低,比较相对峰面积的大小来反映其在热解产物中的含量。但是,由于GC/MS对不同物质的响应因子有一定差别,所以将所有产物的绝对峰面积值相加得到的总峰面积不能严格地代表所有产物的总体产率,只能用于初步地判断两级热解对挥发性有机产物产率的影响[12]。
2 结果与讨论
2.1 两级热解对热解产物分布的影响
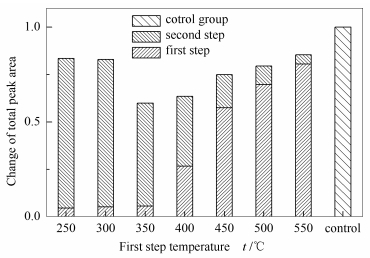
为明确两级热解过程中t1对生物质热解效率的影响,以对照组所得热解产物的总峰面积为基准,对两级热解产物总峰面积的变化进行分析,具体见图 1。由图 1可知,随t1的升高,第一级热解产物总峰面积逐渐增大,因为随着温度的升高,热解强度逐渐增加,总体挥发性有机产物的产率增加,而剩余第二级热解的原料减少,致使第二级热解产物总峰面积呈下降趋势。将第一级热解产物的总峰面积与第二级热解产物的总峰面积相加作为两级热解产物的总峰面积,随t1的升高,两级热解产物的总峰面积呈现先减后增的变化趋势,并且在t1为350 ℃时最小。当t1较低时,第一级热解相当于对黄豆秆进行了烘焙预处理,从而影响了第二级热解产物的生成。当t1为250和300 ℃时,能够产生更有利于生物质热解的预处理效果,而当t1为350 ℃时,烘焙温度过高,可能对生物质热解造成了不利的影响[13]。不同t1条件下的两级热解产物的总峰面积都小于对照组产物的总峰面积,因为对照组在高温段的停留时间较长,热解强度高于实验组。
第一级热解和第二级热解主要产物的相对峰面积见表 2。将主要产物分为酸类、醇类、酮类、呋喃类、酚类、烃类和含氮类化合物,由于检测到的醛类物质较少,故在此不做讨论。
 表 2
黄豆秆两级热解和对照组各类产物相对峰面积的分布
Table 2.
Relative peak area distribution of products from soybean stalk two-step pyrolysis and the control group
表 2
黄豆秆两级热解和对照组各类产物相对峰面积的分布
Table 2.
Relative peak area distribution of products from soybean stalk two-step pyrolysis and the control group
t1/℃ First-step pyrolysis acids alcohols ketones furans phenols nitrides hydrocarbons 250 - - - - - - - 300 - - - - - - - 350 8.38 - - - - - - 400 21.14 3.47 8.77 4.80 12.29 4.85 - 450 13.37 5.28 10.81 4.20 20.77 3.60 - 500 9.70 4.48 8.35 4.27 23.21 2.95 0.97 550 8.93 4.69 8.80 4.05 23.42 2.85 1.04 t1/℃ Second-step pyrolysis acids alcohols ketones furans phenols nitrides hydrocarbons 250 9.52 3.41 7.23 3.49 19.17 2.47 1.40 300 9.43 4.25 7.23 3.44 21.25 2.66 1.54 350 8.29 5.04 7.85 3.65 23.76 2.77 1.78 400 1.05 3.34 6.44 2.93 21.84 0.81 9.48 450 - - 1.41 0.53 2.56 - 20.10 500 - - - - - - 22.78 550 - - - - - - 13.55 Pyrolysis temperature t/℃ Control group acids alcohols ketones furans phenols nitrides hydrocarbons 650 9.33 4.16 8.71 3.58 21.78 2.85 2.72 -:few or undetected 表 2 黄豆秆两级热解和对照组各类产物相对峰面积的分布
Table 2. Relative peak area distribution of products from soybean stalk two-step pyrolysis and the control group由表 2可知,在t1为250和300 ℃的条件下,各类产物的含量都较低,这是由于实际的生物质热解温度比预设的温度要低[11],导致热解强度太低,也可能是因为停留时间过短导致热解不够充分,正如图 1所示,当t1为250和300 ℃时,第一级热解总体挥发性有机产物的产率较低。第一级热解产物中,酸类、呋喃类和含氮类产物的相对峰面积在t1为400 ℃时最大,而醇类和酮类产物相对峰面积的最大值则对应于t1为450 ℃,这与杨晓初[14]对杨木进行的两级热解实验得出的结果比较一致,如线性酸类、呋喃类主要在t1为400-500 ℃时含量较高;酚类产物来源于木质素[15],而木质素的热解温度范围较宽,热解温度越高,热解强度越高,酚类产物生成越多,所以其相对峰面积随t1的升高而增大。与酚类产物相对峰面积的变化趋势相反,含氮类产物的相对峰面积随t1的升高而减小,因为含氮类产物主要来源于生物质中的蛋白质组分[16],而黄豆秆中蛋白质含量较少,且蛋白质热解温度相对较低,当温度升高时其他组分热解产物增多,相应地降低了含氮类产物的含量。第一级热解产物中酸类、酮类和呋喃类等产物主要来源于纤维素和半纤维素[17],其相对峰面积在t1为400和450 ℃时较大,并且大于对照组的相对峰面积,说明其含量更高,能够初步实现生物质的选择性热解。
在第二级热解产物中,随t1的升高,酸类产物的相对峰面积逐渐减小,因为t1越高第一级中纤维素和半纤维素的热解越完全,导致第二级中其热解产物含量越低。烃类产物的相对峰面积在t1低于等于500 ℃时随t1升高而逐渐增加,这是由于随t1的升高,第二级热解原料中氧元素含量逐渐降低[18],且较高的反应温度同样能够使苯环上的含氧官能团脱除[19],因而第二级热解能够得到更多的烃类产物,而当t1为550 ℃时,第二级热解总体挥发性有机产物的产率较低,烃类产物的产率及含量也相对降低。相比第一级热解,第二级热解产物中烃类产物的相对峰面积较大,且当t1为450和500 ℃时均高达20%以上,大于对照组的相对峰面积,说明此条件能够显著提高烃类产物的含量,而Huang等[7]在热解和催化温度都为500 ℃的条件下也能够显著提高烃类产物的含量。
2.2 两级热解对部分高含量产物的选择性
生物质选择性热解的目的在于提高一种或几种目标产物在热解产物中的含量,以使其具备良好的分离和应用价值。根据实验结果,以乙酸、糠醛、愈创木酚、甲苯和苯为目标产物,研究两级热解对其含量的影响。
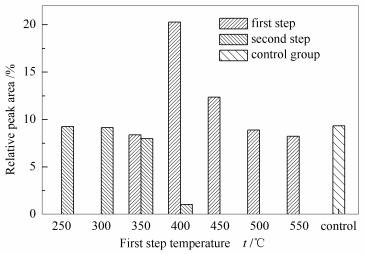
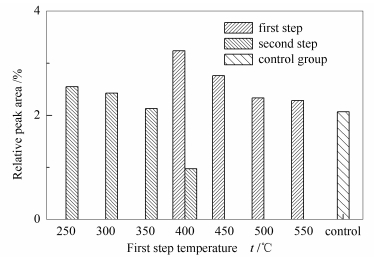
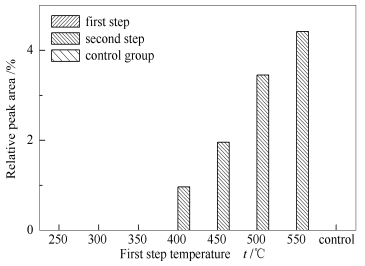
图 2为乙酸相对峰面积的分布。由图 2可知,t1为400和450 ℃时,第一级热解产物中乙酸的相对峰面积比对照组的大,特别在t1为400 ℃时,已经达到20.29%,此时乙酸的含量较高。第一级热解产物中,乙酸的相对峰面积先增后减,因为乙酸主要源于纤维素和半纤维素[17],当t1较低时,其热解强度较低,而t1较高时,热解强度升高,但是木质素热解产物增加又相应降低了乙酸的含量。在第二级热解产物中,只有当t1低于等于400 ℃时才能检测到乙酸,且相对峰面积都小于10%,这一方面, 是因为第一级热解消耗了纤维素和半纤维素; 另一方面, 是因为t2较高,提高了木质素的热解强度。糠醛源于纤维素和半纤维素[17],所以图 3也呈现出与图 2相似的变化趋势,第一级热解产物中糠醛在t1为400 ℃时的相对峰面积为3.24%,高于对照组,而杨晓初[14]在研究中得出,第一级产物中糠醛的含量在t1为300 ℃停留10 s时能够达到最高,这可能是由于生物质原料及热解停留时间的差异等造成的。
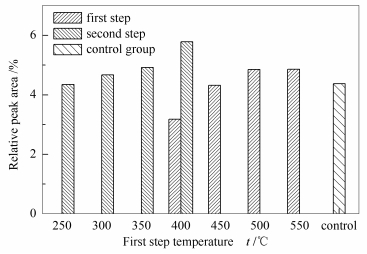
木质素的热解温度范围较宽,其热解产物也较丰富,尤其是芳香类产物的含量和产率都较高[11],下面对其典型的热解产物愈创木酚、甲苯和苯的相对峰面积的分布进行分析。图 4为愈创木酚相对峰面积的分布。由图 4可知,第一级热解产物中,在t1小于400 ℃时没有检测到愈创木酚,可见低温不利于愈创木酚的生成,而t1高于等于400 ℃时愈创木酚的相对峰面积都大于对照组,且在t1为400 ℃时达到5.78%。在第二级热解产物中,t1大于400 ℃时都没有检测到愈创木酚,说明对应的第一级热解已经基本完成了生成愈创木酚的反应。根据王树荣等[20]的研究,当热解温度升高时,木质素内的醚键和C-C键等首先断裂生成了愈创木基和紫丁香基型的酚类,随温度进一步升高则会发生脱甲氧基和脱甲基的反应,愈创木基和紫丁香基型的酚类发生二次裂解生成相应的苯酚及苯二酚等,进而使愈创木酚的含量下降。
甲苯的相对峰面积分布见图 5,第一级热解产物中甲苯的相对峰面积都较小,而且只有t1高于500 ℃时才能检测到甲苯,说明高温有利于甲苯的生成,正如Alén等[19]指出,高温反应能够使得含氧官能团得到脱除,有利于得到芳香烃产物。
第二级热解产物中甲苯的相对峰面积在t1为450、500、550 ℃时都达到了5%以上,其含量比对照组有显著的提高。结合2.1节中的讨论,随t1的升高,第二级热解总体挥发性有机产物的产率逐渐降低,而高温又利于甲苯的生成,所以致使第二级热解产物中甲苯的含量在t1较高时得到了显著提高。
图 6为苯相对峰面积的分布。由图 6可知,第一级热解和对照组产物中均未检测到苯,在t1大于400 ℃时,第二级热解产物中苯的相对峰面积显著增大,在t1为550 ℃时达到4.42%。苯相对峰面积的分布受到生物质中碳、氢、氧含量的影响,随着t1的升高,剩余第二级热解原料中氢和氧的含量都逐渐降低,而碳含量逐渐升高[18],更有利于苯的生成。
3 结论
随第一级热解温度升高,第一级热解产物总峰面积逐渐增大,第二级热解产物总峰面积逐渐减小。第一级热解产物中,酸类、酮类和呋喃类等源于纤维素和半纤维素的产物以及含氮类产物的含量在t1为400和450 ℃时较高。t1为450和500 ℃的条件下第二级热解产物中烃类产物的含量能够达到20%以上。相比对照组,两级热解能够分别实现乙酸、糠醛、愈创木酚、甲苯和苯的富集。t1为400 ℃时,第一级热解产物中乙酸、糠醛的含量分别达到20.29%和3.24%,而此时,第二级热解产物中愈创木酚含量也提高到5.78%;另外,在第二级热解产物中,t1为450-550 ℃时甲苯的含量能够达到5%以上,而在t1为550 ℃时苯的含量能够提高到4.42%。根据生物质中各组分热解温度的差异,设置两级热解温度,可以在第一级和第二级热解中分别获取不同的高含量产物,初步实现生物质的选择性热解。
-
-
[1]
卫新来, 汪志, 阮仁祥, 张颖. 木质纤维素生物质降解产物的化学转化研究进展[J]. 现代化工, 2010,30,(12): 26-31. WEI Xin-lai, WANG Zhi, RUAN Ren-xiang, ZHANG Ying. Progress in chemical transformation of lignocellulosic biomass degradation products[J]. Mod Chem Ind, 2010, 30(12): 26-31.
-
[2]
汪志.选择性催化热解生物质制备高附加值化学品[D].合肥:中国科学技术大学, 2011.WANG Zhi. Selective catalytic pyrolysis of biomass for high value-added chemicals[D]. Hefei: University of Science and Technology of China, 2010.
-
[3]
CARLSON T R, VISPUTE T P, HUBER G W. Green gasoline by catalytic fast pyrolysis of solid biomass derived compounds[J]. ChemSusChem, 2008, 1(5): 397-400. doi: 10.1002/(ISSN)1864-564X
-
[4]
李凯, 郑燕, 龙潭, 朱锡锋. 利用Py-GC/MS研究温度和时间对生物质热解的影响[J]. 燃料化学学报, 2013,41,(7): 845-849. LI Kai, ZHENG Yan, LONG Tan, ZHU Xi-feng. Study on effect of temperature and time on biomass pyrolysis by Py-GC/MS[J]. J Fuel Chem Technol, 2013, 41(7): 845-849.
-
[5]
常胜, 赵增立, 郑安庆, 李海滨. 杉木分级催化热解-气质联用实验分析[J]. 农业机械学报, 2010,41,(6): 93-97. CHANG Sheng, ZHAO Zeng-li, ZHENG An-qing, LI Hai-bin. Step-wise catalytic pyrolysis of fir using pyrolysis-gas chromatography/mass spectrometry[J]. Trans Chin Soc Agric Mach, 2010, 41(6): 93-97.
-
[6]
HAMMER N L, GARRIDO R A, STARCEVICH J, COE C G, SATRIO J A. Two-step pyrolysis process for producing high quality bio-oils[J]. Ind Eng Chem Res, 2015, 54(43): 10629-10637. doi: 10.1021/acs.iecr.5b02365
-
[7]
HUANG Y B, WEI L, JULSON J, GAO Y, ZHAO X H. Converting pine sawdust to advanced biofuel over HZSM-5 using a two-stage catalytic pyrolysis reactor[J]. J Anal Appl Pyrolysis, 2015, 111: 148-155. doi: 10.1016/j.jaap.2014.11.019
-
[8]
张海荣, 庞浩, 石锦志, 廖兵. 生物质化学组分及其液化残渣的热重行为[J]. 化工进展, 2011,30,(10): 2194-2199. ZHANG Hai-rong, PANG Hao, SHI Jin-zhi, LIAO Bing. TG study on major biomass components and its liquefied residues from pyrolysis[J]. Chem Ind Eng Prog, 2011, 30(10): 2194-2199.
-
[9]
曲艳超.低温选择性热解草本类生物质制备4-乙烯基苯酚[D].合肥:中国科学技术大学, 2013.QU Yan-chao. Low temperature selective pyrolysis of herbage biomass for 4-vinylphenol[D]. Hefei: University of Science and Technology of China, 2013.
-
[10]
朱锡锋.生物油制备技术与应用[M].北京:化学工业出版社, 2013.ZHU Xi-feng. Preparation and Application of Bio-oil[M]. Beijing: Chemical Industry Press, 2013.
-
[11]
PATTIYA A, TITILOVE J O, BRIDGWATER A V. Fast pyrolysis of cassava rhizome in the presence of catalysts[J]. J Anal Appl Pyrolysis, 2008, 81(1): 72-79. doi: 10.1016/j.jaap.2007.09.002
-
[12]
陆强, 张栋, 朱锡锋. 四种金属氯化物对纤维素快速热解的影响(Ⅰ) Py-GC/MS实验[J]. 化工学报, 2010,61,(4): 1018-1024. LU Qiang, ZHANG Dong, ZHU Xi-feng. Catalytic effects of four metal chlorides on fast pyrolysis of cellulose (Ⅰ) Py-GC/MS experiments[J]. CIESC J, 2010, 61(4): 1018-1024.
-
[13]
CHEN W H, KUO P C. Isothermal torrefaction kinetics of hemicellulose, cellulose, lignin and xylan using thermogravimetric analysis[J]. Energy, 2011, 36(11): 6451-6460. doi: 10.1016/j.energy.2011.09.022
-
[14]
杨晓初.生物质两级热解特性研究[D].北京:华北电力大学, 2012.YANG Xiao-chu. Study on the characteristics of biomass two-step pyrolysis[D]. Beijing: North China Electric Power University, 2012.
-
[15]
EVANS R J, MILNE T A, SOLTYS M N. Direct mass-spectrometric studies of the pyrolysis of carbonaceous fuels: Ⅲ Primary pyrolysis of lignin[J]. J Anal Appl Pyrolysis, 1986, 9(3): 207-236. doi: 10.1016/0165-2370(86)80012-2
-
[16]
DARVELL L I, BRINDLEY C, BAXTER X C, JONES J M, WILLIAMS A. Nitrogen in biomass char and its fate during combustion-a model compound approach[J]. Energy Fuels, 2012, 26(11): 6482-6491.
-
[17]
吴逸民, 赵增立, 吴文强, 李海滨. 基于裂解气质联用分析的生物质逐级热解研究[J]. 燃料化学学报, 2010,38,(2): 168-173. WU Yi-min, ZHAO Zeng-li, WU Wen-qiang, LI Hai-bin. Step-pyrolysis of biomass using pyrolysis-gas chromatography/mass spectrometry[J]. J Fuel Chem Technol, 2010, 38(2): 168-173.
-
[18]
赵世翔, 姬强, 李忠徽, 王旭东. 热解温度对生物质炭性质及其在土壤中矿化的影响[J]. 农业机械学报, 2015,46,(6): 183-192. ZHAO Shi-xiang, JI Qiang, LI Zhong-hui, WANG Xu-dong. Characteristics and mineralization in soil of apple-derived biochar produced at different temperature[J]. Trans Chin Soc Agric Mach, 2015, 46(6): 183-192.
-
[19]
ALÉN R, KUOPPALA E, OESCH P. Formation of the main degradation compound groups from wood and its components during pyrolysis[J]. J Anal Appl Pyrolysis, 1996, 36(2): 137-148. doi: 10.1016/0165-2370(96)00932-1
-
[20]
王树荣, 骆仲泱.生物质组分热裂解[M].北京:科学出版社, 2013.WANG Shu-rong, LUO Zhong-yang. Pyrolysis of Biomass Components[M]. Beijing: Science Press, 2013.
-
[1]
-
表 1 黄豆秆的元素分析、工业分析和组分分析(收到基)
Table 1. Ultimate, proximate and component analysis of soybean stalk (as received)
Ultimate analysis Proximate analysis Component analysis composition war /% composition war /% composition war /% C 42.63 M 78.26 cellulose 41.44 H 6.28 V 2.90 hemicellulose 20.96 Oa 45.14 FC 14.66 lignin 16.10 N 1.44 A 4.18 extractives 9.95 S 0.33 a: by difference 表 2 黄豆秆两级热解和对照组各类产物相对峰面积的分布
Table 2. Relative peak area distribution of products from soybean stalk two-step pyrolysis and the control group
t1/℃ First-step pyrolysis acids alcohols ketones furans phenols nitrides hydrocarbons 250 - - - - - - - 300 - - - - - - - 350 8.38 - - - - - - 400 21.14 3.47 8.77 4.80 12.29 4.85 - 450 13.37 5.28 10.81 4.20 20.77 3.60 - 500 9.70 4.48 8.35 4.27 23.21 2.95 0.97 550 8.93 4.69 8.80 4.05 23.42 2.85 1.04 t1/℃ Second-step pyrolysis acids alcohols ketones furans phenols nitrides hydrocarbons 250 9.52 3.41 7.23 3.49 19.17 2.47 1.40 300 9.43 4.25 7.23 3.44 21.25 2.66 1.54 350 8.29 5.04 7.85 3.65 23.76 2.77 1.78 400 1.05 3.34 6.44 2.93 21.84 0.81 9.48 450 - - 1.41 0.53 2.56 - 20.10 500 - - - - - - 22.78 550 - - - - - - 13.55 Pyrolysis temperature t/℃ Control group acids alcohols ketones furans phenols nitrides hydrocarbons 650 9.33 4.16 8.71 3.58 21.78 2.85 2.72 -:few or undetected -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0



 下载:
下载:





 下载:
下载:

