
Citation: LIU Yang, HE Kun, LI Xian-qing, HAN Rui, WANG Zhe, XU Hong-wei. Performance of various catalysts in hydropyrolysis of organic matters and reaction mechanisms[J]. Journal of Fuel Chemistry and Technology, 2016, 44(1): 53-59.

不同催化剂上有机质加氢热解行为及催化作用机理研究
English
Performance of various catalysts in hydropyrolysis of organic matters and reaction mechanisms
-
Key words:
- organic matters
- / hydropyrolysis
- / biomarkers
- / catalytic reaction mechanism
-
目前,催化加氢热解技术已被广泛用于煤的液化、油气地球化学以及古沉积环境等众多领域的研究中[1-9]。在烃源岩评价方面,该方法相对于常规的索式抽提得到的烃类产量更高,且生物标志化合物更能反映有机质真实的热演化程度[10-12]。这使其在高过成熟或发生过强烈的次生降解有机质的成熟度确定和油源对比方面具有独特的优势。
作为常用的催化剂,具活性表面的二硫化钼(MoS2) 在很多化学反应中都表现较好的催化效果,也被广泛应用于加氢热解[13-15]。大量的研究表明,该催化剂的加入不仅能很大程度上提高液态烃的产率和有机质的转化率,同时能得到较高产率的各类生物标志物[5, 10-12]。He等[12]通过对比实验和产物定量分析,对MoS2的催化机理进行了深入的探讨。提出在催化加氢热解过程中,二硫化钼的催化作用主要表现在两个方面:一方面,催化剂前驱物分解或MoS2还原生成的H2S引发烃类的自由基反应;另一方面,过渡金属元素Mo所提供的Lewis酸位促进H2的均裂生成H·,加速有机质的催化加氢裂解。实际上,作为常见的Lewis酸类型的催化剂,一些过渡金属的氯化物、氧化物以及沸石类矿物也常能在有机反应中显示出很好的催化效果[16-21]。但这些催化剂在有机质的加氢热解中的应用的报道还极少。众所周知,不同类型的催化剂因催化机理和活性的差异,常表现出不同的产物选择性。通过不同类型催化剂加氢热解的产物产率和特征的对比研究,将有助于针对不同的研究目的选择合适的催化剂。
基于此,研究选择了ZnCl2和NiCl2、Fe2O3、Y型沸石(NaY) 以及制备合成的MoS2分别作为过渡金属氯化物、金属氧化物、沸石和硫化物催化剂,对几种不同类型有机质样品开展了催化加氢热解研究。在对比了不同催化剂的效率及选择性的同时,对催化反应机理进行了初步的探讨。
1 实验部分
1.1 样品和试剂
加氢热解的样品包括一个低熟(杜13) 和一个高成熟(肇深5) 的干酪根及一个低熟煤,基本地球化学特征见表 1。其中,X衍射光谱(XRD) 分析结果表明,煤中含有的主要矿物成分为石英及一些硅酸盐矿物。样品用于模拟实验之前均粉碎至100目左右。加氢热解过程中所用H2为高纯度氢气,δD为-86.525‰。用于族组分分离的氯仿、二氯甲烷、正己烷和乙醇均为分析纯,且使用前均经过蒸馏处理去除杂质。ZnCl2、NiCl2和Fe2O3均为分析纯,NaY沸石及制备催化剂前驱物的(NH4)2MoO4·4H2O为分析纯,(NH4)2S浓度为8%。实验用水为蒸馏水。
 表 1
催化加氢热解样品的地球化学特征
Table 1.
Geochemical characteristic of the organic matters for catalytic hydropyrolysis
表 1
催化加氢热解样品的地球化学特征
Table 1.
Geochemical characteristic of the organic matters for catalytic hydropyrolysis
Sample Depth L/m Layer TOC w/% R0 w/% Elemental compostion of kerogen w/% C H O N Du-13 1 408.5 K 3.14 0.84 60.44 1.231 6.61 1.65 Zhaoshen-5 4 331 C-P - 2.06 72.99 0.296 2.17 1.83 Fuxin coal surface J 71.24 0.55 73.52 5.68 - 1.23 表 1 催化加氢热解样品的地球化学特征
Table 1. Geochemical characteristic of the organic matters for catalytic hydropyrolysis1.2 加氢热解
催化剂MoS2是通过(NH4)2MoO4·4H2O和8% (NH4)2S溶液在冰浴条件下反应制备[12]。加氢热解实验是在中国石油勘探开发研究院地球化学重点实验室的加氢热解装置(Strata Technology LTD.) 上进行[12]。首先准确称量0.5 g干酪根或煤样和0.3 g催化剂,将其混合均匀后装入反应管指定位置,加入15 MPa的氢气,设定温度程序并开始实验。实验采用升温程序为:先以300 ℃/min从常温加热到250 ℃,然后以5 ℃/min加热到520 ℃,最后恒温5 min。液体产物通过充填硅胶并置于液氮冷阱中的收集管来收集。待反应结束后,将收集管中的硅胶回收,用氯仿进行抽提得到液态产物。
1.3 分析方法
液态产物的族组分定量分离是通过标准方法进行的(SY/T 5119-2008)。饱和烃组分的定量色谱-质谱(GC-MS) 分析是应用Trace GC Ultra色谱与DSQ Ⅱ质谱(美国Thermo公司) 联用完成。样品反应前后的元素含量和稳定氢同位素分别是用Vario Micro Cube元素分析仪(德国Elementor公司) 和Flash EA 1112Series同位素分析仪测定的。催化剂前驱物的XRD分析及样品的红外光谱分析分别是用TTR Ⅲ型X射线衍射仪(日本理学公司) 和Nicolet continuum型显微红外光谱仪(美国ThermoFisher公司) 来完成的。
2 结果与讨论
2.1 加氢热解液态产物
2.2 有机质的转化及结构演化
以阜新煤为例,对不同催化剂对有机质的加氢转化和结构演化的影响进行了对比。为了研究不同体系产物产量和组分分布差异的原因,作者对煤样反应后固体残余物的元素含量进行了分析,具体见表 4。
Reaction condition Content w/% C/H* C H O S N Catalyst free 77.04 4.32 6.94 1.02 1.39 1/1.75 ZnCl2 63.57 3.12 5.84 1.43 0.96 1/1.13 NiCl2 62.88 3.17 4.30 1.03 1.03 1/1.20 Fe2O3 45.76 2.34 3.66 1.40 0.82 1/1.11 MoS2 72.39 5.09 6.89 2.81 1.48 1/1.07 *: C/H represents the ratio of carbon conversion to hydrogen in the hydropyrolysis 表 4 阜新煤样加氢热解后固体残余物的元素分析
Table 4. Elemental compositions of solid residues可以假定煤的液化产物是以-CnH2nX-(n=0、1、……;X代表O或S等) 形式存在,则如果反应过程中H2的加氢作用不存在或很微弱,那么煤结构中的C、H转化原子比(C/H) 应该等于或近似等于1:2。根据式(1) 可以计算出阜新煤的单独及各个催化液化反应前后的C/H比值,结果见表 4。
计算结果表明,除了单独加氢热解体系外,四种催化体系的C/H原子比都明显大于1/2。这表明,达到同样量的C转化时,在催化体系中,煤结构中的H消耗的更少。也就是说,催化剂起到了催化加氢的作用,促进了煤液化过程中H2的分解,为产物的生成提供了H。
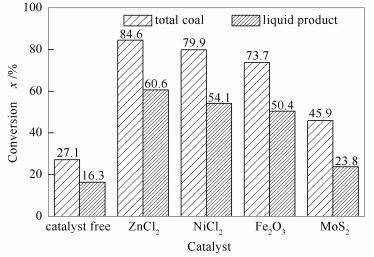
图 4为阜新煤在单独和催化加氢液化过程中的产率。由图 4可知,催化剂的加入明显提高了煤液化的总转化率和液态组分的产率。这表明四种催化剂的存在都能加速煤结构中C-C键的断裂,促进加氢反应的进行。其中,相对于NiCl2来说,ZnCl2似乎更有利于煤的转化。这是因为两种氯化物在煤的液化过程中是以不同形态存在,熔点相对低的ZnCl2能够发生熔融并产生质量传递效应,与煤发生更充分的接触[16]。
2.3 催化反应机制
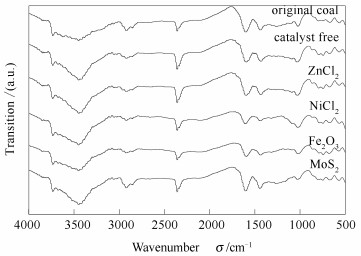
热演化过程中,煤结构中化学基团的变化能代表其反应的途径。为了研究四种催化剂对液化过程中煤结构变化的不同影响,研究利用红外光谱对单独和催化加氢液化反应后的残余物结构进行了分析,结果见图 5。
相对于原始煤样,单独及氯化物、氧化物催化加氢液化的残余物在主要代表-CH2-和-CH3振动吸收处(2 850-3 000 cm-1) 吸收变的要微弱的多,但硫化物液化体系的残余物中没有观察到这样的减弱。单独和ZnCl2体系残余物的代表不饱和键伸缩振动的吸收峰(2 350 cm-1和1 500-1 650 cm-1) 出现明显增强。对于NiCl2、Fe2O3和MoS2体系的残余物,该吸收峰并没有出现明显变化。这是单独热演化过程中,由于液化程度的加深,煤结构中脂肪链的不断释放引起了C=C、C=O和C≡C键的富集。而催化液化过程中存在强烈的加氢作用会在一定程度上抑制煤结构中不饱和键的增多。尽管在ZnCl2体系中也存在加氢作用,但是ZnCl2独有的质量传递效应使得其具有相对较高的液态烃产率。同时,Fe2O3体系残余物在2 350 cm-1处最弱的吸收强度表明该氧化物具有独特的离解H2及促进加氢反应的能力。实际上,有研究证实氧化物表面的活性O能通过吸收烃中H引发烃类的裂解反应[22]。因此,针对Fe2O3催化液化阜新煤的过程,给出了如下反应机理:
Fe2O3结构表面的活性O首先吸收H2中的H形成H·,它们继而分别引发烃类的自由基反应,达到催化加氢的目的。
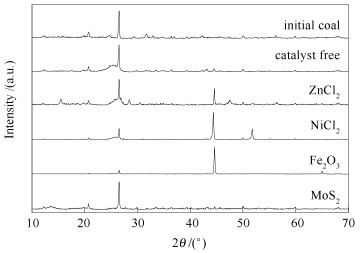
X射线衍射(XRD) 通常能够用来研究热演化过程中化合物的结构变化,为了进一步探讨和证实四种不同类型催化剂的作用机制,研究对单独及催化液化的残余物进行了XRD分析,具体见图 6。由图 6可知,单独热解残余物与原始煤样的X衍射图谱基本没有区别,这是由于原煤中的矿物多为热稳定的硅酸盐类。ZnCl2体系残余物中氯化物的低衍射强度证实其在加氢热解过程中发生了熔融。NiCl2结构在液化反应后没有太大的变化。Fe2O3体系残余物中还原态铁的出现也证实了上述Fe2O3的催化反应机理。MoS2残余物中可检测到微弱的MoS2-x(x < 2) 衍射峰,这表明由前驱物热解得到的活性催化剂MoS2在液化过程中很可能部分被H2还原生成了H2S。
计算可以得到,MoS2体系反应前后样品中硫含量的变化(ΔS) 为44.1 mg,这高于单独液化过程中的ΔS (10.8 mg)。导致这种结果的原因可能有两种:一是催化剂的加入导致煤中含有的S更多的释放出来;二是催化剂前驱物或其分解生成的活性硫化钼催化剂中的S部分以游离态释放出来。尽管研究证实,MoS2对含硫有机物比如噻吩等的脱硫反应具有很好的催化作用,也常被用作石油化工过程中的脱硫剂[23]。但原始阜新煤样中总的S含量仅为30.9 mg,小于反应前后S的减少量,这表明前驱物的分解或催化剂的脱硫对S含量的减少也应存在一定贡献。如1.1中所提,前驱物的主要成分为(NH4)2MoS4,该化合物在有氢气存在条件下,受热会发生如式(4) 的分解反应:
生成的活性催化剂MoS2在受热条件下也会与H2发生了如式(5) 的可逆反应[22]:
由反应式(4) 和(5) 可以看出,无论是早期前驱物的分解反应还是之后催化剂MoS2的加氢还原反应,都会产生一定量的H2S。作为反应活性很强的气体,H2S能迅速的与有机分子比如烃类发生反应生成包括噻吩和二硫化物等不稳定含S化合物,后者受热会进而分解生成含S自由基,并最终引发自由基反应[24]。
基于以上讨论,作者认为,MoS2在煤的加氢液化过程中主要起到以下两个作用:中间产物H2S对自由基反应的引发作用;过渡金属Mo对生成的烃类或自由基片段起到催化裂解及催化加氢的作用。
2.1.2 饱和烃、芳烃和生标组成
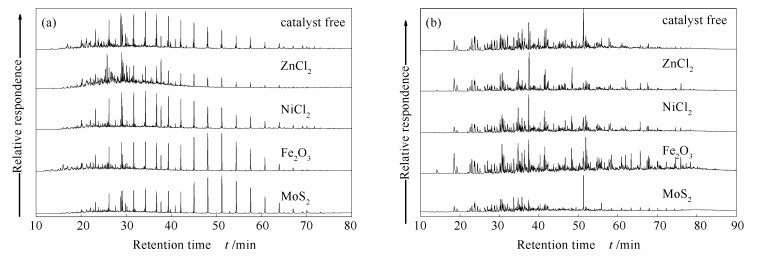
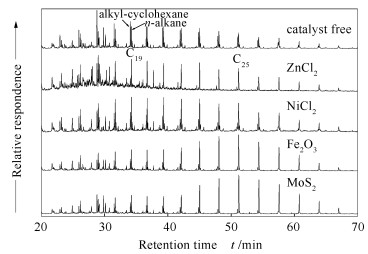
为了更深入了解不同催化剂对液态产物中成分的影响,实验对饱和烃和芳烃进行了色质(GC-MS) 分析。图 2为阜新煤不同催化加氢热解得到液态产物中饱和烃和芳烃组分的总离子色谱图。相对单独加氢热解来说,氯化物(包括ZnCl2和NiCl2) 的加入对饱和烃的分布影响不大,而Fe2O3和MoS2的加入导致了高碳数烃类含量的明显增加(图 2(a))。Fe2O3体系得到的油含有更高相对含量的较重的多环芳烃(PAHs),而MoS2体系中该产物的相对含量则很低(图 2(b))。
图 3为饱和烃组分的m/z 83质量色谱图。由图 3可知,相对单独加氢热解,催化体系中烷基环己烷的相对含量(烷基环己烷含量/正构烷烃含量) 明显偏低。也就是说,催化剂的存在能促进环烷烃结构中支链的β断裂,从而生成小分子烷烃和短链的环烷烃。结合2.1的分析可以得出,催化剂的加入不仅促进了煤液化过程中的加氢反应,还很可能加速了煤结构中支链的C-C键断裂。而不同催化体系得到的总转化率、液态产物产率及组成的差异表明,在煤液化过程中,四种催化剂可能存在不同的催化性能及机理。
表 3为阜新煤在不同催化剂条件下加氢热解产物的生物参数特征。由表 3可知,加氢热解得到的生标成熟度参数明显要低于抽提物,这归因于加氢热解得到的生物标志化合物主要来源于干酪根结构的再次裂解,经历的热演化程度要低于抽提物中的相应组分[12]。部分反应环境的生标参数存在较大差异,比如,ZnCl2催化加氢产物中姥鲛烷相对含量明显高于其他催化加氢产物。同时,几种催化剂加氢热解产物中反映成熟度的生标参数无明显差异。
 表 3
阜新煤不同催化加氢热解产物的生标参数
Table 3.
Biomarker parameters of pyrolysis products from Fuxin coal over different catalysts
表 3
阜新煤不同催化加氢热解产物的生标参数
Table 3.
Biomarker parameters of pyrolysis products from Fuxin coal over different catalysts
Biomarker parameter Extracts* Catalyst free Catalytic conditions ZnCl2 NiCl2 Fe2O3 MoS2 Pr/Ph 7.85 5.47 6.30 4.13 4.32 4.70 Pr/ nC17 4.01 0.68 1.23 0.59 0.51 0.93 Ph/ nC18 0.57 0.12 0.21 0.14 0.11 0.19 CPI 1.87 1.20 1.43 1.22 1.15 1.21 OEP-1 1.34 1.05 1.13 1.06 1.04 1.06 C22/C21 tricyclic terpane 0.43 0.37 0.47 0.34 0.32 0.32 Ts/(Ts+Tm) 0.36 0.33 - 0.23 0.22 0.29 C29 βα /C29 αβ 0.52 0.38 0.45 0.35 0.37 0.42 C30 βα /C30 αβ 0.48 0.41 0.50 0.45 0.46 0.51 C31αβ 22S/(22S+22R) 0.57 0.52 0.49 0.51 0.48 0.46 C32αβ 22S/(22S+22R) 0.56 0.53 0.48 0.50 0.43 0.47 C29 20S/(20S+20R) 0.23 0.26 0.22 0.25 0.24 0.19 C29 ββ/(ββ+αα) 0.23 0.24 0.20 0.24 0.15 0.15 MPI-1 0.33 0.71 0.56 0.65 0.62 0.58 MNR 1.08 2.37 2.16 2.54 2.08 2.00 ENR 0.23 0.24 0.39 0.37 0.44 0.40 *: extracts represent the liquid products obtained by extraction of organic matters 表 3 阜新煤不同催化加氢热解产物的生标参数
Table 3. Biomarker parameters of pyrolysis products from Fuxin coal over different catalysts2.1.1 液态产物产率及组成特征
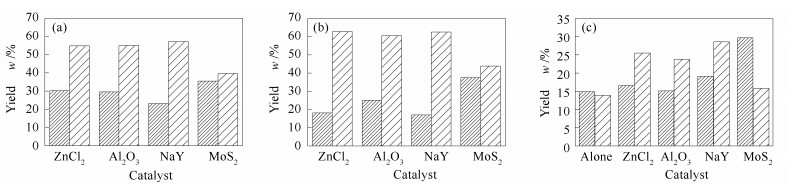
表 2为三种样品在不同催化剂条件下加氢热解得到的液体产物产率及族组成特征。相对于单独加氢热解,催化剂的存在可明显提高液体产物的产率。不同催化剂加氢产物的产率和组成存在明显差异,同时,催化剂对不同成熟度或不同类型样品显示出不同的催化加氢效果。以相对较低成熟度的杜13干酪根样品为例,MoS2催化加氢热解体系得到的液态产物产率为390.9 mg/g干酪根,高于其他催化加氢体系;对于高成熟的肇深5干酪根和低熟的阜新煤样,ZnCl2加氢热解得到的液态产物产率更高。值得注意的是(图 1),MoS2催化加氢热解生成液态产物中饱和烃相对含量要明显高于其他加氢体系,其他催化热解体系得到的芳烃含量相对较高。
 表 2
不同催化剂条件下有机质加氢热解的液体产物产率及组成特征
Table 2.
Yields and compositions of liquid products from catalytic hydropyrolysis of organic matters over different catalysts
表 2
不同催化剂条件下有机质加氢热解的液体产物产率及组成特征
Table 2.
Yields and compositions of liquid products from catalytic hydropyrolysis of organic matters over different catalysts
Sample Catalyst Overall yield of liquid hydrocarbons w/(mg·g-1) Group composition w/% saturates aromatics NSO compounds and asphaltenes Kerogen of Du-13 ZnCl2 292.0 30.2 54.8 15.0 Al2O3 258.0 29.6 55.1 15.3 NaY 298.4 23.2 57.1 19.7 MoS2 390.9 35.5 39.6 24.9 Kerogen of Zhaoshen-5 ZnCl2 40.2 18.1 62.8 19.1 Fe2O3 16.0 25.0 60.5 14.5 Al2O3 17.6 17.0 62.5 20.5 MoS2 18.0 37.5 43.8 18.7 Fuxin coal alone 162.8 14.9 13.9 71.2 ZnCl2 606.0 16.6 25.5 57.9 NiCl2 541.5 15.1 23.8 61.1 Fe2O3 503.6 19.1 28.6 60.3 MoS2 237.8 29.7 15.8 54.5 表 2 不同催化剂条件下有机质加氢热解的液体产物产率及组成特征
Table 2. Yields and compositions of liquid products from catalytic hydropyrolysis of organic matters over different catalysts3 结论
不同类型催化剂加氢热解产物产率和组成存在明显差异,ZnCl2更有利于高成熟和煤岩样品的加氢热解,MoS2催化加氢产物中饱和烃相对含量明显高于其他催化剂,后者催化加氢产物中芳烃含量则相对较高。
氯化物催化加氢产物中饱和烃分布与单独热解较为接近,Fe2O3和MoS2催化加氢产物中高碳数烷烃含量明显偏高。同时,几种催化剂加氢热解产物中生标组成差异不大。
相对NiCl2体系,ZnCl2体系具有更好的催化效果,这是因为后者除了存在催化裂解和催化加氢作用外,还存在质量传递效应。Fe2O3是通过其表面的活性O吸收H2中的H形成H自由基,从而起到催化加氢的效果。对于MoS2体系,其催化机制包括两种:过渡金属Mo的催化加氢及中间产物H2S的自由基引发作用。
-
-
[1]
李保庆. 我国煤加氢热解研究Ⅱ.先锋褐煤加氢及催化加氢热解的热重研究[J]. 燃料化学学报, 1995,23,(2): 186-191. LI Bao-qing. Hydropyrolysis of Chinese coals Ⅱ. Thermogravimetric study on catalytic and non-catalytic hydropyrolysis of Xianfeng lignite[J]. J Fuel Chem Technol, 1995, 23(2): 186-191.
-
[2]
李保庆. 我国煤加氢热解研究Ⅲ.神府煤加氢、催化加氢及H2-CH4气氛下热解的研究[J]. 燃料化学学报, 1995,23,(2): 192-196. LI Bao-qing. Hydropyrolysis of Chinese coals Ⅲ. Catalytic and non-catalytic hydropyrolysis under H2-CH4 of Shenfu bituminous coal[J]. J Fuel Chem Technol, 1995, 23(2): 192-196.
-
[3]
PETERS K E, MOLDOWAN J M. The bionmarker guide: Interpreting molecular fossoils in petroleum and ancient sediments[M]. New Jersey: Prentice Hall, 1993: 170-176.
-
[4]
傅家谟, 盛国英, 许家友, 贾蓉芬, 范善发, 彭平安, EGLINTONG, GOWARA P. 应用生物标志化合物参数判识古沉积环境[J]. 地球化学, 1991,20,(1): 1-12. FU Jia-mo, SHENG Guo-ying, XU Jia-you, JIA Rong-fen, FAN Shan-fa, PENG Ping-an, EGLINTON G, GOWAR A P. Application of biomarker compounds in assessment of paleoenvironxnents of Chinese terrestrial sediments[J]. Geochimica, 1991, 20(1): 1-12.
-
[5]
LOVE G D, SNAPE C E, CAM A D. Release of covalently-bound alkane biomarkers in high yields from kerogen via catalytic hydropyrolysis[J]. Org Geochem, 1995, 23(10): 981-986. doi: 10.1016/0146-6380(95)00075-5
-
[6]
IKENAGA N, KAN-NAN S, SAKODA T, SUZUKI T. Coal hydroliquefaction using highly dispersed catalyst precursors[J]. Catal Today, 1997, 39(1/2): 99-109.
-
[7]
INUKAI Y. Hydroliquefaction of Illinois NO.6 coal with petroleum atmospheric residue using oil-soluble molybdenum catalyst[J]. Fuel Process Technol, 1995, 43(2): 157-167. doi: 10.1016/0378-3820(95)00017-2
-
[8]
岳长涛, 李术元, 徐明, 钟宁宁. 柴油与硫酸镁反应体系模拟实验研究[J]. 石油实验地质, 2010,32,(6): 610-614. YUE Chang-tao, LI Shu-yuan, XU Ming, ZHONG Ning-ning. Simulation experiments on the TSR system of diesel and mangnesium sulfate[J]. Pet Geol Exp, 2010, 32(6): 610-614.
-
[9]
ROCHA J D, BROWN S D, LOVE G D, SNAPE C E. Hydropyrolysis: A versatile technique for solid fuel liquefaction, sulfur speciation and biomarker release[J]. J Anal Appl Pyrolysis, 1997, 40-41: 91-103. doi: 10.1016/S0165-2370(97)00041-7
-
[10]
RUSSELL C A, SNAPE C E, MEREDITH W. The potential of bound biomarker prfiles released from catalytic hydropymlysis to reconstruction basin charging history for oils[C]. Abstract for 21th International Meeting on Organic Geochemistry K rakow. 2003: 160-161.
-
[11]
LOCKHART R S, MEREDIT H W, LOVE G D. Release of bound aliphatic biomarkers via hydropyrolysis from Type Ⅱ kerogen at high maturity[J]. Org Geochem, 2008, 39(8): 1119-1124. doi: 10.1016/j.orggeochem.2008.03.016
-
[12]
HE K, ZHANG S C, MI J K. Mechanism of catalytic hydropyrolysis of sedimentary organic matter with MoS2[J]. Pet Sci, 2011, 8(2): 134-142. doi: 10.1007/s12182-011-0126-0
-
[13]
ZELENSKI C M, DORHOUT P K. Template synthesis of near-monodisperse microscale nanofibers and nanotubes of MoS2[J]. J Am Chem Soc, 1998, 120(4): 734-742. doi: 10.1021/ja972170q
-
[14]
FARAG H, EI-HEDAWY A, SAKAISHI K, KISHIDA M, MOCHIDA I. Catalytic activity of synthesized nanosized molybdenum disulfide for the hydrodesulfurization of dibenzthiophene: Effect of H2S partial pressure[J]. Appl Catal B: Environ, 2009, 91(1/2): 189-197.
-
[15]
SONG J H, CHEN P L, KIM S H. Catalytic cracking of n-hexane over MoO2[J]. J Mol Catal A, 2002, 184(1/2): 197-202.
-
[16]
PINTO F, GULYURTLU I, LOBO L S, CABRITA I. The effect of catalyst blending on coal hydropyrolysis[J]. Fuel, 1999, 78(7): 761-768. doi: 10.1016/S0016-2361(98)00212-9
-
[17]
SONG C S, NOMURA M, MIYAKE M. Coal hydroliquefaction using MoCl3-and NiCl2-containing salts as catalysts: Difference in catalysis between solid and molten catalysis[J]. Fuel, 1986, 65(7): 922-926. doi: 10.1016/0016-2361(86)90199-7
-
[18]
WANG L, CHEN P. Mechanism study of iron-based catalysts in co-liquefaction of coal with waste plastics[J]. Fuel, 2002, 81(6): 811-815. doi: 10.1016/S0016-2361(01)00201-0
-
[19]
HE K, DONG Y M, LI Z. Catalytic ozonation of phenol in water with natural brucite and magnesia[J]. J Hazard Mater, 2008, 159(2/3): 587-592.
-
[20]
HE K, DONG Y M, LIN Y. A facile hydrothermal method to synthesize nanosized Co3O4/CeO2 and study of its catalytic characteristic in catalytic ozonation of phenol[J]. Catal Lett, 2009, 133(1): 209-213.
-
[21]
PRIYANTO U, SAKANISHI K, OKUMA O, MOCHIDA I. Liquefaction of Tanito Harum coal with bottom recycle using FeNi and FeMoNi catalysts supported on carbon nanoparticles[J]. Fuel Process Technol, 2002, 79(1): 51-62. doi: 10.1016/S0378-3820(02)00101-7
-
[22]
SONG C, SAINI A K, YONEYAMA Y. A new process for catalytic liquefaction of coal using dispersed MoS2 catalytic generated in situ with added H2O[J]. Fuel, 2000, 79(3/4): 249-261.
-
[23]
BOONE W P, EKERDT J G. Hydrodesulfurization studies with a single-layer molybdenum disulfite catalyst[J]. J Catal, 2000, 193(1): 96-102. doi: 10.1006/jcat.2000.2884
-
[24]
ZHANG T W, AMRANI A, ELLIS G S, MA Q S, TANG Y C. Experimental investigation on thermochemical sulfate reduction by H2S initiation[J]. Geochim Cosmochim Acta, 2008, 72(14): 3518-3530. doi: 10.1016/j.gca.2008.04.036
-
[1]
-
表 1 催化加氢热解样品的地球化学特征
Table 1. Geochemical characteristic of the organic matters for catalytic hydropyrolysis
Sample Depth L/m Layer TOC w/% R0 w/% Elemental compostion of kerogen w/% C H O N Du-13 1 408.5 K 3.14 0.84 60.44 1.231 6.61 1.65 Zhaoshen-5 4 331 C-P - 2.06 72.99 0.296 2.17 1.83 Fuxin coal surface J 71.24 0.55 73.52 5.68 - 1.23 表 2 不同催化剂条件下有机质加氢热解的液体产物产率及组成特征
Table 2. Yields and compositions of liquid products from catalytic hydropyrolysis of organic matters over different catalysts
Sample Catalyst Overall yield of liquid hydrocarbons w/(mg·g-1) Group composition w/% saturates aromatics NSO compounds and asphaltenes Kerogen of Du-13 ZnCl2 292.0 30.2 54.8 15.0 Al2O3 258.0 29.6 55.1 15.3 NaY 298.4 23.2 57.1 19.7 MoS2 390.9 35.5 39.6 24.9 Kerogen of Zhaoshen-5 ZnCl2 40.2 18.1 62.8 19.1 Fe2O3 16.0 25.0 60.5 14.5 Al2O3 17.6 17.0 62.5 20.5 MoS2 18.0 37.5 43.8 18.7 Fuxin coal alone 162.8 14.9 13.9 71.2 ZnCl2 606.0 16.6 25.5 57.9 NiCl2 541.5 15.1 23.8 61.1 Fe2O3 503.6 19.1 28.6 60.3 MoS2 237.8 29.7 15.8 54.5 表 3 阜新煤不同催化加氢热解产物的生标参数
Table 3. Biomarker parameters of pyrolysis products from Fuxin coal over different catalysts
Biomarker parameter Extracts* Catalyst free Catalytic conditions ZnCl2 NiCl2 Fe2O3 MoS2 Pr/Ph 7.85 5.47 6.30 4.13 4.32 4.70 Pr/ nC17 4.01 0.68 1.23 0.59 0.51 0.93 Ph/ nC18 0.57 0.12 0.21 0.14 0.11 0.19 CPI 1.87 1.20 1.43 1.22 1.15 1.21 OEP-1 1.34 1.05 1.13 1.06 1.04 1.06 C22/C21 tricyclic terpane 0.43 0.37 0.47 0.34 0.32 0.32 Ts/(Ts+Tm) 0.36 0.33 - 0.23 0.22 0.29 C29 βα /C29 αβ 0.52 0.38 0.45 0.35 0.37 0.42 C30 βα /C30 αβ 0.48 0.41 0.50 0.45 0.46 0.51 C31αβ 22S/(22S+22R) 0.57 0.52 0.49 0.51 0.48 0.46 C32αβ 22S/(22S+22R) 0.56 0.53 0.48 0.50 0.43 0.47 C29 20S/(20S+20R) 0.23 0.26 0.22 0.25 0.24 0.19 C29 ββ/(ββ+αα) 0.23 0.24 0.20 0.24 0.15 0.15 MPI-1 0.33 0.71 0.56 0.65 0.62 0.58 MNR 1.08 2.37 2.16 2.54 2.08 2.00 ENR 0.23 0.24 0.39 0.37 0.44 0.40 *: extracts represent the liquid products obtained by extraction of organic matters 表 4 阜新煤样加氢热解后固体残余物的元素分析
Table 4. Elemental compositions of solid residues
Reaction condition Content w/% C/H* C H O S N Catalyst free 77.04 4.32 6.94 1.02 1.39 1/1.75 ZnCl2 63.57 3.12 5.84 1.43 0.96 1/1.13 NiCl2 62.88 3.17 4.30 1.03 1.03 1/1.20 Fe2O3 45.76 2.34 3.66 1.40 0.82 1/1.11 MoS2 72.39 5.09 6.89 2.81 1.48 1/1.07 *: C/H represents the ratio of carbon conversion to hydrogen in the hydropyrolysis -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0


 下载:
下载:





 下载:
下载:

