 图1
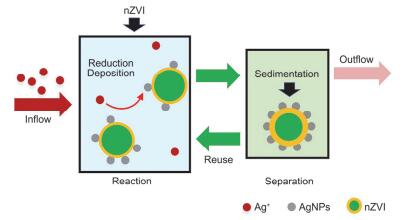
纳米零价铁连续流反应器富集银示意图
Figure1.
The scheme of silver enrichment with nZVI reactor
图1
纳米零价铁连续流反应器富集银示意图
Figure1.
The scheme of silver enrichment with nZVI reactor

Citation: Gu Tianhang, Shi Junming, Hua Yilong, Liu Jing, Wang Wei, Zhang Wei-xian. Enrichment of Silver from Water Using Nanoscale Zero-Valent Iron (nZVI)[J]. Acta Chimica Sinica, 2017, 75(10): 991-997. doi: 10.6023/A17070345

应用纳米零价铁富集银的研究
English
Enrichment of Silver from Water Using Nanoscale Zero-Valent Iron (nZVI)
-
Key words:
- nanoscale zero-valent iron
- / silver
- / enrichment
- / silver nanoparticles
- / nano-iron reactor
-
1 引言
银(Silver, Ag)是一种具有银白色光泽的稀贵金属, 广泛地应用于流通货币、装饰品、工业催化、电子元件制造等领域[1].然而, 随着银需求不断增大及含银矿产的大量开采, 银资源紧缺问题正逐渐突显[2, 3].另一方面, 含银废水(如冶炼废水、电镀废水)、废渣(如尾矿、电子废弃物)等二次资源中的银未被有效回收利用, 仅1997年全球就有1.34×104 t银排入环境[4~6].因此, 研究如何从此类低浓度/低品位二次资源中有效分离/回收银, 具有巨大的社会效益.此外, 纳米银(Silver Nanoparticles, AgNPs)由于具有优良的抗菌、催化及光学特性, 成为目前应用最广泛的纳米材料之一[1, 7, 8].据统计, 全球有438种在售商品含有纳米银, 占所有“纳米”商品种数的24%(2015年)[9].如果能够以含银废水为原料, 生产高附加值的纳米银颗粒, 那么对经济与环境可持续健康发展都将具有重要理论和现实意义.
近年来, 各国学者研究采用不同材料分离水中银离子, 如碳材料、铁材料、螯合树脂、生物材料等[10~14].其中, 纳米零价铁(nanoscale Zero-Valent Iron, nZVI)具有独特“核-壳”结构, 内核为零价铁(Fe0), 外壳为铁(氢)氧化物(如FeOOH), 具有尺寸小、比表面积大、反应活性高、反应产物环境友好等特点[15~17].近期研究表明, nZVI可通过吸附、还原等作用有效分离水中金、银、铀、硒等贵重(类)金属资源, 在重金属废水处理及资源化方面表现出巨大应用潜力[18~23].例如, 学者通过烧杯实验考察nZVI富集银可行性及产物特征, 发现当初始Ag/Fe反应质量比低于1.25时, nZVI可将水中Ag+还原成纳米银颗粒[18]; 另有学者采用介孔限域的方法将nZVI稳定结合于介孔碳管内并考察其对水中痕量金离子(0.01 mg/L)富集能力, 发现nZVI可快速高效富集金离子, 产生的金颗粒粒径仅为5 nm, 可作为双金属催化剂进一步回收再利用[19].
然而, 现有关于nZVI分离水中Ag等稀贵金属资源的结果多来源于实验室烧杯(批次)试验, 尚缺乏对实际应用过程中面临的反应器构型/设计、工艺参数选择及组合优化、反应产物固液分离及回收等问题的研究和讨论[18~23].近年来, 笔者所在研究团队通过“小试-中试-工程”科学放大, 系统探索了nZVI连续处理实际重金属废水可行性, 提出“反应-分离-回用”式连续流反应器模型, 并成功将nZVI应用于含As、Cu、Pb、Zn、Ni等重金属的复杂冶炼废水处理工程[24~26].在实践过程中, 还发现实际废水中常存在多种低浓度稀贵金属离子, 如某冶炼废水中Ag+浓度在0.12~10.54 mg/L之间波动(平均值为1.10 mg/L).通过文献检索, 关于nZVI连续富集回收废水中低浓度Ag的研究鲜有报道.
本文在团队前期研究基础上, 采用“反应-分离-回用”式纳米零价铁反应器(Nano-Iron Reactor, NIR), 探讨nZVI连续富集水中低浓度Ag+的工艺可行性, 考察了相关反应条件影响及反应产物回收价值, 包括: (1) 通过连续流穿透实验研究不同水力停留时间(Hydraulic Retention Time, HRT)对低浓度Ag+(约1 mg/L)富集效果的影响, 分析反应区氧化还原电位(Eh)与Ag富集效果间相关性并进行稳态实验验证; (2) 通过批次实验探究nZVI对银富集性能及关键因素影响, 结合多种固相表征手段进一步证明反应机理及Ag回收价值.本研究将为nZVI富集痕量Ag的应用提供理论依据和指导.
2 结果与讨论
2.1 连续流实验
本文首先探讨了NIR富集Ag+的可行性及可控性. NIR由反应区、分离区及回流装置三部分组成(图 1, 表S1):其中反应区为全混合搅拌釜式反应器, 具有连续处理废水并有一定抗冲击能力的特点; 由于nZVI自身具有磁性, 颗粒间因为偶极间作用会形成链状团聚体, 在反应器中这些链状团聚物会进一步形成微米级团聚体, 平均粒径约7 μm, 尺寸较小, 因此简单的机械搅拌即可达到混合均匀的目的; 进水([Ag+]in=1 mg/L)由蠕动泵连续输入反应区与nZVI充分混合均匀并反应, 而后混合液流入分离区; 分离区为一竖流式沉淀池, 利于nZVI在底部锥形泥斗中沉积浓缩和回流, 根据笔者所在团队前期研究, 当表面负荷为0.5 m3/(m2·h)时(略低于本文最大表面负荷), 92%的nZVI可后经重力沉降实现固液分离, 分离后上清液通过分离区上部三角堰连续流出(出水); 沉积在分离区底部的nZVI经蠕动泵回流至反应区继续参与反应, 以提高nZVI利用率[27].
2.1.1 连续流穿透实验
本部分实验研究了NIR在不同HRT的条件下(表S2) 对Ag+的富集性能.以钠离子(Na+)作为示踪剂比较反应器对Ag+的富集效果, 并监测反应区Eh的变化, 研究Eh与Ag+富集效率的关系.
当HRT=10 min时(图 2A), 出水中Na+浓度快速上升, 2 h后完全穿透([Na+]出水=[Na+]进水), 而9.5 h后Ag+浓度仍低于原水浓度的20%.可见nZVI对Ag+具有极强的截留能力(截留率>80%).当系统HRT为30或60 min(图 2B~2C)时, 反应器对Ag+富集能力提高.在累积进入系统Ag量不变的情况下, 当HRT由10 min延长至60 min, Ag+最大穿透率由19.0%降至4.1%, 这可能是因为HRT的延长增加了Ag+与nZVI的接触时间, 使反应更加充分.
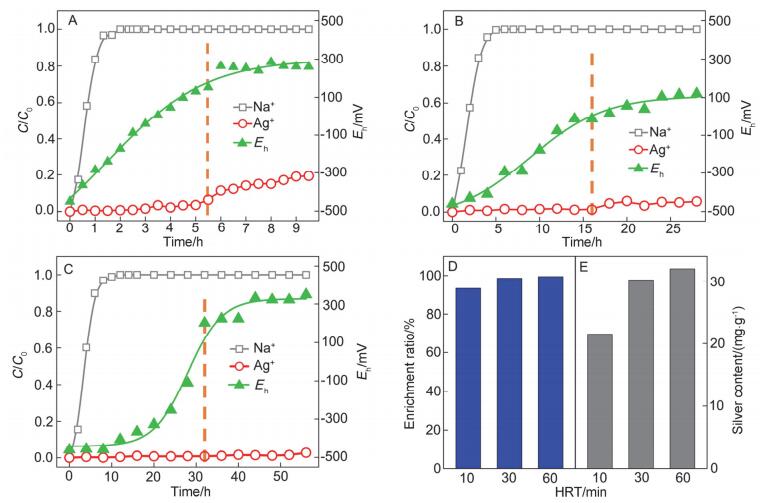 图2
不同水力停留时间条件下Ag+富集情况、出水中Na+浓度变化及反应区Eh变化: (A) HRT=10 min; (B) HRT=30 min; (C) HRT=60 min; (D)平均富集率; (E)反应产物银含量
Figure2.
Effluent concentrations of Ag+ and Na+, and variation of Eh as a function of reaction time under different: (A) HRT=10 min; (B) HRT=30 min; (C) HRT=60 min; (D) average silver enrichment ratio; (E) silver content in final products
图2
不同水力停留时间条件下Ag+富集情况、出水中Na+浓度变化及反应区Eh变化: (A) HRT=10 min; (B) HRT=30 min; (C) HRT=60 min; (D)平均富集率; (E)反应产物银含量
Figure2.
Effluent concentrations of Ag+ and Na+, and variation of Eh as a function of reaction time under different: (A) HRT=10 min; (B) HRT=30 min; (C) HRT=60 min; (D) average silver enrichment ratio; (E) silver content in final products
不同HRT条件下, 反应区Eh和出水中Ag+浓度均存在一定相关性(图 2A~2C).例如HRT=10 min时, 出水中Ag+浓度和反应区内Eh的变化趋势可分为两个阶段:阶段1 (0~5.5 h) Eh快速上升, 出水Ag+浓度稳定在40 μg/L以下(C/C0<0.04);阶段2 (5.5~9.5 h) Eh维持稳定, 出水Ag+浓度快速上升.比较两阶段终点C/C0值, 分别由0.035迅速增加至0.194 (HRT=10 min), 0.013至0.057 (HRT=30 min), 0.011至0.028 (HRT=60 min).因此, 在实际应用过程中, 根据Eh与出水Ag+浓度的关系, 可将Eh作为在线反映出水Ag+浓度的参数, 根据Eh的变化趋势决定投加新鲜nZVI或排出分离区固相产物的时间点.
以HRT=10 min时的结果为例(图 2A), Eh和出水Ag+浓度变化的原因可能是: (1) 阶段1过程中, 分离区表面水力负荷[0.566 m3/(m2·h)]大于nZVI颗粒有效分离的极限表面水力负荷[0.100 m3/(m2·h)], 部分nZVI随出水流失, 因而Eh上升速度快, 同时反应区较高浓度的nZVI促进Ag+被快速稳定富集; 阶段2过程中反应区内nZVI浓度较低, nZVI随出水流失量减少, 因此Eh保持相对稳定, 反应区nZVI浓度过低导致系统对Ag+的富集效率降低, 出水中Ag+浓度明显上升[26~28], 在实际应用中需要添加新鲜nZVI; (2) 阶段1 nZVI颗粒中Fe0含量较高, 还原能力较强, 可快速富集Ag+, 而在阶段2, nZVI经过在较长时间的循环使用中不断受到H2O、混杂的O2及溶液中NO3-的腐蚀, Fe0含量降低, 还原能力减弱, 水质开始恶化, 因此在实际应用中需在适当时间排出反应后固体颗粒.
根据物料守恒计算, 可知在不同HRT条件下(处理17.1 L含银原水), nZVI对Ag+的平均富集率为: 93.3% (10 min)<98.6% (30 min)<99.5% (60 min), 再一次证明延长HRT可提高nZVI的富集效率(图 2D); 当HRT由10 min增加至30 min时, 平均富集率提高了5.3%, 而由30 min至60 min时, 平均富集率仅提高0.9%, 综合考虑富集率及处理效率, HRT设为10 min或30 min较合适.此外, 还可计算出NIR内反应产物(Ag-nZVI)上银含量分别为21.5 (10 min)、30.2 (30 min)、32.0 (60 min) mg/g(图 2E).考虑到nZVI会腐蚀产生(氢)氧化物, 实际银含量会略低于上述三个值, 但仍高于高品位银矿石(6~10 mg/g)[29], 表明利用nZVI可将分散的低品位的银资源富集, 并浓缩至具有较高回收价值的水准.
2.1.2 Eh稳态调控实验
依据2.1.1中出水Ag+浓度和反应区Eh的联系, 可得出以下结论: Eh变化趋势能够反映nZVI对Ag+的富集效率.为了进一步验证这种规律, 模拟了向NIR内间歇性投加新鲜nZVI时系统运行的稳定性.反应开始前向反应区投加0.5 g新鲜nZVI, 之后每次Eh趋于稳定时投加0.1 g新鲜nZVI(投加3次).
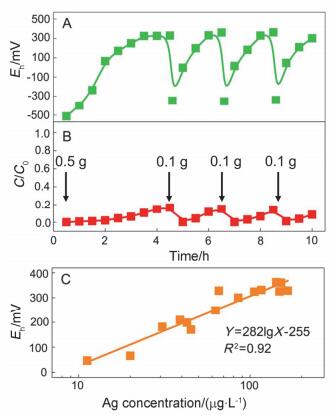
图 3A、3B反映了出水Ag+浓度、反应区Eh的变化.实验结果表明, 连续流穿透实验中Eh和出水Ag+浓度的变化趋势得到多次重现.每次反应进行到一定程度, 随着nZVI的流失及氧化, 反应区内Fe0浓度降低, Eh由约-500 mV上升至约300 mV并趋于平稳, 对Ag+的富集能力会逐渐减弱, 出水中Ag+浓度由3 μg/L上升至165 μg/L; 补充0.1 g新鲜nZVI后, 反应区Fe0浓度显著提高, Eh迅速降低至-350 mV, NIR对Ag+的富集能力提高, 出水中Ag+降低至4 μg/L.
图 3C结果表明:反应区Eh与出水中Ag+浓度的对数(lg[Ag+]出水)存在较好的线性关系, 更直接地证明了反应区Eh能够反映NIR对Ag+的富集性能.以上结果表明:可利用反应区Eh与出水中Ag+浓度之间的联系, 建立Eh调控机制, 以此来调控NIR富集效率.
2.2 批次实验
2.2.1 不同材料对Ag+的富集
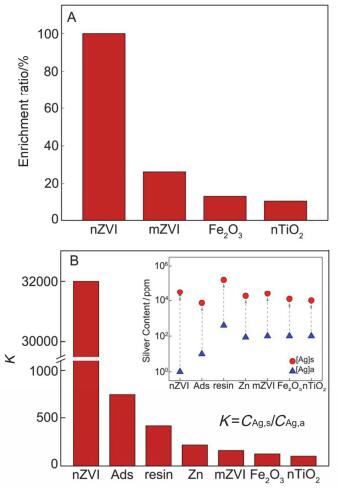
为了研究nZVI富集Ag+的能力, 本部分实验选取与nZVI尺寸或组分相同的三种材料[三氧化二铁(α-Fe2O3); 纳米二氧化钛(nTiO2); 微米零价铁(mZVI)], 比较其对溶液中Ag+ (pH=5) 的富集效果.实验结果如图 4A所示, nZVI、mZVI、α-Fe2O3、nTiO2对Ag+的富集率分别为99.9%、26.3%、12.8%和10.3%.
上述结果的原因可能是: (1) 溶液中nZVI、mZVI、α-Fe2O3、nTiO2颗粒表面吸附位点(-OH)通过吸附作用捕获Ag+; (2) α-Fe2O3和nTiO2仅能通过表面有限的活性位点(-OH)吸附溶液中少量Ag+; 而nZVI、mZVI的主要成分零价铁(Fe0)与Ag+发生氧化还原反应[式(1)]:
nZVI和mZVI可通过还原作用强化对Ag+的富集; (3) nZVI比表面积可达30 m2/g, 而mZVI仅0.01~1 m2/g[30], 在相同投加量情况下, nZVI具有更多活性位点, 反应活性更强; (4) mZVI与Ag+反应过程中产生的铁氧化物沉积在颗粒表面, 降低了Fe0与Ag+之间的电子传递效率, 阻碍反应的进一步进行[31, 32], 而nZVI壳层存在缺陷, 可作为电子传递通道, 整个壳层可视为半导体, 因此效率受表面氢氧化物沉积影响不明显.
由图 4B可见, nZVI对Ag+的分离系数(K=104.51 L/kg)比其它材料(K: 102.01~102.87 L/kg)高1~3个数量级[33~35], 可将水相中低浓度的Ag+富集至固相.实验结果表明, nZVI可高效、快速富集溶液中的Ag+.
上述实验结果表明, nZVI是一种高效富集Ag+的材料, 可通过吸附、还原等作用将溶液中Ag+高效、快速富集.既能回收废水中的银资源, 也能保证出水水质, 减少银对生态系统及人体健康造成的危害.
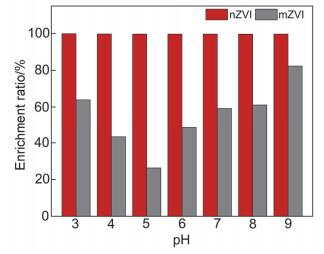
2.2.2 初始pH对Ag+富集的影响
溶液pH影响颗粒表面电荷分布、离子形态, 进而影响固相颗粒表面离子的传质过程.因此, 本工作研究了溶液初始pH(3~9) 对nZVI、mZVI富集Ag+的影响.实验结果表明, 不同溶液初始pH条件下, nZVI对Ag+的富集率均大于99%; mZVI对Ag+的富集率由63.9% (pH=3) 降至26.3% (pH=5), 又上升至83.3% (pH=9) (图 5).
在pH为3~9的AgNO3溶液中, 银以Ag+的形式存在. nZVI和mZVI表面等电点约为8.3[15], 因此当溶液pH<8.3时, 颗粒表面以正电荷为主, 不利于对Ag+的吸附; 当pH>8.3时, 颗粒表面带负电荷, 促进对Ag+的吸附.
在当前反应条件下(nZVI或mZVI投加量=1 g/L, [Ag+]=100 mg/L), nZVI比表面积大, 反应活性高, 投加至溶液(初始pH 3~9) 中会迅速与H2O等物质反应, 产生OH-, 使溶液pH快速稳定在7.5~9.5范围内[15], 并且nZVI主要通过还原作用(Ag+→Ag)富集溶液中的Ag+, 体系具有强还原性, 因此富集结果受pH影响微弱.mZVI主要通过吸附、还原作用富集Ag+.低pH条件下, mZVI表面带正电, 但表面钝化层脱落后裸露出的新鲜零价铁具有较强还原作用, 促进颗粒对Ag+的富集, 因此低pH利于Ag+的去除; 高pH条件下, mZVI表面钝化层负电荷比例提高后吸附作用增强, 进而对Ag+的去除率提高.实验结果表明, 在当前实验条件下, nZVI富集Ag+的过程基本不受溶液初始pH影响.
2.2.3 nZVI投加量的影响
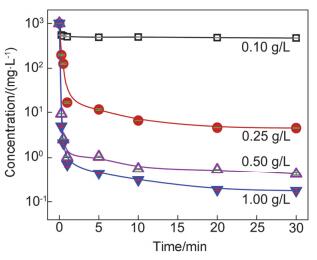
不同nZVI投加量的条件下, Ag+富集动力学过程如图 6所示.投加0.10 g/L nZVI时, 1 min内Ag+被快速分离且溶液中Ag+浓度到平衡, 30 min时Ag+富集率为53%.当nZVI浓度增加至0.25、0.50和1.00 g/L时, 富集99%以上Ag+所需时间分别为5 min、15 s和10 s.实验结果表明, nZVI对Ag+有强富集能力, 且提高nZVI投加量时, nZVI颗粒中对Ag+的吸附位点增多, 加快了nZVI颗粒Ag+富集速率.
图S1为不同初始水质负荷(Ag/nZVI, m/m)条件下nZVI对Ag+的富集能力.当水质负荷为0.05~4.50 g-Ag+/g-nZVI时, nZVI对Ag+的富集能力呈线性递增趋势; 当负荷大于4.50 g-Ag+/g-nZVI时, nZVI对Ag+的富集能力趋于饱和, 达到最大值5.30 g-Ag/g-nZVI. nZVI主要成分Fe0具有较强的还原能力, 可还原Ag+[式(1)], 反应产物结构态亚铁(Fe2+)可还原Ag+[式(2)]:
因此1 mol/L Fe0可还原3 mol/L Ag+, 计算可得其理论最大富集能力可达5.78 g-Ag/g-nZVI.实际反应过程中, nZVI中还原组分(Fe0、结构态亚铁)会受到H2O及其它氧化性组分(O2及NO3-等)的影响, 实际最大富集能力为5.30 g-Ag/g-nZVI, 略低于理论值.
2.3 产物固相表征
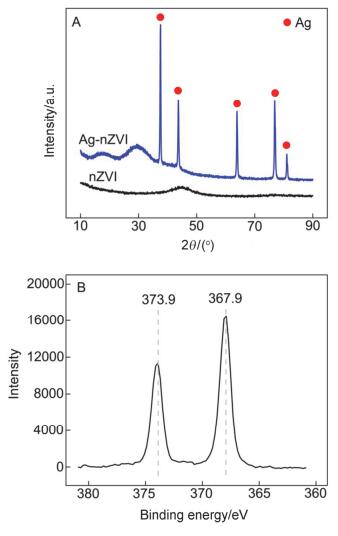
图 7A为新鲜nZVI及其与Ag+反应后固相产物(Ag-nZVI)的XRD谱图: nZVI在2θ=44.9°存在一个弱且宽化的衍射峰, 为α-Fe(0).而反应产物在2θ=37.9°、44.1°、64.2°、77.2°和81.3°产生较为尖锐的衍射峰, 与Ag0的(JCPDS 65-2871) 标准衍射图谱相吻合, 表明Ag+被nZVI还原为单质银(Ag0).为进一步确定nZVI与Ag+反应后Ag元素的价态, 对反应后的固体进行了高分辨XPS测定, 图 7B为产物表面Ag 3d的图谱, 两个峰Ag 3d3/2和Ag 3d5/2的结合能位于367.9 eV与373.9 eV, 此结果与Zhang等[18]研究相一致, 再次证明nZVI表面银元素为Ag0.
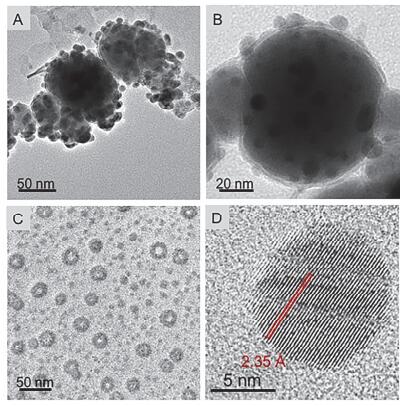
反应产物中单质银物相、元素价态确定之后, 通过HR-TEM研究产物形貌结构.图S2为新鲜nZVI, 呈链球状, 粒径约为100 nm, 具有明显“核-壳”结构, 表面氧化物层厚度约3 nm. 图 8A和图 8B为反应后的Ag-nZVI, 可发现产物颗粒表面附着有直径4~10 nm球形颗粒.使用聚乙烯吡咯烷酮K-30(PVP)和稀硫酸处理后[36], nZVI载体被除去, 球形颗粒从载体上分离, 分布均匀(图 8C).对图中100个纳米颗粒粒径进行统计:粒径范围9~32 nm, 平均值16.4 nm.单个纳米颗粒(图 8D)为球形, 直径约10 nm, 晶面间距(2.35?)与银单质相吻合, 进一步证实了反应产物为AgNPs.反应产物Ag-nZVI的Ag-Fe双金属结构可形成原电池, 可能可作为负载型AgNPs催化剂, 而分离后的AgNPs进一步纯化后可能可应用于医疗卫生领域.
上述结果表明nZVI富集Ag+的过程中, Ag+被还原为单质银并以球形纳米颗粒的形式附着在nZVI颗粒表面, 简单地使用稀硫酸溶解含铁固体和聚乙烯吡咯烷酮K-30(PVP)分散之后, 即可获得AgNPs.
3 结论
本文研究并证实“反应-分离-回用”式NIR工艺能够高效富集低浓度Ag+(约1 mg/L).反应产物Ag-nZVI中Ag的含量可达32.0 mg/g, 可解决分散银资源富集回收的问题; Eh调控机制稳定可靠, 可反映NIR富集效果, 将出水Ag+浓度控制在较低水平.相比于其他常用的吸附/还原材料, nZVI富集效率及速率高, 受pH影响小, 通过吸附、还原作用对Ag的最大富集负荷可达5.3 g-Ag/g-nZVI.使用PVP和稀硫酸处理反应后nZVI颗粒即可得到高结晶度的球形(10 nm)纳米银(AgNPs)单质.
4 实验部分
4.1 nZVI制备
采用经典液相还原法[15], 即将NaBH4 (0.2 mol/L)逐滴加至FeCl3 (0.05 mol/L)溶液中制备得到nZVI[式(3)]:
新鲜制备的nZVI使用去离子水和无水乙醇多次洗涤后低温(4 ℃)保存于无水乙醇中.
4.2 连续流实验
纳米零价铁连续流反应器(图 1)运行参数如表S2所示.反应过程中在预设时间点取沉淀池出水, 过0.22 μm水相滤膜后加入HNO3 (4%, V/V)酸化, 测定溶解态Ag、Fe离子浓度.反应结束后取反应区nZVI混合物真空干燥后称重, 经HNO3加热消解后使用电感耦合等离子发射光谱仪(ICP-OES)测定其中Ag的固含量.同时监控反应区内Eh的变化.
4.3 批次实验
本部分研究了材料种类、溶液浓度、初始pH及nZVI投加量对Ag+富集的影响.
研究不同材料的影响时, 向50 mL玻璃瓶中加入40 mL AgNO3溶液([Ag+]=100 mg/L, pH=5.0), 通入高纯氮气(>99.999%) 30 min后, 分别加入0.04 g固体材料, 放置于恒温摇床中(25 ℃, 200 r/min)反应4 h.分离系数K计算公式如式(4) 所示:
式中K (L/kg)代表分离系数, CAg, a (mg/L)和CAg, s (mg/kg)分别代表溶液中初始Ag+浓度以及富集后固相上Ag的含量.
研究溶液初始pH对nZVI、mZVI富集Ag+ (100 mg/L)的影响时, 使用HNO3 (0.1 mol/L)和NaOH (0.1 mol/L)将初始pH调节至3.0、4.0、5.0、6.0、7.0、8.0、9.0, 后续实验步骤同上.
研究溶液初始浓度对nZVI富集Ag+的影响时, 在一系列浓度梯度AgNO3溶液(初始pH=5.0) 中加入1.0 g/L nZVI, 其余步骤同上.
研究nZVI投加量对其富集Ag+的影响时, 在多口烧瓶中加入1000 mL AgNO3溶液([Ag+]=1000 mg/L, 初始pH=5.0), 通入高纯氮气30 min后, 分别投加0.10、0.25、0.50、1.00 g nZVI, 间隔一定时间取样测定混合液中剩余Ag+浓度.
本部分所有实验均重复三次, 图中显示数据为三次平行实验的算术平均值.
4.4 固相表征
nZVI与AgNO3反应后的固相产物分为两份.其中一份样品不做任何前处理, 即Ag-nZVI, 另一份样品使用PVP (4 g/L)和过量稀硫酸处理, 所用稀硫酸体积比20%, PVP浓度4 g/L, 恒温(60 ℃)水浴加热后离心, 取底部沉淀, 保存在4 g/L PVP中.采用HR-TEM、XRD、XPS分析相关材料形貌、物相及表面Ag的价态.
-
-
[1]
Yu, S. L.; Yin, Y. G.; Liu, J. F. Environ. Sci.-Proc. Imp. 2013, 15, 78.
-
[2]
Syed, S. Waste. Manage. 2016, 50, 234. doi: 10.1016/j.wasman.2016.02.006
-
[3]
World Silver Survey, 2017, GFMS Limited/The Silver Institute. http://www.silverinstitute.org
-
[4]
Benn, M. T.; Westerhoff, P. Environ. Sci. Technol. 2008, 42, 4133. doi: 10.1021/es7032718
-
[5]
Zhou, X. X.; Liu, J. F.; Yuan, C. G.; Chen, Y. S. J. Anal. Atom. Spectrom. 2016, 31, 2285. doi: 10.1039/C6JA00243A
-
[6]
Eckelman, M. J.; Graedel, T. E. Environ. Sci. Technol. 2007, 41, 6283. doi: 10.1021/es062970d
-
[7]
李冉, 卢艳莹, 雷凯翔, 李福军, 程方益, 陈军, 化学学报, 2017, 75, 199. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345762.shtmlLi, R.; Lu, Y. Y.; Lei, K. X.; Li, F. J.; Cheng, F. Y.; Chen, J. Acta Chim. Sinica 2017, 75, 199(in Chinese). http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345762.shtml
-
[8]
王超, 邓楠, 王玲玲, 许定健, 姚小泉, 有机化学, 2016, 36, 1034. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=yjhu201605015&dbname=CJFD&dbcode=CJFQWang, C.; Deng, N.; Wang, L. L.; Xu, D. J.; Yao, X. Q. Chinese J. Org. Chem. 2016, 36, 1034(in Chinese). http://kns.cnki.net/KCMS/detail/detail.aspx?filename=yjhu201605015&dbname=CJFD&dbcode=CJFQ
-
[9]
Vance, M. E.; Kuiken, T.; Vejerano, E. P.; McGinnis, S. P.; Hochella, M. F.; Rejeski, D.; Hull, M. S. Beilstein. J. Nanotech. 2015, 6, 1769. doi: 10.3762/bjnano.6.181
-
[10]
Song, X. H.; Gunawan, P.; Jiang, R. R.; Leong, S. S. J.; Wang, K.; Xu, R. J. Hazard. Mater. 2011, 194, 162. doi: 10.1016/j.jhazmat.2011.07.076
-
[11]
Zhou, Y. M.; Gao, B.; Zimmerman, R. A.; Cao, X. D. Chemosphere 2014, 117, 801. doi: 10.1016/j.chemosphere.2014.10.057
-
[12]
Celik. Z.; Gulfen. M.; Aydin, A. O. J. Hazard. Mater. 2010, 174, 556. doi: 10.1016/j.jhazmat.2009.09.087
-
[13]
Wang, H. Y.; Gao, H.; Sun, J. S.; Li, J.; Su, Y. X.; Ji, Y. L.; Gong, C. M. Desalination 2011, 270, 258. doi: 10.1016/j.desal.2010.11.053
-
[14]
Huo, H. Y.; Su, H. J.; Tan, T. W. Chem. Eng. J. 2009, 150, 139. doi: 10.1016/j.cej.2008.12.014
-
[15]
黄潇月, 王伟, 凌岚, 张伟贤, 化学学报, 2017, 75, 529. doi: 10.11862/CJIC.2017.063Huang, X. Y.; Wang, W.; Ling, L.; Zhang, W. X. Acta Chim. Sinica 2017, 75, 529(in Chinese). doi: 10.11862/CJIC.2017.063
-
[16]
Mu, Y.; Jia, F. L.; Ai, Z. H.; Zhang, L. Z. Environ. Sci.-Nano 2017, 4, 27. doi: 10.1039/C6EN00398B
-
[17]
Fu, F. L.; Dionysiou, D. D.; Liu, H. J. Hazard. Mater. 2014, 267, 194. doi: 10.1016/j.jhazmat.2013.12.062
-
[18]
Zhang, Y. L.; Yan, J.; Dai, C. M.; Li, Y. T.; Zhou, Y.; Zhou, X. F. J. Nanopart. Res. 2015, 17, 1110.
-
[19]
Teng, W.; Fan, J. W.; Wang, W.; Bai, N.; Liu, R.; Liu, Y.; Deng, Y. H.; Kong, B.; Yang, J. P.; Zhao, D. Y.; Zhang, W. X. J. Mater. Chem. A 2017, 5, 4478. doi: 10.1039/C6TA10007D
-
[20]
Ling, L.; Zhang, W. X. J. Am. Chem. Soc. 2015, 137, 2788. doi: 10.1021/ja510488r
-
[21]
Sheng, G. D.; Yang, P. J.; Tang, Y. N.; Hu, Q. Y.; Li, H.; Ren, X. M.; Hu, B. W.; Wang, X. K.; Huang, Y. Y. Appl. Catal. B-Environ. 2016, 193, 189. doi: 10.1016/j.apcatb.2016.04.035
-
[22]
夏雪芬, 滑熠龙, 黄潇月, 凌岚, 张伟贤, 化学学报, 2017, 75, 594. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract346105.shtmlXia, X. F.; Hua, Y. L.; Huang, X. Y.; Ling, L.; Zhang, W. X. Acta Chim. Sinica 2017, 75, 594(in Chinese). http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract346105.shtml
-
[23]
Sheng, G. D.; Alsaedi, A.; Shammakh, W.; Monaquel, S.; Sheng, J.; Wang, X. K.; Li, H.; Huang, Y. Y. Appl. Carbon. 2016, 99, 123. doi: 10.1016/j.carbon.2015.12.013
-
[24]
Li, S. L.; Wang, W.; Liu, Y. Y.; Zhang, W. X. Chem. Eng. J. 2014, 254, 115. doi: 10.1016/j.cej.2014.05.111
-
[25]
Wang, W.; Hua, Y. L.; Li, S. L.; Yan, W. L.; Zhang, W. X. Chem. Eng. J. 2016, 304, 79. doi: 10.1016/j.cej.2016.06.069
-
[26]
Li, S. L.; Wang, W.; Liang, F. P.; Zhang, W. X. J. Hazard. Mater. 2017, 322, 163. doi: 10.1016/j.jhazmat.2016.01.032
-
[27]
Wang, W.; Li, S. L.; Lei, H.; Pan, B. C.; Zhang, W. X. Chem. Eng. J. 2015, 260, 616. doi: 10.1016/j.cej.2014.09.042
-
[28]
Shi, Z. Q.; Nurmi, T. J.; Tratnyek, G. P. Environ. Sci. Technol. 2011, 45, 1586. doi: 10.1021/es103185t
-
[29]
Sverdrup, H.; Koca, D.; Ragnarsdottir, V. K. Resour. Conserv. Recy. 2014, 83, 121. doi: 10.1016/j.resconrec.2013.12.008
-
[30]
Liang, L. P.; Yang, W. J.; Guan, X. H.; Li, J. L.; Xu, Z. J.; Wu, J.; Huang, Y. Y.; Zhang, X. Z. Water Res. 2013, 47, 5846. doi: 10.1016/j.watres.2013.07.011
-
[31]
Guan, X. H.; Sun, Y. K.; Qin, H. J.; Li, J. X.; Lo, I. M. C.; He, D.; Dong, H. R. Water Res. 2015, 75, 224. doi: 10.1016/j.watres.2015.02.034
-
[32]
Liang, L. P.; Sun, W.; Guan, X. H.; Huang, Y. Y.; Choi, W. Y.; Bao, H. L.; Li, L. N.; Jiang, Z. Water Res. 2014, 49, 371. doi: 10.1016/j.watres.2013.10.026
-
[33]
Nitayaphat, W.; Jintakosol, T. J. Clean. Prod. 2015, 87, 850. doi: 10.1016/j.jclepro.2014.10.003
-
[34]
Wang, Y.; Ma, X. J.; Li, Y. F.; Li, X. L.; Yang, L. Q.; Ji, L.; He, Y. Chem. Eng. J. 2012, 209, 394. doi: 10.1016/j.cej.2012.07.143
-
[35]
Ju, S. H.; Zhang, Y. F.; Zhang, Y.; Xue, P. Y.; Wang, Y. H. J. Hazard. Mater. 2011, 192, 554. doi: 10.1016/j.jhazmat.2011.05.049
-
[36]
Yin, Y. G.; Shen, M. H.; Tan, Z. Q.; Yu, S. J.; Liu, J. F.; Jiang, G. B. Environ. Sci. Technol. 2015, 49, 6581. doi: 10.1021/es5061287
-
[1]
-
图 2 不同水力停留时间条件下Ag+富集情况、出水中Na+浓度变化及反应区Eh变化: (A) HRT=10 min; (B) HRT=30 min; (C) HRT=60 min; (D)平均富集率; (E)反应产物银含量
Figure 2 Effluent concentrations of Ag+ and Na+, and variation of Eh as a function of reaction time under different: (A) HRT=10 min; (B) HRT=30 min; (C) HRT=60 min; (D) average silver enrichment ratio; (E) silver content in final products
Reaction conditions: nZVI dosage=0.5 g, [Ag+]in=1.0 mg/L, initial pH=7.0, 25 ℃
图 3 Eh稳态调控实验结果: (A)反应区Eh变化; (B)出水Ag+浓度变化; (C)反应区Eh和出水Ag+浓度的相关性
Figure 3 Results of Eh regulating experiments: (A) changes of Eh in reaction zone; (B) Ag+ concentration in effluent; (C) relationship between Eh and Ag+ concentration in effluent
Reaction conditions: HRT=10 min, [Ag+]in=1.0 mg/L, initial pH=7.0, 25 ℃
图 4 不同材料对Ag+富集效果: (A)总体富集率; (B)分离系数; 插图为富集前后Ag在水相和固相上含量变化
Figure 4 Enrichment performances of Ag+ by different materials: (A) total enrichment ratio; (B) separation coefficient; Inset: Ag content in liquid and solid phase
Reaction conditions: material dosage=1.0 g/L, [Ag+]0=100 mg/L, initial pH=5.0, rotating speed=200 r/min, reaction time=4 h, 25 ℃
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 12
- 文章访问数: 2755
- HTML全文浏览量: 465


 下载:
下载:







 下载:
下载:

