 图 1
样品的XRD图
Figure 1.
XRD patterns of these samples
图 1
样品的XRD图
Figure 1.
XRD patterns of these samples

Citation: Zheng Zhuo, Wu Zhenguo, Xiang Wei, Guo Xiaodong. Preparation and Electrochemical Performance of High Rate Spherical Layered LiNi0.5Co0.2Mn0.3O2 Cathode Material for Lithium-Ion Batteries[J]. Acta Chimica Sinica, 2017, 75(5): 501-507. doi: 10.6023/A16110594

高倍率球形锂离子电池正极材料LiNi0.5Co0.2Mn0.3O2的制备及其电化学性能研究
-
关键词:
- 锂离子电池
- / 正极材料
- / 碳酸盐共沉淀法
- / LiNi0.5Co0.2Mn0.3O2
- / 高倍率性能
English
Preparation and Electrochemical Performance of High Rate Spherical Layered LiNi0.5Co0.2Mn0.3O2 Cathode Material for Lithium-Ion Batteries
-
1 引言
当前, 锂离子电池作为最具前景的新能源材料被广泛应用于手提电子设备、大型储能设备、电动汽车和混合动力汽车[1~6].为了满足人们日益增长的对高能量需求, 制备性能优异的锂离子电池正极材料尤为重要, 因为它是限制锂离子电池进一步发展的技术瓶颈.在这些正极材料中, 层状三元高镍正极材料Li[Ni1-xMx]O2因为其低毒性、低成本和高比容量引起了人们广泛的关注[7~10].然而, 这类材料也存在着一些亟需解决的问题, 比如在电化学循环过程中晶格内的氧原子会逐渐脱离主体结构形成高度脱锂状态的Li1-δ[Ni1-xMx]O2, 导致热稳定性较差.与此同时, 因为Ni4+十分活泼不稳定会促使Li1-δ[Ni1-xMx]O2结构进一步转变为NaCl型结构的LixNi1-xO, 最终使得电池的循环稳定性和倍率性能较差[11~13].
研究表明合成方法是影响材料电化学性能优劣的主要原因之一, 因为合成方法会极大地影响材料的纯度、晶体结构、颗粒形貌以及晶体内部的原子混排[14, 15].通常制备三元高镍正极氧化物LiNi0.5Co0.2Mn0.3O2的方法有固相合成法[16]、溶胶-凝胶法[17]、喷雾干燥法[18]、水热法[19]和共沉淀法[20]等. Li等[16]以过渡金属氧化物(Co3O4, NiO2和MnO2)和锂盐(Li2CO3)为原料, 采用固相合成法制备了LiNi0.5Co0.2Mn0.3O2材料, 其在2.75~4.25 V, 0.2C的放电比容量为151 mAh•g-1, 循环50次后容量保持率为93%. Kong等[17]采用溶胶-凝胶法制备得到了大孔结构的LiNi0.5Co0.2Mn0.3O2材料, 其在2.5~4.3 V, 50 mA•g-1的首次放电比容量为167.9 mAh•g-1, 在1000 mA•g-1的最大放电比容量为138.2 mAh•g-1. Xie等[18]采用喷雾干燥法合成了类球形结构的LiNi0.5-Co0.2Mn0.3O2材料, 其在2.7~4.3 V, 0.1C倍率下的首次放电比容量为163 mAh•g-1, 循环50次后的容量保持率为92.6%. Li等[19]采用水热法制备得到了球形度良好的LiNi0.5Co0.2Mn0.3O2材料, 其在3.0~4.3 V, 0.1C时的首次放电比容量为169.6 mAh•g-1, 在4C时的放电比容量在120 mAh•g-1左右.在这些合成方法中, 固相合成法由于固相原料需要长时间的研磨混合, 且混合均匀程度有限, 无法实现Ni, Co, Mn在原子级别的均匀接触, 因此, 材料在组成、结构及粒度分布方面存在较大差别, 电化学性能不理想.而溶胶-凝胶法、喷雾干燥法和水热法均存在工艺复杂、成本高等问题, 且制得材料的振实密度往往较低(能量密度较低), 对电化学性能的提升有限, 不利于工业化应用, 所以目前合成高镍LiNi0.5Co0.2Mn0.3O2材料的主要方法为共沉淀法, 其工艺能实现过渡金属元素在原子水平的均匀混合, 且制得材料的晶体结构完整、各成份元素分布均匀.相比于氢氧化物共沉淀法[20], 碳酸盐共沉淀法的合成条件更加简单易行, 不需要在沉淀过程中为了防止Mn(OH)2氧化进行惰性气体保护或添加还原剂, 故本工作选择碳酸盐共沉淀法来制备高镍LiNi0.5Co0.2Mn0.3O2材料.研究结果表明, 我们制得的LiNi0.5Co0.2Mn0.3O2材料晶体结构完善, 具有良好的球形形貌, 颗粒度分布均匀, 电化学性能优异, 尤其是具有超高倍率性能(30C, 96 mAh•g-1).同时该材料的振实密度较高(2.1 g•cm-3), 具有良好的储能能力(0.1C的比能量密度为687.83 Wh•kg-1, 体积能量密度为1444.45 Wh•L-1), 有用于制作商业化高能量密度锂离子电池的潜力.
2 结果与讨论
2.1 材料结构与形貌分析
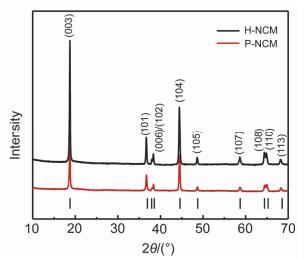
图 1为样品的XRD图.由图可发现, 两样品均具有典型的六方层状α-NaFeO2结构, R3m空间群[21, 22], 没有其他杂峰的存在.用Jada6.0软件对两样品进行精修计算, 精修后的晶胞参数值列于表 1. H-NCM和P-NCM两样品I(003)/I(104)的值分别为1.7071和1.4839, 表明H-NCM样品锂层中具有更低的Li+/Ni2+阳离子混排[21, 22].这种结构混排是造成电化学性能不佳的主要原因之一, 因为Ni2+进入Li层会降低总的充放电比容量和Li+的离子导电率. c/a值反映主体结构的三角扭曲程度, 其值越大, 则对应材料的层状六方晶体结构越完整[21~23].因此, H-NCM (c/a=4.9964) 样品比P-NCM (c/a=4.9732) 样品具有更加有序的α-NaFeO2结构.基于XRD的分析, 可以合理地推断H-NCM的电化学性能将优于P-NCM.
Sample a/Å c/Å c/a I(003)/I(104) H-NCM 2.8534 14.2571 4.9964 1.7071 P-NCM 2.8626 14.2365 4.9732 1.4839 表 1 样品的XRD精修结果
Table 1. Refined lattice parameters of these samples图 2a, 2b为P-NCM样品的SEM图, 由图可发现样品是由平均一次颗粒径在400 nm左右的小颗粒无规则团聚而成. H-NCM样品的二次颗粒为球形(图 2c~2e), 且均为单分散颗粒, 每个二次颗粒都是由类球形或多面体一次粒子致密团聚而成. 图 2f为H-NCM样品的颗粒度分布图, 其颗粒粒度均匀, 粒度分布范围较窄, 中位粒径D50为4.84 μm.对样品的振实密度进行测试, 测试结果表明H-NCM样品的振实密度较高, 为2.1 g•cm-3左右, 而P-NCM样品的振实密度仅为1.5 g•cm-3.
图 3a为P-NCM样品的TEM图, 图中测量的晶面间距为0.47 nm, 与层状LiMO2 (M=Ni, Co, Mn)结构的(003) 晶面间距相对应[24]. 图 3b为其相应的选区电子衍射(SAED)图, 其对应的衍射斑点为[121]晶带轴的情况, 且由衍射斑点图可知P-NCM样品为单晶结构, 内部原子排布为O3结构的层状相[25, 26]. 图 3c为H-NCM样品的TEM图, 可测出晶格条纹间距为0.47 nm, 与层状结构的(003) 晶面间距相一致, 其SAED图(图 3d)为[0001]晶带轴的衍射情况, 包含两套衍射斑:一种是由六个明亮的斑点组成的六边形, 另一种是夹杂在两个明亮斑点中间的两个暗斑点.由以前的文献报道可知, 这是属于过渡金属层原子的[
$\sqrt 3 \times \sqrt 3 $ ]R30°排列, 这种排列方式具有稳定的晶体结构和最低的形成能量[25~27].2.2 电化学性能测试
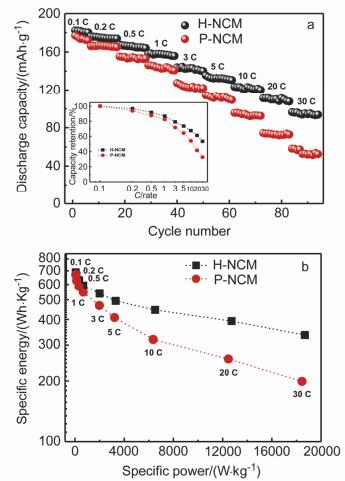
图 4a为样品在2.7~4.3 V下的倍率循环性能图. H-NCM样品的倍率循环性能和放电比容量都相对于P-NCM样品有了较大提升.在0.1~30 C时, 其放电比容量分别为182, 176, 167, 158, 144, 135, 123, 111和96 mAh•g-1, 相比于NCM样品的放电比容量177, 166, 155, 146, 127, 114, 95, 74和58 mAh•g-1有较大的提高.内嵌图为两样品在不同倍率下的容量保持率, 可看出随着电流密度的增加, H-NCM样品优异的高倍率性能优势逐渐显现, 在高倍率放电时还能保持较高的容量保持率. H-NCM样品在0.2C, 0.5C, 1C, 3C, 5C, 10C, 20C和30C相对于0.1C的容量保持率分别为96.7% 91.7%, 86.8%, 79.2%, 73.6%, 67.6%, 61.2%和53.4%. H-NCM样品倍率性能显著提升的原因可归结于以下两方面: (1) 完善的α-NaFeO2层状结构和较低的Li+/Ni2+混排, 这种稳定的晶体结构相比于易坍塌的结构更加易于在高倍率下锂离子的快速脱嵌; (2) 微纳球形结构, 可提供更多Li+活性位点, 起到纳米反应器作用, 缓冲体积变化产生的机械应力, 保持纳米晶体结构单元的稳定性. 图 4b为样品的Ragone图, 比能量密度(Es)和功率密度(Ps)可由下式进行计算[28, 29]: Es=QV=∫Q(V)dV, Ps=IV=I∫dV, 其中Q, V和I分别代表比容量(mAh•g-1)、电压(V)和电流密度(mA•g-1).可发现随着电流密度的增加, 两样品的能量密度差值逐渐增大, P-NCM样品在0.1C时的比能量密度为670.14 Wh•kg-1(体积能量密度为1005.21 Wh•L-1), 在30C时仅为199.18 Wh•kg-1 (体积能量密度为298.77 Wh•L-1); 而H-NCM样品在0.1C时比能量密度为687.83 Wh•kg-1(体积能量密度为1444.45 Wh•L-1), 在30C时仍为335.27 Wh•kg-1(体积能量密度为: 704.07 Wh•L-1), 显示出该电极材料在高功率密度工作时仍能保持较高的能量密度.
图 5为H-NCM样品经倍率性能(30C)测试后的SEM图.由图可发现, 经过高倍率电化学性能测试后, 该材料的二次颗粒形貌基本还能保持较好的球形度, 说明材料的结构稳定, 对电化学性能有利.
图 6a和6b分别为P-NCM和H-NCM样品的循环性能测试.在2.7~4.3 V, 1C下循环100次后, H-NCM样品表现出优异的循环稳定性能, 其在1C的首次放电容量为159 mAh•g-1, 循环100次后容量仍为150 mAh• g-1; P-NCM样品在循环100次后的放电比容量为128 mAh•g-1, 容量保持率为87.4%.图中的内嵌图为两样品在首次和第100次的dQ/dV曲线.从首次dQ/dV曲线可发现, 样品在充(放)电时氧化峰(还原峰)电位约3.75 V (3.72 V), 对应着Li+在晶格中的脱嵌过程, 发生Ni2+/ Ni4+的氧化还原反应.在循环100次后, 两样品的dQ/dV曲线中氧化峰向高电位方向移动, 还原峰向低电位方向移动, 这种现象为电池的极化, 是由于电池的内阻在电化学循环过程中逐渐增大所引起[30].通过对比两样品氧化峰和还原峰移动的电位差可发现, H-NCM样品的极化程度相对较低, 具有优异的电化学可逆性, 同时这个现象也可以很好地解释为什么H-NCM样品的循环稳定性更好. 图 6c和6d分别为这两种材料在不同循环次数下的充放电曲线图, 随着倍率的增加, 放电曲线变短, 电压平台逐渐降低, H-NCM样品的放电电压平台衰减较小, 说明该电极材料的极化现象相对来说不严重, 材料晶体结构更加稳定.
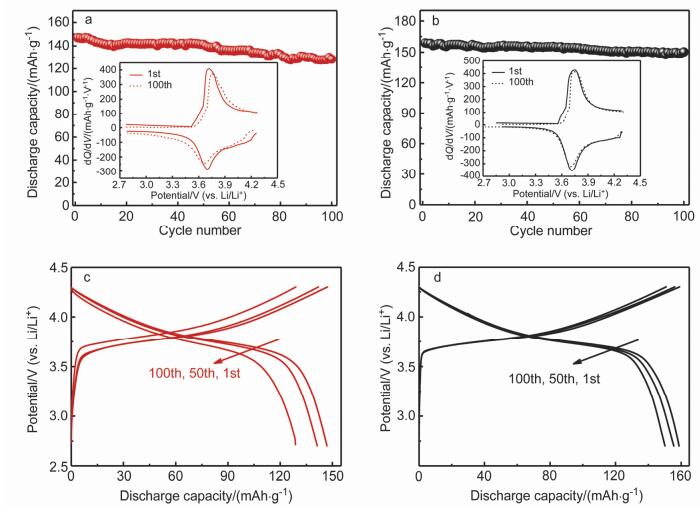 图 6
样品(a) P-NCM, (b) H-NCM在2.7~4.3 V, 1C下的循环稳定性以及不同循环次数下的dQ/dV图及(c) P-NCM, (d) H-NCM不同循环次数下的充放电曲线图
Figure 6.
Cycling stability and the dQ/dV plots of different cycles of these samples at 1C between 2.7 and 4.3 V of (a) P-NCM, (b) H-NCM and charge/discharge curves at different cycles of (c) P-NCM, (d) H-NCM
图 6
样品(a) P-NCM, (b) H-NCM在2.7~4.3 V, 1C下的循环稳定性以及不同循环次数下的dQ/dV图及(c) P-NCM, (d) H-NCM不同循环次数下的充放电曲线图
Figure 6.
Cycling stability and the dQ/dV plots of different cycles of these samples at 1C between 2.7 and 4.3 V of (a) P-NCM, (b) H-NCM and charge/discharge curves at different cycles of (c) P-NCM, (d) H-NCM
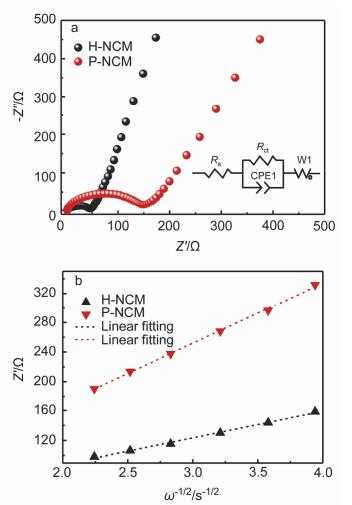
为了更深层次研究这两个材料电化学性能差异的原因, 进行了电化学阻抗图谱(EIS)测试, 两样品的Nyquist曲线和经Zview软件拟合的等效电路图(内嵌图)如图 7a所示.样品的阻抗谱都是由高频区的一个半圆和低频区的一条斜线组成.高频区的半圆和Z'轴的截距表示电池的固有阻抗(Rs), 包括颗粒间的接触电阻、电解液电阻以及其他物理阻抗.半圆代表电极-电解液界面位置的电荷转移阻抗(Rct).低频区的斜线为Warburg阻抗(W1), 表示Li+在固相材料中的扩散阻力[31, 32].样品的等效电路图拟合结果列于表 2.可发现两样品的Rs值基本一致, 但Rct值呈现出较大差异, H-NCM样品为48.6 Ω, P-NCM样品为149.3 Ω, 说明H-NCM样品具有更好的Li+传导能力.同时, 为了更直观地比较两样品的Li+传输能力, 采用如下公式对两样品的锂离子扩散系数(DLi+)进行了拟合计算[33, 34]:
 表 2
样品的等效电路图拟合结果以及相应的DLi+值
Table 2.
Fitting results of equivalent circuit from Nyquist curves for the samples
表 2
样品的等效电路图拟合结果以及相应的DLi+值
Table 2.
Fitting results of equivalent circuit from Nyquist curves for the samples
Sample Rs/Ω Rct/Ω DLi+/(cm2•s-1) H-NCM 2.7 48.6 3.8×10-11 P-NCM 2.6 149.3 2.3×10-12 表 2 样品的等效电路图拟合结果以及相应的DLi+值
Table 2. Fitting results of equivalent circuit from Nyquist curves for the samples式中R为气体常数, T为绝对温度; Rct为界面转移阻抗; A为电极面积, n为每摩尔的电子转移量(对于Li+为1), F为法拉第常数, C为Li+在电极中的摩尔浓度, σ为Warburg系数.样品的Warburg系数(σ)通过Eq. 2以及图 7b的dZ'/dω-1/2斜率计算拟合得到.经Eq. 1计算得到H-NCM和P-NCM样品的DLi+分别为3.8×10-11和2.3×10-12 cm2•s-1, 说明样品H-NCM可在离子传输过程中提供更多的Li+参与到电极反应中, 所以其倍率性能优异, 而P-NCM样品因为其DLi+较低, 故而在高倍率下放电比容量衰减较快.
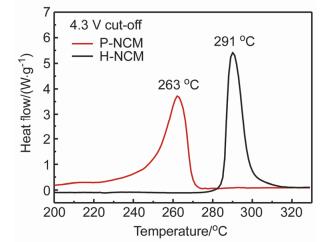
为了研究两材料的热稳定性, 对在4.3 V充电后的两电极材料进行差示扫描量热仪(DSC)测试, 测试结果如图 8所示.图中两材料都可观察到明显的放热峰, 对应着电极材料与电解液之间的放热反应以及电极材料中的氧原子从晶格中的脱出[35]. P-NCM材料的放热峰在263 ℃附近, 放热量为622.4 J•g-1; 而H-NCM材料的放热峰在291 ℃, 放热量为518.4 J•g-1.无论是从发生放热反应的温度, 还是放热量的多少, 都显示出H-NCM的热稳定性要优于P-NCM.
3 结论
采用碳酸盐共沉淀-高温固相法合成了微球形LiNi0.5Co0.2Mn0.3O2材料, 对其颗粒形貌、晶体结构和电化学性能进行了系统研究. XRD和TEM的结果表明这种球状LiNi0.5Co0.2Mn0.3O2材料具有完善的层状α-NaFeO2结构, 过渡金属层原子呈[
$ \sqrt 3 \times \sqrt 3 $ ]R30°排布.电化学测试结果证实该材料的电化学性能优异, 在2.7~4.3 V, 1C下循环100次后的容量保持率为94.6%, 在30C的高倍率下, 其放电比容量仍为96 mAh•g-1.同时, 该材料的振实密度较高(2.1 g•cm-3), 在0.1C时比能量密度为687.83 Wh•kg-1(体积能量密度为1444.45 Wh•L-1), 在30C时仍为335.27 Wh•kg-1(体积能量密度为704.07 Wh•L-1), 有用于制作商业化高能量密度锂离子电池的潜力. EIS测试结果也证明了该材料具有较高的锂离子扩散系数(3.8×10-11 cm2•s-1), 可以在离子传输过程中提供更多的Li+参与到电极反应中.该材料制备方法工艺简单、效率高、在高倍率下具有较好的电化学性能, 有利于实现工业化生产的可能, 而且可为今后制备高能量密度型的锂离子电池正极材料提供参考.4 实验部分
4.1 材料合成
将NiSO4•6H2O, CoSO4•7H2O及MnSO4•H2O按物质的量之比5:2:3配成2 mol•L-1的混合溶液, Na2CO3和NH3•H2O分别配制成2和4 mol•L-1的溶液.然后将配好的三种溶液分别缓慢滴加到反应釜中, 反应温度控制在50 ℃, 反应pH=8.0, 反应搅拌速度为1500 r/min.待反应沉淀完全之后, 在60 ℃下陈化12 h, 然后抽滤洗涤除去多余的SO42-和Na+, 再在100 ℃下干燥12 h得到Ni0.5Co0.2Mn0.3CO3前驱体粉末.最后前驱体粉体与化学计量比的Li2CO3固相混合(Li2CO3过量5%), 在氧气气氛下550 ℃预烧6 h, 再在850 ℃煅烧14 h制得微球形LiNi0.5Co0.2Mn0.3O2正极材料(命名为H-NCM).
作为对比, 还制备了亚微米尺寸的LiNi0.5Co0.2-Mn0.3O2样品(命名为P-NCM).将化学计量比的LiNO3, Ni(NO3)2•6H2O, Co(NO3)2•6H2O和Mn(CH3COO)2•4H2O溶于去离子水中配成1 mol•L-1的混合溶液, 并与NH4HCO3和NH3•H2O的混合溶液(2 mol•L-1)一起加入到反应釜中, 反应温度控制在50 ℃, 反应pH=8.0, 反应搅拌速度为1500 r/min.待反应沉淀完全之后, 在60 ℃下陈化12 h, 再在真空100 ℃下干燥一晚上, 然后将干燥粉体在氧气气氛下550 ℃预烧6 h, 再在850 ℃下煅烧14 h得到最终材料成品.
4.2 材料表征
X射线衍射(XRD)用于分析样品的晶体结构, 仪器为菲利普公司的PW1730多晶转靶X射线仪(Cu Kα靶, λ=1.5418 Å), 扫描角度范围为10°~70°.样品的形貌和颗粒尺寸用日本日立(Hitachi) S-4800扫描电子显微镜(SEM)进行表征和分析.样品的微观结构使用日本电子JEM-2100高分辨透射电镜(TEM)进行表征和分析.采用英国马尔文公司的MS2000激光粒度分析仪测试样品的颗粒度分布情况.采用深圳三诺电子仪器有限公司生产的型号为JZ-1的振实密度仪测定样品的振实密度.采用德国耐驰公司的差示扫描量热仪(DSC 204F1) 分析电极材料与电解液之间的热稳定性, 测量温度范围为200~330 ℃, 升温速率为1 ℃/min.
4.3 材料的电化学性能测试
活性物质、乙炔黑、粘结剂(PVDF)按照质量比为80:13:7混合, 并加入适量的N-甲基吡咯烷酮调配成糊状.将这些湿浆料均匀涂覆在集流体铝箔上, 再在真空下100 ℃干燥10 h, 然后将干燥好的铝箔切成直径为14 mm的圆片, 并在20 MPa下压实得到电池的正极片, 每个极片上的活性物质质量在3~4 mg•cm-2.最后在充满氩气气氛的手套箱中将正极片、锂片(负极)、隔膜(Celgard 2400) 和电解液组装成CR2032扣式电池.电解液为1 mol•L-1的LiPF6与碳酸乙烯酯(EC)和碳酸二甲酯(DMC)(体积比为1:1).本工作在室温下进行充放电性能测试, 充放电电压为2.7~4.3 V, 1C=180 mA•g-1.采用德国Zennium IM6电化学工作站对电池的电化学阻抗谱(EIS)进行测试, 测试频率范围在100 kHz~10 mHz, 扰动电压为5 mV, 得到的数据用Zview 2软件进行电化学元件模型数值拟合分析.
-
-
[1]
Tarascon, J. M.; Armand, M. Nature 2001, 414, 359. doi: 10.1038/35104644
-
[2]
Dunn, B.; Kamath, H.; Tarascon, J. M. Sience 2011, 334, 928. doi: 10.1126/science.1212741
-
[3]
Mahmood, N.; Zhang, C. Z.; Yin, H.; Hou, Y. L. J. Mater. Chem. A 2014, 2, 15. doi: 10.1039/C3TA13033A
-
[4]
Yu, X. Q.; Lyu, Y. C.; Gu, L.; Wu, H. M.; Bak, S. M.; Zhou, Y. N.; Amine, K.; Ehrlich, S. N.; Li, H.; Nam, K. W.; Yang, X. Q. Adv. Energy Mater. 2014, 4, 1300950. doi: 10.1002/aenm.201300950
-
[5]
吕之阳, 冯瑞, 赵进, 范豪, 徐丹, 吴强, 杨立军, 陈强, 王喜章, 胡征, 化学学报, 2015, 73, 1013. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345154.shtmlLv, Z. Y.; Feng, R.; Zhao, J.; Fan, H.; Xu, D.; Wu, Q.; Yang, L. J.; Chen, Q.; Wang, X. Z.; Hu, Z. Acta Chim. Sinica 2015, 73, 1013. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345154.shtml
-
[6]
邱振平, 张英杰, 夏书标, 董鹏, 化学学报, 2015, 73, 992. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htmQiu, Z. P.; Zhang, Y. J.; Xia, S. B.; Dong, P. Acta Chim. Sinica 2015, 73, 992. http://www.cnki.com.cn/Article/CJFDTOTAL-SYQY201603027.htm
-
[7]
Bi, Y.; Yang, W.; Du, R.; Zhou, J.; Liu, M.; Liu, Y.; Wang, D. J. Power Sources 2015, 283, 211. doi: 10.1016/j.jpowsour.2015.02.095
-
[8]
Kim, Y. ACS Appl. Mater. Interfaces 2012, 4, 2329. doi: 10.1021/am300386j
-
[9]
林和成, 杨勇, 化学学报, 2009, 67, 104. doi: 10.3321/j.issn:1001-4861.2009.01.019Lin, H. C.; Yang, Y. Acta Chim. Sinica 2009, 67, 104. doi: 10.3321/j.issn:1001-4861.2009.01.019
-
[10]
Sun, Y. K.; Myung, S. T.; Park, B. C.; Prakash, J.; Belharouak, I.; Amine, K. Nat. Mater. 2009, 8, 320. doi: 10.1038/nmat2418
-
[11]
Cho, J.; Jung, H.; Park, Y.; Kim, G.; Lim, H. S. J. Electrochem. Soc. 2000, 147, 15. doi: 10.1149/1.1393137
-
[12]
Abraham, D. P.; Twesten, R. D.; Balasubramanian, M.; Petrov, I.; McBreen, J.; Amine, K. Electrochem. Commun. 2002, 4, 620. doi: 10.1016/S1388-2481(02)00388-0
-
[13]
Woo, S. U.; Yoon, C. S.; Amine, K.; Belharouak, I.; Sun, Y. K. J. Electrochem. Soc. 2007, 154, A1005. doi: 10.1149/1.2776160
-
[14]
Lin, B.; Wen, Z.; Gu, Z.; Huang, S. J. Power Sources 2008, 175, 564. doi: 10.1016/j.jpowsour.2007.09.055
-
[15]
Whitfield, P. S.; Davidson, I. J.; Cranswick, L. M. D.; Swainson, I. P.; Stephens, P. W. Solid State Ionics 2005, 176, 463. doi: 10.1016/j.ssi.2004.07.066
-
[16]
李伟伟, 李丽, 杨理, 有色金属(冶炼部分), 2014, 7, 53. doi: 10.3969/j.issn.1007-7545.2014.07.016Li, W. W.; Li, L.; Yang, L. Nonferrous Met. 2014, 7, 53. doi: 10.3969/j.issn.1007-7545.2014.07.016
-
[17]
Kong, J. Z.; Zhai, H. F.; Ren, C.; Gao, M. Y.; Zhang, X.; Li, H.; Li, J. X.; Tang, Z.; Zhou, F. J. Alloys Compd. 2013, 577, 507. doi: 10.1016/j.jallcom.2013.07.007
-
[18]
Xie, L. S.; Lin, Q. Q.; Li, H. C.; Wang, Z. G.; Wang, C. F.; Hu, M. C.; Huang, R. H. Mater. Sci. 2017, 7, 72.
-
[19]
Li, Y. J.; Han, Q.; Ming, X. Q.; Ren, M. M.; Li, L.; Ye, W. Q.; Zhang, X. Z.; Xu, H.; Li, L. Ceram. Int. 2014, 40, 14933. doi: 10.1016/j.ceramint.2014.06.090
-
[20]
Yang, Z. G.; Guo, X. D.; Xiang, W.; Hua, W. B.; Zhang, J.; He, F. R.; Wang, K.; Xiao, Y.; Zhong, B. H. J. Alloys Compd. 2017, 699, 358. doi: 10.1016/j.jallcom.2016.11.245
-
[21]
Zhang, J. B.; Zhong, Y. J.; Shi, X. X.; Zheng, Z.; Hua, W. B.; Chen, Y. X.; Liu, W. Y.; Zhong, B. H. Chin. J. Chem. 2015, 33, 1303. doi: 10.1002/cjoc.v33.11
-
[22]
Hua, W. B.; Wang, Y. J.; Zhong, Y. J.; Wang, G. P.; Zhong, B. H.; Fang, B. Z.; Guo, X. D.; Liao, S. X.; Wang, H. J. Chin. J. Chem. 2015, 33, 261. doi: 10.1002/cjoc.v33.2
-
[23]
Ahn, W.; Lim, S. N.; Jung, K. N.; Yeon, S. H.; Kim, K. B.; Song, H. S.; Shin, K. H. J. Alloys Compd. 2014, 609, 143. doi: 10.1016/j.jallcom.2014.03.123
-
[24]
Li, J.; Xiong, S.; Liu, Y.; Ju, Z.; Qian, Y. Nano Energy 2013, 2, 1249. doi: 10.1016/j.nanoen.2013.06.003
-
[25]
Yabuuchi, N.; Koyama, Y.; Nakayama, N.; Ohzuku, T. J. Electrochem. Soc. 2005, 152, A1434. doi: 10.1149/1.1924227
-
[26]
Gabrisch, H.; Yi, T.; Yazami, R. Electrochem. Solid-State Lett. 2008, 11, A119. doi: 10.1149/1.2919713
-
[27]
Koyama, Y.; Tanaka, I.; Adachi, H.; Makimura, Y.; Ohzuku, T. J. Power Sources 2003, 119~121, 644.
-
[28]
Zhu, Z.; Yan, H.; Zhang, D.; Li, W.; Lu, Q. J. Power Sources 2013, 224, 13. doi: 10.1016/j.jpowsour.2012.09.043
-
[29]
Shaju, K. M.; Bruce, P. G. Adv. Mater. 2006, 18, 2330. doi: 10.1002/(ISSN)1521-4095
-
[30]
Wu, F.; Li, N.; Su, Y. F.; Shou, H. F.; Bao, L. Y.; Yang, W.; Zhang, L. J.; An, R.; Chen, S. Adv. Mater. 2013, 25, 3722. doi: 10.1002/adma.v25.27
-
[31]
Striebel, K. A.; Sakai, E.; Cairns, E. J. J. Electrochem. Soc. 2002, 149, A61. doi: 10.1149/1.1427075
-
[32]
Wang, L.; Zhao, J.; He, X.; Gao, J.; Li, J.; Wan, C.; Jiang, C. Int. J. Electrochem. Sci. 2012, 7, 345.
-
[33]
Mai, L.; Li, S.; Dong, Y.; Zhao, Y.; Luo, Y.; Xu, H. Nanoscale 2013, 5, 4864. doi: 10.1039/c3nr01490h
-
[34]
Li, B.; Han, C.; He, Y. B.; Yang, C.; Du, H.; Yang, Q. H.; Kang, F. Energy Environ. Sci. 2012, 5, 9595. doi: 10.1039/c2ee22591c
-
[35]
Zhou, P. F.; Meng, H. J.; Zhang, Z.; Chen, C. C.; Lu, Y. Y.; Cao, J.; Cheng, F. Y.; Chen, J. J. Mater. Chem. A 2017, 5, 2724. doi: 10.1039/C6TA09921A
-
[1]
-
图 6 样品(a) P-NCM, (b) H-NCM在2.7~4.3 V, 1C下的循环稳定性以及不同循环次数下的dQ/dV图及(c) P-NCM, (d) H-NCM不同循环次数下的充放电曲线图
Figure 6 Cycling stability and the dQ/dV plots of different cycles of these samples at 1C between 2.7 and 4.3 V of (a) P-NCM, (b) H-NCM and charge/discharge curves at different cycles of (c) P-NCM, (d) H-NCM
表 1 样品的XRD精修结果
Table 1. Refined lattice parameters of these samples
Sample a/Å c/Å c/a I(003)/I(104) H-NCM 2.8534 14.2571 4.9964 1.7071 P-NCM 2.8626 14.2365 4.9732 1.4839 表 2 样品的等效电路图拟合结果以及相应的DLi+值
Table 2. Fitting results of equivalent circuit from Nyquist curves for the samples
Sample Rs/Ω Rct/Ω DLi+/(cm2•s-1) H-NCM 2.7 48.6 3.8×10-11 P-NCM 2.6 149.3 2.3×10-12 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 1
- 文章访问数: 1428
- HTML全文浏览量: 167





 下载:
下载:







 下载:
下载:

