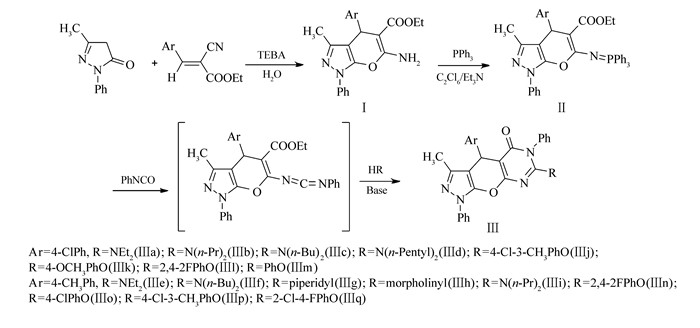
 Scheme1.
Synthesis route of pyrazolopyranopyrimidin-4(3H)-one(Ⅲ)
Scheme1.
Synthesis route of pyrazolopyranopyrimidin-4(3H)-one(Ⅲ)

Citation: LIU Jianchao, REN Qingyun, HE Hongwu. Synthesis and Biological Activity of Pyrazolo[4', 3':5, 6]pyrano[2, 3-d]pyrimidine Derivatives[J]. Chinese Journal of Applied Chemistry, 2017, 34(11): 1279-1286. doi: 10.11944/j.issn.1000-0518.2017.11.160502

吡唑并[4', 3':5, 6]吡喃并[2, 3-d]嘧啶化合物的合成与生物活性
-
关键词:
- 氮杂Wittig反应
- / 吡唑并嘧啶
- / 吡喃并嘧啶
- / 生物活性
English
Synthesis and Biological Activity of Pyrazolo[4', 3':5, 6]pyrano[2, 3-d]pyrimidine Derivatives
-
Key words:
- Aza-Wittig reaction
- / pyrazolopyrimidine
- / pyranopyrimidine
- / biological activity
-
嘧啶酮及稠合嘧啶酮类化合物由于其广泛的生物活性备受生物及化学家的关注,这主要是由于在生命体内具有重要生理作用的小分子,如嘌呤类似物大多具有类似嘧啶酮环的结构。早期的生理学研究表明,含嘧啶环的化合物具有一系列的生物活性如抗病毒、抗过敏以及抗癌作用等[1-4]。近期研究发现,吡喃并嘧啶酮类化合物具有抗微生物、抗氧化活性[5-6],一些吡喃并嘧啶酮类衍生物可以用于治疗早期神经衰退症和结核病药物[7-8]。该类化合物的合成一般是由含嘧啶酮骨架化合物与醛酮等经过加成缩合而成[9-10],这些反应往往需要特定条件和催化剂,产物分离困难,操作繁琐。本文利用连续的氮杂Wittig反应制备含氮杂环化合物的前期基础[11],通过活性基团拼接原理设计并合成了一类新型的吡唑并吡喃并嘧啶类化合物,以期筛选出具有良好生物活性的新型农药或医药先导体分子。
1 实验部分
1.1 仪器和试剂
WRS-1B型数字熔点仪(北京泰克仪器有限公司,温度未经校正);AVATAR-360型傅里叶变换红外光谱仪(FTIR, 美国Nicolet公司);Mercury 400型400 MHz超导核磁共振仪(NMR, 美国Varian公司);Vario EL Ⅲ型元素分析仪(德国ELEMENTER公司);Smart Apex CCD型单晶X射线衍射仪(XRD, 德国Bruck公司)。乙腈和三乙胺(使用前重新蒸馏);1-苯基-3-甲基-5-吡唑酮、乙醇、二氯甲烷(CaCl2干燥)、二硫化碳、各种芳香醛、苯肼、乙酰乙酸乙酯、各种酚及仲胺均为分析纯试剂;均购自上海国药集团化学试剂有限公司。
1.2 合成路线
以1-苯基-3-甲基-5-吡唑酮与芳基亚甲基氰乙酸乙酯为起始原料,经3步反应获得目标化合物。首先由吡唑酮与芳基亚甲基氰乙酸乙酯反应制得关环产物吡唑并吡喃化合物Ⅰ,由吡唑并吡喃化合物Ⅰ与三苯基膦和六氯乙烷反应制得相应的膦亚胺Ⅱ,膦亚胺Ⅱ再与苯基乙氰酸酯反应制得碳二亚胺中间体,该中间体与胺在醇钠作催化剂的条件下关环制得2-烷氨基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲa~Ⅲi), 与酚在催化量碳酸钾作用下关环制得2-芳氧基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲh~Ⅲq)。具体合成路线如Scheme 1所示。
1.3 中间体的合成
参照文献[12]的方法合成了取代苯亚甲基氰乙酸乙酯。在50 mL单口烧瓶中加入1-苯基-3-甲基-5-吡唑酮(5 mmol)、取代苯亚甲基氰乙酸乙酯(5 mmol),苄基三乙基氯化铵(TEBA)(0.2 g)和10 mL水,在搅拌下于90 ℃反应4 h。冷至室温,抽滤,固体用95%乙醇重结晶, 即得3-甲基-6-氨基-4-芳基-1-苯基-1, 4-二氢吡喃并[2, 3-c]吡唑-5-甲酸乙酯(Ⅰ)[13-14]。
3-甲基-6-氨基-4-甲基苯基-1-苯基-1, 4-二氢吡喃并[2, 3-c]吡唑-5-甲酸乙酯(Ⅰa):白色固体, mp 147.2~147.6 ℃; 1H NMR(CDCl3, 400 Hz), δ:7.09~7.74(m, 9H, Ar—H), 5.17(s, 2H, N—H), 4.31(s, 1H, CH of pyranyl), 3.93~4.16(m, 2H, OCH2), 2.26(s, 3H, CH3of benzyl), 2.13(s, 3H, CH3 of pyrazolyl), 1.01(t, J=7.2 Hz, 3H, CH3)。
3-甲基-6-氨基-4-氯苯基-1-苯基-1, 4-二氢吡喃并[2, 3-c]吡唑-5-甲酸乙酯(Ⅰb):白色固体, mp 155.6~156.3 ℃; 1H NMR(CDCl3, 400 Hz), δ:7.22~7.74(m, 9H, Ar—H), 5.23(s, 2H, N—H), 4.36(s, 1H, CH of pyranyl), 3.93~4.16(m, 2H, OCH2), 2.15(s, 3H, CH3 of pyrazolyl), 1.01(t, J=7.2 Hz, 3H, CH3)。
3-甲基-6-氨基-4-芳基-1-苯基-1, 4-二氢吡喃并[2, 3-c]吡唑-5-甲酸乙酯(Ⅰ)(15 mmol)加入到100 mL三颈烧瓶中,依次加入60 mL无水乙腈和三苯基膦7.86 g(30 mmol), 再缓慢加入六氯乙烷7.11 g(30 mmol),在搅拌下缓慢滴加无水三乙胺8.3 mL,室温下搅拌4~5 h后,过滤,用无水乙醇洗涤以除去三苯基氧膦(mp 157~158 ℃), 真空干燥, 当芳基为对甲基苯基时, 产物产率93%;当芳基为对氯苯基时, 产率90%。
4-甲基苯基取代膦亚胺(Ⅱa):白色固体,mp 193.5~193.7 ℃; 1H NMR(CDCl3, 400 Hz), δ:6.99~7.80(m, 24H, Ar—H), 4.94(s, 1H, CH of pyranyl), 4.06~4.09(m, 2H, OCH2), 2.27(s, 3H, CH3 of benzyl), 1.97(s, 3H, CH3 of pyrazolyl), 1.12(t, J=7.2 Hz, 3H, CH3); MS(70 eV) m/z(%):649.3(M+, 65), 242(29), 77(100)。
4-氯苯基取代膦亚胺(Ⅱb):白色固体, mp 192.7~193.6 ℃;1H NMR(CDCl3, 400 Hz), δ:7.00~7.89(m, 24H, Ar—H), 4.87(s, 1H, CH of pyranyl), 4.10~4.12(m, 2H, OCH2), 2.29(s, 3H, CH3of pyrazolyl), 1.34(t, J=7.2 Hz, 3H, CH3); MS(70 eV) m/z(%):669.1(M+, 4), 481(49), 183(27), 111(51), 77(100)。
1.4 目标产物的合成
在干燥过的膦亚胺Ⅱ(1 mmol)的二氯甲烷溶液中,室温并N2气保护下加入苯基异氰酸酯(0.14 g, 1.1 mmol)。反应液静置6~12 h, 加压脱去部分溶剂,加入适量乙醚/石油醚(体积比1:2)以析出三苯氧膦,除去溶剂后得到中间体碳二亚胺,不经处理可直接进入下一步反应。
在上述得到的碳二亚胺的CH2Cl2(10 mL)溶液中,N2气保护下加入烷基胺(1.1 mmol)。搅拌约6 h,除去溶剂,再加入10 mL无水乙醇和几滴醇钠。搅拌约3~5 h,浓缩溶剂,残余物用二氯甲烷/石油醚重结晶得到纯的2-烷氨基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲa~Ⅲi)。
在碳二亚胺的CH3CN(15 mL)溶液中,加入各种不同的取代酚(1.1 mmol)以及催化量的固体K2CO3(0.012 g, 0.1 mmol),在75 ℃左右搅拌回流3~6 h。过滤,滤液浓缩,残余物用二氯甲烷/石油醚重结晶得到纯的2-烷氧基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲj~Ⅲq)。
2-二乙基氨基-3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲa):白色固体(产率57%), mp 268.6~268.9 ℃;1H NMR(400 MHz, CDCl3), δ:0.85(t, J=7.2 Hz, 6H, 2CH3), 1.95(s, 3H, CH3 of pyrazolyl), 3.08~3.19(m, 4H, 2NCH2), 4.97(s, 1H, CH), 7.22~7.86(m, 14H, Ar—H); IR(KBr), σ/cm-1:1680(C=O), 1632, 1518(Ph), 1544(C=N), 1355, 1133(C—O);元素分析C31H28ClN5O2测定值(计算值)/%:C 69.37(69.20), H 5.45(5.25), N 12.83(13.02)。
2-二正丙基氨基-3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲb):白色固体(产率57%), mp 270.3~270.7 ℃;1H NMR(400 MHz, CDCl3), δ:0.72(t, J=7.2 Hz, 6H, 2CH3), 1.24~1.26(m, 4H, 2CH2), 1.96(s, 3H, CH3 of pyrazolyl), 2.91~3.09(m, 4H, 2NCH2), 4.96(s, 1H, CH), 7.22~7.87(m, 14H, Ar—H); IR(KBr), σ/cm-1:1677(C=O), 1633, 1516(Ph), 1543(C=N), 1363, 1133(C—O); 元素分析C33H32ClN5O2测定值(计算值)/%:C 69.68(70.02), H 5.65(5.70), N 12.29(12.37)。
2-二正丁基氨基-3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲc):白色固体(产率46%), mp 269.9~270.5 ℃; 1H NMR(400 MHz, CDCl3), δ:0.83(t, J=7.2 Hz, 6H, 2CH3), 1.08~1.31(m, 8H, 2CH2CH2), 1.97(s, 3H, CH3 of pyrazolyl), 2.94~3.13(m, 4H, 2NCH2), 4.97(s, 1H, CH), 7.22~7.87(m, 14H, Ar—H); IR(KBr), σ/cm-1:1675(C=O), 1631, 1517(Ph), 1544(C=N), 1364, 1134(C—O);元素分析C35H36ClN5O2测定值(计算值)/%:C 70.33(70.75), H 6.20(6.11), N11.83(11.79)。
2-二正戊基氨基-3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲd):白色固体(产率56%), mp 238.4~239.0 ℃;1H NMR(400 MHz, CDCl3), δ:0.86(t, J=7.2 Hz, 6H, 2CH3), 1.04~1.09(m, 4H, 2CH2), 1.16~1.26(m, 4H, 2CH2), 1.33~1.35(m, 4H, 2CH2), 1.97(s, 3H, CH3 of pyrazolyl), 2.93~2.96(m, 2H, NCH2), 3.08~3.14(m, 2H, NCH2), 4.97(s, 1H, CH), 7.21~7.87(m, 14H, Ar—H); IR(KBr), σ/cm-1:1674(C=O), 1628, 1517(Ph), 1543(C=N), 1364, 1134(C—O); 元素分析C37H40ClN5O2测定值(计算值)/%:C 71.30(71.42), H 6.52(6.48), N 11.34(11.26)。
2-二乙基氨基-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲe):白色固体(产率70%), mp 262.5~262.9 ℃;1H NMR(400 MHz, CDCl3), δ:0.84(t, J=7.2 Hz, 6H, 2CH3), 1.97(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 3.09~3.17(m, 4H, 2NCH2), 4.97(s, 1H, CH), 7.06~7.87(m, 14H, Ar—H); IR(KBr), σ/cm-1:1682(C=O), 1634, 1516(Ph), 1544(C=N), 1355, 1134(C—O);元素分析C32H31N5O2测定值(计算值)/%:C 74.47(74.25), H 6.11(6.04), N 13.74(13.53)。
2-二正丁基氨基-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲf):白色固体(产率50%), mp 245.0~245.3 ℃;1H NMR(400 MHz, CDCl3), δ: 0.83(t, J=7.2 Hz, 6H, 2CH3), 1.08~1.15(m, 4H, 2CH2), 1.30~1.33(m, 4H, 2CH2), 1.98(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 2.92~2.95(m, 2H, NCH2), 3.08~3.14(m, 2H, NCH2), 4.96(s, 1H, CH), 7.06~7.88(m, 14H, Ar—H); IR(KBr), σ/cm-1:1676(C=O), 1631, 1516(Ph), 1544(C=N), 1363, 1134(C—O); 元素分析C36H39N5O2测定值(计算值)/%:C 75.60(75.36), H 6.89(6.85), N 12.18(12.21)。
2-(1-哌啶基)-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲg):白色固体(产率65%), mp>300 ℃;1H NMR(400 MHz, CDCl3), δ:1.25~1.27(m, 4H, (CH2)2), 1.42~1.44(m, 2H, CH2), 1.97(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 3.13~3.15(m, 4H, 2NCH2), 4.98(s, 1H, CH), 7.06~7.86(m, 14H, Ar—H); IR(KBr), σ/cm-1:1674(C=O), 1630, 1513(Ph), 1543(C=N), 1366, 1135(C—O);元素分析C33H31N5O2测定值(计算值)/%:C 75.02(74.84), H 5.87(5.90), N 13.28(13.22)。
2-(1-吗啡啉基)-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲh):白色固体(产率74%), mp 292.8~293.3 ℃;1H NMR(400 MHz, CDCl3), δ:2.03(s, 3H, CH3 of pyrazolyl), 2.30(s, 3H, CH3 of benzyl), 3.19(t, J=4 Hz, 4H, 2NCH2), 3.47(t, J=4 Hz, 4H, 2OCH2), 5.03(s, 1H, CH), 7.13~7.89(m, 14H, Ar—H); IR(KBr), σ/cm-1:1683(C=O), 1633, 1516(Ph), 1544(C=N), 1366, 1137(C—O);元素分析C32H29N5O3测定值(计算值)/%:C 72.48(72.30), H 5.55(5.50), N 13.33(13.17)。
2-二正丙基氨基-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲi):白色固体(产率62%), mp 241.5~242.0 ℃;1H NMR(400 MHz, CDCl3), δ:0.71(t, J=7.2 Hz, 6H, 2CH3), 1.20~1.24(m, 2H, CH2), 1.32~1.37(m, 2H, CH2), 1.99(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 2.87~2.93(m, 2H, NCH2), 3.05~3.11(m, 2H, NCH2), 4.96(s, 1H, CH), 7.06~7.87(m, 14H, Ar—H); IR(KBr), σ/cm-1:1675(C=O), 1632, 1513(PH), 1543(C=N), 1362, 1133(C—O);元素分析C34H35N5O2测定值(计算值)/%:C 74.82(74.84), H 6.39(6.47), N 12.98(12.83)。
2-(4-氯-3-甲基苯氧基) -3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲj):白色固体(产率55%), mp 288.6~289.3 ℃;1H NMR(400 MHz, CDCl3), δ:1.96(s, 3H, CH3 of pyrazolyl), 2.37(s, 3H, CH3 of benzyl), 5.07(s, 1H, CH), 6.96~7.75(m, 17H, Ar—H); IR(KBr), σ/cm-1:1700(C=O), 1637, 1543, 1510(Ph), 1559(C=N), 1400, 1138(C—O);元素分析C34H24Cl2N4O3测定值(计算值)/%:C 67.14(67.22), H 3.98(3.98), N 9.19(9.22)。
2-(4-甲氧基苯氧基) -3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲk):白色固体(产率47%), mp>300 ℃;1H NMR(400 MHz, CDCl3), δ:1.96(s, 3H, CH3 of pyrazolyl), 3.82(s, 3H, OCH3), 5.07(s, 1H, CH), 6.88~7.75(m, 18H, Ar—H); IR(KBr), σ/cm-1:1695(C=O), 1636, 1595, 1506(Ph), 1559(C=N), 1405, 1252, 1205, 1138(C—O); 元素分析C34H25ClN4O4测定值(计算值)/%:C 69.37(69.33), H 4.24(4.28), N 9.57(9.51)。
2-(2, 4-二氟苯氧基)-3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲl):白色固体(产率68%), mp 292.9~293.0 ℃;1H NMR(400 MHz, CDCl3), δ:1.96(s, 3H, CH3 of pyrazolyl), 5.07(s, 1H, CH), 7.23~7.74(m, 17H, Ar—H); IR(KBr), σ/cm-1:1698(C=O), 1637, 1601, 1508(Ph), 1561(C=N), 1399, 1249, 1196, 1138(C—O);元素分析C33H21ClF2N4O3测定值(计算值)/%:C 66.76(66.61), H 3.51(3.56), N 9.43(9.42)。
2-苯氧基-3, 8-二苯基-5-(4-氯苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲm):白色固体(产率53%), mp 285.7~286.0 ℃;1H NMR(400 MHz, CDCl3), δ:1.96(s, 3H, CH3 of pyrazolyl), 5.08(s, 1H, CH), 7.10~7.75(m, 19H, Ar—H); IR(KBr), σ/cm-1:1687(C=O), 1637, 1601, 1517(Ph), 1558(C=N), 1403, 1253, 1203, 1136(C—O);元素分析C33H23ClN4O3测定值(计算值)/%:C 70.77(70.90), H 4.15(4.15), N 10.06(10.02)。
2-(2, 4-二氟苯氧基)-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲn):白色固体(产率67%), mp>300 ℃;1H NMR(400 MHz, CDCl3), δ:1.97(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 5.06(s, 1H, CH), 6.89~7.74(m, 17H, Ar—H); IR(KBr), σ/ cm-1:1689(C=O), 1637, 1600, 1509(Ph), 1561(C=N), 1387, 1248, 1195, 1137(C—O);元素分析C34H24F2N4O3测定值(计算值)/%:C 71.28(71.07), H 4.28(4.21), N 9.94(9.75)。
2-(4-氯苯氧基)-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲo):白色固体(产率65%), mp 284.9~285.5 ℃;1H NMR(400 MHz, CDCl3), δ:1.99(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 5.06(s, 1H, CH), 7.05~7.76(m, 18H, Ar—H); IR(KBr), σ/cm-1:1693(C=O), 1635, 1601, 1518(Ph), 1557(C=N), 1407, 1250, 1204, 1137(C—O);元素分析C34H25ClN4O3测定值(计算值)/%:C 71.42(71.26), H 4.42(4.40), N 9.85(9.78)。
2-(4-氯-3-甲基苯氧基)-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲp):白色固体(产率54%), mp 262.2~262.5 ℃;1H NMR(400 MHz, CDCl3), δ:1.99(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 2.37(s, 3H, CH3), 5.06(s, 1H, CH), 6.96~7.76(m, 17H, Ar—H); IR(KBr), σ/cm-1:1698(C=O), 1636, 1602, 1517(Ph), 1557(C=N), 1400, 1252, 1229, 1137(C—O);元素分析C35H27ClN4O3测定值(计算值)/%:C 71.90(71.61), H 4.66(4.64), N 9.62(9.54)。
2-(2-氯-4-氟苯氧基)-3, 8-二苯基-5-(4-甲基苯基)-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮(Ⅲq):白色固体(产率64%), mp 282.9~283.7 ℃;1H NMR(400 MHz, CDCl3), δ:1.98(s, 3H, CH3 of pyrazolyl), 2.29(s, 3H, CH3 of benzyl), 5.07(s, 1H, CH), 7.08~7.72(m, 17H, Ar—H); IR(KBr), σ/cm-1:1694(C=O), 1636, 1601, 1490(Ph), 1561(C=N), 1398, 1245, 1184, 1138(C—O);元素分析C34H24ClFN4O3测定值(计算值)/%:C 69.18(69.09), H 4.12(4.09), N 9.53(9.48)。
2 结果与讨论
2.1 中间体及目标化合物的合成
在制备3-甲基-6-氨基-4-芳基-1-苯基-1, 4-二氢吡喃并[2, 3-c]吡唑-5-甲酸乙酯Ⅰ时,本文尝试采用TEBA作催化剂,在水溶液中反应。文献[13]报道的反应条件与本文获得产物的反应条件有一点差异:文献报道该反应须在90 ℃反应3 h,但在实际反应中,发现该反应在如此高的温度下反应物发生聚集,成团后反应无法正常进行。只有采用室温条件并延长反应时间的方法,才顺利得到所需要的产物。
膦亚胺Ⅱ的制备过程中,中间体Ⅰ与PPh3、C2Cl6、NEt3的物质的量的比在1:2:2:4最佳,这样可使原料顺利反应完全。膦亚胺Ⅱ与苯基乙氰酸酯反应制得碳二亚胺中间体,该中间体与胺在醇钠作催化剂的条件下关环制得2-烷氨基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮, 与酚在催化量碳酸钾作用下关环制得2-芳氧基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮。这是一个典型的串联氮杂Wittig反应。因为碳二亚胺极易水解,所以不必分离直接进行下一步的反应,同时需要保持体系绝对无水。碳二亚胺与胺的反应在常温下即可进行,但低于0 ℃则反应不完全。碳二亚胺与仲胺的反应较容易,与伯胺则很难反应,推测可能是由于电子效应的影响大于位阻效应的缘故。
2.2 波谱解析
在目标化合物的红外光谱数据中,羰基在1670~1690 cm-1有明显的(C=O)强伸缩振动吸收峰,为典型的环羰基吸收。苯环上尖而弱的C—H伸缩振动吸收带在3000~3100 cm-1区域内,苯环与吡唑并吡喃并嘧啶的环骨架振动在1630、1600、1540和1510 cm-1处形成特征吸收峰组,C—O—C的振动吸收在1133 cm-1附近。目标化合物1H NMR谱的各个峰也均得到了验证。当5位被对氯苯基取代时,2.0处附近的单峰是吡唑环上甲基的吸收峰;被对甲基苯基取代时,2.0处附近的单峰是吡唑环上甲基的吸收峰, 而2.30处的单峰则是对甲基苯基上甲基的吸收峰。4.97或5.10处出现的信号分别是对氯苯基取代或对甲基苯基取代的吡喃环CH的质子吸收峰,在7.22~7.86之间的多重峰是苯环上氢的峰。元素分析数据结果中,理论值与计算值非常符合,其相对误差基本在0.5%范围内。
2.3 X射线单晶衍射分析与晶体结构
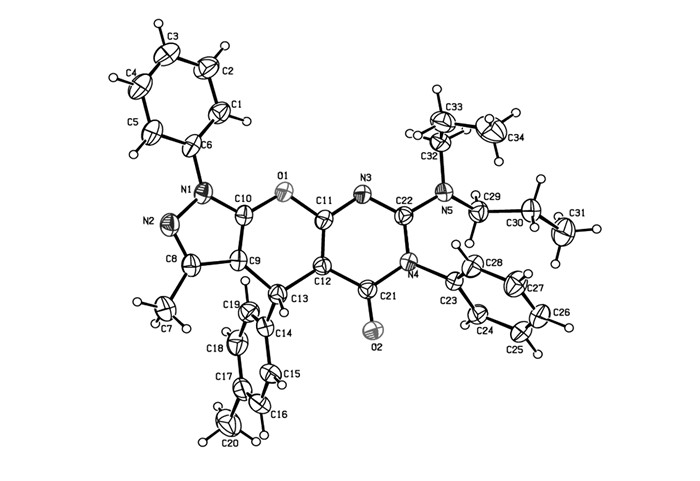
化合物Ⅲi溶于无水乙醇中培养得到无色透明单晶,选取尺寸为0.30 mm×0.20 mm×0.20 mm的无色晶体放置在X射线单晶衍射仪上,测定温度为20 ℃,采用石墨单色化的MoKα(λ=0.071073 nm)射线,以ω/2θ扫描方式在1.76°<θ<25.00°范围内共收集到5128个独立衍射点,其中I>2σ(I)的可观测衍射点2947个。晶体结构采用直接法使用SHELXL-97程序[15]解出,对F2进行全矩阵最小二乘法修正。所有的非氢原子经各向异性修正。最终的偏离因子为R=0.0562,Rw=0.1636,差值电子云密度的最高和最低峰为146和-191 e/nm3。化合物Ⅲi的分子晶体结构图见图 1。晶体结构分析表明,化合物Ⅲi晶体为三斜晶系,空间群P-1,晶胞参数为a=0.8970(10) nm, b=1.3596(14) nm, c=1.4387(15) nm,α=111.213(19)°, β=98.88(2)°, γ=108.88(2)°, Z=2, V=1.473(3) nm3, Dc=1.231 mg/m3, μ=0.078 mm-1, F(000)=580。化合物晶体数据已存于剑桥晶体数据库,CCDC号为6429960。
2.4 目标化合物的生物活性
采用离体平面皿法对本系列的化合物进行了杀菌活性的测试。试用菌种为:棉花枯萎菌(Fusarium oxysporum)、水稻纹枯菌(Rhizoctonia solani)、黄瓜灰霉菌(Botrytis cinereapers)、小麦赤霉菌(Gibberella zeae)、苹果轮纹菌(Botryosphaeria berengerinan)及玉米小斑菌(Bipilaris maydis),处理剂量为50 mg/L。具体的测试结果见表 1。
Compounds Fusarium oxysporum/% Rhizoctonia solani/% Botrytis cinereapers/% Gibberella zeae/% Botryosphaeria berengerinan/% Bipilaris maydis/% Ⅲa 25 41 54 26 28 36 Ⅲb 29 0 54 16 14 63 Ⅲc 29 37 54 13 43 68 Ⅲd 37 49 57 30 33 63 Ⅲe 54 76 89 47 76 79 Ⅲf 54 60 60 23 38 58 Ⅲg 50 68 86 43 67 68 Ⅲh 63 91 100 90 90 89 Ⅲi 42 53 69 37 52 63 Ⅲj 29 35 66 27 48 63 Ⅲk 58 77 94 57 67 74 Ⅲl 67 92 100 90 86 89 Ⅲm 42 51 54 30 29 53 Ⅲn 46 74 83 33 67 68 Ⅲo 33 55 66 33 48 63 Ⅲp 44 50 72 38 77 58 Ⅲq 46 69 77 47 62 47 in vitro 50 mg/L, inhibition rate%. 委托浙江省化工研究院农药生测研究所对所合成化合物进行了室内杀虫活性的测定,测试对象为水稻褐飞虱(Nilaparvatalegen)三龄中期幼虫和粘虫(Mythimaseparata)三龄中期幼虫,均为室内常年累代饲养虫种。对照药为敌敌畏(O, O-dimethyl-O-2, 2-dichlorovinylphosphate, DDVP),测试结果见表 2。
Compounds Nilaparvatalegen/% Mythimaseparata/% Compounds Nilaparvatalegen/% Mythimaseparata/% Ⅲa 0.0 100.0 Ⅲj 0.0 75.0 Ⅲb 0.0 25.0 Ⅲk 0.0 60.0 Ⅲc 0.0 100.0 Ⅲl 3.3 0.0 Ⅲd 3.3 42.9 Ⅲm 0.0 50.0 Ⅲe 0.0 55.0 Ⅲn 6.7 63.2 Ⅲf 0.0 65.0 Ⅲo 0.0 76.5 Ⅲg 0.0 55.0 Ⅲp 0.0 68.8 Ⅲh 3.3 10.0 Ⅲq 0.0 65.0 Ⅲi 6.7 73.3 DDVP 99.0 100.0 in vitro 50 mg/L, inhibition rate%. 实验结果表明,在50 mg/L剂量下该类化合物对水稻纹枯菌、黄瓜灰霉菌、小麦赤霉菌、苹果轮纹菌及玉米小斑菌均有一定的杀菌活性,部分化合物对黄瓜灰霉菌显示了较好的抑制效果。有3个化合物Ⅲh、Ⅲk、Ⅲl对黄瓜灰霉菌的抑制效果达到90%以上,其中化合物Ⅲh、Ⅷl对上述5种菌均显示了优良的抑制活性。
目标化合物对水稻褐飞虱、粘虫等靶标的室内生测筛选结果表明:该类化合物对水稻褐飞虱无明显的杀虫活性,但发现对粘虫具有较高的活性,其中有10个化合物对粘虫的抑制率为60%以上,特别是化合物Ⅲa和Ⅲc在500 mg/L的剂量下,对粘虫的抑制率为100.0%,与对照药敌敌畏相当,显示了较高的杀虫活性,值得进一步研究。
3 结论
本文应用串联氮杂Wittig反应,首先将1-苯基-3-甲基-5-吡唑酮与芳基亚甲基氰乙酸乙酯经过加成和关环得到吡唑并吡喃化合物,由吡唑并吡喃化合物与三苯基膦和六氯乙烷反应制得相应的膦亚胺,膦亚胺再与苯基乙氰酸酯反应制得碳二亚胺,碳二亚胺与胺在醇钠作催化剂的条件下再次关环制得2-烷氨基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮, 与酚在催化量碳酸钾作用下关环制得2-芳氧基-3, 8-二苯基-5-芳基-6-甲基-5, 8-二氢-4H-吡唑并[4′, 3′:5, 6]吡喃并[2, 3-d]嘧啶-4(3H)-酮。全部反应条件温和,操作简单,总体收率较高。对合成的目标化合物进行了室内的杀菌和杀虫活性测试,结果表明:该类化合物具有一定的杀菌活性,其中部分化合物对黄瓜灰霉菌(Botrytis cinereapers)在50 mg/L剂量下显示了优异的杀菌活性;对水稻褐飞虱无明显的杀虫活性,但发现对粘虫具有较好的杀灭活性,如化合物Ⅲa和Ⅲc在500 mg/L的剂量下对粘虫的抑制率达到100.0%,与对照药敌敌畏相当。
-
-
[1]
Haraguchi K, Kubota Y, Tanaka H. Ring Opening of Nucleoside 1', 2'-Epoxides with Organoaluminum Reagents:Stereoselective Entry to Ribonucleosides Branched at the Anomeric Position[J]. J Org Chem, 2004, 69(6): 1831-1836. doi: 10.1021/jo030262u
-
[2]
Cushman M, Sambaiah T, Jin G. Design, Synthesis, and Evaluation of 9-D-Ribitylamino-1, 3, 7, 9-Tetrahydro-2, 6, 8-Purinetriones Bearing Alkyl Phosphate and α, α-Difluorophosphonate Substituents as Inhibitors of Riboflavin Synthase and Lumazine Synthase[J]. J Org Chem, 2004, 69(3): 601-612. doi: 10.1021/jo030278k
-
[3]
Depecker G, Patino N, Giorgio C D. Cyclic PNA-based Compound Directed Against HIV-1 TAR RNA:Modelling, Liquid-phase Synthesis and TAR Binding[J]. Org Biomol Chem, 2004, 2(1): 74-79. doi: 10.1039/b311775h
-
[4]
Wnuk S F, Lewandowska E, Companioni D R. Synthesis and Cytotoxicity of 9-(2-Deoxy-2-Alkyldithio-β-D-Arabinofuranosyl)purine Nucleosides Which are Stable Precursors to Potential Mechanistic Probes of Ribonucleotide Reductases[J]. Org Biomol Chem, 2004, 2(1): 120-126. doi: 10.1039/B311504F
-
[5]
Aly H M, Kamal M M. Efficient One-pot Preparation of Novel Fused Chromeno[2, 3-d]pyrimidine and Pyrano[2, 3-d] Pyrimidine Derivatives[J]. Eur J Med Chem, 2012, 47(1): 18-23.
-
[6]
Saundne A R, Vijaykumar K, Vaijinath A V. Synthesis of Novel 2-Amino-4-(5'-Substituted 2'-Phenyl-2H-Indol-3'-yl)-6-Aryl-4H-Pyran-3-Carbonitrile Derivatives as Antimicrobial and Antioxidant Agents[J]. Bioorg Med Chem Lett, 2013, 23(7): 1978-1984. doi: 10.1016/j.bmcl.2013.02.036
-
[7]
Clinch K, Watt D K, Dixon R A. Synthesis of Cyclic Pyranopterin Monophosphate, A Biosynthetic Intermediate in the Molybdenum Cofactor Pathway[J]. J Med Chem, 2012, 56(5): 1730-1738.
-
[8]
Kamdar N R, Haveliwala D D, Mistry P T. Design, Synthesis and in vitro Evaluation of Antitubercular and Antimicrobial Activity of some Novel Pyranopyrimidines[J]. Eur J Med Chem, 2010, 45(11): 5056-5063. doi: 10.1016/j.ejmech.2010.08.014
-
[9]
Kazemi-Red R, Azizian J, Kefayati H. Electrogenerated Acetonnitrile Anions/tetrabutylammonium Cations:An Effective Catalytic System for the Synthesis of Novel Chromeno[3', 4':5, 6] Pyrano[2, 3-d]Pyrimidines[J]. Tetrahedron Lett, 2014, 55(50): 6887-6890. doi: 10.1016/j.tetlet.2014.10.099
-
[10]
程青芳, 许兴友, 王启发. 水介质中微波促成一锅法合成吡喃并[2, 3-d]嘧啶[J]. 应用化学, 2010,27,(6): 673-676. CHEN Qingfang, XU Xingyou, WANG Qifa. One-pot Synthesis of Pyrano[2, 3-d]Pyrimidine Derivatives in Aqueous Media under Microwave Irradiatio[J]. Chinese J Appl Chem, 2010, 27(6): 673-676.
-
[11]
刘建超, 梁英, 贺红武. 6-烷氨(氧)基-3-甲硫基-1H-吡唑并[3, 4-d]嘧啶-4(5H)-酮衍生物的合成与生物活性[J]. 应用化学, 2014,31,(8): 922-927. LIU Jianchao, LIANG Ying, HE Hongwu. Synthesis and Biological Activity of 6-Alkylamino(oxy)-3-Methylthio-1H-Pyrazolo[3, 4-d]Pyrimidin-4(5H)-One Derivatives[J]. Chinese J Appl Chem, 2014, 31(8): 922-927.
-
[12]
戴桂元, 史达清, 周龙虎. FK/Al2O3催化下的Knoevenagel缩合反应[J]. 应用化学, 1995,12,(3): 103-104. DAI Guiyuan, SHI Daqing, ZHOU Longhu. Knoevenagel Condensation Catalyzed by Potassium Fluoride/Alumina[J]. Chinese J Appl Chem, 1995, 12(3): 103-104.
-
[13]
史达清, 张姝, 庄启亚. 水中α, β-不饱和酮与3-甲基-1-苯基-2-吡唑啉-5-酮的加成反应[J]. 有机化学, 2003,23,(9): 1036-1038. SHI Daqing, ZHANG Shu, ZHUANG Qiya. Michael Addition of 3-Methyl-2-pyrazolin-5-one to α, β-Unsaturated Ketones in Water[J]. Chinese J Org Chem, 2003, 23(9): 1036-1038.
-
[14]
Muthusamy S, Babu S A, Gunanath C. 1, 8-Diazabicyclo[5.4.0] Undec-7-Ene(DBU):A Powerful Catalyst for the Michael Addition Reaction of β-Ketoesters to Acrylates and Enones[J]. Synth Commu, 2002, 32(21): 3247-3254. doi: 10.1081/SCC-120014028
-
[15]
Sheldrick G M. SHELXS97 and SHELXL97[P]. Germanry:University of Gottingen, 1997.
-
[1]
-
表 1 化合物的杀菌活性结果
Table 1. Fungicidal activity of title compounds
Compounds Fusarium oxysporum/% Rhizoctonia solani/% Botrytis cinereapers/% Gibberella zeae/% Botryosphaeria berengerinan/% Bipilaris maydis/% Ⅲa 25 41 54 26 28 36 Ⅲb 29 0 54 16 14 63 Ⅲc 29 37 54 13 43 68 Ⅲd 37 49 57 30 33 63 Ⅲe 54 76 89 47 76 79 Ⅲf 54 60 60 23 38 58 Ⅲg 50 68 86 43 67 68 Ⅲh 63 91 100 90 90 89 Ⅲi 42 53 69 37 52 63 Ⅲj 29 35 66 27 48 63 Ⅲk 58 77 94 57 67 74 Ⅲl 67 92 100 90 86 89 Ⅲm 42 51 54 30 29 53 Ⅲn 46 74 83 33 67 68 Ⅲo 33 55 66 33 48 63 Ⅲp 44 50 72 38 77 58 Ⅲq 46 69 77 47 62 47 in vitro 50 mg/L, inhibition rate%. 表 2 化合物的杀虫活性结果
Table 2. Insecticidal activity of title compounds
Compounds Nilaparvatalegen/% Mythimaseparata/% Compounds Nilaparvatalegen/% Mythimaseparata/% Ⅲa 0.0 100.0 Ⅲj 0.0 75.0 Ⅲb 0.0 25.0 Ⅲk 0.0 60.0 Ⅲc 0.0 100.0 Ⅲl 3.3 0.0 Ⅲd 3.3 42.9 Ⅲm 0.0 50.0 Ⅲe 0.0 55.0 Ⅲn 6.7 63.2 Ⅲf 0.0 65.0 Ⅲo 0.0 76.5 Ⅲg 0.0 55.0 Ⅲp 0.0 68.8 Ⅲh 3.3 10.0 Ⅲq 0.0 65.0 Ⅲi 6.7 73.3 DDVP 99.0 100.0 in vitro 50 mg/L, inhibition rate%. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 4
- 文章访问数: 1028
- HTML全文浏览量: 157


 下载:
下载:

 下载:
下载:

