 图1
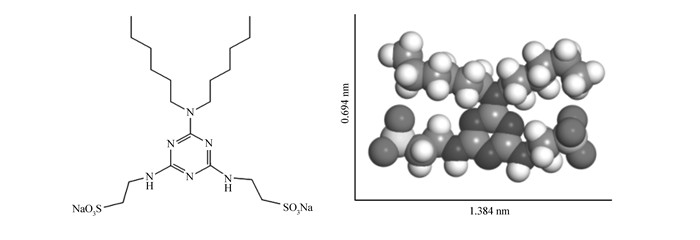
MXC6的分子结构图和三维结构模型
Figure1.
Molecular structure and 3D structure model of MXC6
图1
MXC6的分子结构图和三维结构模型
Figure1.
Molecular structure and 3D structure model of MXC6

Citation: BI Haoyu, LIANG Yaqin, LI Yan. Adsorption of p-Cresol on X-Type Gemini Surfactant-modified Hydrotalcite-like Nanocomposite[J]. Chinese Journal of Applied Chemistry, 2017, 34(11): 1329-1335. doi: 10.11944/j.issn.1000-0518.2017.11.160507

X型Gemini表面活性剂改性类水滑石的制备及其吸附对甲酚性能
-
关键词:
- X型Gemini表面活性剂
- / 类水滑石
- / 剥离-重组
- / 对甲酚
- / 吸附
English
Adsorption of p-Cresol on X-Type Gemini Surfactant-modified Hydrotalcite-like Nanocomposite
-
酚类化合物是一种极性、疏水和可离子化的有机化合物,是水环境中的主要污染物,对人、畜危害极大[1]。因此,急需开发含酚废水处理技术,吸附法是处理有机物废水的有效方法之一,其最大优点是设备简单、操作方便,且能从污水中富集分离污染物,实现废物资源化[2]。
类水滑石化合物(HTlc)是由二价金属离子和三价金属离子组成的具有水滑石层状结构的氢氧化物。由于HTlc独特的晶体层状结构(即层片带结构正电荷和层间有可交换的阴离子)、强亲水性、较大的比表面和良好的水分散性,使其在污水处理中具有非常广阔的应用前景[3-4]。但是,也正是由于其强亲水性和层板的正电性,使其难以有效去除疏水性有机物,如酚类化合物[5]。
通过对HTlc改性,制备表面活性剂-HTlc纳米复合物[6-8],可有效去除废水中的有机物,其中,表面活性剂多为含一个疏水基和一个亲水极性头基构成的传统表面活性剂。Gemini表面活性剂具有两个亲水基团和两个亲油基团,且两个双亲基团通过化学键连接,具有优良的水溶性和极高的表面活性,近年来被广泛研究应用[9]。
本文采用剥离-重组法将较大分子结构的X型Gemini表面活性剂组装于HTlc层间,制备了Gemini表面活性剂改性HTlc,即Gemini表面活性剂-HTlc纳米复合物,并研究了其吸附对甲酚性能。
1 实验部分
1.1 仪器和试剂
D8 ADVANCE型粉末X射线衍射仪(XRD, 德国布鲁克公司),CuKα射线,管电压40 kV管电流30 mA,扫描范围2°~70°;Avatar 370型傅里叶变换红外光谱仪(FTIR, 美国Nicolet公司),KBr压片,分辨率1 cm-1,400~4000 cm-1;TU-1900型紫外可见分光光度计(上海普析通用仪器有限责任公司);Z2000型原子吸收仪(日本日立公司);Autosorb iQ型全自动比表面和孔径分布分析仪(美国康塔公司);Vario EL型元素分析仪(德国Elmentar公司)。
Mg(NO3)2·6H2O、Al(NO3)3·9H2O、氨水、甲酰胺、对甲酚等试剂均为分析纯(上海晶纯生化科技股份有限公司),双子表面活性剂(记作MXC6,结构式如图 1所示)为中北大学化工与环境学院提供。实验用水为二次蒸馏水。
1.2 改性类水滑石的制备
Mg3Al HTlc采用非稳定态共沉淀法制备[10]:取适量Mg(NO3)2·6H2O和Al(NO3)3·9H2O[n(Mg2+):n(Al3+)=3:1]溶于蒸馏水,且Mg2+和Al3+离子浓度之和为0.5 mol/L,搅拌下加入一定量体积比为1:4(氨水:H2O)的氨水溶液,至溶液pH值为9~10,N2气氛围下静止老化1 h,抽滤并洗涤沉淀,至滤液pH=7,将滤饼密封于具塞广口瓶,353 K恒温胶溶24 h,得Mg3Al HTlc溶胶。Mg3Al HTlc溶胶于373 K恒温烘干研磨备用。
取0.2 g Mg3Al HTlc至于含10 mL甲酰胺的烧杯中,超声分散10 min至无色透明,再缓慢滴入0.2 g MXC6/10 mL乙醇溶液,立即产生沉淀,磁力搅拌30 min,悬浮液于12000 r/min离心15 min,蒸馏水洗涤2次,乙醇洗涤1次,所得固体产物于353 K烘至恒重,得MXC6-HTlc纳米复合物。
1.3 样品表征
对Mg3Al HTlc和MXC6-HTlc样品分别进行XRD、FTIR和比表面表征;通过原子吸收仪测定样品中Mg、Al含量;采用元素分析仪测定MXC6-HTlc样品中C、H、N、S元素含量,计算HTlc层板中Al元素与层间MXC62-离子的摩尔比。
1.4 吸附实验
采用批量平衡吸附法进行实验。在系列100 mL具塞锥形瓶中分别先后加入50 mL对甲酚溶液(0~40 mg/L)和0.05 g MXC6-HTlc纳米复合物,摇匀,于293 K(303或313 K)恒温振荡一定时间,悬浮液于12000 r/min离心20 min,用紫外可见分光光度计(λmax=277 nm)测定上清液中对甲酚的吸光度,计算对甲酚浓度。同时做空白实验以消除误差。根据吸附前后对甲酚浓度变化计算吸附量。
当对甲酚浓度取40 mg/L时,考察吸附动力学和体系pH值(5~10,用稀盐酸或NaOH溶液调节)对吸附的影响。除考察温度和pH值对吸附影响外,其它实验均在293 K和未调节体系pH值(约7.5)条件下进行。以上实验均平行测定3次,结果取平均值。
作为比较,实验考察了293 K时对甲酚在HTlc上的吸附动力学、热力学和pH值对吸附的影响。
2 结果与讨论
2.1 样品表征
图 2A为HTlc和MXC6-HTlc的XRD图谱。从图 2A可知,HTlc样品XRD谱线的最大衍射强度特征峰出现在9.91°,对应层间距d003为0.89 nm,这与其层间为NO3-离子相符。HTlc的d003值随层间离子大小及排布方式的改变而改变[11],重组后MXC6-HTlc的初级衍射峰d003向低角度发生偏移至3.42°,对应层间距d003为2.60 nm,表明层间距增大,层间离子改变。由于HTlc层板厚度约为0.48 nm[12],则MXC6-HTlc层间高度为2.12(=2.60-0.48) nm左右。根据Gaussian 03软件PM3半经验分子轨道法优化计算得到MXC62-离子的长和宽分别为1.384和0.694 nm(图 1),因此推测MXC62-离子以沿长轴倾斜于层板的方式双层交错排布于层间,其中上下两层MXC62-离子的两条疏水链在中间相互靠近,每个MXC62-离子中的一个SO3-基团通过氢键和静电作用与HTlc上下层板相结合,另一个SO3-基团与相邻MXC62-离子中疏水烷基链的端基靠近(图 2B)。
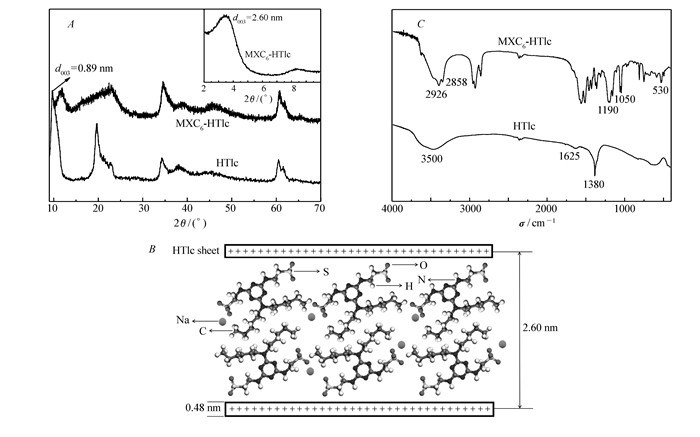 图2
HTlc和MXC6-HTlc的XRD图谱(内插图为MXC6-HTlc的小角衍射图谱)(A);MXC6在MXC6-HTlc层间取向模拟(B);HTlc和MXC6-HTlc的FTIR图谱图(C)
Figure2.
Powder XRD spectra of HTlc and MXC6-HTlc(Inset is the small angle diffraction pattern of MXC6-HTlc)(A); simulation of the orientation of MXC6 in MXC6-HTlc(B); FTIR spectra of HTlc and MXC6-HTlc(C)
图2
HTlc和MXC6-HTlc的XRD图谱(内插图为MXC6-HTlc的小角衍射图谱)(A);MXC6在MXC6-HTlc层间取向模拟(B);HTlc和MXC6-HTlc的FTIR图谱图(C)
Figure2.
Powder XRD spectra of HTlc and MXC6-HTlc(Inset is the small angle diffraction pattern of MXC6-HTlc)(A); simulation of the orientation of MXC6 in MXC6-HTlc(B); FTIR spectra of HTlc and MXC6-HTlc(C)
图 2C为HTlc和MXC6-HTlc的FTIR图谱。HTlc的FTIR谱线出现了类水滑石的特征吸收峰:约3500 cm-1处吸收峰对应于层板上羟基的伸缩振动;约1625 cm-1处吸收峰对应于层间水分子νH—O—H弯曲振动;约1380 cm-1处吸收峰为NO3-特征振动峰。MXC6-HTlc谱线中产生了C—H伸缩振动吸收峰(2850~2960 cm-1)和磺酸基的主要特征峰(1190、1050和530 cm-1),表明MXC6已组装于HTlc层板间;且在约1380 cm-1处存在微弱吸收峰,表明层间仍有少量NO3-离子。
表 1给出了HTlc和MXC6-HTlc样品的比表面积和元素组成。由表 1可知,MXC6-HTlc比表面积低于HTlc比表面积,这是因为粒子在改性后表面疏水性增强,易发生聚集使比表面积降低,这与You等[13]报道的结果相似。元素分析结果表明,HTlc和MXC6-HTlc样品中的Mg元素与Al元素摩尔比与制备时溶液中的比值(3:1)接近;MXC6-HTlc样品中MXC62-离子与Al3+离子的摩尔比为0.83,表明:1)层间仍有少量NO3-离子存在,这与红外表征结果一致;2)MXC62-离子中仅有一个SO3-离子中和HTlc层板正电荷,另一个SO3-离子的负电荷被进入层间的Na+离子平衡(如图 2B所示)。
 表 1
HTlc和MXC6-HTlc样品的比表面积和元素分析以及MXC6-HTlc中MXC6的插入量
Table 1.
Specific surface areas and chemical analysis results of HTlc and MXC6-HTlc, and the intercalated amount of MXC6 in MXC6-HTlc
表 1
HTlc和MXC6-HTlc样品的比表面积和元素分析以及MXC6-HTlc中MXC6的插入量
Table 1.
Specific surface areas and chemical analysis results of HTlc and MXC6-HTlc, and the intercalated amount of MXC6 in MXC6-HTlc
Sample Specific surface area/(m2·g-1) n(Mg):n(Al) n(Al):n(MXC6) Intercalated amount of w(MXC6)/% HTlc 18.75 2.64:1 - - MXC6 11.71 2.57:1 1:0.83 57.7 2.2 吸附结果
2.2.1 吸附动力学
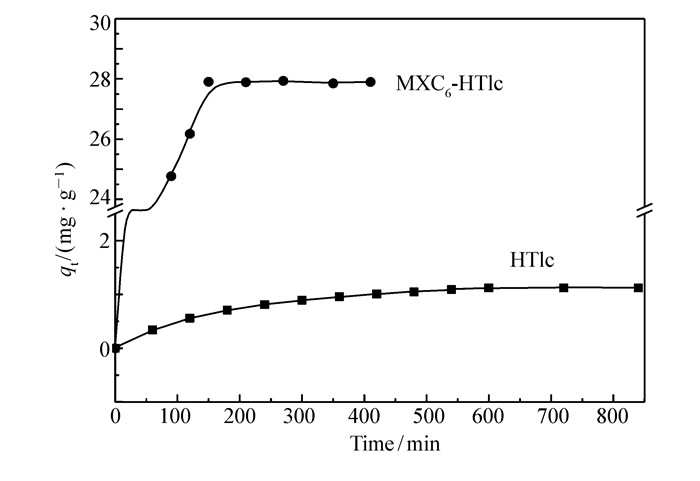
图 3为293 K时HTlc和MXC6-HTlc吸附40 mg/L对甲酚的动力学曲线。由图 3可知,MXC6-HTlc对对甲酚的吸附量显著高于HTlc,表明MXC6-HTlc层间MXC62-离子对吸附起决定性作用。由于HTlc表面和层间均具有强亲水性,对疏水性对甲酚吸附能力较弱,而MXC6-HTlc疏水性增强,吸附能力明显增强。将图 3中实验数据分别带入准一级动力学和准二级动力学方程拟合,求出平衡吸附量(qe, cal)和相关系数(R2),结果见表 2。
 表 2
准一级和准二级动力学模型对HTlc和MXC6-HTlc吸附对甲酚动力学数据拟合参数
Table 2.
Parameters obtained from pseudo-first-order and pseudo-second-order kinetic models for p-cresol adsorption on HTlc and MXC6-HTlc
表 2
准一级和准二级动力学模型对HTlc和MXC6-HTlc吸附对甲酚动力学数据拟合参数
Table 2.
Parameters obtained from pseudo-first-order and pseudo-second-order kinetic models for p-cresol adsorption on HTlc and MXC6-HTlc
Adsorbent qe, exp/(mg·g-1) Pseudo-first-order Pseudo-second-order k1/min-1 qe, cal/(mg·g-1) R2 k2/(g·mg-1·min-1) qe, cal/(mg·g-1) R2 HTlc 1.12 0.005 6 1.13 0.994 1 0.003 3 1.49 0.909 9 MXC6-HTlc 27.93 0.023 8 28.22 0.996 0 0.000 9 1.84 0.9612 准一级动力学方程:
准二级动力学方程:
式中,t为吸附时间(min);qt为t时刻吸附量(mg/g);qe为平衡吸附量(mg/g);k1为准一级速率常数(min-1);k2为准二级速率常数[g/(mg·min)]。
由表 2可知,HTlc和MXC6-HTlc对对甲酚的吸附动力学均符合准一级动力学方程,且所得平衡吸附量(qe, cal)与实验测定平衡吸附量(qe, exp)较接近,表明对甲酚在HTlc和MXC6-HTlc上的吸附均主要表现为物理吸附,这一结果与HTlc和有机-HTlc吸附其它酚类物质的结果相似[6, 14-15]。
2.2.2 pH值对吸附的影响
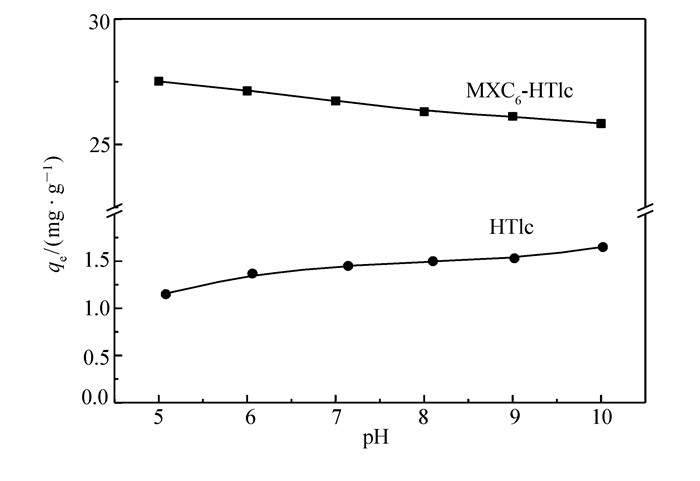
图 4为293 K时HTlc和MXC6-HTlc对对甲酚的吸附量随体系pH值变化曲线。由图 4可知,在实验pH值(5~10)研究范围内,HTlc和MXC6-HTlc的吸附量分别随pH值增加而增加和降低。
2.2.3 温度对吸附的影响
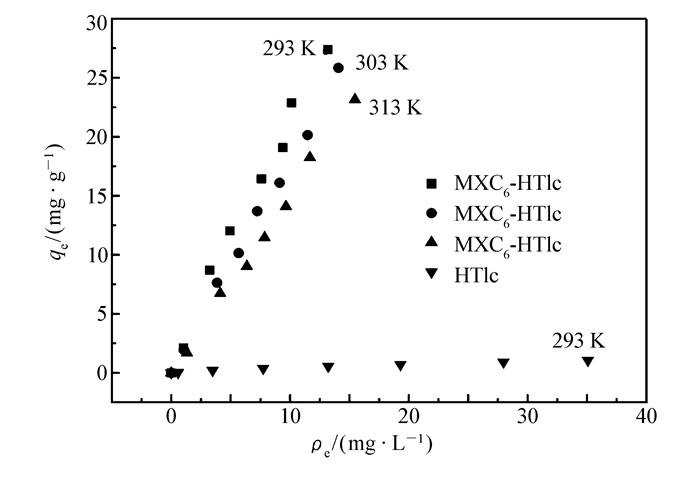
图 5为293 K(和303 K、313 K)时HTlc和MXC6-HTlc吸附对甲酚的等温线。由图 5可知,在相同温度下,HTlc和MXC6-HTlc对对甲酚的平衡吸附量(qe)均随平衡浓度(ρe)增加而增加;在实验温度范围内,对甲酚在MXC6-HTlc上的吸附量随温度升高而降低。将图 5中的数据分别用Langmuir、Freundlich和linear等温方程拟合,结果见表 3。
 表 3
不同温度时MXC6-HTlc吸附对甲酚的等温方程
Table 3.
Adsorption isotherm equations of p-cresol on MXC6-HTlc at different temperatures
表 3
不同温度时MXC6-HTlc吸附对甲酚的等温方程
Table 3.
Adsorption isotherm equations of p-cresol on MXC6-HTlc at different temperatures
Adsorbent T/K Langmuir eq. Freundlich eq. Linear eq. HTlc 293 $ \frac{1}{{{q_{\rm{e}}}}} = 15.54\cdot\frac{1}{{{\rho _{\rm{e}}}}} + 0.58 $
R2=0.9921; qm=1.7 mg/gln qe=0.8127ln ρe-2.73
R2=0.9782qe=0.028ρe+ 0.11
R2=0.9738MXC6-HTlc 293 $\frac{1}{{{q_{\rm{e}}}}} = 0.48\cdot\frac{1}{{{\rho _{\rm{e}}}}}-0.0083 $
R2=0.9914; qm=-120.5 mg/gln qe=0.98ln ρe+0.84
R2=0.9832qe= 2.07ρe+ 0.78
R2=0.9878MXC6-HTlc 303 $ \frac{1}{{{q_{\rm{e}}}}} = 0.55\cdot\frac{1}{{{\rho _{\rm{e}}}}}-0.0012 $
R2=0.9989; qm=-83.3 mg/gln qe=0.99ln ρe+0.63
R2=0.9971qe= 1.79pe+ 0.18
R2=0.9975MXC6-HTlc 313 $ \frac{1}{{{q_{\rm{e}}}}} = 0.81\cdot\frac{1}{{{\rho _{\rm{e}}}}}-0.018 $
R2=0.9943; qm=-55.6 mg/gln qe=1.06ln ρe+0.27
R2=0.9930qe=1.51ρe-0.12
R2=0.9961Langmuir方程:
Freundlich方程:
Linear方程:
式中,KL(L/mg)、KF(mg(1-1/n)·L1/n/g)和Kd(L/g)为相应的吸附平衡常数;qm(mg/g)为饱和吸附量;n为与吸附有关的常数;a为常数。
由表 3可知,Langmuir方程可最佳拟合293 K时HTlc吸附对甲酚热力学数据,表明对甲酚在HTlc上的吸附为单分子层吸附。Langmuir、Freundlich和Linear方程均可较好拟合对甲酚在MXC6-HTlc上的吸附,但用Langmuir方程拟合所得qm为负值,无意义;Freundlich方程拟合后n值接近1,说明数据更适于用Linear方程描述,表明对甲酚通过分配作用进入MXC6-HTlc层间[16-17],且有较大吸附量,表明吸附量与其相对较小的比表面没有直接关系。在实验温度范围内,Kd值随温度升高而降低,说明MXC6-HTlc对对甲酚的吸附亲和力随温度升高而减小,吸附量随温度升高而降低。
2.3 吸附机理
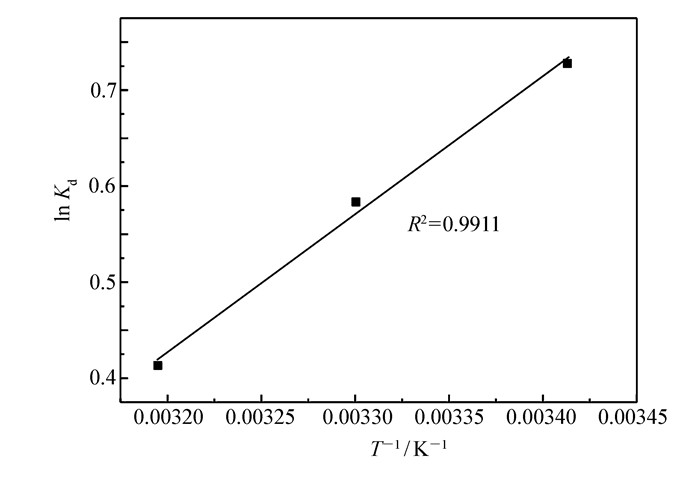
对甲酚在HTlc上吸附的主要原因:HTlc层板带正电,对甲酚在实验pH值下部分解离带负电,二者静电吸引,产生物理吸附,由于对甲酚解离度随pH值增加而增加,故吸附量也随之增加(图 4)。对甲酚在MXC6-HTlc上吸附的主要驱动力:MXC6-HTlc层间具有MXC62-离子形成的疏水区,根据相似相溶原理,对甲酚可通过分配作用进入MXC6-HTlc层间疏水区(物理吸附),使吸附量显著提升(图 5)。随pH值增加,对甲酚离子增多,亲水性增强,吸附量降低(图 4)。以Linear方程的ln Kd对1/T作图(
$ \ln {K_{\rm{d}}} =-\frac{{\Delta H}}{R}\cdot\frac{1}{T} + \frac{{\Delta S}}{R} $ ),结果如图 6。由图 6可知,ln Kd与1/T呈较好的线性关系(R2=0.9911),由直线斜率求得吸附过程焓变ΔH为-11.97 kJ/mol;由直线截距求得吸附过程熵变ΔS为-34.75 J/(mol·K)。说明吸附为放热、熵减的过程,随温度升高,吸附量降低。3 结论
通过剥离-重组法制备了MXC6-HTlc纳米复合材料,实现了对水中对甲酚的有效吸附。MXC6-HTlc对对甲酚的吸附影响因素主要有溶液的pH值、初始浓度、吸附时间和温度;吸附动力学较好地符合准一级动力学方程,Linear方程能较好地描述吸附过程,即对甲酚可通过分配作用进入MXC6-HTlc层间疏水区,且吸附为放热、熵减小的过程。
-
-
[1]
Ahmaruzzaman M. Adsorption of Phenolic Compounds on Low-Cost Adsorbents:A Review[J]. Adv Colloid Interface Sci, 2008, 143(1/2): 48-67.
-
[2]
QU J. Research Progress of Novel Adsorption Processes in Water Purification:A Review[J]. J Environ Sci-China, 2008, 20(1/2): 1-13.
-
[3]
Miyata S. Anion-Exchange Properties of Hydrotalcite-Like Compounds[J]. Clay Clay Miner, 1983, 31(4): 305-311. doi: 10.1346/CCMN
-
[4]
Williams G R, O'Hare D. Towards Understanding, Control and Application of Layered Double Hydroxide Chemistry[J]. J Mater Chem, 2006, 16(30): 3065-3074. doi: 10.1039/b604895a
-
[5]
Chuang Y H, Tzou Y M, Wang M K. Removal of 2-Chlorophenol from Aqueous Solution by Mg/Al Layered Double Hydroxide(LDH) and Modified LDH[J]. Ind Eng Chem Res, 2008, 47(11): 3813-3819. doi: 10.1021/ie071508e
-
[6]
Chaara D, Bruna F, Ulibarri M A. Organo/Layered Double Hydroxide Nanohybrids Used to Remove Nonionic Pesticides[J]. J Hazard Mater, 2011, 196(1): 350-359.
-
[7]
Chuang Y H, Liu C H, Tzou Y M. Comparison and Characterization of Chemical Surfactants and Bio-surfactants Intercalated with Layered Double Hydroxides(LDHs) for Removing Naphthalene from Contaminated Aqueous Solutions[J]. Colloids Surf A, 2010, 366(1/2/3): 170-177.
-
[8]
Gao Z Y, Du B, Zhang G Y. Adsorption of Pentachlorophenol from Aqueous Solution on Dodecylbenzenesulfonate Modified Nickel-Titanium Layered Double Hydroxide Nanocomposites[J]. Ind Eng Chem Res, 2011, 50(9): 5334-5345. doi: 10.1021/ie101766e
-
[9]
水玲玲, 郑利强, 刘少杰. 双子表面活性剂的研究进展[J]. 日用化学工业, 2001,31,(2): 28-31. SHUI Lingling, ZHENG Liqiang, LIU Shaojie. The Research Progression of Gemini Surfactants[J]. China Surfact Deterg Cosemet, 2001, 31(2): 28-31.
-
[10]
Qiu D P, Hou W G. Synthesis and Characterization of Indole-3-butyric Acid/Hydrotalcite-Like Compound Nanohybrids[J]. Chinese J Chem, 2009, 27(10): 1879-1885. doi: 10.1002/cjoc.v27:10
-
[11]
Cavani F, Trifiro F, Vaccari A. Hydrotalcite-type Anionic Clays:Preparation, Properties and Applications[J]. Catal Today, 1991, 11(2): 173-301. doi: 10.1016/0920-5861(91)80068-K
-
[12]
Wang J, Zhou J, Li Z. Magnetic, Luminescent Eu-doped Mg-Al Layered Double Hydroxide and Its Intercalation for Ibuprofen[J]. Chem Eur J, 2010, 16(48): 14404-14411. doi: 10.1002/chem.201000602
-
[13]
You Y, zhao H, Vance G F. Surfactant-enhanced Adsorption of Organic Compounds by Layered Double Hydroxides[J]. Colloids Surf A, 2002, 205(3): 161-172. doi: 10.1016/S0927-7757(01)01137-2
-
[14]
Li Y, Bi H, Jin Y. Facile Preparation of Rhamnolipid-layered Double Hydroxide Nanocomposite for Simultaneous Adsorption of p-Cresol and Copper Ions from Water[J]. Chem Eng J, 2017, 308(1): 78-88.
-
[15]
Zaghouane-Boudiafa H, Boutahala M, Tiar C. Treatment of 2, 4, 5-Trichlorophenol by MgAl-SDBS Organo-Layered Double Hydroxides:Kinetic and Equilibrium Studies[J]. Chem Eng J, 2011, 173(1): 36-41. doi: 10.1016/j.cej.2011.07.032
-
[16]
You Y, Zhao H T, Vance G F. Hybrid Organic-Inorganic Derivatives of Layered Double Hydroxide and Dodecylbenzenesulfonate:Preparation and Adsorption Characteristics[J]. J Mater Chem, 2002, 12(4): 907-912. doi: 10.1039/b106811c
-
[17]
Chiou C T, Peters L J, Freed V H. A Physical Concept of Soil-Water Equilibria for Nonionic Organic Compounds[J]. Science, 1979, 206(4420): 831-832. doi: 10.1126/science.206.4420.831
-
[1]
-
图 2 HTlc和MXC6-HTlc的XRD图谱(内插图为MXC6-HTlc的小角衍射图谱)(A);MXC6在MXC6-HTlc层间取向模拟(B);HTlc和MXC6-HTlc的FTIR图谱图(C)
Figure 2 Powder XRD spectra of HTlc and MXC6-HTlc(Inset is the small angle diffraction pattern of MXC6-HTlc)(A); simulation of the orientation of MXC6 in MXC6-HTlc(B); FTIR spectra of HTlc and MXC6-HTlc(C)
表 1 HTlc和MXC6-HTlc样品的比表面积和元素分析以及MXC6-HTlc中MXC6的插入量
Table 1. Specific surface areas and chemical analysis results of HTlc and MXC6-HTlc, and the intercalated amount of MXC6 in MXC6-HTlc
Sample Specific surface area/(m2·g-1) n(Mg):n(Al) n(Al):n(MXC6) Intercalated amount of w(MXC6)/% HTlc 18.75 2.64:1 - - MXC6 11.71 2.57:1 1:0.83 57.7 表 2 准一级和准二级动力学模型对HTlc和MXC6-HTlc吸附对甲酚动力学数据拟合参数
Table 2. Parameters obtained from pseudo-first-order and pseudo-second-order kinetic models for p-cresol adsorption on HTlc and MXC6-HTlc
Adsorbent qe, exp/(mg·g-1) Pseudo-first-order Pseudo-second-order k1/min-1 qe, cal/(mg·g-1) R2 k2/(g·mg-1·min-1) qe, cal/(mg·g-1) R2 HTlc 1.12 0.005 6 1.13 0.994 1 0.003 3 1.49 0.909 9 MXC6-HTlc 27.93 0.023 8 28.22 0.996 0 0.000 9 1.84 0.9612 表 3 不同温度时MXC6-HTlc吸附对甲酚的等温方程
Table 3. Adsorption isotherm equations of p-cresol on MXC6-HTlc at different temperatures
Adsorbent T/K Langmuir eq. Freundlich eq. Linear eq. HTlc 293 $ \frac{1}{{{q_{\rm{e}}}}} = 15.54\cdot\frac{1}{{{\rho _{\rm{e}}}}} + 0.58 $
R2=0.9921; qm=1.7 mg/gln qe=0.8127ln ρe-2.73
R2=0.9782qe=0.028ρe+ 0.11
R2=0.9738MXC6-HTlc 293 $\frac{1}{{{q_{\rm{e}}}}} = 0.48\cdot\frac{1}{{{\rho _{\rm{e}}}}}-0.0083 $
R2=0.9914; qm=-120.5 mg/gln qe=0.98ln ρe+0.84
R2=0.9832qe= 2.07ρe+ 0.78
R2=0.9878MXC6-HTlc 303 $ \frac{1}{{{q_{\rm{e}}}}} = 0.55\cdot\frac{1}{{{\rho _{\rm{e}}}}}-0.0012 $
R2=0.9989; qm=-83.3 mg/gln qe=0.99ln ρe+0.63
R2=0.9971qe= 1.79pe+ 0.18
R2=0.9975MXC6-HTlc 313 $ \frac{1}{{{q_{\rm{e}}}}} = 0.81\cdot\frac{1}{{{\rho _{\rm{e}}}}}-0.018 $
R2=0.9943; qm=-55.6 mg/gln qe=1.06ln ρe+0.27
R2=0.9930qe=1.51ρe-0.12
R2=0.9961 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 5
- 文章访问数: 1479
- HTML全文浏览量: 139


 下载:
下载:





 下载:
下载:

