 图 图式1
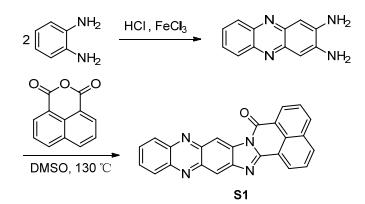
荧光传感器分子S1的合成路线
Figure 图式1.
Synthetic route of the fluorescence chemosensor S1
图 图式1
荧光传感器分子S1的合成路线
Figure 图式1.
Synthetic route of the fluorescence chemosensor S1

Citation: Li Xiang, Lin Qi, Qu Wenjuan, Li Qiao, Chen Xiaobin, Li Wenting, Zhang Youming, Yao Hong, Wei Taibao. A Novel Imidazophenazine Lactam Reaction Type Recognition Cyanide Ion Fluorescence Probe[J]. Chinese Journal of Organic Chemistry, 2017, 37(4): 889-895. doi: 10.6023/cjoc201611008

一种咪唑并吩嗪内酰胺反应型识别氰离子的荧光探针
English
A Novel Imidazophenazine Lactam Reaction Type Recognition Cyanide Ion Fluorescence Probe
-
Key words:
- phenazine derivative
- / fluorescence sensor
- / detecting anions
-
吩嗪及其衍生物组成了一大类含氮杂环化合物[1], 它们广泛存在于自然界中, 对这类天然产物的分离鉴别以及合成研究一直受到学者的关注[2].就合成方法而言, 它们可以由各种各样的细菌产生, 也可以由人工合成, 具有合成简单、易于修饰等特点.吩嗪衍生物具有较大的共轭系统, 荧光量子产率较高、发射谱带较窄、斯托克斯位移较大、最大吸收与发射波长在可见光区, 并且, 易于被质子化具有一定的电子接受能力[3, 4].因而吩嗪类化合物被广泛应用于生物、医学及有机光电材料领域中[5~7].近年来, 吩嗪衍生物在超分子化学领域应用也受到关注, 研究者们发现吩嗪具有良好的荧光发色基团, 可用于对阳离子、阴离子和中性分子的识别基团[8, 9].因此研究吩嗪类化合物在有机荧光离子识别传感器方面的新应用具有重要意义.
荧光传感器是能够将分子识别事件通过分子的荧光信号有效表达出来的分子器件[10~15].近年来, 氰化物荧光传感器已经发展成为超分子化学中最为活跃的研究领域之一[16~18].由于氰化物具有很强的毒性, 因此对我们的生存环境造成了巨大危害[19].例如:工业纤维制造, 黄金提取和电镀过程中所排放的含氰废水、废气, 以及在杀虫剂和除草剂中所排放和使用的氰化物, 都对我们日常饮食、饮水以及大气造成严重污染[20~22]; 甚至, 汽车尾气和烟草燃烧时产生的烟雾中也都含有氰化物[23].据测量:人在吸烟时, 血液中的氰化物含量会显著升高[24].此外, 一些食物当中也含有氰化物.例如:木薯、发芽土豆、苦杏仁以及一些水果的种子当中[25, 26].少量的氰根离子可以与人体血红细胞结合进而在短时间内使人窒息死亡[27].根据世界卫生组织 (WHO) 规定, 日常饮用水中CN-含量不得高于1.9 µmol•L-1[28, 29].因此, 合成简单、高选择性、高灵敏度的氰化物荧光传感器显得十分重要, 长期以来受到研究者们的重视.
此外, 为了解决荧光传感器分子在实际应用过程中存在的一些问题, 拓展其应用范围, 通过物理或化学方法将荧光传感器分子固载到固体材料上是离子荧光化学传感器发展成为新型实用型材料的一种有效方法.这种方法可以将高选择性、高灵敏度、可视化等优良性能的荧光传感器分子与载体材料的特性相结合, 从而实现荧光材料在离子识别、吸附和生物应用的多功能化、高性能化以及检测过程的可视化[30].鉴于此, 在我们多年来研究超分子化学及分子离子识别的基础上[31~41], 通过2, 3-二氨基吩嗪与1, 8-萘二甲酸酐反应, 合成了一种新型咪唑并吩嗪内酰胺荧光传感器S1, 研究了其阴离子识别性能, 结果发现, 其对CN-具有专一选择性识别功效, 是一种反应型识别CN-的荧光传感器分子.此外, 我们将它负载于固态硅胶之上, 这种负载了荧光传感器分子S1的固体材料不仅对固体的NaCN具有比色识别效果, 而且对纯水相中的氰根离子也有同样的效果, 是一种检测的新材料.
1 结果与讨论
1.1 荧光传感器分子的构筑
荧光传感器分子S1是以2, 3-二氨基吩嗪为母体, 1, 8-萘二酸酐为修饰基团的荧光分子. Scheme 1为荧光传感器分子S1的合成路线.
1.2 反应条件探索
根据文献报道, 邻苯二胺可以与环状酸酐或二元酰氯等酰化试剂反应, 得到不同的环状产物, 其中有:苯并咪唑, 环状内酰胺以及苯并咪唑的N-酰化内酰胺类化合物等产物[42~47].为此我们对邻苯二胺与1, 8-萘二酸酐的反应条件进行了考察, 结果见表 1.
Entry Molar ratioa t/℃ t/h Solvent Yield% 1 1:1.0 80 8 DMF 22.2 2 1:1.2 80 8 DMF 29.0 3 1:1.5 80 8 DMF 30.5 4 1:1.2 100 8 DMF 34.1 5 1:1.2 120 8 DMF 43.3 6 1:1.2 130 8 DMF 44.3 7 1:1.2 130 12 DMF 49.5 8 1:1.2 130 18 DMF 56.7 9 1:1.2 130 24 DMF 60.2 10 1:1.2 130 24 DMSO 63.4 a n(2, 3-二氨基吩嗪):n(1, 8-萘二酸酐). 表 1 反应条件的优化
Table 1. Optimization of reaction conditions首先考察了投料比对产率的影响.由表 1可以看出, 随着1, 8-萘二酸酐的物质的量增大, 反应产物的产率逐渐升高 (表 1, Entries 1~3).然而, 当2, 3-二氨基吩嗪与1, 8-萘二酸酐的物质的量比为1:1.5时, 相较1:1.2倍时, 产率只提高了1%左右.在产率提高不是很大的情况下, 考虑到成本控制的因素, 选取2, 3-二氨基吩嗪与1, 8-萘二酸酐的物质的量比为1:1.2.升高温度同样有利于产物的生成 (表 1, Entries 2, 4~6), 但考虑到实验室安全问题, 没有继续提升温度, 只选择反应温度为130 ℃.之后, 又对反应时间进行考察, 当反应时间为24 h时, 产率最高 (表 1, Entries 6~9).最后将溶剂由DMF换为DMSO发现产率有所提高 (表 1, Entries 9, 10).
最终确定合成S1的最佳反应条件为: 2, 3-二氨基吩嗪与2, 3-二氨基吩嗪的物质的量比为1:1.2, 温度为130 ℃, 反应时间为24 h, 溶剂为DMSO.
1.3 含水量对传感器分子S1荧光的影响
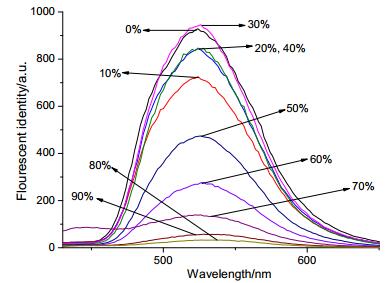
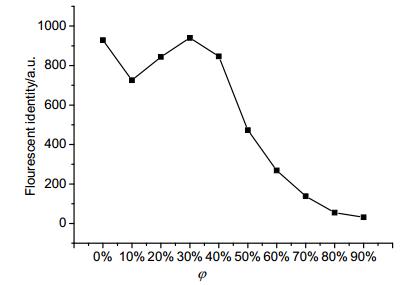
不同的含水量对荧光传感器分子的荧光具有较大影响.含水量对传感器分子S1的荧光强度影响如图 1和图 2所示.从图中可以看到, 当含水量从0%增加到10%时, S1的荧光强度随溶液中含水量的增加而减弱.此时水的加入使S1产生堆积, 但这种堆积较为无序, 因此导致荧光减弱[48, 49].当含水量从10%增加到30%时, S1的荧光强度随溶液中含水量的增加而增强[50, 51].此时的S1堆积相对较为有序, 进而产生聚集态荧光, 因此导致荧光增强.当含水量从30%增加到90%时, S1的荧光强度随溶液中含水量的增加而减弱, 直到猝灭.说明此时大量的水使得S1发生了水解, 导致荧光猝灭.
1.4 荧光传感器分子S1对CN-的识别
由以上结果可以看出, 含水量对传感器分子S1荧光的影响较大.为了尽量减免这种影响, 将荧光传感器分子S1配制成浓度为2.0×10-5 mol/L的DMSO溶液, 并分别向其中加入50倍化学计量的各种阴离子 (F-, Cl-, Br-, I-, AcO-, H2PO4 -, HSO4-, ClO4-, CN-和SCN-).当加入F-, AcO-和H2PO4三种离子时, 对传感器分子S1的溶液有轻微的影响, 而CN-的加入使溶液颜色变化明显, 如图 3所示.说明传感器分子S1在自然光条件下对CN-不具有十分良好的专一选择性.然后我们进行了荧光测定, 其荧光光谱图见图 4.可以看出, S1在524 nm处出现了一个明显的宽荧光发射峰 (λex=385 nm).当加入CN-时, 524 nm处的荧光发射峰大幅度降低并发生红移.此外, 除SCN-离子的加入使得S1荧光光谱略微减弱, 其它阴离子 (F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-和ClO4-) 的加入对S1溶液的荧光强度几乎没有改变, 相应的在三用紫外分析仪下可以裸眼观察到加入CN-后, 溶液的荧光颜色由亮黄色变为橘红色, 而其它阴离子的对溶液荧光颜色没有影响 (图 5).这说明传感器分子S1对CN-具有很好的专一选择性, 可以实现在DMSO溶液中对CN-的专一选择性识别.
 图 3
在传感器分子S1 (c=2.0×10-5 mol/L) 的DMSO溶液中分别加入不同阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的照片
Figure 3.
Photograph of chemosensor S1 (c=2.0×10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F -, Cl -, Br - , I - , AcO -, H2 PO 4 -, HSO4-, ClO4-, CN- and SCN-(c=1.0×10-2 mol/L)
图 3
在传感器分子S1 (c=2.0×10-5 mol/L) 的DMSO溶液中分别加入不同阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的照片
Figure 3.
Photograph of chemosensor S1 (c=2.0×10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F -, Cl -, Br - , I - , AcO -, H2 PO 4 -, HSO4-, ClO4-, CN- and SCN-(c=1.0×10-2 mol/L)
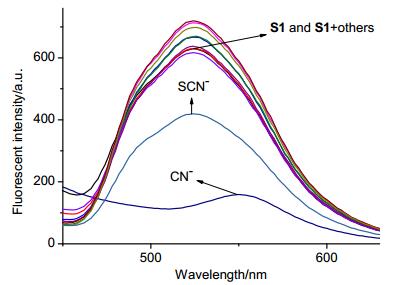 图 4
在传感器分子S1 (c=2.0×10-5 mol/L) 的DMSO溶液中分别加入50倍化学计量的各种阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的荧光发射光谱
Figure 4.
Fluorescence emission spectrum of chemosensor S1
(c=2.0×10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN- and SCN- (c=1.0× 10-2 mol/L)
图 4
在传感器分子S1 (c=2.0×10-5 mol/L) 的DMSO溶液中分别加入50倍化学计量的各种阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的荧光发射光谱
Figure 4.
Fluorescence emission spectrum of chemosensor S1
(c=2.0×10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN- and SCN- (c=1.0× 10-2 mol/L)
 图 5
在传感器分子S1的 (c=2.0×10-5 mol/L) DMSO溶液中分别加入不同阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的比色效果图
Figure 5.
Colorimetric renderings of chemosensor S1 (c=2.0× 10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN - and SCN - (c = 1.0 × 10 - 2 mol/L)
图 5
在传感器分子S1的 (c=2.0×10-5 mol/L) DMSO溶液中分别加入不同阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的比色效果图
Figure 5.
Colorimetric renderings of chemosensor S1 (c=2.0× 10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN - and SCN - (c = 1.0 × 10 - 2 mol/L)
1.5 荧光传感器分子S1对选择性识别CN﹣的抗干扰实验
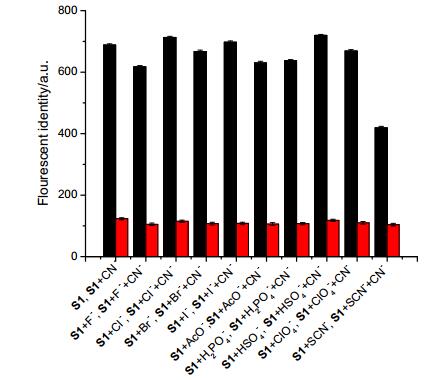
抗干扰性能对荧光离子传感器选择性识别来说, 是一个非常重要的指标.为了研究传感器分子S1对CN-选择性识别的抗干扰能力, 我们做了如下抗干扰实验:将50倍化学计量的F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-和SCN-分别加入到传感器分子S1的溶液中, 进行荧光光谱测定, 结果发现, 除了SCN-的加入使得S1溶液荧光略微降低, 其余阴离子的加入对S1溶液荧光强度几乎没有影响.再将等量的CN-分别加入到上述体系中, 此时溶液在524 nm处的荧光强度降低.取最大荧光发射峰处 (524 nm) 的数据作柱状抗干扰图 (图 6, λex=385 nm).从图 6可以看出, 传感器分子S1对CN-的识别在其它阴离子加入后没有受到影响, 说明传感器分子S1对CN-的识别具有良好的抗干扰能力.
1.6 荧光传感器分子S1识别CN-的机理探讨
为了初步探讨传感器分子对CN-的识别机理, 我们对荧光传感器分子S1和S1+CN-做了荧光光谱对比, 发现当CN-加入后, 传感器分子S1在524 nm处的最大发射峰明显降低并且发生红移.通过质谱检测发现:在S1+NaCN体系中, 从质谱图上可以得到在413.2237处出现了[M+H]+分子离子峰, 通过分析我们认为是由荧光传感器分子S1与CN-进行亲核加成反应生成相应的酰基氰, 后者不稳定, 进一步水解, 生成相应的羧酸, 进而转为相应的钠盐, 该钠盐的分子量为412.3838.
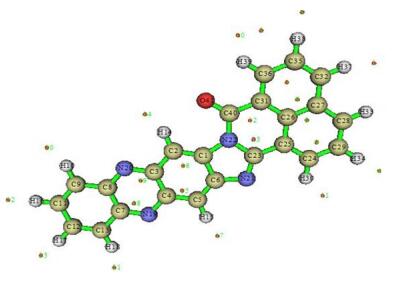
为了进一步弄清楚传感器分子对CN-的识别机理, 根据量子化学计算对传感器分子S1做了分子表面静电势分析 (图 7).结果显示:荧光传感器分子S1表面静电势负值的极大点在羰基C原子附近, 其值为-1.84 eV.说明荧光传感器分子S1的羰基碳原子不稳定、反应活性高, 容易发生亲核加成反应导致开环.
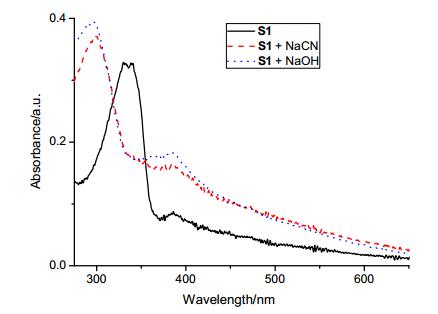
为了进一步证明氰根加成产物为加成水解产物, 分别对荧光传感器分子S1, S1+NaCN和S1+NaOH进行了紫外对比实验 (图 8).从紫外对比图中可以看到, S1+ NaCN和S1+NaOH的紫外吸收峰相似, 说明S1+ NaCN和S1+NaOH体系中有相同的物质产生, S1的碱性水解产物为开环的羧酸钠盐.
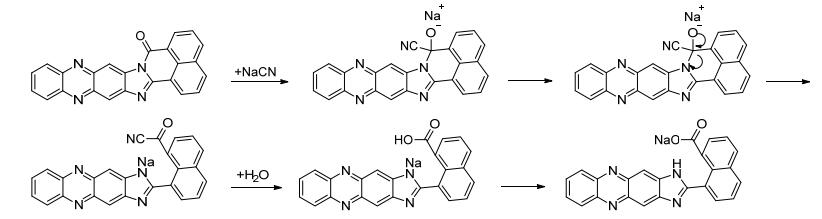
根据以上各实验, 我们认为荧光传感器分子S1识别CN-机理, 如Scheme 2所示:首先由CN-对传感器分子S1羰基位亲核加成, C—N键断裂生成酰基氰, 后者不稳定发生水解生成羧酸, 最后羧基氢与氮上的钠离子发生交换生成相应的钠盐.
1.7 荧光传感器分子S1对CN-的最低检测限与荧光量子产率的测定
在室温条件下, 我们通过向传感器分子S1的DMSO溶液加入不同浓度的CN-后, 测定荧光光谱的变化, 并利用3sB/S[52]计算其最低检测限, 得到荧光光谱的最低检测限为9.96×10-7 mol/L.这一数值低于世界卫生组织 (WHO) 所规定的饮用水中氰离子的含量 (<1.9×10-6 mol/L).通过与表 3中已报道的CN-探针最低检测限比较, 发现S1对CN-的检测具有检测限较低的优点, 有一定的实际应用价值.此外, 我们以硫酸奎宁做标准参比物, 对S1与CN-反应前后的荧光量子产率做了测定[53].其荧光量子产率分别为0.701和0.211, 说明S1与CN-反应后荧光量子产率明显降低.
1.8 负载S1的固体材料制备及其应用
为了使荧光传感器分子S1识别CN-能够在实际中得到更加简便易行的应用, 我们将S1固载于硅胶上, 并用于固体NaCN识别和NaCN水溶液的识别:称取0.0054 g荧光传感器分子S1, 然后加入到0.6 g硅胶 (100~200目, 无色粉末) 中, 倒入研钵研磨, 直到研磨均匀后倒出三分之一固体粉末, 我们可以观察到此时固体粉末为淡黄色, 在365 nm三用紫外分析仪下发出亮黄色荧光.再从研钵中倒出三分之一粉末, 加入0.0024 g NaCN后继续研磨, 使其充分被研磨后, 倒出粉末, 我们可以观察到粉末颜色略微变化, 相应的在365 nm三用紫外分析仪下荧光由黄色变为红色 (图 9).很显然荧光传感器分子S1可以识别固体NaCN.最后, 向研钵中剩余的三分之一粉末中, 加入NaCN水溶液, 接着在365 nm三用紫外分析仪下观察荧光颜色, 发现相应的荧光颜色变为红色, 说明该固体材料可以直接识别水相中的氰根离子.
2 结论
本文利用简便方法合成了一种新型荧光传感器分子S1, 对其合成条件进行了优化.然后研究了S1在DMSO中的荧光光谱性质及其对CN-的荧光识别响应性.研究结果表明:当加入不同种类的阴离子后, 只有CN-离子使溶液的荧光颜色由黄色变为橘红色, 表现出专一选择性识别效果.同时, 抗干扰实验结果显示, S1具有良好的抗干扰性能.在这些实验结果的基础上, 我们探讨了S1识别CN-的机理, 以及传感器分子S1对CN-的荧光光谱最低检测限, 发现S1识别CN-是一种新的反应型识别机理, 其最低检测限为9.96×10 - 7 mol/L.最后将其负载于硅胶上, 制备了一种新型固体识别材料, 该材料不仅可以识别固体NaCN, 而且可以识别纯水相中的CN-根离子, 为氰根离子的识别提供了行之有效的新方法, 具有一定的实际应用价值.
3 实验部分
3.1 仪器与试剂
邻苯二胺、浓盐酸、浓硫酸、硫酸奎宁、FeCl3•6H2O、氢氧化钠、1, 8-萘二酸酐、乙醇、氮氮二甲基甲酰胺 (DMF)、二甲基亚砜 (DMSO) 均为阿拉丁分析纯级试剂.
1 H NMR使用Mercury-600BB型核磁共振仪测定, TMS为内标; IR使用Digilab FTS-3000 FT-IR型红外光谱仪 (KBr压片) 测定; 熔点使用X-4数字显示显微熔点测定仪测定 (温度计未校正); 三用紫外分析仪 (上海安亭电子仪器厂); 紫外光谱使用日本岛津UV-2550紫外-可见吸收光谱仪测定, 测量使用光程为1 cm的石英比色皿; 荧光光谱使用RF-5301型荧光光谱仪 (日本Shimadzu公司); ZAB-HS型质谱仪 (英国VG公司).
3.2 实验方法
3.2.1 2, 3-二氨基吩嗪的合成
将50 mmol邻苯二胺 (5.4 g) 加入500 mL的圆底烧瓶中.然后, 将8.33 mL浓盐酸稀释于250 mL蒸馏水中, 将此稀释后的盐酸溶液加入到500 mL的圆底烧瓶中, 电磁搅拌使邻苯二胺完全溶解.将58 g FeCl3•6H2O溶解于75 mL蒸馏水中, 然后, 用滴液漏斗缓慢滴加至上述溶液当中 (有红色沉淀生成).滴加完毕后, 室温搅拌反应24 h.待反应结束后, 抽滤, 并用3 mol/L的盐酸溶液洗涤固体3~5次 (洗去FeCl3和未反应的邻苯二胺), 将所得的红色固体溶于250 ml沸水中, 再加入75 mL 2 mol/L的NaOH溶液, 产生黄色沉淀, 搅拌15 min左右, 沉降1 h, 待溶液冷却至室温, 抽滤得到橘黄色沉淀.将所得沉淀用蒸馏水洗涤2~3次, 烘干.得2, 3-二氨基吩嗪[58], 产率75%. m.p.>300 ℃.
3.2.2 荧光传感器分子S1的合成及结构表征
将0.2216 g (1.0 mmol) 2, 3-二氨基吩嗪和0.2453 g (1.2 mmol) 1, 8-萘二甲酸酐置于50 mL圆底烧瓶中, 加入20 mL DMSO后, 搅拌, 使其完全溶解.将此混合溶液于130 ℃油浴锅中, 加热, 回流24 h.待反应结束后, 将反应瓶冷却至室温, 抽虑, 得到褐色沉淀, 用热的乙醇溶液洗涤沉淀2~3次, 烘干, 得到产物S1, 产率为63.4%. m.p.>300 ℃; 1H NMR (DMSO-d6, 600 MHz) δ: 8.67~8.45 (d 2H, ArH), 8.00~7.80 (m 4H, ArH), 8.67~ 8.45 (m 6H, ArH); 13C NMR (DMSO-d6, 150 MHz) δ: 162.73, 161.14, 135.82, 132.89, 127.99, 119.48; IR (KBr) v: 1771, 1739, 1580, 1510, 1304, 1500 cm-1; HRMS calcd for C24H13N4O [M+H]+ 372.1011, found 373.1084.
辅助材料 (Supporting Information) S1的核磁氢谱、核磁碳谱及高分辨质谱.这些材料可以免费从本刊网站 (http://sioc-journal.cn/) 上下载.
-
-
[1]
Chen, J.-J.; Chen, W.; He, H.; Li, D.-B.; Li, W.-W.; Xiong, L.; Yu, H.-Q. Environ. Sci. Technol. 2013, 47, 1033. doi: 10.1021/es304189t
-
[2]
Ahuja, E. G.; Janning, P.; Mentel, M.; Graebsch, A.; Breinbauer, R.; Hiller, W.; Costisella, B.; Thomashow, L. S.; Mavrodi, D. V.; Blankenfeldt, W. J. Am. Chem. Soc. 2008, 130, 17053. doi: 10.1021/ja806325k
-
[3]
Yang, L.; Li, X.; Qu, Y.; Qu, W.-S.; Zhang, X.; Hang, Y.-D.; Agren, H.; Hua, J.-L. Sen. Actuators, B 2014, 203, 833. doi: 10.1016/j.snb.2014.07.045
-
[4]
Gu, P.-Y.; Zhao, Y.-B.; He, J.-H.; Zhang, J.; Wang, C.-Y.; Xu, Q.-F.; Lu, J.-M.; Sun, X.-W.; Zhang, Q.-C. J. Org. Chem. 2015, 80, 3030. doi: 10.1021/jo5027707
-
[5]
陈薇, 苏建华, 田禾, 中国科学:化学, 2016, 46, 325.Chen, W.; Su, J.-H, ; Tian, H. Sci. China: Chem. 2016, 46, 325 (in Chinese).
-
[6]
Zhou, H.-T.; Sun, L.; Chen, W.; Tian, G.-J.; Chen, Y.; Li, Y.-R.; Su. J.-H. Tetrahedron 2016, 72, 2300. doi: 10.1016/j.tet.2016.03.036
-
[7]
Metz, A. E.; Podlesny, E. E.; Carroll, P. J.; Klinghoffer, A. N.; Kozlowski, M. C. J. Am. Chem. Soc. 2014, 136, 10601. doi: 10.1021/ja506137j
-
[8]
Aggarwal, K.; Khurana, J. M. J. Lumin. 2015, 167, 146. doi: 10.1016/j.jlumin.2015.06.027
-
[9]
Wei, T.-B.; Wu, G.-Y.; Shi, B.-B.; Lin, -Q.; Yao, H.; Zhang, Y.-M. Chin. J. Chem. 2014, 32, 1238. doi: 10.1002/cjoc.v32.12
-
[10]
张鹏, 张有明, 林奇, 姚虹, 魏太保, 有机化学, 2014, 34, 1300. http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtmlZhang, P.; Zhang, Y.-M.; Lin, Q.; Yao, H.; Wei, T.-B. Chin. J. Org. Chem. 2014, 34, 1300 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtml
-
[11]
李长伟, 杨栋, 尹兵, 郭媛, 有机化学, 2016, 36, 787. http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtmlLi, C.-W.; Yang, D.; Yin, B.; Guo, Y. Chin. J. Org. Chem. 2016, 36, 787 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtml
-
[12]
高冠斌, 龚德君, 张明曦, 孙涛垒, 化学学报, 2016, 74, 363.Gao, G.-B.; Gong, D.-J.; Zhang, M.-X.; Sun, T.-L. Acta. Chim. Sinica. 2016, 74, 363 (in Chinese).
-
[13]
张应鹏, 尤彩霞, 杨云裳, 刘小育, 郭慧琛, 董玉莹, 有机化学, 2016, 36, 1401. http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtmlZhang, Y.-P.; You, C.-X.; Yang, Y.-S.; Liu, X.-Y.; Guo, H.-C.; Dong, Y.-Y. Chin. J. Org. Chem. 2016, 36, 1401 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtml
-
[14]
苏娜, 杨美盼, 孟文斐, 杨秉勤, 有机化学, 2015, 35, 175. http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtmlSu, N.; Yang, M.-P.; Meng, W.-P.; Yang, B.-Q. Chin. J. Org. Chem. 2015, 35, 175 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtml
-
[15]
于海波, 李红玲, 张新富, 肖义, 方沛菊, 吕春娇, 侯伟, 化学学报, 2015, 73, 450.Yu, H.-B.; Li, H.-L.; Zhang, X.-F.; Xiao, Y.; Fang, P.-J.; Lü, C.-J.; Hou, W. Acta Chim. Sinica 2015, 73, 450 (in Chinese).
-
[16]
Zang, L.-B.; Wei, D.-Y.; Wang, S.-C.; Jiang, S.-M. Tetrahedron 2012, 68, 636. doi: 10.1016/j.tet.2011.10.105
-
[17]
Gupta, A. S.; Garg, A.; Paul, K.; Luxami, V. J. Lumin. 2016, 173, 165. doi: 10.1016/j.jlumin.2016.01.009
-
[18]
Jo, J. Y.; Olasz, A.; Chen, C. H.; Lee, D. J. Am. Chem. Soc. 2013, 135, 3620. doi: 10.1021/ja312313f
-
[19]
Yan, L.-R.; Yang, M.-P.; Leng, X.; Zhang, M.; Long, Y.; Yang, B.-Q. Tetrahedron 2016, 72, 4361. doi: 10.1016/j.tet.2016.05.082
-
[20]
Yoo, M.; Park, S.; Kim, H. J. Sen. Actuators, B 2015, 220, 788. doi: 10.1016/j.snb.2015.06.021
-
[21]
Kim, D.; Na, S.; Y.; Kim, H. J. Sen. Actuators, B 2016, 226, 227. doi: 10.1016/j.snb.2015.11.122
-
[22]
Wang, S. T.; Chir, J. L.; Jhong, Y.; Wu, A. T. J. Lumin. 2015, 167, 413. doi: 10.1016/j.jlumin.2015.06.046
-
[23]
Yang, L.; Li, X.; Yang, J.-B.; Qu, Y.; Hua, J.-L. ACS Appl. Mater. Interfaces 2013, 5, 1317. doi: 10.1021/am303152w
-
[24]
杨林, 张潇, 瞿卫松, 花建丽, 影像科学与光化学, 2014, 32, 1.Yang, L.; Zhang, X.; Qu, W.-S.; Hua, J.-L. Imaging Sci. Photochem. 2014, 32, 1 (in Chinese).
-
[25]
Wang, F.; Wang, L.; Chen, X. Q.; Yoon, J. Y. Chem. Soc. Rev. 2014, 43, 12. doi: 10.1039/C3CS90101G
-
[26]
Dagiliene, M.; Martynaitis, V.; Krisiucniene, V.; Krikstolaityte, S.; Sackus, A. ChemistryOpen 2015, 4, 363. doi: 10.1002/open.v4.3
-
[27]
Wang, K.-N.; Ma, L.; Liu, G.-Q.; Cao, D.-X.; Guan, R.-F.; Liu, Z.-Q. Dyes Pigm. 2016, 126, 104. doi: 10.1016/j.dyepig.2015.11.019
-
[28]
Lee, K. S.; Kim, H. J.; Kim, G. H.; Shin, I.; Hong, J. I. Org. Lett. 2008, 10, 49. doi: 10.1021/ol7025763
-
[29]
El-Shishtawy, R. M.; Al-Zahrani, F. A. M.; Al-amshany, Z. M.; Asiri, A. M. Sen. Actuators, B 2017, 240, 288. doi: 10.1016/j.snb.2016.08.168
-
[30]
孟庆涛, 博士论文, 大连理工大学, 大连, 2011.Meng, Q.-T. Ph.D. Dissertation, Dalian University of Technology, Dalian, 2011 (in Chinese).
-
[31]
Shi, B.-B.; Zhang, P.; Wei, T.-B.; Yao, H.; Lin, Q.; Liu, J.; Zhang, Y.-M. Tetrahedron 2013, 69, 7981. doi: 10.1016/j.tet.2013.07.007
-
[32]
Shi, B.-B.; Zhang, Y.-M.; Wei, T.-B.; Lin, Q.; Yao, H.; Zhang, P.; You, X.-M. Sens. Actuators, B 2014, 190, 555. doi: 10.1016/j.snb.2013.09.043
-
[33]
林奇, 朱鑫, 陈佩, 符永鹏, 张有明, 魏太保, 化学学报, 2013, 71, 1516. doi: 10.7503/cjcu20130108Lin, Q.; Zhu, X.; Chen, P.; Fu, Y. P.; Zhang, Y. M.; Wei, T. B. Acta Chim. Sinica 2013, 71, 1516 (in Chinese). doi: 10.7503/cjcu20130108
-
[34]
Gao, G.-Y.; Qu, W.-J.; Shi, B.-B.; Lin, Q.; Yao, H.; Yang, W.-L.; Zhang, Y.-M.; Wei, T.-B. Spectrochim. Acta, Part A 2014, 121, 514. doi: 10.1016/j.saa.2013.11.004
-
[35]
Gao, G.-Y.; Qu, W.-J.; Shi, B.-B.; Lin, Q.; Yao, H.; Zhang, Y.-M.; Chang, J.; Cai, Y.; Wei, T.-B. Sens. Actuators, B 2015, 213, 501. doi: 10.1016/j.snb.2015.02.077
-
[36]
Hu, J.-Y.; Liu, R.; Zhu, X.-L.; Cai, X.; Zhu, H.-J. Chin. Chem. Lett. 2015, 26, 339. doi: 10.1016/j.cclet.2014.10.028
-
[37]
Wei, T.-B.; Li, W.-T.; Li, Q.; Su, J.-X.; Qu, W.-J. Lin, Q.; Yao, H.; Zhang, Y.-M. Tetrahedron Lett. 2016, 57, 2767. doi: 10.1016/j.tetlet.2016.05.028
-
[38]
Wei, T.-B.; Li, W.-T.; Li, Q.; Qu, W.-J.; Li, H.; Yan, G.-T.; Lin, Q.; Yao, H.; Zhang, Y.-M. RSC Adv. 2016, 6, 43832. doi: 10.1039/C6RA06769G
-
[39]
Li, W.-T.; Wu, G.-Y.; Qu, W.-J.; Li, Q.; Lou, J.-C.; Lin, Q.; Yao, H.; Zhang, Y.-M.; Wei, T.-B. Sens. Actuators, B 2017, 239, 671. doi: 10.1016/j.snb.2016.08.016
-
[40]
张有明, 王雅琳, 林奇, 王丹丹, 魏太保, 有机化学, 2009, 29, 575. http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtmlZhang, Y.-M.; Wang, Y.-L.; Lin, Q.; Wang, D.-D.; Wei, T.-B. Chin. J. Org. Chem. 2009, 29, 575 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtml
-
[41]
魏太保, 王军, 罗榕, 张有明, 有机化学, 2007, 27, 1381. http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtmlWei, T.-B.; Wang, J.; Luo, R.; Zhang, Y.-M. Chin. J. Org. Chem. 2007, 27, 1381 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/volumn/home.shtml
-
[42]
Zhao, J.; Li, J.; Gao, J.; Kjelleberg, S. L. A.; Loo, S. C. J.; Zhang, Q. J. Heterocycl. Chem. 2015, 52, 1699. doi: 10.1002/jhet.v52.6
-
[43]
Sahoo, P. K.; Giri, C.; Haldar, T. S.; Puttreddy, R.; Rissanen, K.; Mal, P. Eur. J. Org. Chem. 2016, 1283.
-
[44]
Liu, X, X.; Weinert, Z. J.; Sharafi, M.; Liao, C. Y.; Li, J. N.; Schneebeli, S. T. Angew. Chem., Int. Ed. 2015, 54, 12772. doi: 10.1002/anie.201506793
-
[45]
Miao, S. B.; Bangcuyo, C. G.; Smith, M. D.; Bunz, U. H. F. Angew Chem., Int. Ed. 2006, 118, 677. doi: 10.1002/(ISSN)1521-3757
-
[46]
Wu, J.-S.; Rui, X.-H.; Long, G.-K.; Chen, W.-Q.; Yan, Q.-Y.; Zhang, Q.-C. Angew. Chem., Int. Ed. 2015, 54, 7354. doi: 10.1002/anie.v54.25
-
[47]
Hu, J. W.; Zhang, G. H.; Shih, H. H.; Jiang, X. Q.; Suna, P. P.; Cheng, C. H. J. Organomet. Chem. 2008, 693, 2798. doi: 10.1016/j.jorganchem.2008.05.030
-
[48]
Lucas, M.-D.; Wang, J.-F.; Nick, A.; Li, H.; Liu, T-B.; Pang, Y. J. Phys. Chem. B 2016, 120, 766. doi: 10.1021/acs.jpcb.5b10909
-
[49]
Yang, J.-R.; Fang, H.-P.; Gao, Y. J. Phys. Chem. Lett. 2016, 7, 1788. doi: 10.1021/acs.jpclett.6b00574
-
[50]
Zhou, H.-T.; Sun, L.; Chen, W.; Tian, G.-J.; Chen, Y.; Li, Y.-R.; Su, J.-H. Tetrahedron 2016, 72, 2300. doi: 10.1016/j.tet.2016.03.036
-
[51]
Zhou, H.-T.; Mei, J.; Chen, Y.-A.; Chen, C.-L.; Chen, W.; Zhang, Z.-Y.; Su, J.-H.; Chou, P.-T.; Tian, H. Small 2016, 12, 6542. doi: 10.1002/smll.v12.47
-
[52]
Yang, Y.-T.; Yin, C.-X.; Huo, F.-J.; Chao, J.-B.; Zhang, Y.-B.; Cheng, F.-Q. Sens. Actuators, B 2014, 193, 220. doi: 10.1016/j.snb.2013.11.094
-
[53]
Li, Q.; Zhang, J.-H.; Cai, Y.; Qu, W.-J.; Gao, G.-Y.; Lin, Q.; Yao, H.; Zhang, Y.-M.; Wei, T.-B. Tetrahedron 2015, 71, 857. doi: 10.1016/j.tet.2014.12.047
-
[54]
Shive, M.-S.-C.; Tanuja, B.; Bhaskar, G. Tetrahedron Lett. 2008, 49, 6646. doi: 10.1016/j.tetlet.2008.09.033
-
[55]
Celso, R. N.; Leandro, G. N.; Vanderlei, G. M. Anal. Chem. 2015, 87, 362. doi: 10.1021/ac504037v
-
[56]
Ji, H. K.; Seong, Y. L.; Hye, M. A.; Cheal, K. Sens. Actuators, B 2017, 242, 25. doi: 10.1016/j.snb.2016.11.026
-
[57]
Duan, Y.-L.; Zheng, Y.-S. Talanta 2013, 107, 332. doi: 10.1016/j.talanta.2013.01.048
-
[58]
史兵兵, 硕士论文, 西北师范大学, 兰州, 2014.Shi, B.-B. M.S. Thesis, Northwest Normal University, Lanzhou, 2014 (in Chinese).
-
[1]
-
图 3 在传感器分子S1 (c=2.0×10-5 mol/L) 的DMSO溶液中分别加入不同阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的照片
Figure 3 Photograph of chemosensor S1 (c=2.0×10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F -, Cl -, Br - , I - , AcO -, H2 PO 4 -, HSO4-, ClO4-, CN- and SCN-(c=1.0×10-2 mol/L)
图 4 在传感器分子S1 (c=2.0×10-5 mol/L) 的DMSO溶液中分别加入50倍化学计量的各种阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的荧光发射光谱
Figure 4 Fluorescence emission spectrum of chemosensor S1 (c=2.0×10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN- and SCN- (c=1.0× 10-2 mol/L)
图 5 在传感器分子S1的 (c=2.0×10-5 mol/L) DMSO溶液中分别加入不同阴离子F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN-和SCN- (c=1.0×10-2 mol/L) 的比色效果图
Figure 5 Colorimetric renderings of chemosensor S1 (c=2.0× 10-5 mol/L) in DMSO solution were added to 50 times the stoichiometric amount of various anions F-, Cl-, Br-, I-, AcO-, H2PO4-, HSO4-, ClO4-, CN - and SCN - (c = 1.0 × 10 - 2 mol/L)
表 1 反应条件的优化
Table 1. Optimization of reaction conditions
Entry Molar ratioa t/℃ t/h Solvent Yield% 1 1:1.0 80 8 DMF 22.2 2 1:1.2 80 8 DMF 29.0 3 1:1.5 80 8 DMF 30.5 4 1:1.2 100 8 DMF 34.1 5 1:1.2 120 8 DMF 43.3 6 1:1.2 130 8 DMF 44.3 7 1:1.2 130 12 DMF 49.5 8 1:1.2 130 18 DMF 56.7 9 1:1.2 130 24 DMF 60.2 10 1:1.2 130 24 DMSO 63.4 a n(2, 3-二氨基吩嗪):n(1, 8-萘二酸酐). -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 8
- 文章访问数: 2683
- HTML全文浏览量: 96



 下载:
下载:










 下载:
下载:

