 图1
使用牺牲模版法制备的反蛋白石结构薄膜局部排列规整的区域
Figure1.
Crack-less domain of Inverse opal structure fabricated by sacrificing colloidal template
图1
使用牺牲模版法制备的反蛋白石结构薄膜局部排列规整的区域
Figure1.
Crack-less domain of Inverse opal structure fabricated by sacrificing colloidal template

Citation: Luo Wenhao, Zhu Shuihong, Lin Youhui, Liu Xiang Yang. Preparation of Crack-free Inverse-opal Films by Template/Matrix Co-assembly[J]. Acta Chimica Sinica, 2017, 75(10): 1010-1016. doi: 10.6023/A17050236

二元共组装法制备无裂痕反蛋白石结构薄膜的研究
English
Preparation of Crack-free Inverse-opal Films by Template/Matrix Co-assembly
-
Key words:
- co-assembly
- / inverse-opal structure
- / crack-free
- / colloidal spheres
-
1 引言
自组装技术作为一种成本低、易操作的工艺, 在制备具有纳米微孔结构的固体材料上有着极大的优势[1].其中, 通过将胶体小球组装模板进行浇筑复刻得到的反蛋白石多孔材料尤其受到人们的普遍关注.这是因为反蛋白石结构可以通过胶体自组装的方式获得多层次的、形貌相对均一的周期结构[2, 3], 且被证明在光学[4, 5]、组织工程[6]、传感器[7]等领域有着重要的应用.
尽管常规的自组装方式能得到有序的反蛋白石结构薄膜, 但是其符合严格周期排列, 有序无缺陷的区域较小, 通常长度不超过10 μm[9].这是由于通过自组装方法得到的反蛋白石总是会产生随机的缺陷或裂痕[10, 11], 而有缺陷裂痕的反蛋白石结构会降低整个材料的稳定性, 致使光学和力学性质下降, 从而限制了自组装方法得到的有序多孔薄膜的应用范围.针对这一问题, 人们近年来开发了各种不同的新方法来可控制备大面积有序多孔薄膜[8].
二元或者多元体系的组装一直是化学领域研究的热点, 通过适当的选取两种或者多种材料直接混合, 再利用一定的成型方式, 就有机会直接得到多功能结构有序的复合材料, 例如, 功能化的纤维[12]、薄膜[13, 14]和气凝胶[15].迄今, 直接用共组装制备光子晶体反蛋白石结构的方式相对较少.将基质材料的前驱体溶液与胶体小球混合后共同组装, 直接得到已被基质材料填充好的有序光子晶体模板, 有望获得完美无裂痕的反蛋白石结构薄膜.本工作分别以正硅酸乙酯(TEOS)和再生丝素蛋白溶液为前驱体, 与聚苯乙烯微球共混, 在玻璃片上进行垂直沉降, 得到二氧化硅与胶体小球的共组装体和丝素蛋白与胶体小球的共组装体, 再分别用高温煅烧和溶剂溶解的方式去除胶体模板, 得到多孔的二氧化硅和丝素蛋白薄膜.最后, 用扫描电镜和透反显微镜等对所形成的组装结构及其光学性质进行了表征.
2 结果与讨论
2.1 制备反蛋白石薄膜的常规方法
反蛋白石薄膜通常用牺牲模板法得到, 该方法有三个步骤: (1) 使胶体小球预先组装成一个密堆积的模板; (2) 将胶体小球的模板浸润到可以形成固体的前驱体母相溶液中; (3) 待浸润的溶液固化后, 选择性地去除胶体模板从而生成反蛋白石结构[19, 20].
如图 1所示, 运用该方法无论对于能水解固化的小分子, 如正硅酸乙酯, 还是对于能自组装交联的生物大分子蚕丝丝素蛋白, 均能得到相对规整的反蛋白石结构.但对于样品整体来说, 如图 2所示, 这样的制备方法会产生大量的缺陷[9], 这是由于胶体小球的模板在干燥过程中, 水分的挥发会在小球之间的空隙中产生应力, 从而产生裂纹[21, 22].缺陷的产生极大地限制了反蛋白石结构薄膜的应用, 为解决这一问题, 有许多研究讨论了自组装的动力学机理并尝试了多种优化方式[23~25], 但到现在为止, 仍然没有一个相对可靠的、成本较低的、容易普及的制备大面积(厘米级别)多层无缺陷反蛋白石结构薄膜的方法.
 图1
使用牺牲模版法制备的反蛋白石结构薄膜局部排列规整的区域
Figure1.
Crack-less domain of Inverse opal structure fabricated by sacrificing colloidal template
图1
使用牺牲模版法制备的反蛋白石结构薄膜局部排列规整的区域
Figure1.
Crack-less domain of Inverse opal structure fabricated by sacrificing colloidal template
2.2 二氧化硅反蛋白石结构薄膜的形貌表征
为解决前述问题, 我们尝试使用了共组装的方法制备二氧化硅反蛋白石结构. 图 3为通过正硅酸乙酯与PS微球的共组装得到的二氧化硅反蛋白石结构薄膜.从图 3a~3c中可以看到, 通过共组装方法能够得到大尺度(长度>200 μm)严格周期排列,无缺陷的二氧化硅反蛋白石结构薄膜,远超常规制备方式所得到的无缺陷区域(一般长度不超过10 μm).这表明正硅酸乙酯与PS微球混合后进行的共组装相比PS微球单独的自组装能抑制大范围缺陷的产生.
对于含有同一浓度TEOS前驱体的共混溶液, 调整胶体小球的浓度能显著改变后续共组装所形成薄膜的厚度和有序程度.如图 4a所示, 当在混合溶液中加入的TEOS前驱体溶液含量为固定的0.15 mL时, 调整胶体小球的浓度, 最终得到的薄膜在宏观上对光的反射效果有明显的差别, 这意味着PS小球的浓度和TEOS前驱体溶液的浓度必须符合一定的比例才能达到较好的效果. 图 4b~4e进一步展示了对于同一浓度的TEOS前驱体与不同浓度小球共组装后得到的薄膜在厚度和结构有序度上的差别.如图 4b所示, 所得薄膜的厚度与小球的浓度线性相关.而通过不同条件下反蛋白石结构的微观形貌可以看出只有当PS小球的浓度控制在适当的范围时, 薄膜才表现出最佳的结构有序度.如图 4e所示, 当胶体小球的浓度过低时, 在薄膜上一些本应被小球占据的空间会被水解得到的二氧化硅完全填充, 从而形成一个类似“补丁”的区域, 防止了裂痕的产生; 而当小球的浓度较高时, 随着薄膜整体厚度的增加, 薄膜最终仍然会形成沿着小球取向的三角形裂纹, 如图 4c所示.我们推测, 这种形状裂纹的形成是由于填充在小球间隙中的二氧化硅不能完全消除干燥过程中所产生的应力, 而随着薄膜厚度的增长, 成型过程中积累的应力就会增多, 当应力积累到一定大小后就会导致裂纹的产生.当胶体小球的浓度与TEOS匹配时, 则能获得大面积的无裂痕反蛋白石结构薄膜, 如图 4d所示.
 图4
(a) 垂直沉降得到的二氧化硅反蛋白石光子晶体宏观图像、(b)通过SEM截面表征得到的光子晶体层数和胶体小球浓度的关系图(可以看到小球浓度需要保持在一定范围才能最大限度的避免缺陷)及(c~e)不同胶体小球浓度对应的微观形貌
Figure4.
(a) Optical photography of the SiO2 inverse opal films, (b) Number of layers of photonic crystal changed along with the particle concentration (particle numbers should be limited into a small range in order to prevent flaws) and (c~e) different morphology of SiO2 inverse opal structure with different colloidal concentration
图4
(a) 垂直沉降得到的二氧化硅反蛋白石光子晶体宏观图像、(b)通过SEM截面表征得到的光子晶体层数和胶体小球浓度的关系图(可以看到小球浓度需要保持在一定范围才能最大限度的避免缺陷)及(c~e)不同胶体小球浓度对应的微观形貌
Figure4.
(a) Optical photography of the SiO2 inverse opal films, (b) Number of layers of photonic crystal changed along with the particle concentration (particle numbers should be limited into a small range in order to prevent flaws) and (c~e) different morphology of SiO2 inverse opal structure with different colloidal concentration
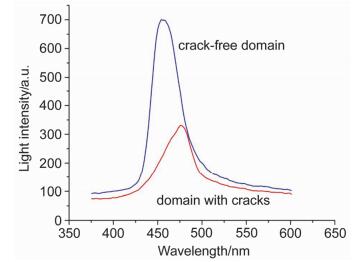
接着, 我们还用光纤光谱仪观察对比了大面积无缺陷反蛋白石结构的光子晶体和有大量缺陷的反蛋白石光子晶体的反射光谱.从图 5可以看到, 对于同一光源, 在对应光子禁带波段上[26], 具有规整结构的反蛋白石薄膜相比于有大量缺陷的反蛋白石薄膜有着更强的反射光信号.除此以外, 二者的反射峰也不太一致, 我们推测这是由于胶体微球在组装过程中产生缺陷, 导致整个光子晶体薄膜的排列周期发生了变化(间距变大, 二氧化硅组分增加), 进而导致有大量缺陷的反蛋白石薄膜峰位发生了红移.根据布拉格定律[27]:
其中λmax是光谱的最高反射峰位; d111是晶格周期常数, 其数值等价为
$ \sqrt {2/3} D$ ; neff是反蛋白石结构的等效折射率; θ是光源的入射角; nc和n0分别是二氧化硅的折射率和空气的折射率; D是制备反蛋白石结构过程中所用到的胶体微球的直径; f是光子晶体的填充系数, 它反映了光子晶体中不同组分所占的比例.对于反蛋白石结构的光子晶体而言, 当有缺陷生成时, 二氧化硅在单位体积内会填充更多的空间, 从而提高neff的数值, 进而会使最终反射光谱的峰位发生红移.综上, 反射强度和峰位置改变都进一步证明, 通过共组装方式, 可以有效减少反蛋白石结构薄膜中的缺陷, 能显著提高该薄膜作为光子晶体的反射效率.2.3 丝素蛋白反蛋白石结构薄膜的形貌表征
除了TEOS前驱体与胶体小球的共组装体系外, 我们还尝试了大分子丝素蛋白与胶体微球的共组装体系. 图 6显示了丝素蛋白与胶体微球共组装后的微观形貌.从图中可以看出二者的结合并没有形成有序的结构, 相反, 几乎所有的胶体小球都没有进行有序的排列, 由此说明大分子丝素蛋白并不适用于共组装法来制备反蛋白石结构.从图 6a中可以看到, 小球的表面附着上了一层丝素蛋白, 且在后续使用四氢呋喃清洗胶体小球的模板后, 如图 6c所示, 明显有大量的小球被完全包裹在丝素蛋白形成的凝胶中无法被溶解清洗掉.因此, 我们猜测, 最终小球无序排列的原因是由于丝素蛋白分子与胶体小球之间有较强的亲和力, 从而抑制了小球与小球之间的相互作用, 进而削弱了小球的自组装效应.
2.4 丝素蛋白分子与胶体微球的相互作用研究
为了进一步确认丝素蛋白分子与聚苯乙烯微球表面的相互作用阻碍了微球的有序自组装, 本文将丝素蛋白/聚苯乙烯微球共混30 min后进行反复离心处理, 取重新分散的悬浮液滴加在洗干净的硅片或者玻璃片上, 待样品干燥后分别用扫描电镜和荧光共聚焦显微镜观察.从图 7a可以看出, 纯的聚苯乙烯微球表面非常光滑.与蚕丝共混后, 若胶体小球和丝素蛋白没有相互作用, 游离的丝素蛋白分子在反复离心过程中会被分离出去.而我们的扫描图像图 7b可以看到小球表面不再光滑, 而是变得十分毛糙.这表明丝素蛋白与胶体小球具有一定的相互作用, 仍然有大量的丝素蛋白在胶体小球的表面富集.荧光共聚焦图像7c也可以看到PS小球包覆了一层FITC修饰的丝素蛋白.此外, 根据已有文献的研究[16], 胶体小球表面的羟基和丝素蛋白的氨基会产生氢键相互作用, 二者的相互作用使得丝素蛋白分子极为容易在含有羟基的PS微球表面附着, 并发生异相生长.综上, 我们认为大分子丝素蛋白与胶体小球表面产生较强作用, 二者的相互作用对胶体小球的组装有抑制作用, 从而不能通过与胶体小球产生有序的共组装来制备无缺陷反蛋白石薄膜.
 图7
(a) 未经丝素蛋白处理的聚苯乙烯微球在纯水条件下的组装和(b)被丝素蛋白生长过聚苯乙烯微球的自组装的SEM图像及(c)在被FITC修饰的丝素蛋白溶液中浸泡过的聚苯乙烯微球的荧光图像
Figure7.
SEM images of self-assembly of (a) original polystyrene nanoparticles and (b) polystyrene nanoparticles incubated by silk and (c) fluorescent image of polystyrene nanoparticles incubated by FITC-labeled silk fibroin
图7
(a) 未经丝素蛋白处理的聚苯乙烯微球在纯水条件下的组装和(b)被丝素蛋白生长过聚苯乙烯微球的自组装的SEM图像及(c)在被FITC修饰的丝素蛋白溶液中浸泡过的聚苯乙烯微球的荧光图像
Figure7.
SEM images of self-assembly of (a) original polystyrene nanoparticles and (b) polystyrene nanoparticles incubated by silk and (c) fluorescent image of polystyrene nanoparticles incubated by FITC-labeled silk fibroin
2.5 共组装法的优势与局限性
如图 8所示, 与传统的牺牲模板法相比, 基质前驱体溶液与聚苯乙烯小球共组装策略具有两个十分明显的优点.第一, 在制备反蛋白石薄膜上缩短了操作流程, 提高了效率.第二, 共组装法可以有效避免缺陷的产生.例如, 我们已成功运用共组装法合成大面积无缺陷的二氧化硅反蛋白石薄膜.但是共组装法也有一定的局限性.为了让小球能在基质前驱体溶液中有序的组装, 需要避免选取与胶体小球有较大作用力的基质.也就是说, 该方法不适用于基质前驱体与胶体小球有较强相互作用的体系.例如丝素蛋白-胶体小球共组装体系, 由于胶体小球和丝素蛋白具有较强的相互作用, 会促使丝素蛋白在胶体小球表面快速吸附, 阻碍小球和小球之间自身的组装效应.
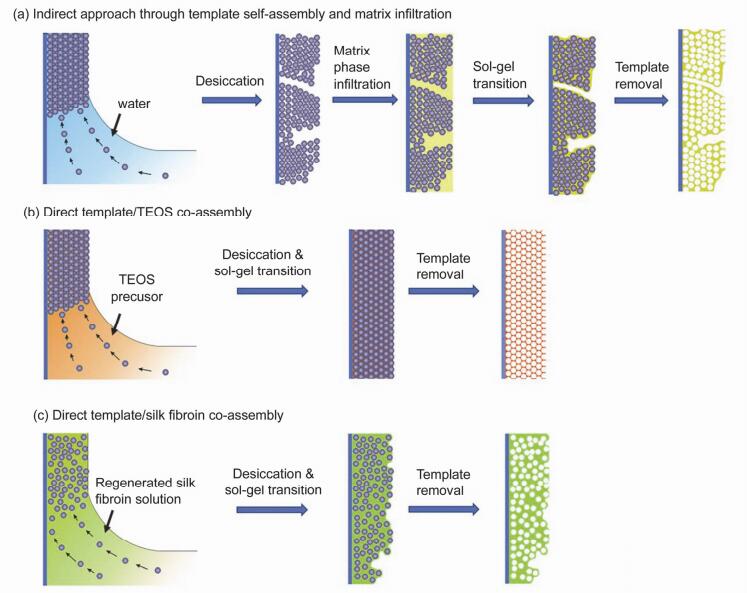 图8
(a) 反蛋白石结构光子晶体的传统的制备方法和(b)正硅酸乙酯和聚苯乙烯微球共同组装的示意图及(c)丝素蛋白和聚苯乙烯微球共同组装的示意图
Figure8.
(a) Schematic illustration of "conventional" colloidal template self-assembly for the fabrication of inverse-opal films, (b) co-assembly of TEOS & polystyrene nanoparticles, and (c) co-assembly of silk fibroin & polystyrene nanoparticles
图8
(a) 反蛋白石结构光子晶体的传统的制备方法和(b)正硅酸乙酯和聚苯乙烯微球共同组装的示意图及(c)丝素蛋白和聚苯乙烯微球共同组装的示意图
Figure8.
(a) Schematic illustration of "conventional" colloidal template self-assembly for the fabrication of inverse-opal films, (b) co-assembly of TEOS & polystyrene nanoparticles, and (c) co-assembly of silk fibroin & polystyrene nanoparticles
3 结论
探讨了将胶体小球分散在两种基质前驱体(TEOS前驱体溶液和丝素蛋白再生溶液)中进行共组装, 进而除去模板制备无裂痕反蛋白石结构薄膜的可行性.结果证明, TEOS前驱体自身的溶胶凝胶转变不会明显影响到胶体小球的有序自组装.通过选取合适浓度的TEOS前驱体和PS微球混合悬浮液, 可以直接共组装得到内部小球排列规整的薄膜, 再去除微球模板即可得到大面积无缺陷的二氧化硅反蛋白石薄膜.而大分子丝素蛋白与胶体小球有着较强的亲和力, 易附着在胶体小球表面, 该过程会抑制胶体小球之间有序的自组装, 不适用于大面积无缺陷反蛋白石薄膜的制备.本实验说明, 选择合适的二元体系进行共组装能简化操作流程, 可以得到大面积、无缺陷的反蛋白石薄膜.该方法为制备性能更好的反蛋白石结构材料提供了新的途径, 相信通过该方法所优化制备的无裂痕反蛋白石薄膜能被更广泛应用到各个相关领域.
4 实验部分
4.1 仪器与试剂
箱式电阻炉: sx2-4-10, 上海一恒科技有限公司. SEM图像: SU-70扫描电镜, 样品表面喷金处理; 反射光谱:海洋光学USB2000+光纤光谱仪; 荧光图像:莱卡Leica TCS SP8共聚焦激光显微镜.碳酸氢钠:分析纯, 上海国药集团化学试剂有限公司; 溴化锂:分析纯, 上海阿拉丁生化科技股份有限公司; 苯乙烯:化学纯, 广东汕头市西陇化工; 无水乙醇:分析纯, 广东汕头市西陇化工; 氢氧化钠:化学纯, 广东汕头市西陇化工; 浓硫酸:分析纯, 广东汕头市西陇化工; 30%过氧化氢:分析纯, 广东汕头市西陇化工; 过硫酸铵:分析纯, 广东汕头市西陇化工; 丙烯酸:分析纯, 广东汕头市西陇化工; 正硅酸乙酯:分析纯, 广东汕头市西陇化工; 盐酸:分析纯36%~38%, 广东汕头市西陇化工; 四氢呋喃:分析纯, 广东汕头市西陇化工.
4.2 聚苯乙烯微球的制备
按文献[16]中的方法, 采用无皂乳液聚合法制备单分散的聚苯乙烯(PS)微球, 具体的制备过程如下.首先, 量取300 mL超纯水, 38.5 mL苯乙烯(St)和0~333 µL丙烯酸(AA)加入四口烧瓶, 密封, 通氮气, 充分搅拌20 min后开始加热.温度达到70 ℃并稳定后, 再将10 mL配置好的17.5 mg/mL引发剂过硫酸铵全部注入烧瓶内, 继续反应7 h.最后, 将反应完成液用定量滤纸过滤后离心3次, 去掉上清液, 加入超纯水溶解后低温存储.通过电位粒度仪(Mastersizer 2000) 检测, 试验中所用的PS微球多分散性指数PDI均小于0.01.
4.3 丝素蛋白再生溶液的制备
取适量蚕茧置于0.5 wt%的碳酸氢钠水溶液中, 煮沸并配合搅拌处理脱胶30 min, 用清水煮沸漂洗30 min.将上述步骤重复操作两次, 再用清水煮沸漂洗两次后置于烘箱中, 在60 ℃下烘干24 h.将脱胶丝素蛋白溶解于过滤后的9.4 mol·L-1溴化锂水溶液中, 放置在60 ℃的烘箱中密封溶解4 h后, 将溶液装入截留分子量为3500D的透析袋中, 用去离子水进行透析处理48 h, 即得到透明的丝素蛋白溶液[17, 18].
4.4 正硅酸乙酯与聚苯乙烯微球的共组装
配置正硅酸乙酯(TEOS)的前驱体溶液:将正硅酸乙酯、0.1 mol·L-1的盐酸和无水乙醇以质量比2:2:3的比例混合, 并在室温下搅拌1 h以备使用.配置0.075~0.5 wt%的PS小球悬浮液.取20 mL PS小球悬浮液放入玻璃瓶中, 并加入0.15 mL正硅酸乙酯前驱体溶液.将1 cm×4 cm的玻璃片竖直插入上述混合溶液的玻璃瓶中.之后, 将玻璃瓶静置于65 ℃的烘箱里, 待干燥挥发后, 取出玻璃片, 并放在高温电阻箱中, 2 h内升温至500 ℃, 保持2 h后, 待其缓慢降温至室温, 即可得到具有反蛋白石结构的二氧化硅薄膜.
4.5 丝素蛋白与聚苯乙烯微球的共组装
配置浓度为0.1 wt%的PS小球悬浮液, 并与浓度为0.4 wt%的丝素蛋白溶液以1:1的比例混合, 取20 mL共混溶液放入玻璃瓶中, 将1 cm×4 cm的玻璃片竖直插入装有上述混合溶液的玻璃瓶中, 并放置在60 ℃的烘箱中干燥24 h.干燥挥发后, 取出玻璃片放在四氢呋喃溶液中, 浸泡1 h后取出, 用去离子水反复冲洗, 即可得到丝素蛋白的多孔薄膜.
4.6 丝素蛋白分子的荧光标记
将1 mL浓度为0.5 mol/mL的碳酸钠溶液与10 mL浓度为70 mg/mL的丝素蛋白溶液混合.配置浓度为5 mg/mL的异硫氰酸荧光素(FITC)的二甲基亚砜(DMSO)溶液, 取1.4 mL缓缓加入上述已经配置好的丝素蛋白混合溶液.在暗室中搅拌2 h后, 用清水透析6 h, 即可获得被FITC标记的丝素蛋白溶液.
4.7 丝素蛋白与聚苯乙烯微球相互作用研究
在研究丝素蛋白与聚苯乙烯相互作用时, 为方便SEM和荧光共聚焦观察, 我们在该部分实验选用2 µm的PS微球.取经过离心再分散处理过的200 μL浓度为0.01 g/mL的PS微球单分散溶液, 与1 mL浓度为5 mg/mL未修饰或FITC修饰过的丝素蛋白溶液混合.待丝素蛋白分子与PS微球混合上30 min后, 通过多次离心处理, 除去混合溶液中游离的丝素蛋白分子, 将沉淀再分散到1 mL的超纯水中, 制成悬浮液.分别取适量纯净的PS微球悬浮液和与丝素蛋白作用过的PS微球悬浮液滴涂在硅片或者玻璃片上, 待干燥后, 通过SEM和荧光共聚焦表征来研究分析小球与丝素蛋白的相互作用情况.
-
-
[1]
Whitesides, G. M.; Grzybowski, B. Science 2002, 295, 2418. doi: 10.1126/science.1070821
-
[2]
Zhao, X.; Su, F.; Yan, Q.; Guo, W.; Bao, X. Y.; Lv, L.; Zhou, Z. J. Mater. Chem. 2006, 16, 637. doi: 10.1039/B513060C
-
[3]
Holland, B. T.; Blanford, C. F.; Stein, A. Science 1998, 281, 538. doi: 10.1126/science.281.5376.538
-
[4]
Arsenault, A. C.; Clark, T. J.; von Freymann, G.; Cademartiri, L.; Sapienza, R.; Bertolotti, J.; Vekris, E.; Wong, S.; Kitaev, V.; Manners, I. Nat. Mater. 2006, 5, 179. doi: 10.1038/nmat1588
-
[5]
Rinne, S. A.; García-Santamaría, F.; Braun, P. V. Nat. Photonics 2008, 2, 52. doi: 10.1038/nphoton.2007.252
-
[6]
Choi, S. W.; Xie, J.; Xia, Y. Adv. Mater. 2009, 21, 2997. doi: 10.1002/adma.v21:29
-
[7]
Lee, K.; Asher, S. A. J. Am. Chem. Soc. 2000, 122, 9534. doi: 10.1021/ja002017n
-
[8]
李扬; 齐利民, 化学学报, 2015, 73, 869. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345002.shtmlLi, Y.; Qi, L.-M. Acta Chim. Sinica 2015, 73, 869. http://sioc-journal.cn/Jwk_hxxb/CN/abstract/abstract345002.shtml
-
[9]
Hatton, B.; Mishchenko, L.; Davis, S.; Sandhage, K. H.; Aizenberg, J. Proc. Natl. Acad. Sci. U. S. A. 2010, 107, 10354. doi: 10.1073/pnas.1000954107
-
[10]
Lytle, J. C.; Stein, A. Annual Review of Nano Research, Vol. 1, Eds.:Cao, G. Z.; Brinker, C. J., World Scientific Publishing Co., Singa-pore, 2006, 1, pp. 1~14.
-
[11]
Velev, O. D.; Lenhoff, A. M. Curr. Opin. Colloid. Interface Sci. 2000, 5, 56. doi: 10.1016/S1359-0294(00)00039-X
-
[12]
蒋伏广, 姚晋荣, 陈新, 邵正中, 化学学报, 2009, 67, 1675. doi: 10.3321/j.issn:0567-7351.2009.14.023Jiang, F.-G.; Yao, J.-R.; Chen, X.; Shao, Z.-Z. Acta Chim. Sinica 2009, 67, 1675. doi: 10.3321/j.issn:0567-7351.2009.14.023
-
[13]
Tu, H.; Yu, R.; Lin, Z.; Zhang, L.; Lin, N.; Yu, W. D.; Liu, X. Y. Adv. Funct. Mater. 2016, 26, 9032. doi: 10.1002/adfm.v26.48
-
[14]
Ke, G.-Z.; Xie, H.-F.; Ruan, R.-P.; Yu, W.-D. Energy Convers. Manage. 2010, 51, 2294. doi: 10.1016/j.enconman.2010.04.001
-
[15]
Liu, R.; Wan, L.; Liu, S.; Pan, L.; Wu, D.; Zhao, D. Adv. Funct. Mater. 2015, 25, 526. doi: 10.1002/adfm.v25.4
-
[16]
Chen, Z.; Zhang, H.; Lin, Z.; Lin, Y.; van Esch, J. H.; Liu, X. Y. Adv. Funct. Mater. 2016, 26, 8978. doi: 10.1002/adfm.v26.48
-
[17]
Nagarkar, S.; Nicolai, T.; Chassenieux, C.; Lele, A. Phys. Chem. Chem. Phys. 2010, 12, 3834. doi: 10.1039/b916319k
-
[18]
曹惠, 陈新, 邵正中, 化学学报, 2008, 66, 2059. doi: 10.3321/j.issn:0567-7351.2008.18.007Cao, H.; Chen, X.; Shao, Z.-Z. Acta Chim. Sinica 2008, 66, 2059. doi: 10.3321/j.issn:0567-7351.2008.18.007
-
[19]
Schroden, R. C.; Al-Daous, M.; Blanford, C. F.; Stein, A. Chem. Mater. 2002, 14, 3305. doi: 10.1021/cm020100z
-
[20]
Diao, Y. Y.; Liu, X. Y.; Toh, G. W.; Shi, L.; Zi, J. Adv. Funct. Mater. 2013, 23, 5373. doi: 10.1002/adfm.v23.43
-
[21]
Wong, S.; Kitaev, V.; Ozin, G. A. J. Am. Chem. Soc. 2003, 125, 15589. doi: 10.1021/ja0379969
-
[22]
Zhou, Z.; Zhao, X. Langmuir 2005, 21, 4717. doi: 10.1021/la046775t
-
[23]
Zhang, T. H.; Kuipers, B. W.; Groenewold, J.; Kegel, W. K. Soft Matter. 2015, 11, 297. doi: 10.1039/C4SM02273D
-
[24]
Zhang, T. H.; Liu, X. Y. Chem. Soc. Rev. 2014, 43, 2324. doi: 10.1039/C3CS60398A
-
[25]
Chabanov, A. A.; Jun, Y.; Norris, D. J. Appl. Phys. Lett. 2004, 84, 3573. doi: 10.1063/1.1737066
-
[26]
Huang, Y.; Zhou, J.; Su, B.; Shi, L.; Jiang, L. J. Am. Chem. Soc. 2012, 134, 17053. doi: 10.1021/ja304751k
-
[27]
Busch, K.; John, S. Phys. Rev. E 1998, 58, 3896.
-
[1]
-
图 4 (a) 垂直沉降得到的二氧化硅反蛋白石光子晶体宏观图像、(b)通过SEM截面表征得到的光子晶体层数和胶体小球浓度的关系图(可以看到小球浓度需要保持在一定范围才能最大限度的避免缺陷)及(c~e)不同胶体小球浓度对应的微观形貌
Figure 4 (a) Optical photography of the SiO2 inverse opal films, (b) Number of layers of photonic crystal changed along with the particle concentration (particle numbers should be limited into a small range in order to prevent flaws) and (c~e) different morphology of SiO2 inverse opal structure with different colloidal concentration
图 7 (a) 未经丝素蛋白处理的聚苯乙烯微球在纯水条件下的组装和(b)被丝素蛋白生长过聚苯乙烯微球的自组装的SEM图像及(c)在被FITC修饰的丝素蛋白溶液中浸泡过的聚苯乙烯微球的荧光图像
Figure 7 SEM images of self-assembly of (a) original polystyrene nanoparticles and (b) polystyrene nanoparticles incubated by silk and (c) fluorescent image of polystyrene nanoparticles incubated by FITC-labeled silk fibroin
图 8 (a) 反蛋白石结构光子晶体的传统的制备方法和(b)正硅酸乙酯和聚苯乙烯微球共同组装的示意图及(c)丝素蛋白和聚苯乙烯微球共同组装的示意图
Figure 8 (a) Schematic illustration of "conventional" colloidal template self-assembly for the fabrication of inverse-opal films, (b) co-assembly of TEOS & polystyrene nanoparticles, and (c) co-assembly of silk fibroin & polystyrene nanoparticles
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 17
- 文章访问数: 3343
- HTML全文浏览量: 638





 下载:
下载:







 下载:
下载:

