 图1
Cu(BDC)(4, 4′-Bipy)0.5(a)、Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)的红外图谱
Figure1.
FT-IR spectra of Cu(BDC)(4, 4′-Bipy)0.5(a) and Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)
图1
Cu(BDC)(4, 4′-Bipy)0.5(a)、Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)的红外图谱
Figure1.
FT-IR spectra of Cu(BDC)(4, 4′-Bipy)0.5(a) and Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)

Citation: GONG Wenpeng, CHEN Dan, YANG Shuijin. Adsorption of Methyl Violet by an Anionic Metal-Organic Framework Cu(BDC-NH2)(4, 4'-Bipy)0.5 (BDC=Terephthalicacid, Bipy=Bipyridine)[J]. Chinese Journal of Applied Chemistry, 2017, 34(11): 1321-1328. doi: 10.11944/j.issn.1000-0518.2017.11.170015

一种阴离子型三维金属有机框架材料Cu (BDC-NH2)(4, 4'-Bipy)0.5(BDC=对苯二甲酸根,Bipy=联吡啶)的制备及其对甲基紫的吸附性能
English
Adsorption of Methyl Violet by an Anionic Metal-Organic Framework Cu(BDC-NH2)(4, 4'-Bipy)0.5 (BDC=Terephthalicacid, Bipy=Bipyridine)
-
在纺织、皮革、纸张、印刷、染料、塑料等行业生产中,产生大量染料的工业废水,这些废水已经成为一个极为严峻的环境问题,对水资源甚至生态系统造成了严重的威胁。染料废水的处理方法主要有吸附法、氧化降解法和絮凝物沉淀法[1]。其中,吸附法被人们广泛应用于各种废水的处理[2]。
金属有机框架材料(MOF)可作为一种吸附剂,具有大表面积、孔隙率高、热稳定性好、孔尺寸多样、孔表面官能团功能设计可调等优点,在新兴能源和生态环境相关的储氢、捕获温室气体(CO2和CH4)和非均相催化等方面得到了较多的研究[3-4]。同时,金属有机骨架材料可用于处理有机染料废水,在该领域研究前景广阔。目前,吸附废水中有机染料的金属有机骨架材料主要有MIL-100、MIL-101系类金属有机骨架和UIO-66等[5-6]。离子型MOF可以通过离子交换的方式来实现对这些染料的多组分吸附和分离[7]。
近年来,三维骨架Zn(BDC)(4, 4′-Bipy)0.5(BDC=对苯二甲酸根,4, 4′-Bipy=4, 4′-联吡啶)、Cu(BDC)(4, 4′-Bipy)0.5、Cu(BDC-OH)(4, 4′-Bipy)、M(bdc)(ted)0.5(M=Co、Zn、Ni、Cu,bdc=BDC,ted=三乙烯二胺)[8-11]等气体吸附和催化方面研究较多,未见在吸附染料废水方面的研究。本文采用溶剂热法,利用2-氨基对苯二甲酸、4, 4′-联吡啶配体和硝酸铜在溶剂热的条件下,制备一种的阴离子型三维MOF材料Cu(BDC-NH2)(4, 4′-Bipy)0.5,并研究了材料对甲基紫(MV)吸附性能。
1 实验部分
1.1 仪器和试剂
Nicolet 5700型红外拉曼光谱仪(美国Nicolet公司),采取KBr压片法;Pert PRO型X射线衍射仪(荷兰帕纳科公司),由石墨单色器滤波,用铜靶Kα1辐射,在管电压40 kV,管电流40 mA的条件下测定,扫描范围2θ=5°~45°;比表面积采用ASAP2020 V4.03(美国麦克公司)进行测试;Pyris diamond型TG/DTA热重分析仪(美国Perkin-elmer公司);Zeta电势采用Nano ZS 90(美国Malvern公司)进行测试;S-4800型扫描电子显微镜(日本日立公司)。
硝酸铜(Cu(NO3)2·3H2O,天津市天力化学试剂有限公司)、2-氨基对苯二甲酸(H2BDC-NH2,萨恩化学技术(上海)有限公司)、4, 4′-联吡啶(4, 4′-Bipy,上海山浦化工有限公司),以上试剂均为分析纯、无水乙醇、N, N-二甲基甲酰胺(DMF)、甲基紫(MV)均购自国药集团,均为分析纯试剂;二次蒸馏水(自制);
1.2 三维金属有机骨架Cu(BDC-NH2)(4, 4′-Bipy)0.5的制备
1.2.1 Cu(BDC)(4, 4′-Bipy)0.5的制备
参考文献[8]方法,取0.1143 g Cu(NO3)2·3H2O(0.473 mmol)、0.075 g H2BDC(0.473 mmol)、0.0369 g的4, 4′-Bipy(0.2365 mmol)于反应釜中,加入20 mL乙醇和20 mL DMF,室温下,搅拌30 min,在恒温干燥烘箱中90 ℃,反应24 h。反应结束后自然降至室温,得到的材料用DMF和正己烷交替洗涤5~6次。将洗好的吸附剂在60、120 ℃温度下,各真空干燥12 h,得到Cu(BDC)(4, 4′-Bipy)0.5。
1.2.2 Cu(BDC-NH2)(4, 4′-Bipy)0.5的制备
取0.1143 g Cu(NO3)2·3H2O(0.473 mmol)、0.0857 g H2BDC-NH2(0.473 mmol)、0.0369 g的4, 4′-Bipy(0.2365 mmol)于反应釜中,加入20 mL乙醇和20 mL DMF,室温下,搅拌30 min,在恒温干燥烘箱中,130 ℃,反应24 h。反应结束后,自然降至室温,得到的材料用DMF洗涤5次。将洗好的吸附剂在60、120 ℃温度下,各真空干燥12 h,得到Cu(BDC-NH2)(4, 4′-Bipy)0.5。
1.3 三维金属有机骨架Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附MV溶液
在MV溶液中加入一定量的Cu(BDC-NH2)(4, 4′-Bipy)0.5进行吸附实验,由甲基紫标准曲线和下列公式计算其吸附量。
式中,ρ0和ρt为MV初始和t时的质量浓度(mg/L);V分别为溶液体积(L); m吸附剂质量(g)和qt吸附量(mg/g)。
2 结果与讨论
2.1 三维金属有机骨架复合材料Cu(BDC-NH2)(4, 4′-Bipy)0.5的表征
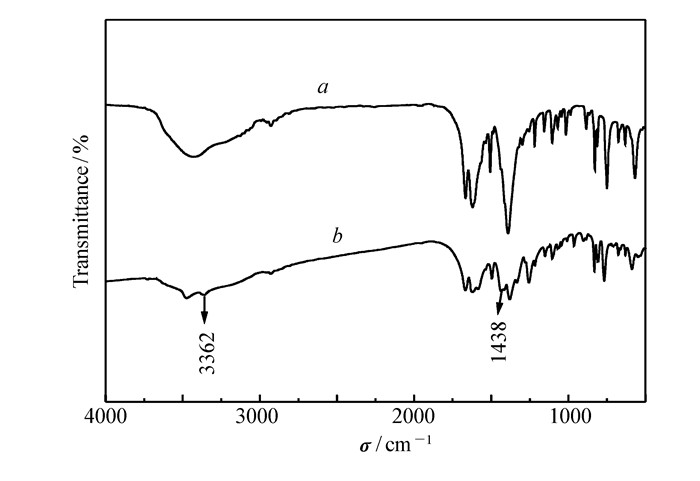
通过红外光谱表征了Cu(BDC)(4, 4′-Bipy)0.5和Cu(BDC-NH2)(4, 4′-Bipy)0.5的结构,如图 1所示。可见,Cu(BDC)(4, 4′-Bipy)0.5的主要吸收峰与文献[8]一致,相比而言Cu(BDC-NH2)(4, 4′-Bipy)0.5除保留了Cu(BDC)(4, 4′-Bipy)0.5的基本骨架特征吸收峰,出现了新的吸收峰,1438 cm-1附近的吸附峰为—NH的特征峰,而—NH2的对称和反对称伸缩振动吸收峰出现在3000~3400 cm-1处,说明氨基成功的连接在Cu(BDC)(4, 4′-Bipy)0.5上,成功制备了Cu(BDC-NH2)(4, 4′-Bipy)0.5。
 图1
Cu(BDC)(4, 4′-Bipy)0.5(a)、Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)的红外图谱
Figure1.
FT-IR spectra of Cu(BDC)(4, 4′-Bipy)0.5(a) and Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)
图1
Cu(BDC)(4, 4′-Bipy)0.5(a)、Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)的红外图谱
Figure1.
FT-IR spectra of Cu(BDC)(4, 4′-Bipy)0.5(a) and Cu(BDC-NH2)(4, 4′-Bipy)0.5(b)
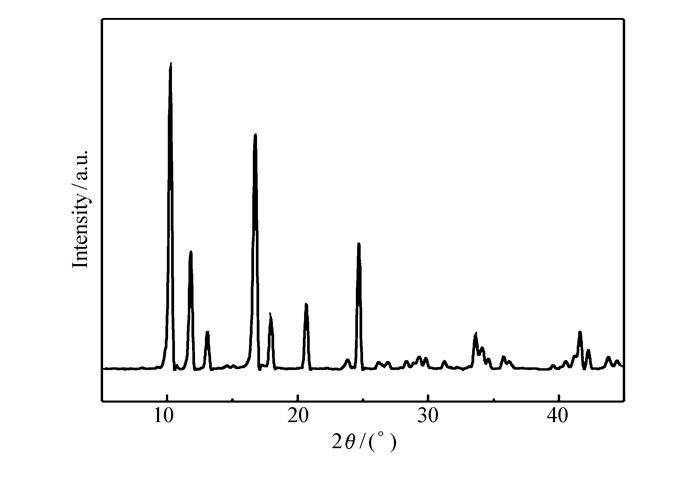
通过X射线衍射仪表征了Cu(BDC-NH2)(4, 4′-Bipy)0.5的晶体结构,如图 2所示。从图 2可以看出,Cu(BDC-NH2)(4, 4′-Bipy)0.5的XRD主要衍射峰集中在2θ=10°~25°区间内,与文献[8-9]基本一致,同时衍射峰强度表明Cu(BDC-NH2)(4, 4′-Bipy)0.5具有良好有序结构。
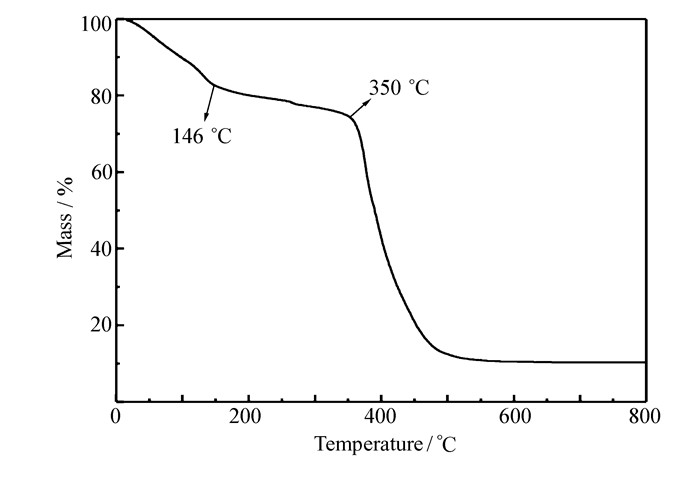
通过热重分析仪研究了Cu(BDC-NH2)(4, 4′-Bipy)0.5的热稳性,如图 3所示。可见,随着温度的升高,Cu(BDC-NH2)(4, 4′-Bipy)0.5逐渐失重。从17 ℃到146 ℃是Cu(BDC-NH2)(4, 4′-Bipy)0.5失去物理吸附水、孔道中的溶剂以及未反应的原料;Cu(BDC-NH2)(4, 4′-Bipy)0.5在350 ℃下可稳定存在。BET表征数据详见表 1。可见,BET比表面积为124.2 m2/g。
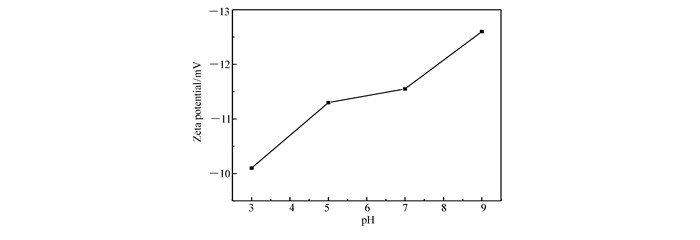
Sample SBET/(m2·g-1) Vtotal/(cm3·g-1) D/nm Cu(BDC-NH2)(4, 4′-Bipy)0.5 124.2 0.1 0.2 Cu(BDC-NH2)(4, 4′-Bipy)0.5的Zeta Potential分析谱图见图 4。
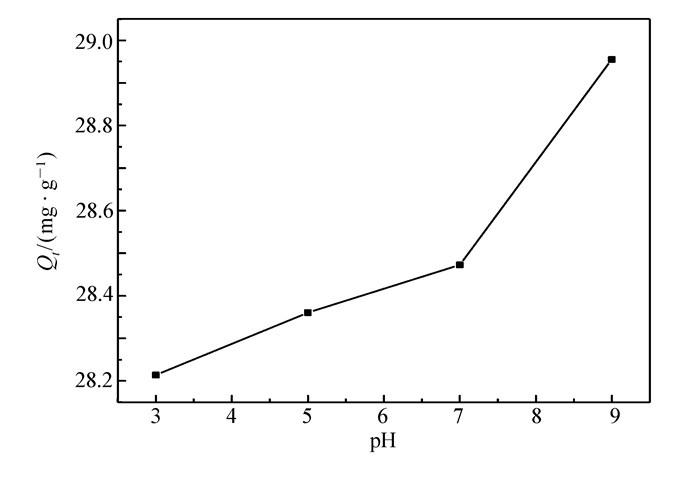
由图 4可知,Cu(BDC-NH2)(4, 4′-Bipy)0.5在水溶液中Zeta电势均为负值,其中在pH=9的情况下,Cu(BDC-NH2)(4, 4′-Bipy)0.5的Zeta电势值最大,所以Cu(BDC-NH2)(4, 4′-Bipy)0.5在pH=9的情况下吸附甲基紫效果较好。
通过扫描电子显微镜观测了Cu(BDC-NH2)(4, 4′-Bipy)0.5的微观形貌,如图 5所示。可见,Cu(BDC-NH2)(4, 4′-Bipy)0.5呈现为形状规则的立体结构,而且表面多孔。
2.2 Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附甲基紫的研究
2.2.1 甲基紫溶液的pH值对吸附效果的影响
取10 mg吸附剂,于不同pH值的20 mL 15 mg/L甲基紫溶液中振荡2 h,在20 ℃下考察甲基紫溶液的pH值对吸附效果的影响。
由图 6可知,Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的吸附能力随溶液初始pH值的升高而升高。pH=3时吸附效果不佳,这可能与大量的H+与阳离子染料竞争吸附活性位点有关[12]。选取甲基紫溶液的pH值为3~9探究pH值对吸附效果的影响是因为当pH<3时,甲基紫的最大吸收波长会发生变化,而当pH>9时,甲基紫会分解。溶液pH值对吸附的影响主要是通过改变吸附剂和吸附质所带的电荷,进而影响吸附剂和吸附质之间的静电作用来实现的[13]。
2.2.2 初始质量浓度对吸附效果的影响
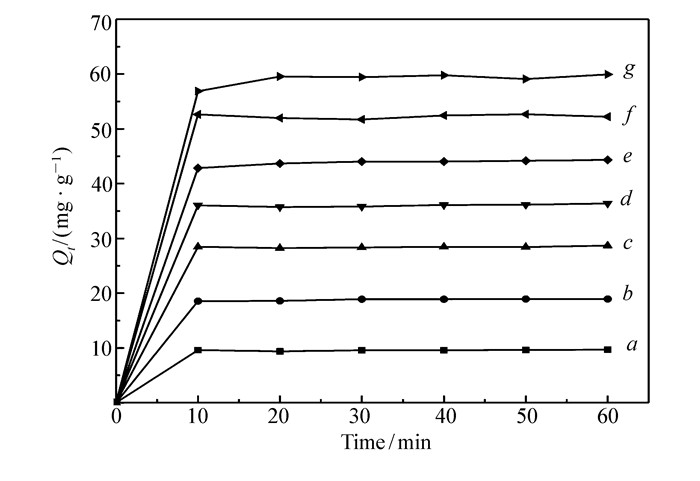
取10 mg吸附剂,于20 mL浓度分别为5、10、15、20、25、30、35 mg/L的甲基紫溶液中并调节pH=9进行振荡,每10 min测1次样,在20 ℃下考察甲基紫初始质量浓度对吸附的影响。
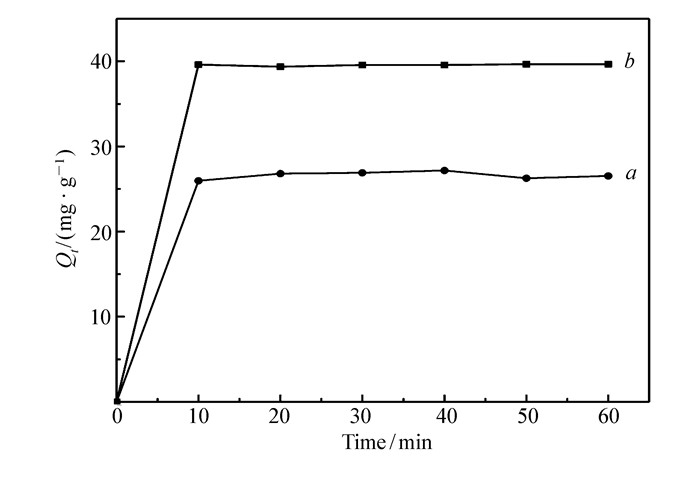
如图 7所示,Cu(BDC-NH2)(4, 4′-Bipy)0.5的吸附量10 min内达到吸附平衡。同时吸附量随着MV初始浓度的增加而增加,这是因为甲基紫溶液浓度增加,使Cu(BDC-NH2)(4, 4′-Bipy)0.5表面与甲基紫溶液主体的浓度差增加,吸附的推动力增大,从而吸附量增加[14]。
2.2.3 温度对吸附效果的影响
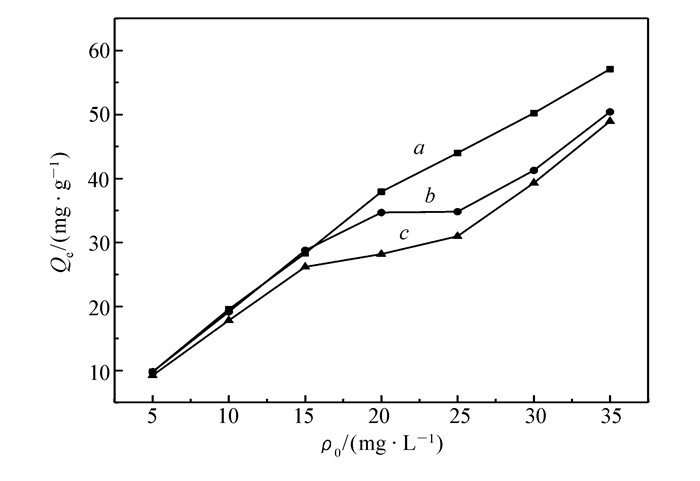
取10 mg吸附剂,于pH=9浓度为5、10、15、20、25、30、35 mg/L的20 mL甲基紫溶液中,恒温振荡6 h,考察温度对吸附效果的影响。
由图 8可知,Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的吸附量随着温度升高而降低,说明吸附的过程是放热的过程;可能是在较高温度下,甲基紫的溶解度增大,Cu(BDC-NH2)(4, 4′-Bipy)0.5与染料间的作用减少的缘故[15]。
2.2.4 背景离子对吸附效果的影响
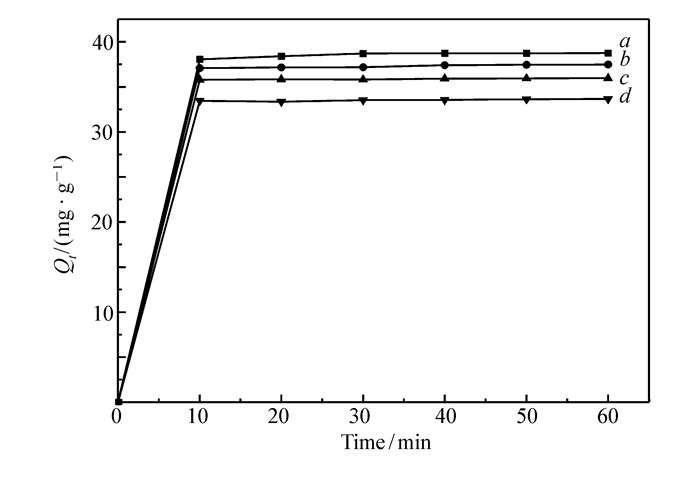
取10 mg吸附剂,于pH=9浓度为20 mg/L的20 mL甲基紫溶液中,分别加入10 mmol的KCl、NaCl和HCl,恒温振荡1 h,考察背景离子对吸附效果的影响。
由图 9可知,加入金属阳离子后甲基紫的吸附量均减少,这是因为溶液中存在的金属阳离子会与甲基紫竞争Cu(BDC-NH2)(4, 4′-Bipy)0.5的吸附位点,从而对吸附产生干扰;加入HCl后甲基紫的吸附量降低了5 mg/g,这是因为在酸性条件下材料的Zeta电势值较小,同时H+也与材料产生竞争吸附,从而导致吸附量下降,从而说明材料主要是通过静电作用和范德华力进行吸附作用。
2.2.5 Cu(BDC)(4, 4′-Bipy)0.5与Cu(BDC-NH2)(4, 4′-Bipy)0.5的吸附效果对比
分别取10 mg Cu(BDC)(4, 4′-Bipy)0.5和Cu(BDC-NH2)(4, 4′-Bipy)0.5,于20 mL浓度为20 mg/L、pH=9的甲基紫溶液中,进行振荡,每10 min测1次样,考察Cu(BDC)(4, 4′-Bipy)0.5和Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫吸附效果对比。
由图 10可知,Cu(BDC-NH2)(4, 4′-Bipy)0.5的吸附量与Cu(BDC)(4, 4′-Bipy)0.5相比提高了15 mg/g,说明pH=9时,Cu(BDC-NH2)(4, 4′-Bipy)0.5中的氨基质子化减弱,从而与Cu(BDC)(4, 4′-Bipy)0.5相比增加了材料的范德华力和吸附活性位点,增大了吸附效果。
2.3 吸附等温方程的确定
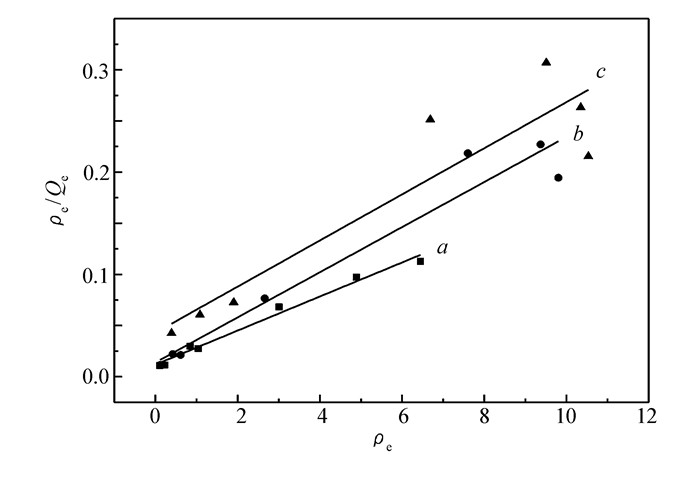
在探讨温度影响的基础上,我们进一步研究了甲基紫的两种等温吸附模型(Langmuir和Freundlich)。其中Langmuir线性方程[16]等式如下:
式中,qe和qm(mg/g)分别是平衡时Cu(BDC-NH2)(4, 4′-Bipy)0.5的吸附量和最大单层吸附量,ρe(mg/L)是平衡时甲基紫的质量浓度,KL(L/mg)是Langmuir的吸附常数。将ρe对ρe/qe作图(图 10),线性关系表明,Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附甲基紫符合Langmuir吸附模型,计算得到的相关参数见表 2。
 表 2
甲基紫的等温吸附曲线参数
Table 2.
Isotherm parameters the adsorption of methyl violet by Cu(BDC-NH2)(4, 4′-Bipy)0.5 at different temperature
表 2
甲基紫的等温吸附曲线参数
Table 2.
Isotherm parameters the adsorption of methyl violet by Cu(BDC-NH2)(4, 4′-Bipy)0.5 at different temperature
Temperature/K Langmuir Freundlich Qm/(mg·g-1) KL/(L·mg-1) RL R2 KF/(mg·g-1) n R2 293 60.09 1.404 4 0.048 81 0.993 3 29.54 2.57 0.969 1 303 45.35 1.586 3 0.043 57 0.976 4 23.71 3.33 0.930 6 313 43.64 0.524 5 0.103 7 0.926 1 15.68 2.56 0.932 2 Langmuir等温吸附的基本特性,可以用RL的值来表示[16]:
式中,KL(L/mg)是Langmuir等温方程的吸附常数,ρ0(mg/L)为染料的初始浓度。RL说明了相应的温度下吸附剂的吸附能力:RL>1时不利于吸附;0<RL<1时为良好吸附;RL=0时为不可逆吸附;RL=1时为线性吸附。Cu(BDC-NH2)(4, 4′-Bipy)0.5在20、30、40 ℃吸附甲基紫的RL值分别为:0.04881、0.04357和0.1038,从而表明Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的吸附是良好吸附。
Freundlich吸附等温方程[16]一般表示为:
式中,KF大致的表明了吸附剂的吸附能力,1/n说明了吸附强的大小。表 2中计算出了相关参数。
表 2中计算出了Langmuir、Freundlich两种等温吸附模型的相关参数。由表中数据可知,该实验数据更符合Langmuir等温吸附模型,而且也有文献[16]报道利用Langmuir等温吸附模型解释吸附剂从染料溶液中吸附染料。
2.4 吸附动力学的确定
为了探究该吸附过程的控制机制,参考文献[16]的方法,将实验数据通过两种动力学模型来拟合。
由表 3可知,在15、20 mg/L下Cu(BDC-NH2)(4, 4′-Bipy)0.5的拟二级动力学计算而得的线性相关系数R2的数值远远高于拟一级动力学,且拟二级动力学模型的线性相关系数(R2)分别等于1。此外,实验值Qe, exp (mg/g)与拟一级动力学公式计算得出的吸附量Qe, cal (mg/g)完全不相符合,而与拟二级动力学计算得到的吸附量(表 3)的数值相吻合。因此表明拟二级动力学模型能很好地描述Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的吸附,对甲基紫的吸附属化学吸附控制[17]。
 表 3
甲基紫在不同浓度下拟一级动力学和拟二级动力学参数
Table 3.
Parameters of pseudo-first-order and pseudo-second-order adsorption kinetics model in different initital concentration
表 3
甲基紫在不同浓度下拟一级动力学和拟二级动力学参数
Table 3.
Parameters of pseudo-first-order and pseudo-second-order adsorption kinetics model in different initital concentration
Kinetics model ρ0/(mg·L-1) Qe, exp/(mg·g-1) Qe, cal/(mg·g-1) K1/min-1;K2/(g·mg-1·min-1) R2 Psedo-first-order model 15 27.29 3.47 0.571 5 0.915 7 20 38.42 4.46 0.325 4 0.834 8 Psedo-second-order model 15 27.29 27.74 0.258 9 1 20 38.42 39.28 0.121 8 1 2.5 热力学参数
在293、303和313 K温度下进行Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附甲基紫的实验,参照参考文献[18]的方法,计算吉布斯自由能(ΔGo)、焓变(ΔHo)和熵变(ΔSo),得出相关热力学参数见表 4。
 表 4
Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附甲基紫的热力学参数
Table 4.
The thermodynamic parameters of adsorption MV onto Cu(BDC-NH2)(4, 4′-Bipy)0.5
表 4
Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附甲基紫的热力学参数
Table 4.
The thermodynamic parameters of adsorption MV onto Cu(BDC-NH2)(4, 4′-Bipy)0.5
ΔG/(kJ·mol-1) ΔH/(kJ·mol-1) ΔS/(J·mol-1·K-1) 293 K 303 K 313 K -8.097 -6.727 -4.875 -52.28 -150.48 3 结论
通过溶剂热法合成得到一种阴离子型三维金属有机框架(MOF)材料Cu(BDC-NH2)(4, 4′-Bipy)0.5(BDC=对苯二甲酸根,Bipy=联吡啶),研究其对甲基紫溶液的吸附性能。结果表明,常温和pH=9条件下,Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的吸附效果较好,Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的吸附符合Langmuir等温吸附模型,其吸附过程由拟二级动力学模型拟合,推定属化学吸附控制。在溶液pH=9,温度为20 ℃条件下Cu(BDC-NH2)(4, 4′-Bipy)0.5对甲基紫的最大吸附量为60.09 mg/g。
-
-
[1]
Auta M, Hameed B. Modifiedmesoporous Clay Adsorbent for Adsorption Isothermand Kinetics of Methylene Blue[J]. Chem Eng J, 2012, 198(4): 219-227.
-
[2]
何燕萍, 谭衍曦, 张健. 基于尺寸识别和离子交换实现有机染料分离的一例阴离子型MOF[J]. 化学学报, 2014,72,(12): 1228-1232. HE Yanping, TAN Yanxi, ZHANG Jian. An Anionic MOF for Separation of Organic Dyes via Cationic-Exchange and Size-Exclusion[J]. Acta Chim Sin, 2014, 72(12): 1228-1232.
-
[3]
Dang D, Wu P, He C. Homochiral Metal-Organic Frameworks for Heterogeneous Asymmetric Catalysis[J]. J Am Chem Soc, 2016, 132(41): 14321-3.
-
[4]
穆翠枝, 徐峰, 雷威. 功能金属-有机骨架材料的应用[J]. 化学进展, 2007,19,(9): 1345-1356. CHEN Cuizhi, XU Feng, LEI Wei. Application of Functional Metal-Organic Framework Materials[J]. Prog Chem, 2007, 19(9): 1345-1356.
-
[5]
Hasan Z, Jhung S H. Removal of Hazardous Organics from Water Using Metal-Organic Frame Works(MOFs):Plausible Mechanisms for Selective Adsorptions[J]. J Hazard Mater, 2015, 283: 329-339. doi: 10.1016/j.jhazmat.2014.09.046
-
[6]
杨成雄, 王士伟, 严秀平. 金属-有机骨架对苯二甲酸酯-铝吸附水中酚类化合物动力学和热力学[J]. 应用化学, 2016,33,(9): 1040-1046. YANG Chengxiong, WANG Shiwei, YAN Xiuping. Adsorption Thermodynamics and Kinetics of Phenols on Metal-Organic Framework Aluminum Terephthalate in Water[J]. Chinese J Appl Chem, 2016, 33(9): 1040-1046.
-
[7]
Xue A, Zhou S, Zhao Y. Effective NH2-grafting on Attapulgite Surfaces for Adsorption of Reactive Dyes[J]. Hazard Mater, 2011, 194(5): 7-14.
-
[8]
Chen Z X, Xiang S C, Arman H D. Three-dimensional Pillar-layered Copper(Ⅱ) Metal_Organic Framework with Immobilized Functional OH Groups on Pore Surfaces for Highly Selective CO2/CH4 and C2H2/CH4 Gas Sorption at Room Temperature[J]. Inorg Chem, 2011, 50(8): 3442-3446. doi: 10.1021/ic102347b
-
[9]
Chen B L, Liang C D Yang J. A Microporous Metal-Organic Framework for Gas-Chromatographic Separation of Alkanes[J]. Angew Chem Int Ed, 2006, 45(9): 1390-1393. doi: 10.1002/(ISSN)1521-3773
-
[10]
徐玲. 几种苯多酸金属配合物的合成、结构和性质研究[D]. 福州: 中国科学院福建物质结构研究所, 2005.XU Ling. Syntheses, Structures and Properties of Coordination Polymers Containing Several Kinds of Benzene Polycarboxylate Acids[D]. Fuzhou:Fujian Institute of Research on the Structure, 2005(in Chinese).
-
[11]
Peng L, Wu S J, Yang X Y. Application of Metal Organic Frameworks M(bdc)(ted)0.5(M=Co, Zn, Ni, Cu) in the Oxidation of Benzyl Alcohol[J]. RSC Adv, 2016, 6(76): 72433-72438. doi: 10.1039/C6RA12799A
-
[12]
Monash P, Pugazhenthi G. Adsorption of Crystal Violet Dye From Aqueous Solution Using Mesoporous Materials Synthesized at Room Temperature[J]. Adsorption, 2009, 15(4): 390-450. doi: 10.1007/s10450-009-9156-y
-
[13]
Sun R Q, Sun L B, Chun Y. Catalytic Performance of Porous Carbons Obtained by Chemical Activation[J]. Carbon, 2008, 46(13): 1757-1764. doi: 10.1016/j.carbon.2008.07.029
-
[14]
Luo H M, Zhao X, Chen N L. Research on the Adsorptive Mechanism and Capability of Modified Coke Powder to Methylene Blue[J]. Ion Exch Adsorpt, 2011, 27(2): 152-159.
-
[15]
Iqbal M J, Ashiq M N. Adsorption of Dyes from Aqueous Solution on Activated Charcoal[J]. J Hazard Mater B, 2007, 139(1): 57-66. doi: 10.1016/j.jhazmat.2006.06.007
-
[16]
Liu X X, Gong W P, Luo J. Selective Adsorption of Cationic Dyes from Aqueous Solution by polyoxometalate-Based Metal-Organic Framework Composite[J]. Appl Surf Sci, 2016, 362: 517-524. doi: 10.1016/j.apsusc.2015.11.151
-
[17]
Hameed B H. Equilibrium and Kinetic Studies of Methyl Violet Sorption by Agricultural Waste[J]. Hazard Mater, 2008, 154(1/2/3): 204-212.
-
[18]
Chen S H, Zhang J, Zhang C L. Equilibrium and Kinetic Studies of Methyl Orange and Methyl Violet Adsorption on Activated Carbon Derived from Phragmites australis[J]. Desalination, 2010, 252(1/2/3): 49-156.
-
[1]
-
表 1 Cu(BDC-NH2)(4, 4′-Bipy)0.5的比表面结构参数
Table 1. Structural properties of Cu(BDC-NH2)(4, 4′-Bipy)0.5
Sample SBET/(m2·g-1) Vtotal/(cm3·g-1) D/nm Cu(BDC-NH2)(4, 4′-Bipy)0.5 124.2 0.1 0.2 表 2 甲基紫的等温吸附曲线参数
Table 2. Isotherm parameters the adsorption of methyl violet by Cu(BDC-NH2)(4, 4′-Bipy)0.5 at different temperature
Temperature/K Langmuir Freundlich Qm/(mg·g-1) KL/(L·mg-1) RL R2 KF/(mg·g-1) n R2 293 60.09 1.404 4 0.048 81 0.993 3 29.54 2.57 0.969 1 303 45.35 1.586 3 0.043 57 0.976 4 23.71 3.33 0.930 6 313 43.64 0.524 5 0.103 7 0.926 1 15.68 2.56 0.932 2 表 3 甲基紫在不同浓度下拟一级动力学和拟二级动力学参数
Table 3. Parameters of pseudo-first-order and pseudo-second-order adsorption kinetics model in different initital concentration
Kinetics model ρ0/(mg·L-1) Qe, exp/(mg·g-1) Qe, cal/(mg·g-1) K1/min-1;K2/(g·mg-1·min-1) R2 Psedo-first-order model 15 27.29 3.47 0.571 5 0.915 7 20 38.42 4.46 0.325 4 0.834 8 Psedo-second-order model 15 27.29 27.74 0.258 9 1 20 38.42 39.28 0.121 8 1 表 4 Cu(BDC-NH2)(4, 4′-Bipy)0.5吸附甲基紫的热力学参数
Table 4. The thermodynamic parameters of adsorption MV onto Cu(BDC-NH2)(4, 4′-Bipy)0.5
ΔG/(kJ·mol-1) ΔH/(kJ·mol-1) ΔS/(J·mol-1·K-1) 293 K 303 K 313 K -8.097 -6.727 -4.875 -52.28 -150.48 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 2
- 文章访问数: 1301
- HTML全文浏览量: 251



 下载:
下载:










 下载:
下载:

